Argent
L'argent est l'élément chimique de numéro atomique 47, de symbole Ag.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Le corps simple argent est un métal précieux — alors parfois appelé argent métallique ou plus simplement argent métal, ou encore métal blanc[12] — dont le nom désigne aussi en français dans le langage courant les pièces et billets de monnaie, voire par extension une certaine somme « d'argent ». Cependant, les économistes distinguent, à la différence du langage courant, l’argent métal ou réserve métallique de la monnaie comme outil de régulation des échanges économiques. Le faible niveau des réserves de ce métal en fait une matière première minérale critique.
Généralités et présentation de l'élément argent
Le mot français vient du terme latin argentum, i de même signification.
L’origine lointaine du mot, par le grec argyros, viendrait d’un étymon indo-européen commun *arg- signifiant « blanc brillant, laiteux et clair » et serait l’équivalent en sanskrit de ar-jun signifiant également « brillant »[13].
Ce métal précieux, malléable et très ductile, est blanc et brillant, comme le rappelle son nom. Dédié à la Lune ou à la déesse lunaire Artémis/Diane, il figure depuis l'Antiquité parmi les sept métaux sacrés, bien connus et même survalorisés par l'alchimie médiévale. Il est connu par la fabrication multi-millénaire de bijoux, de monnaies, ainsi que pour ses applications industrielles croissantes au XXe siècle.
Il s'agit d'un métal de transition, élément du groupe 11.
Isotopes
L'argent possède 38 isotopes connus, de nombre de masse variant entre 93 et 130, et 36 isomères nucléaires. Parmi ces isotopes, deux sont stables, 107Ag et 109Ag et constituent la totalité de l'argent naturel, dans un ratio 51,8/48,2 et quatorze radio-isotopes sont instables entre 102 et 117. On attribue à l'argent une masse atomique standard de 107,868 2(2) u.
Les isotopes de masse 112 et 117 sont des produits de fission de l'uranium.
Occurrences dans les milieux naturels, minéralogie et géologie
L'argent est un élément rare.
Le clarke s'élève à 0,1 g/t[14].

L'argent est présent dans le sous-sol à l'état natif, c'est l'argent natif du Mexique, du Pérou, du Chili, de Saxe, du lac Supérieur ou de Norvège, il est assez rare en cristaux isolés, mais fréquent en fils contournés et minces placages, à surface généralement altérée de teinte sombre ou très souvent dispersés en une multitude de structures réticulaires ou filaires. Il forme des amas parfois sous la forme de veines et filons à gangues siliceuse ou carbonatée, plus rarement dispersé en pépites compactes.
Il est plus souvent présent sous forme de sulfures comme argentine ou argyrose Ag2S, acanthite monoclinique ou argentite cubique, parfois mélangés à d'autres sulfures de plomb, de cuivre, d'antimoine, etc., comme la pyrargyrite 3 Ag2S. Sb2S3 sulfure double d'antimoine et d'argent, et son homologue As 3 Ag2S. As2S3. Il existe aussi sous forme d'halogénures naturels d'argent, AgCl comme la chlorargyrite ou la cérargyrite, AgBr ou la bromargyrite, les AgI ou l'iodargyrite.
Il peut être intimement associé avec l'or, par exemple en alliage dans l'électrum ou en combinaison commune avec le tellure dans la petzite.
Avec une concentration de 0,000 04 g/m3 d'eau de mer, ce sont environ cent millions de tonnes qui sont dissoutes dans les océans.
Gisements exploitables et techniques de production
Il est récupéré depuis l'Antiquité, parfois intensément au Moyen Âge des minerais de galène argentifère.
Il peut être extrait avantageusement des minerais argentifères pauvres, exploités pour le cuivre ou le plomb, par exemple des gisements communs de blende, de galène ou de pyrite, par chloruration et amalgamation. Il s'agit de récupération de sous-produits lors du traitement du cuivre et du plomb.
Le traitement de la galène donne du « plomb d'œuvre » qui peut contenir des quantités non négligeables d'argent. L'affinage de ce plomb argentifère spécifique s'opérait par cristallisations successives avec l'aide de sept chaudières. Le plomb argentifère est fondu, il refroidit lentement et le plomb presque pur reste au fond du bain. L'écumoire retirait sept huitièmes du plomb et ainsi de suite pendant trois opérations d'affinage similaire pour obtenir un Pb presque pur.
Mais les alliages Pb/Ag communs à faible teneur d'argent, de l'ordre de 0,5 % à 1 %, restent une matière première de la fabrication de l'argent. Il est possible de procéder à des fusions sélectives, éventuellement des fusions de zones, en utilisant le diagramme Pb/Ag.
Le zincage ou « désargentation du plomb » par le zinc était une autre technique complémentaire, le zinc, captant dans sa phase dix fois son poids d'argent, s'empare de l'argent du plomb d'œuvre. L'alliage triple Ag Pb Zn se retrouve en écume à la surface du plomb fondu, il est prélevé par une boîte percée de petits trous, lors de trois traitements. Une distillation permet d'éliminer l'essentiel du zinc, le bain étant débarrassé des restes de Zn par des eaux surchauffées sous pression, qui ont comme effet d'oxyder le zinc et les autres métaux les plus électronégatifs.
La coupellation permet de séparer l'argent du plomb. Selon l'ancienne méthode, il faut chauffer à l'air l'alliage Pb/Ag en présence de phosphates d'os. Le plomb métal s'oxyde en PbO qui est absorbé par la coupelle poreuse. L'argent précieux et stable reste inaltéré. Voici la réaction de base :
- Pb solide fondu en alliage avec l'argent + ½ O2 gaz réactif de l'air, apporté par une tuyère → PbO litharge, oxyde fusible qui s'écoule
Aujourd'hui, les procédés de cyanuration utilisant les complexes métalliques de l'ion cyanure dans l'eau sont utilisés.
- Pb(Ag) alliage Pb avec l'argent + NaCN cyanure de sodium → Na[Ag(CN)2] complexe soluble + Pb plomb non réactif, donc séparé
- 2 Na[Ag(CN)2] aqueux + Zn0 → 2 NaCN cyanure de sodium + Zn(CN)2 complexe de cyanure de zinc plus stable + 2 Ag0
L'argent est raffiné par électrolyse.
Corps simple et composés chimiques
Propriétés physiques et chimiques du corps simple
Le corps simple Ag de couleur blanche, apprécié pour son éclat blanc métal particulier et sa réflectance optique rehaussée par un polissage, est un cristal cubique, métal malléable et très ductile, de densité avoisinant 10,5.
Il fond légèrement au-dessus de 960,5 °C et s'évapore complètement entre 1 950 °C et 2 212 °C, selon la présence d'impuretés. La corructation est une lumière vive, ponctuelle, émise par ce métal au moment de son refroidissement après fusion lorsque le voile composé d’oxydes et de fondant en surface se déchire emporté par le borax. Cette solidification s'accompagne souvent de rochage (libération des gaz dissous par la phase liquide, composés principalement d'oxygène) qui peut faire gonfler le métal ou provoquer des cloques.
Il s'agit du corps métal meilleur conducteur de la chaleur et de l'électricité dans les conditions de température et de pression normales.
Ce métal noble présente une résistance chimique aux agents chimiques parfois à températures élevées. Il est insoluble dans l'eau et dans les alcalis. Il peut être inoxydable dans certaines atmosphères contrôlées.
Il est attaqué toutefois par les sulfures, par exemple communément par ceux contenus dans les aliments, d'où le noircissement de la vaisselle en argent parfois observé. Les sulfures présents dans l'atmosphère réagissent avec l'argent pour former Ag2S. Le ternissement est accéléré par la présence de cuivre dans les alliages. On peut éviter le ternissement en le stockant avec du papier imprégné d'acétate de cuivre ou de cadmium, qui ont plus d'affinité pour H2S[7].
Traiter l'argent par électrolyse avec une solution de chromate alcalin retarde le ternissement[4].
Il est attaqué par les acides nitrique et sulfurique, le dernier à chaud. Il est soluble dans le cyanure de potassium KCN aqueux, ce qui explique le procédé de cyanuration précédemment décrit.
Solubilité
L'acide de choix pour dissoudre l'argent est l'acide nitrique :
La dissolution dans l'acide sulfurique concentré chaud est plus économique en acide :
ou :
L'argent est attaqué par l'eau régale, l'acide chromique, les solutions de permanganate, l'acide persulfurique, l'acide sélénique et les solutions aqueuses d'halogènes libres. Les réactions peuvent être ralenties par la formation d'une couche protectrice (AgCl par exemple)[4].
Il est également soluble dans les hydroxydes alcalins fondus en présence d'air et dans les peroxydes fondus[15].
Analyse
On peut analyser un échantillon en le dissolvant dans de l'acide nitrique et en précipitant l'argent sous forme d'AgCl[7]. Le seuil de détection est de 0,1 µg l−1. Contrairement aux autres chlorures, peu solubles, le chlorure d'argent est soluble dans l'ammoniaque[4].
Les halogénures d'argent peuvent être dissous dans NaKCO3 fondu. L'argent est précipité sous forme métallique et peut être séparé par dissolution dans l'eau[4].
Alliages notables
- L'électrum, alliage naturel ou artificiel d'or et d'argent fin.
- L'argent Britannia, un alliage dont la composition massique est à 95,84 % d'argent fin et à 4,16 % d'autres métaux, généralement du cuivre. Le titre au millième de l'argent Britannia est de 958.
- L'argent sterling (aussi appelé argent premier titre) est un alliage dont la composition massique est à 92,5 % d'argent et à 7,5 % d'autre métal, généralement du cuivre. Le titre au millième de l'argent sterling est au minimum de 925.
- L'Argentium, un alliage mis au point en 1998 qui ajoute à l'argent sterling du Germanium, ce qui permet de limiter le ternissement[16].
Composés chimiques
La valence Ag(I) est la principale, à côté des marginales Ag(II) et Ag(III) et des exceptionnelles -II, -I, IV.
Le cation Ag+ qui possède un assez gros rayon ionique 1,15 Å est oxydant[17].
Les apprentis chimistes le connaissent pour ces combinaisons simples avec les halogènes, soit les halogénures d'argent comme chlorure d'argent AgCl cubique, le bromure d'argent AgBr ainsi que le fluorure d'argent AgF et l'iodure d'argent AgI α et β, respectivement de maille hexagonale et cubique.
Citons parmi ces composés les plus communs :
- l'oxyde simple d'Ag (I) Ag2O oxydant et l'oxyde mixte d'Ag I et III Ag(I) Ag(III)O2 ;
- l'hydroxyde d'argent ;
- les sulfures d'argent Ag2S orthorhombique, monoclinique et cubique ;
- le sulfate d'argent Ag2SO4 ;
- le sulfite d'argent Ag2SO3 ;
- le nitrate d'argent AgNO3 ;
- le nitrite d'argent AgNO2 ;
- le phosphate d'argent Ag3PO4 ;
- l'arséniate d'Ag Ag3AsO4 ;
- le chromate d'argent Ag2CrO4 ;
- le chlorate d'argent AgClO3, le chlorite d'argent AgClO2 et le perchlorate AgClO4 ;
- le bromate d'argent AgBrO3 ;
- le iodate d'argent AgIO3 ;
- le carbonate d'argent Ag2CO3 ;
- le thiocyanate d'argent AgSCN ;
- le cyanure d'argent AgCN ;
- l'acétate d'argent AgC2H3O2 ;
- le tartrate d'argent, l'oxalate d'argent.
Il existe aussi le tellurure d'argent, le permanganate d'argent, le fulminate d'argent, l'hexafluoroarséniate d'argent, le tétrachloroaluminate d'argent, le diéthyldithiocarbamate d'argent
Utilisations
L’argent métal et/ou ses principaux alliages sont utilisés par exemple :
- en joaillerie et en orfèvrerie comme métal précieux (argent massif) ou comme métal de recouvrement (métal argenté, obtenu par galvanoplastie) ;
- pour confectionner des médailles et des pièces de monnaie de prestige ;

- dans l'industrie des matériaux de contact mécanique et l'industrie atomique. Le métal et ses alliages ont des propriétés inoxydables et de résistance à l'usure intéressantes. C'est un matériau de revêtement de choix, pour assurer protection et étanchéité ;
- en électronique et électricité, car il présente une meilleure conductivité électrique que le cuivre, et reste conducteur même en partie oxydé ; dans l'industrie aéronautique, il permet la protection des dispositifs électroniques. Il présente des propriétés de résistance à la fatigue et d'anticorrosion. Il sert de dopant et/ou de revêtement pour des céramiques de type Bi-Pb-Sr-Ca-Cu-O supraconductrices ;
- en musique et en sonorisation, l'argent est utilisé dans la fabrication d'instruments de musique et forme d'excellentes membranes ou bobines pour actionner les tweeters de haut-parleur ;
- en médecine et chirurgie dentaire (amalgame).
L'argent est un excellent catalyseur en chimie. Les bromure et iodure d'argent sont employés en émulsions en photographie « argentique », ces sels d’argent étant photosensibles ; l'argent colloïdal a été utilisé comme médicament.
Bijouterie

Le deuxième domaine avec environ 7 700 tonnes au début des années 1990 est la bijouterie et l’orfèvrerie. L’argent est utilisé pour fabriquer des objets et des bijoux (pendentifs, bracelets, colliers…) tout ceci est possible car l’argent possède une propriété qui permet de concevoir ces œuvres : sa bonne malléabilité. L’argent est souvent allié à de faibles quantités de cuivre pour renforcer ses caractéristiques mécaniques. L'argent le plus courant en bijouterie est l'argent 925. Un poinçon 925 signifie que le bijou est fabriqué avec au moins 92,5 % d'argent pur et authentifie la qualité du métal précieux[18]. Cet alliage est appelé « argent sterling ». On l’utilise aussi allié à l’or, ou en plaquage (de 3 à 5 microns d’épaisseur pour la bijouterie, de 20 à 30 microns pour l’argenterie).
Photographie
Le troisième domaine est la photographie, avec environ 5 600 tonnes au début des années 1990. Les cristaux d’halogénures d’argent sensibles à la lumière sont l’élément essentiel des films et papiers photographiques. Ce secteur est en décroissance constante depuis plusieurs années en raison du développement de la photographie numérique. Le marché de la radiographie est devenu plus important que le marché de grand-public.
La photographie était la plus grande consommatrice d’argent avant que les procédés modernes permettent de récupérer l’argent dans les bains de développement, et ainsi de le recycler en bonne partie. La diminution du nombre de pellicules argentiques commercialisées, en raison de l’avènement du numérique, a également contribué à en réduire considérablement le besoin.
Applications monétaires
- Autrefois massivement frappé pour la monnaie, l’argent est désormais utilisé pour produire pièces et médailles avec 1 300 tonnes.
- On peut signaler aussi qu’une partie de l’argent est stockée ou déstockée par les États et les investisseurs (en 2004, vente de 1 920 t par les états et stockage d’environ 1 300 tonnes par les investisseurs).
- Après l'apparition de l'Euro, la France ne frappait plus de monnaie en argent ; depuis 2008, elle frappe de nouveau des pièces de collection en argent ayant un cours légal limité au territoire national (les Semeuses de Joaquin Jimenez).
Alimentation
- L’argent est utilisé en confiserie, principalement en Extrême-Orient.
- Il a une action germicide et bactéricide. La sulfadiazine argentique, composé d'argent métal et d'un sulfamide et commercialisée sous le nom de spécialité Flammazine possède des propriétés bactéricides. L'argent était employé dans des ustensiles destinés aux enfants afin de les protéger contre des maladies dont l’origine n’était pas connue à ces époques. L’expression naître avec une petite cuillère en argent dans la bouche vient de ce phénomène, son utilisation récente comme indication de richesse n’est qu’une conséquence. Les Vénitiens transportaient eau, vin et vinaigre dans des réservoirs en argent pour les conserver et lors de la conquête de l’ouest américain, les pionniers protégeaient leur réserve d’eau en plaçant des pièces de monnaie en argent dans leurs outres ou leurs barriques.
- L'argent est aussi un additif alimentaire industriel, E174[19].
Musique
- L’argent est utilisé en plaquage pour recouvrir certaines cordes de guitare, en général les plus graves.
- Il est aussi l'un des matériaux les plus utilisés, depuis le XIXe siècle, pour la fabrication des flûtes traversières. On trouve également à présent des pavillons de cuivres (trombones notamment) fabriqués en argent massif.
Nanotechnologies
- En 2008, selon les producteurs, environ 500 t/an de nano-argent (ou nanoargent, « nano-silver » pour les anglophones) auraient été produits, sous forme d'ions argent, de particules d’argent protéinées (silver proteins) ou de colloïdes utilisés comme biocide (1/5e de la production) ou bactéricide ou pour d'autres usages dans des domaines variés dont le textile avec par exemple des chaussettes bactéricides et anti-odeurs. On en trouve aussi dans des cosmétiques, sprays, revêtements de matériaux métalliques (réservoirs métalliques d'aspirateurs sans sac), plastiques, vernis, peintures, plans de travail, pansements, parois de réfrigérateurs, climatiseurs, emballages alimentaires[20]… Les nanoparticules d'argent peuvent former de 50 % à 80 % du poids de l'argent d'un colloïde, les 20 à 50 % restant étant des ions argent. La production de nano-argent aurait été multipliée par 500 de 2000 à 2004, mais certains produits (argent protéiné notamment) usurpent le nom de nano-argent, n'étant que microniques ou submillimétriques. L'étiquetage ne permet pas de discerner l'efficacité (variable) de ces produits. On manque par ailleurs de données sur le relargage de nanoargent (nanoparticules ou ions argent) dans l'environnement. Il peut atteindre au moins 15 % à plus de 90 % du produit pour certains usages (jusqu'à 100 % de perte en quatre lavages pour certaines chaussettes, même si elles n'ont pas été portées et lavées à la main)[21].
Différents types morphologiques peuvent être produits en jouant sur les phénomènes de précipitation et cristallisation ; cubes, cubes creux, sphères, particules à facettes, grains pyramidaux dont la réactivité et les propriétés (toxicité notamment) varient. 1 cm3 d'une concentration à 1 ppm de nanoparticules d'argent représente 25 000 milliards de ces particules[21]. Combinées à du phosphate de calcium, l'activité de particules de vingt à cinquante nanomètres de nano-argent peut être jusqu'à 1000 fois supérieure, ce qui laisse présager des impacts environnementaux.
Parmi 800 nano-produits répertoriés dans les années 2000 par le Woodrow Wilson Institute, 56 % étaient fabriqués à partir de nano-argent (le plus souvent à partir de nanoparticules d'argent). Des évaluations estiment qu'en 2015, il pourrait en être produit 1 000 à 5 000 tonnes par an, ce qui correspondrait à 1/3 de l'actuelle production mondiale d’argent)[21].
Des rats exposés aux nanoparticules de 15 nanomètres inhalées présentent ensuite ces particules dans tout l’organisme (cerveau y compris), avec des effets qu’on ignore. Un article de février 2009 a conclu que des nanoparticules d’argent testées en association avec du cuivre (argent seul et argent colloïdal) pour différentes tailles de nanoparticules interféraient avec la duplication de l’ADN[21]. À forte dose, une argyria est possible[21]. Enfin, une résistance bactérienne au traitement par nano-argent peut apparaître, comme pour les autres traitements antibiotiques.
Mécanique
L'argent a une bonne résistance à l'effort, il est utilisé dans les vilebrequins de locomotives diesel. On le retrouve également dans les roulements à billes des turbines, où on fait appel à ses propriétés autolubrifiantes.
Contacts électriques
Enfermé entre deux feuilles de papier mylar, il est utilisé dans les contacts électriques des claviers d'ordinateurs[7]. Il est aussi utilisé pour recouvrir les contacteurs en cuivre des TGV.
Miroirs
Une solution de nitrate d'argent, de soude, d'ammoniaque et de sucre (ou de formaldéhyde) est utilisée pour déposer une couche d'argent sur le verre, le verre étant préalablement traité avec SnCl2. Ce procédé sert notamment à fabriquer les bouteilles isothermes, les CD[7] ou les décorations de sapins de Noël[4].
Toxicologie
Tous les sels d'argent sont toxiques.
L'argent est aussi un polluant et un contaminant.
- Très toxique pour les bactéries, les champignons et de nombreux organismes à sang froid, l'argent est extrêmement toxique pour les larves de mollusques alors que les adultes peuvent le bioaccumuler en quantité importante .
Pour des raisons mal comprises, l'être humain en supporte des doses bien plus élevées que ces organismes. L'absorption d'argent dans la circulation du sang de l’organisme humain ne semble pas avoir d’effet direct en dessous d'un certain seuil, mais un excès provoque une maladie dite argyrisme qui donne à la peau et au blanc de l'œil un teint gris-bleuâtre, voire noirâtre.
Écotoxicologie
Au-delà de 0,4 ng/litre, l'argent est considéré comme un indicateur de pollution (par le nitrate d'argent par exemple).
- Des baies très polluées comme la Baie de San Francisco et celle de Caroline du Sud en contiennent jusqu'à 20 ng/litre voire plus.
- Les organismes marins filtreurs peuvent en accumuler des doses préoccupantes (par exemple, 0,01 à 58 mg kg−1 de chair, en poids sec, relevé dans des moules aux États-Unis, ou 1,8 à 11 mg kg−1 dans des huitres (p.s.)[22]).
- L'argent pourrait ainsi contribuer à certains déséquilibres écologiques et au phénomène de zones marines mortes qui caractérise certaines baies.
- En France, de 2003 à 2007, l'Ifremer a constaté que les moules en contiennent localement de grandes quantités entre l'estuaire de la Seine et la façade maritime picarde, selon la cartographie interactive des données de surveillance obligatoire pour les métaux, HAP, PCB, DDT, lindane dans la chair des huîtres et moules[23].
- En France toujours, alors que beaucoup de métaux lourds tendent à diminuer dans la chair des poissons pêchés en mer et commercialisés depuis les années 1990, l'argent reste stable ou a même pu localement dans les années 2000 significativement augmenter[24].
Économie
L'argent a été utilisé comme monnaie dans la plupart des civilisations au même titre que l'or. Jusqu'à l'instauration du système de l'Étalon-or à la fin du XIXe siècle en Occident, la plupart des pays européens ainsi que les États-Unis ou encore le Mexique fonctionnaient dans le cadre d'un régime monétaire appelé bimétallisme dans lequel une monnaie or et une monnaie argent circulaient conjointement. Le bimétallisme a été accusé par les économistes de favoriser une certaine instabilité des cours de la monnaie et donc de provoquer une instabilité de l'économie. On parlera dans ce cadre de la fameuse loi de Gresham, du nom d'un commerçant et financier britannique du XVIe siècle, qui a démontré que la mauvaise monnaie avait tendance à chasser la bonne. Cela signifie que dans le cadre d'un système monétaire où deux étalons monétaires coexistent, l'un finit par chasser l'autre, en l'occurrence l'or qui devient de ce fait rare et recherché. Cette concurrence entre les monnaies peut avoir des répercussions défavorables sur l'économie en favorisant la spéculation et en bouleversant la hiérarchie des prix. L'abandon du bimétallisme n'a cependant pas sonné la fin de l'argent en tant que monnaie. Ainsi en France jusqu'aux années 1970, des pièces en argent massif ont été frappées. Parmi celles-ci, on peut citer la célèbre pièce de 5 Francs sur laquelle figure en effigie la semeuse, une femme qui sème des grains de blé. Ces pièces font encore l'objet d'une cotation et donc peuvent servir de support d'investissement. Par ailleurs, l'argent en tant que métal précieux peut être utilisé pour placer ses liquidités. Le placement peut se faire sous forme de pièces, mais aussi de lingots ou encore de lingotins (d'une taille plus petite que les lingots). Le cours du lingot varie en fonction du cours de l'once d'argent. L'argent comme l'or fait en effet l'objet d'une double cotation sur le marché de Londres et sur le marché New Yorkais. Dans les deux cas, les mouvements observés sont à la fois liés aux fondamentaux (demande de métaux précieux, volume de production, perspectives macro-économiques…), mais aussi à la spéculation. Il faut d'ailleurs le noter, les cours de l'argent varient davantage que ceux de l'or. On constate généralement que les cours de l'argent amplifient les variations observées sur les cours de l'or à la hausse comme à la baisse.
Consommation
La consommation d’argent en 2004 dans le monde a été de l’ordre de 26 000 tonnes.
La consommation dépasse la production depuis plusieurs années. On estime que l'argent risque de devenir un métal rare :
- Selon Mansoor Barati, spécialiste des métaux rares et de leur recyclage à l’université de Toronto, on pourrait épuiser les stocks connus aux alentours de 2029 au rythme de la production actuelle : 23 000 tonnes en 2013, selon le Silver Institute contre une demande de 30 000 tonnes. Le service géologique des États-Unis estime quant à lui que l’épuisement pourrait intervenir dès 2021, d’autres que les stocks d’argent dans le monde disparaîtront entre 2023 et 2028 ou encore en 2037[25].
Généralités
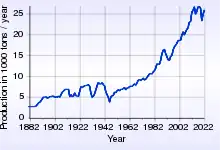
L’argent provient de mines ou du recyclage.
En 2004 :
- la production minière a été de l’ordre de 19 700 tonnes ;
- la quantité d’argent recyclé a été de l’ordre de 5 600 tonnes.
Selon l’USGS, la production d’argent dans le monde en 2008 était estimée à 20 900 tonnes d’argent soit 671 millions d’onces.
L’argent est extrait soit de mines dont il est le principal métal, soit de mines d’autres métaux dont l’argent est en quelque sorte un sous-produit ; c’est ainsi que :
En 2011, la production était de 23 689 tonnes d’argent, soit 761,6 millions d’onces[26].
Pays producteurs
Globalement, les Amériques ont produit un peu plus de la moitié de l’argent extrait dans le monde.
| Pays | Production 2013 | % monde | |
|---|---|---|---|
| 1 | Mexique | 5 278,3 t | 20,7 % |
| 2 | Pérou | 3 673,3 t | 14,4 % |
| 3 | Chine | 3 670,2 t | 14,4 % |
| 4 | Australie | 1 841,3 t | 7,2 % |
| 5 | Russie | 1 412,1 t | 5,5 % |
| 6 | Bolivie | 1 281,5 t | 5,0 % |
| 7 | Chili | 1 219,3 t | 4,8 % |
| 8 | Pologne | 1 169,5 t | 4,6 % |
| 9 | États-Unis | 1 088,6 t | 4,3 % |
| 10 | Argentine | 768,3 t | 3,0 % |
| 11 | Canada | 647 t | 2,5 % |
| 12 | Kazakhstan | 615,8 t | 2,4 % |
| 13 | Inde | 376,4 t | 1,5 % |
| 14 | Suède | 335,9 t | 1,3 % |
| 15 | Guatemala | 323,5 t | 1,3 % |
| Total monde | 23 689 | 100 % | |
Chiffres de 2013, source : Silver Institute, 2013
Histoire
Le matériau argent, métal ductile et malléable, est connu au Néolithique, avant 5000 av. J.-C., par diverses pièces d'ornement, vaisselles et bibelots.
La première extraction connue date de 3000 av. J.-C., en Anatolie. Ces premiers filons représentaient une ressource de valeur pour les civilisations qui ont fleuri dans le Proche Orient, ainsi que pour la Crète et la Grèce, tout au long de l’Antiquité.
Les monnaies les plus anciennes en argent, souvent à valeur d'échange global entre autorités, sont sous forme de trépieds, de vases, d'anneaux, de barres et lingots de tailles uniformes. À la fin du IIIe millénaire av. J.-C. existent ainsi des barres et autres lingots d'argent de masse constante, munis d'un sceau officiel, parmi le matériel archéologique mis au jour en Cappadoce. Ces formes assez massives peuvent être considérées comme des devises de métal.
Vers 2000 av. J.-C., des mesures de grains d'argent attestent d'une monnaie de compte existante en Mésopotamie, à côté d'autres outils monétaires sophistiqués adaptés au calcul et au crédit.
À peu près en 1200 av. J.-C., le centre de production d’argent serait établi aux mines de Laurium, en Grèce, d’où il continue d’alimenter les empires naissants de la région. Dans le bassin méditerranéen, la civilisation créto-mycénienne développe l'art de mise en valeur de l'argenterie, diffusant le ciselage, le bosselage et le damasquinage. Les Phéniciens diversifient les rares sources d'approvisionnement en exploitant les mines de la péninsule ibérique.
Les Assyriens au VIIIe siècle av. J.-C. mentionnent sur les pièces et morceaux d'argent leur teneur garantie en argent, ce sont les premières indications explicites du titre.
À l'âge classique grec, au VIe siècle av. J.-C., l'argent ou l'électrum des mines du Laurion sert à décorer les statues (thésaurisation) et/ou à fondre de la monnaie en pièces communes, rondes et aplaties. Les Perses achéménides contemporains ont laissé de belles amphores en argent en Asie mineure. Il faut attendre le Ve siècle et le IVe siècle pour que les peuples gaulois, subissant une forte influence de la civilisation méditerranéenne, initient, essentiellement par imitation grecque, leurs propres monnayages d'argent.
Bien avant 80 à 100 apr. J.-C., sous l'apogée de l'empire antonin, l’Espagne s'est imposée à son tour comme la capitale de la production d’argent. Les mines ibériques sont le principal fournisseur de l’Empire Romain au Ier siècle. Jusqu'aux crises du Bas-Empire, l'essor de la production d'argent demeure constante. Outre les monnaies, les vaisselles, les bibelots divers, les lampadaires, les tables et lits ouvragés, les bustes l'attestent[27].
À partir du IVe siècle apr. J.-C., l'art de l'argenterie rejoint l'orfèvrerie sacrée. L'ornementation en relief atteint un apogée avec la demande chrétienne, le perforage, la niellure, le ciselage et l'émail argent caractérisent cette technique d'ornement précise, qui apparaît dans toute sa splendeur avec la cassette de l'église San Nazaro à Milan réalisée au IVe siècle et les portes du baptistère du Latran à Rome au Ve siècle. Les plats, patènes et burettes forment une partie du trésor des vieilles cathédrales. La production byzantine, de même que l'occident barbare, n'oublient pas les armes et bijoux d'apparat[28].
À la suite de l’invasion de l’Espagne par les peuples arabo-berbères ou maures, l'extraction d’argent ibérique ne sert plus la péninsule européenne. L'exploitation minière européenne se répartit vers un plus grand nombre de pays miniers déjà localement actifs, dont la plupart se situent en Europe centrale. La plupart des découvertes des plus grandes mines d’argent se sont faites du fait de la demande croissante entre 750 et 1200 apr. J.-C., incluant celles faites en Allemagne et en Europe de l’Est. La période carolingienne, amenant le faste dans les églises et les monastères bénédictins hégémoniques, favorise l'art de l'argenterie et de l'orfèvrerie. Il s'agit d'une véritable thésaurisation que l'art monastique, notamment l'ordre bénédictin de Cluny, perpétue malgré les risques de pillage jusqu'au Xe et XIe siècles. Les évêchés gardent leurs décorations en argent, ainsi l'autel de Vuolvinius recouvert de feuilles et plaques d'argent doré avec ornementation en relief, élevé dans l'église Saint Ambroise de Milan au IXe siècle. L'argenterie sacrée marque indéniablement l'art souvent préservé jusqu'à nos jours des cathédrales et monastères allemands, comme à Aix-la-Chapelle, Ratisbonne, Essen, Bamberg, Trèves, Hilsdesheim. L'argent placé en couverture sert à protéger les manuscrits sacrés de la cathédrale de Trèves.
L'essor de l'art gothique en France, puis en Flandres et en Allemagne ne tarit pas l'attrait pour l'argenterie. Reliquaires, tabernacles, objets de culte divers montrent des motifs ornementaux en bosselage et à plat, à l'instar des aiguières et des plats-bassins profanes.
L'argenterie italienne connaît un âge d'or au Quattrocento, avec des artistes prolifiques tels que Lorenzo Ghiberti, Michelozzo, Antonio del Pollaido, Andrea del Venochio. L'autel du baptistère de Florence et surtout l'art profane produisant de la vaisselle d'art, des candélabres et de multiples statuettes témoignent de cette profuse création.
Le demi-millénaire compris entre 1000 et 1500 est une période significative durant laquelle augmente le nombre de mines qui sont découvertes, ainsi que celui des avancées technologiques et améliorations de production métallurgique médiévale qui en découlent.
Cependant, aucun événement historique concernant l’argent ne peut rivaliser avec la découverte du Nouveau Monde en 1492 et sa première exploitation séculaire. Cette importante découverte et les années qui la suivent ont réinventé le rôle de l’argent à travers le monde.
L'exploitation des mines du Potosí[29] après 1545-1555 a conduit à une extraction d’argent telle, qu’elle éclipse alors tout ce qui avait pu se produire avant dans ce domaine. L'année 1575 marque le début de l'arrivée massive de l'argent de Potosí en France[30]. Entre 1500 et 1800, la Bolivie, le Pérou et le Mexique ont effectué à eux trois plus de 85 % de la production et du commerce mondial de l'argent.

Au XVIIe siècle, le style et les techniques des argentiers français, un art codifié par Charles Lebrun et placé sous l'égide royale, gagne les autres pays européens. Le goût de l'argenterie commune - vaisselles, éléments de meubles ou ornements d'ameublement - gagne la noblesse et la riche bourgeoisie française. Mais le siècle des Lumières voit apparaître un désintérêt pour l'argent alors que la porcelaine fait fureur, le déclin de l'usage de l'argent pour la vaisselle est rapide, malgré quelques chocolatières d'exception. Le rococo conserve l'ornementation à base d'argenterie, avant que le néo-classicisme anglais, illustré par l'architecte-décorateur Robert Adam (1728-1792) n'influence durablement l'Angleterre et son art de vivre des élites vers une conservation presque hiératique des anciennes pratiques françaises.
L'argent métal précieux a été à différentes reprises considéré comme un étalon monétaire. C'est le cas du "Franc en argent", institué par la loi du 7 germinal an XI, le franc germinal comportant 5 g d'argent au titre de 900/1000. De facto s'instaure un bimétallisme (or/argent) qui s'impose jusqu'en 1873. Pendant la période révolutionnaire, le rapport de valeur or/argent se fixe à 1 sur 15,5 alors qu'au milieu du XVIe siècle, il était seulement de 1 sur 10,75.
Au XIXe siècle, plusieurs autres pays ont commencé à contribuer plus considérablement, notamment les États-Unis, avec la découverte du filon Comstock au Nevada. La production d’argent mondiale a continué à grandir, passant de 40 à 80 millions d’onces de production annuelle durant les années 1870.
La période allant de 1876 à 1920 a représenté une explosion tant dans le domaine de l’innovation technologique que dans l’exploitation de nouvelles régions dans le monde entier. La quantité produite au cours du dernier quart du XIXe siècle a quadruplé par rapport à la production moyenne de ses 75 premières années, passant à presque 120 millions d’onces de production annuelle. De même, de nouvelles découvertes en Australie, Amérique centrale et Europe ont considérablement augmenté la quantité mondiale de production d’argent.
À la fin du XIXe siècle, l'argenterie industrielle s'impose, le placage industriel cède la place à la galvanoplastie où s'illustre le Français Ruolz avant l'anglais Elkington en 1899.
Les deux décennies entre 1900 et 1920 ont abouti à une augmentation de la production mondiale de 50 % et ont élevé son total à environ 190 millions d’onces. Ces augmentations ont découlé de découvertes faites au Canada, États-Unis, Afrique, Mexique, Chili, Japon et bien d’autres pays. La conséquence économique, rendue inévitable par la hausse de la production mondiale malgré la demande soutenue, entraîne une chute radicale de valeur et d'intérêt pour l'argent. En 1914, à la fin de la Belle Époque, le kilogramme d'argent fin équivaut encore environ à 90 francs or. En 1933, le kilogramme d'Ag fin n'en vaut plus que la moitié en valeur réelle. La chute est à cette époque marquée par le succès du totalitarisme amplifiée par les ventes massives d'argent de l'Allemagne.
Au cours du dernier siècle, de nouvelles technologies ont également contribué à une hausse massive de la production mondiale d’argent. Les avancées majeures ont consisté en le forage par machines à vapeur, l’extraction, l’aspiration de l’eau dans les tunnels et l’amélioration des transports. En outre, les progrès techniques dans l’industrie minière ont amélioré la capacité à séparer l’argent du reste des minerais et ont permis de traiter un plus grand nombre de minerais contenant l’argent.
De telles méthodes ont été critiques à l’augmentation du volume de production future, puisque de nombreux filons productifs se sont vus épuisés vers la fin du XIXe siècle.
Le XXe siècle montre que l'argent est encore un métal américain, les Amériques assurant au milieu des années 1960, 60 % de la production mondiale (8 340 t). La région de Mexico, associée à la sierra Madre et au désert de Mapuni, ont longtemps assuré la première place au Mexique. En 1965, la production de ce pays passait en seconde position, avec 1 254 t, derrière le Pérou assurant 1 284 t. Venait ensuite les États-Unis avec 1 213 t (Idaho en tête), le Canada 1 025 t (Ontario, Colombie britannique), l'URSS 840 t, l'Australie 526 t, le Japon 519 t, l'Allemagne fédérale 324 t, la Suède 124 t et la France 140 t.
À ce jour, la production annuelle mondiale atteint en moyenne 671 millions d’onces, soit 21 000 t.
Recyclage
Les réserves d'argent (sur la base des contraintes économiques et techniques actuelles) sont de 270 000 tonnes pour une production annuelle mondiale de 21 300 tonnes (en 2008), ce qui correspond à seulement 13 années de production annuelle.
Le gisement collectable pour recyclage est constitué par :
- les cartes électroniques, avec une concentration en métal de 0,3 %, sous forme de métal ou d'alliages (en baisse : les cartes mères d’ordinateur ne contiendraient plus que 0,1 % d’argent en 2010) ;
- les bains photographiques (en déclin en raison de l'apparition de la photographie numérique), avec une concentration de 1 à 2 g/l, sous forme de sels d'argent ;
- les bains d'argentage pour le dépôt d’une couche d’argent (revêtements métalliques, miroirs dans l'industrie optique, verre), avec une concentration de 1 à 5 g/l, sous forme de AgCN ;
- et les films radio et papier, avec une concentration de 3 à 12 g/kg, sous forme d'halogénures d'argent (chlorure et bromure).
Le taux de recyclage du métal est de 30 à 50 % pour les principales applications. Cependant, l'argent est de plus en plus utilisé dans des applications où le métal est présent en très faibles proportions (électronique principalement, applications photovoltaïques et verrerie dans une moindre mesure). Dans ces cas, l’argent est plus difficilement recyclable.
En France, le gisement collectable est de 210 tonnes, et le gisement collecté est de 60 tonnes[32].
Notes et références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, , 89e éd., p. 10-203
- (en) Ullmann's Encyclopedia of Industrial Chemistry, Release 2004, 7th Edition, Silver, Silver Compounds, and Silver Alloys, Wiley-VCH Verlag GmbH & Co, DOI 10.1002/14356007.a24_107
- Procès-verbaux du Comité international des poids et mesures, 78e session, 1989, pp. T1-T21 (et pp. T23-T42, version anglaise).
- Entrée « Silver, Powder » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 13 février 2010 (JavaScript nécessaire)
- (en) Samuel F. Etris, Kirk-Othmer encyclopedia of chemical technology 4th ed. : Silver and silver alloys, vol. 22, John Wiley & Sons.
- Base de données Chemical Abstracts interrogée via SciFinder Web le 15 décembre 2009 (résultats de la recherche)
- « Argent » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « ChemIDPlus » (consulté le )
- « Comment le métal blanc a façonné le monde (Arte) Quand la Chine découvrait l’argent… », sur Télé 7 Jours (consulté le ).
- Ernout, A. et Meillet, A., Dictionnaire Étymologique de la langue latine. Histoire des mots, Paris, Librairie C. Klicksieck, (OCLC 79138165)
- Alain Foucault, op. cit.
- « Silver, elemental » dans la base de données Hazardous Substances Data Bank, consulté le
- « Argent fin, Argent Sterling, Argentium… », sur Tulipes en janvier, (consulté le )
- C'est le plus gros parmi les cations dits "à valence principale" des métaux de transition.
- « L'Argent, un métal précieux », Futura sciences, 0/02/2008 (lire en ligne, consulté le )
- (en) Victoria Emerton et Eugenia Choi, Essential Guide to Food Additives, Royal Society of Chemistry, (lire en ligne).
- Inventaire suisse de l’utilisation des nano-argents
- "L'analyse bénéfices / risques appliquée aux nanotechnologies : le cas du nano-argent", Paris, 2 avril 2009
- Ifremer, Surveillance du milieu marin, travaux du Réseau National d'Observation de la Qualité du Milieu Marin ; Le RNO : programmes actuels - L'argent, le cobalt, le nickel et le vanadium dans les mollusques du littoral français - Les carottes sédimentaires, mémoire de la contamination ; Bulletin Ifremer, 2002 Télécharger en Pdf
- Les contaminants chimiques dans les huîtres et les moules du littoral français / Résultats du réseau de surveillance ROCCH (ex RNO) pour la période 2003-2007
- (en) Thierry Guérin, Rachida Chekri, Christelle Vastel, Véronique Sirot, Jean-Luc Volatier, Jean-Charles Leblanc et Laurent Noël, Determination of 20 trace elements in fish and other seafood from the French market ; Food Chemistry, Volume 127, Issue 3, 1 August 2011, Pages 934-942 ; Doi:10.1016/j.foodchem.2011.01.061 (Résumé)
- Fin de l’argent métal : mines épuisées en 2029 ? ConsoGlobe
- Silver Production 2011, sur le site silverinstitute.org
- D'abord, les restes figés dans la cendres d'Herculanum et de Pompéi, par exemple au musée archéologique de Naples, ensuite les objets de fouilles de Boscoreale conservé au musée du Louvre à Paris, enfin les trouvailles de Hildesheim au musée allemand de Berlin ou les réserves du musée national de Turin, par les objets de Bosco Marengo comme le buste de Lucius Verus, en donnent un premier aperçu.
- Elle peut être observée au musée de Saint-Germain-en-Laye.
- Gildas Salaün, « Potosi, l'argent du Nouveau Monde », Monnaie magazine, , p. 50-55 (ISSN 1626-6145).
- Gildas Salaün, « 1575 : une inondation d'argent », Monnaie magazine, mai - juin 2021, p. 50-55 (ISSN 1626-6145).
- (en) Marcin Latka, « Silver sarcophagus of Saint Stanislaus », artinpl (consulté le )
- ADEME, « Étude du potentiel de recyclage de certains métaux rares », juillet 2010, 1re partie, fiche de l'argent, p. 18-25
Bibliographie
- (fr+en) Alain Foucault, Jean-François Raoult, Fabrizio Cecca et Bernard Platevoet, Dictionnaire de Géologie, 8e éd., édition Dunod, 2014, 416 p. Avec la simple entrée argent, p. 24.
- Robert Collongues, article « Argent, métal », Encyclopædia Universalis, 2010, première page.
- Pierre Blazy et El-Aïd Jdid, Métallurgie de l’argent, Techniques de l'ingénieur, 2006, lire en ligne.
- Paul Pascal, Nouveau traité de chimie minérale, 3. Groupe Ib, généralités, cuivre, argent, or (avec t. 20, Alliages métalliques), Paris, Masson, (réimpr. 1966), 32 vol. (BNF 37229023).
Voir aussi
Articles connexes
- Andorite IV
- Archéométallurgie
- Argyrophilie
- Akçe
- Amalgame
- Arbre de Diane (chimie)
- Argent Britannia, Argent sterling
- Argent natif
- Argenterie
- Argentimétrie, dosage à l'aide de sels d'argent, par exemple Méthode de Charpentier - Volhard
- Argenture
- Argyropée
- Benjaminite
- Billon (alliage)
- Boum en argent du Colorado, ruées vers l'argent
- catalyseur d'oxydation d'alcènes ou de réaction d'élimination
- Coloration à l'argent en histologie
- Composés de l’ion argent
- Denier, Quinaire, Sesterce, silique, Miliarense
- Dyscrasite ou argent antimoniale des anciens
- Électrum
- Éléments de la période 5
- Freibergite, cuivre gris argenté
- Galvanostégie
- Gros blanc, Teston
- Histoire des mines d'argent
- Ion argent
- Ionisation cuivre-argent
- Isotopes de l'argent
- Kreuzer, Thaler
- Livre ou marc, unités anciennes de pesée de l'argent
- Métal argenté
- Miargyrite
- Nano-argent
- Naumannite
- Niellage, émail sur argent, cloisonné
- or blanc
- Papyrus de Leyde
- Pièce en argent, piastre
- Photographie argentique, Types d'émulsions argentiques
- Pile à cathode oxyde d'argent
- Pierre de touche, contrôle du titre par l'essai par voie humide de Gay-Lussac
- Pyrargyrite
- Réal espagnol
- Réaction de Tollens ou "test du miroir d'argent" (aldéhydes, oses)
- Rixdale
- Routhiérite
- Statère
- Stéphanite (minéral)
- Transmétallation avec les complexes carbéniques d'argent
- Trésor de Carthage
- Vermeil, un alliage contenant de l’argent.
- Xanthoconite
Liens externes
- Ressources relatives à la santé :
- Ressource relative aux beaux-arts :
- (en) Grove Art Online
- Notices dans des dictionnaires ou encyclopédies généralistes :
- L'argent, SCF.
- Cours de l'or, de l'argent, du palladium et du platine
- Dossier pluridisciplinaire sur l'argent, Futura sciences.
- « Étude du potentiel de recyclage de certains métaux rares », ADEME, juillet 2010, fiche métal de l'argent : 1re partie, p. 18-25.
- (en) « Technical data for Silver » (consulté le ), avec en sous-pages les données connues pour chaque isotope.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||




