Tennesse
Le tennesse, souvent désigné par son nom anglais tennessine, est l'élément chimique de numéro atomique 117. Il a pour symbole Ts[alpha 1]. Il correspond à l'ununseptium (Uus) de la dénomination systématique de l'IUPAC, et est encore appelé élément 117 dans la littérature. Il a été synthétisé pour la première fois en janvier 2010 par les réactions 249Bk (48Ca, 3n) 294Ts et 249Bk (48Ca, 4n) 293Ts à l'Institut unifié de recherches nucléaires (ОИЯИ ou JINR) à Doubna, en Russie. L'IUPAC a confirmé son identification en décembre 2015 et lui a donné en novembre 2016 son nom anglais définitif en référence au Tennessee, État américain où se trouve le laboratoire national d'Oak Ridge d'où provient la cible de berkélium ayant permis la synthèse de l'élément 117[6].
| Tennesse | |||||||||||
| |||||||||||
| Position dans le tableau périodique | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbole | Ts | ||||||||||
| Nom | Tennesse | ||||||||||
| Numéro atomique | 117 | ||||||||||
| Groupe | 17 | ||||||||||
| Période | 7e période | ||||||||||
| Bloc | Bloc p | ||||||||||
| Famille d'éléments | Indéterminée | ||||||||||
| Configuration électronique | [Rn] 5f14 6d10 7s2 7p5 | ||||||||||
| Électrons par niveau d’énergie | Peut-être[1] 2, 8, 18, 32, 32, 18, 7 | ||||||||||
| Propriétés atomiques de l'élément | |||||||||||
| Masse atomique | [294] | ||||||||||
| Isotopes les plus stables | |||||||||||
| Propriétés physiques du corps simple | |||||||||||
| État ordinaire | Présumé solide[4] - [1] | ||||||||||
| Masse volumique | 7,1 à 7,3 g/cm3[4] | ||||||||||
| Divers | |||||||||||
| No CAS | [5] | ||||||||||
| Précautions | |||||||||||
 Radioélément à activité notable |
|||||||||||
| Unités du SI & CNTP, sauf indication contraire. | |||||||||||
C'est un transactinide très radioactif, dont l'isotope connu le plus stable, le 294Ts, a une période radioactive d'environ 51 ms. Situé sous l'astate dans le tableau périodique des éléments, il appartient au bloc p et serait probablement de nature métallique[7], plus précisément un métal pauvre.
Dénomination systématique et nom en français
L'ancien nom ununseptium relève de la dénomination systématique attribuée par l'Union internationale de chimie pure et appliquée (IUPAC) aux éléments chimiques inobservés ou dont la caractérisation expérimentale n'est pas encore formellement validée. Il est composé de racines latines signifiant « un-un-sept » et du suffixe -ium générique pour les noms d'éléments chimiques.
La découverte de l'élément 117 a été confirmée par l'IUPAC le 30 décembre 2015[8]. Le 8 juin 2016, la division de chimie inorganique de l'IUPAC annonça sa décision de retenir comme nom finaliste (en anglais) tennessine, de symbole Ts. Une consultation publique fut ouverte jusqu'au 8 novembre 2016[9] - [10]. L'IUPAC l'adopta définitivement le 28 novembre 2016[11].
La traduction du nom anglais tennessine dans les langues autres que l'anglais a posé certaines difficultés inédites, notamment en français, dans la mesure où il ne se terminait pas en -ium, immédiatement transposable dans de nombreuses langues. Par une recommandation d'avril 2016, l'IUPAC avait en effet indiqué que le nom anglais des éléments du groupe 17 devait normalement avoir la désinence -ine[12]. L'usage en français a alors largement repris la forme anglaise tennessine à travers la presse[13] et les magazines[14] - [15], ainsi que par le ministère de l'Éducation du Québec[16]. La forme tennesse, déduite par continuité avec le nom des autres éléments du groupe 17 — qui, hormis le fluor, ont en français la désinence -e — a d'abord été attestée assez marginalement[17], puis a été proposée par la banque de données terminologiques et linguistiques du gouvernement du Canada[18] et a finalement été retenue en mars 2017 par la Société chimique de France[19] et publié en juin 2017 au Journal officiel[20] - [21].
Synthèse
La première synthèse de l'élément 117 est le fruit d'une collaboration entre le laboratoire national d'Oak Ridge (ORNL) à Oak Ridge, dans le Tennessee, et l'Institut unifié de recherches nucléaires (JINR) à Doubna, dans l'oblast de Moscou. L'ORNL était alors le seul laboratoire au monde à pouvoir fournir la cible en berkélium nécessaire à l'expérience, tandis que l'équipe d'Iouri Oganessian au JINR disposait d'installations en mesure de détecter les nucléides résultant de la fusion de cette cible avec des projectiles de calcium 48[23]. Le berkélium de la cible a été produit par irradiation neutronique sur une durée d'environ 250 jours dans le High Flux Isotope Reactor (en) de l'ORNL de sept cibles contenant un mélange de microsphères de CmO2 et de poudre d'aluminium. Environ 50 g d'actinides sont présents dans chacune des cibles utilisées par le High Flux Isotope Reactor, majoritairement du curium (42 g), de l'américium (5 g) et du plutonium (3 g). Après irradiation, les cibles ont été conservées trois à quatre mois pour réduire la concentration d'iode 131 puis 22,2 mg de berkélium a été isolé des autres constituants. Six cibles de 6,0 cm2 ont été assemblées à partir de celui-ci au Research Institute of Atomic Reactors (en) par déposition de BkO2 (équivalent à 0,31 mg cm−2 de berkélium 249). Les cibles ont ensuite été placées à Doubna face au faisceau d'ions calcium 48, sur un disque tournant à 1 700 tours par minute[24] - [25].
L'équipe du JINR a annoncé en janvier 2010 avoir observé la désintégration radioactive de l'élément 117 à travers deux chaînes de désintégration grâce au « séparateur de recul à gaz de Doubna »[26] (DGFRS-I)[27] : l'une correspondant à un isotope impair-impair (294Ts, 117 protons et 177 neutrons) ayant subi six désintégrations α avant une fission spontanée, et l'autre correspondant à un isotope impair-pair (293Ts, 117 protons et 176 neutrons) ayant subi trois désintégrations α avant une fission spontanée :
Ces données ont été transmises au laboratoire national de Lawrence Livermore (LLNL) pour des analyses plus poussées, et les résultats complets ont été publiés le 9 avril 2010[24], révélant que les deux isotopes observés pouvaient avoir une période radioactive de plusieurs dizaines, voire centaines de millisecondes.
La section efficace de cette réaction est estimée autour de 2 picobarns ; les nucléides 293Ts et 294Ts obtenus ont chacun une chaîne de désintégration a priori assez longue, allant jusqu'au dubnium, voire au lawrencium, ce qui a permis leur caractérisation :

Tous les produits de désintégration de l'élément 117 étaient inconnus avant cette expérience, de sorte que leurs propriétés ne pouvaient servir à confirmer la validité de cette expérience. Une seconde synthèse fut réalisée en 2012 par la même équipe du JINR, qui obtint cette fois sept noyaux d'élément 117. Les résultats de cette expérience confirmèrent ceux de la première synthèse[3]. Enfin, deux noyaux supplémentaires d'élément 117 furent synthétisés en 2014 au Centre de recherche sur les ions lourds (GSI) à Darmstadt, en Allemagne, par une équipe conjointe du GSI et de l'ORNL à l'aide de la même réaction que celle réalisée au JINR[2] ; l'équipe du GSI avait initialement songé à explorer les réactions alternatives 244Pu (51V, xn) 295-xTs, et, éventuellement, 243Am (50Ti, xn) 293-xTs[28], s'ils ne parvenaient pas à obtenir du 249Bk de l'ORNL.
Stabilité des isotopes
La stabilité des nucléides décroît rapidement au-delà du curium (élément 96) lorsque le numéro atomique augmente. À partir du seaborgium (no 106), tous les isotopes connus ont une période radioactive ne dépassant pas quelques minutes, tandis que celle de l'isotope le plus stable du dubnium (no 105), qui le précède dans le tableau périodique, est de 30 h, et qu'aucun élément chimique de numéro atomique supérieur à 82 (correspondant au plomb) n'a d'isotope stable[29]. Cependant, pour des raisons qui ne sont pas encore bien comprises, la stabilité des noyaux atomiques tend à légèrement croître autour des numéros atomiques 110 à 114, ce qui semble indiquer la présence d'un « îlot de stabilité ». Ce concept, qui a été théorisé par Glenn Seaborg, expliquerait pourquoi les transactinides ont une période radioactive supérieure à celle prédite par le calcul. L'élément 117 possède le second numéro atomique le plus élevé parmi les éléments identifiés — seul l'oganesson est situé après lui dans le tableau périodique — et son isotope 294Ts a une demi-vie d'environ 51 ms, sensiblement supérieure à la valeur théorique qui avait été utilisée dans la publication rendant compte de sa découverte[24]. L'équipe du JINR considère que ces données constituent une preuve expérimentale de l'existence de l'îlot de stabilité[30].

L'isotope 295Ts aurait une période de 18 ± 7 ms. Il pourrait être possible de le produire à l'aide d'une réaction 249Bk (48Ca, 2n) 295Ts semblable à celle ayant déjà permis de produire les isotopes 294Ts et 293Ts. La probabilité de cette réaction serait cependant au plus 17 de celle de produire du 294Ts[31] - [32] - [33]. Une modélisation tenant compte de l'effet tunnel permet de prédire l'existence de plusieurs isotopes de l'élément 117 jusqu'au 303Ts. Selon ces calculs, le plus stable d'entre eux serait le 296Ts, avec une période 40 ms pour la désintégration α[34]. Des calculs par le modèle de la goutte liquide donnent des résultats semblables, suggérant une tendance à l'accroissement de stabilité pour les isotopes plus lourds que le 301Ts, avec une période partielle supérieure à l'âge de l'univers pour le 335Ts si on ignore la désintégration β[35].
Propriétés
Dans la mesure où le caractère métallique s'affirme au détriment du caractère halogène lorsqu'on descend le long de la colonne no 17 du tableau périodique, on s'attend à ce que la tendance se poursuive avec l'élément 117, de sorte qu'il aurait probablement des propriétés de métal pauvre encore plus marquées que celles de l'astate[7]. Le potentiel standard du couple rédox Ts/Ts− vaudrait –0,25 V, de sorte que, à la différence des halogènes, l'élément 117 ne devrait pas être réduit l'état d'oxydation –1 dans les conditions standard[1] - [36].
Par ailleurs, les halogènes forment des molécules diatomiques unies par des liaisons σ, dont le caractère antiliant s'accentue lorsqu'on descend le long du groupe 17. Celle de la molécule de diastate At2, qui n'a jamais été caractérisée expérimentalement, est supposée déjà très antiliante et n'est énergétiquement plus très favorable, de sorte qu'on s'attend à ce que la molécule diatomique Ts2 soit en fait unie essentiellement par une liaison π[1] ; le chlorure TsCl — écriture qui n'a aucun rapport avec le chlorure de tosyle, couramment abrégé TsCl également — aurait quant à lui une liaison simple entièrement π.
Enfin, la théorie VSEPR prédit que tous les trifluorures d'éléments du groupe 17 ont une géométrie moléculaire en T. Cela a été observé pour tous les trifluorures d'halogènes, qui présentent une structure notée AX3E2 dans laquelle l'atome central A est entouré par trois ligands X et deux paires d'électrons E. C'est par exemple le cas du trifluorure de chlore ClF3. On pourrait s'attendre à observer le même phénomène pour l'élément 117, cependant, les effets relativistes sur son cortège électronique, notamment d'interaction spin-orbite, rendent plus probable une géométrie trigonale pour la molécule TsF3, en raison du caractère davantage ionique de la liaison entre le fluor et l'élément 117, qui pourrait s'expliquer par la plus grande différence d'électronégativité entre ces deux éléments[37].
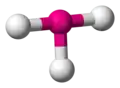 Le trifluorure d'iode IF3 a une géométrie en T.
Le trifluorure d'iode IF3 a une géométrie en T.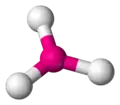 La géométrie du TsF3 serait trigonale.
La géométrie du TsF3 serait trigonale.
Les effets dus aux interactions spin-orbite tendent globalement à croître avec le numéro atomique, dans la mesure où la quantité de mouvement des électrons croît avec lui, ce qui rend les électrons périphériques plus sensibles aux effets relativistes pour les éléments superlourds[39]. Dans le cas de l'élément 117, ceci a pour effet d'abaisser les niveaux d'énergie des sous-couches 7s et 7p, ce qui a pour effet de stabiliser les électrons correspondants, bien que deux des niveaux d'énergie 7p sont davantage stabilisés que les quatre autres[40]. La stabilisation des électrons 7s relève de l'effet de paire inerte ; la séparation de la sous-couches 7p entre électrons stabilisés et électrons moins stabilisés est modélisée comme une séparation du nombre quantique azimutal ℓ de 1 à 12 et 32 respectivement[39]. La configuration électronique de l'élément 117 peut par conséquent être représentée par 7s2
7p2
1⁄2 7p3
3⁄2[1].
Les autres sous-couches sont également affectées par ces effets relativistes. Ainsi, les niveaux d'énergie 6d sont également séparés en quatre niveaux 6d3/2 et six 6d5/2 et remontent à proximité des niveaux 7s[40], bien qu'on n'ait pas calculé de propriétés chimiques particulières liées aux électrons 6d pour l'élément 117. L'écart entre les niveaux 7p1/2 et 7p3/2 est anormalement élevé : 9,8 eV[40] ; il n'est que de 3,8 eV pour la sous-couche 6p de l'astate, pour lequel la chimie des électrons 6p1/2 apparaît déjà comme « limitée »[39]. C'est la raison pour laquelle on s'attend à ce que la chimie de l'élément 117, si elle peut être étudiée, diffère de celle du reste du groupe 17.
Notes et références
Notes
- Ts est également le symbole du groupe tosyle (CH3C6H4SO2) en chimie organique, et de la téraseconde (1012 s) en physique.
Références
- (en) Darleane C. Hoffman, Diana M. Lee et Valeria Pershina, « Transactinide Elements and Future Elements », The Chemistry of the Actinide and Transactinide Elements, , p. 1652-1752 (ISBN 978-94-007-0210-3, DOI 10.1007/978-94-007-0211-0_14, Bibcode 2011tcot.book.1652H, lire en ligne)
- (en) J. Khuyagbaatar, A. Yakushev, Ch. E. Düllmann, D. Ackermann, L.-L. Andersson, M. Asai, M. Block, R. A. Boll, H. Brand, D. M. Cox, M. Dasgupta, X. Derkx, A. Di Nitto, K. Eberhardt, J. Even, M. Evers, C. Fahlander, U. Forsberg, J. M. Gates, N. Gharibyan, P. Golubev, K. E. Gregorich, J. H. Hamilton, W. Hartmann, R.-D. Herzberg, F. P. Heßberger, D. J. Hinde, J. Hoffmann, R. Hollinger, A. Hübner, E. Jäger, B. Kindler, J. V. Kratz, J. Krier, N. Kurz, M. Laatiaoui, S. Lahiri, R. Lang, B. Lommel, M. Maiti, K. Miernik, S. Minami, A. Mistry, C. Mokry, H. Nitsche, J. P. Omtvedt, G. K. Pang, P. Papadakis, D. Renisch, J. Roberto, D. Rudolph, J. Runke, K. P. Rykaczewski, L. G. Sarmiento, M. Schädel, B. Schausten, A. Semchenkov, D. A. Shaughnessy, P. Steinegger, J. Steiner, E. E. Tereshatov, P. Thörle-Pospiech, K. Tinschert, T. Torres De Heidenreich, N. Trautmann, A. Türler, J. Uusitalo, D. E. Ward, M. Wegrzecki, N. Wiehl, S. M. Van Cleve et V. Yakusheva, « 48Ca+249Bk Fusion Reaction Leading to Element Z =117: Long-Lived α-Decaying 270Db and Discovery of 266Lr », Physical Review Letters, vol. 112, no 17, , article no 172501 (PMID 24836239, DOI 10.1103/PhysRevLett.112.172501, Bibcode 2014PhRvL.112q2501K, lire en ligne)
- (en) Yu. Ts. Oganessian, F. Sh. Abdullin, C. Alexander, J. Binder, R. A. Boll, S. N. Dmitriev, J. Ezold, K. Felker, J. M. Gostic, R. K. Grzywacz, J. H. Hamilton, R. A. Henderson, M. G. Itkis, K. Miernik, D. Miller, K. J. Moody, A. N. Polyakov, A. V. Ramayya, J. B. Roberto, M. A. Ryabinin, K. P. Rykaczewski, R. N. Sagaidak, D. A. Shaughnessy, I. V. Shirokovsky, M. V. Shumeiko, M. A. Stoyer, N. J. Stoyer, V. G. Subbotin, A. M. Sukhov, Yu. S. Tsyganov, V. K. Utyonkov, A. A. Voinov et G. K. Vostokin,, « Experimental studies of the 249Bk + 48Ca reaction including decay properties and excitation function for isotopes of element 117, and discovery of the new isotope 277Mt », Physical Review C, vol. 87, no 5, , article no 054621 (DOI 10.1103/PhysRevC.87.054621, Bibcode 2013PhRvC..87e4621O, lire en ligne)
- (en) Danall Bonchev et Verginia Kamenska, « Predicting the properties of the 113-120 transactinide elements », Journal of Physical Chemistry, vol. 85, no 9, , p. 1177-1186 (DOI 10.1021/j150609a021, lire en ligne)
- Base de données Chemical Abstracts interrogée via SciFinder Web le 15 décembre 2009 (résultats de la recherche).
Le CAS publié par ailleurs (notamment webElements) est celui de l'ion. - (en) Bill Cabage, « 'Tennessine' acknowledges state institutions' roles in element's discovery », sur Laboratoire national d'Oak Ridge, (consulté le ).
- (en) « Is Element 117 a Halogen or a Metal? », sur GSI (Centre de recherche sur les ions lourds), GSI Helmholtzzentrum für Schwerionenforschung GmbH (consulté le ).
- « IUPAC - International Union of Pure and Applied Chemistry: Discovery and Assignment of Elements with Atomic Numbers 113, 115, 117 and 118 », sur www.iupac.org (consulté le ).
- « Les nouveaux éléments s'appelleront Nihonium, Moscovium, Tennessine (sic) et Oganesson », sur Libération.fr (consulté le ).
- (en) IUPAC is naming the four new elements nihonium, moscovium, tennessine, and oganesson, sur iupac.org, le .
- (en) « Elements 113, 115, 117, and 118 are now formally named nihonium (Nh), moscovium (Mc), tennessine (Ts), and oganesson (Og) », .
-
(en) Willem H. Koppenol, John Corish, Javier García-Martínez, Juris Meija et Jan Reedijk, « How to name new chemical elements (IUPAC Recommendations 2016) », Pure and Applied Chemistry, vol. 88, no 4, , p. 401-405 (DOI 10.1515/pac-2015-0802, lire en ligne) :
« The names of all new elements should have an ending that reflects and maintains historical and chemical consistency. This would be in general “-ium” for elements belonging to groups 1–16, “-ine” for elements of group 17 and “-on” for elements of group 18 »
. - « Quatre nouveaux éléments du tableau périodique sont sur le point d’être baptisés », sur Le Devoir, (consulté le ).
- « Quatre nouveaux éléments dans le tableau périodique », sur Québec Science, (consulté le ).
- « Science et Avenir » [PDF] (consulté le ).
- « Annexe III – Tableau de la classification périodique des éléments », sur Ministère de l'Éducation, de l'Enseignement supérieur et de la Recherche du gouvernement du Québec, (consulté le ), p. 13.
- Luc Tremblay, « Tableau périodique » [PDF], sur collège Mérici, (consulté le ).
- « Tennesse », sur TERMIUM Plus, (consulté le ).
- Claude Andrieux, Daniel Thévenot, Jean-Pierre Foulon, Collège d’experts de terminologie de la chimie et des matériaux de la Commission d’enrichissement de la langue française, « Le tennesse : nom préconisé en français pour l’élément 117 », Actualité chimique, no 416, 14 mars 2017, Société chimique de France.
- « Vocabulaire de la chimie et des matériaux (2018) », sur Ministère de la Culture (consulté le ).
- « Nouveaux éléments chimiques (liste de termes, expressions et définitions adoptés) », sur Legifrance, (consulté le ).
- (en) Lauren Schenkman, « Finally, Element 117 Is Here! », sur Science, (consulté le ).
- (en) Yu. Ts. Oganessia, J. H. Hamilton et V. K. Utyonkov, « Discovery of the New Element Z=117 and Confirmation of 115 », sur EPJ Web of Conferences, (consulté le ).
- (en) Yu. Ts. Oganessian, F. Sh. Abdullin, P. D. Bailey, D. E. Benker, M. E. Bennett, S. N. Dmitriev, J. G. Ezold, J. H. Hamilton, R. A. Henderson, M. G. Itkis, Yu. V. Lobanov, A. N. Mezentsev, K. J. Moody, S. L. Nelson, A. N. Polyakov, C. E. Porter, A. V. Ramayya, F. D. Riley, J. B. Roberto, M. A. Ryabinin, K. P. Rykaczewski, R. N. Sagaidak, D. A. Shaughnessy, I. V. Shirokovsky, M. A. Stoyer, V. G. Subbotin, R. Sudowe, A. M. Sukhov, Yu. S. Tsyganov, V. K. Utyonkov, A. A. Voinov, G. K. Vostokin et P. A. Wilk, « Synthesis of a New Element with Atomic Number Z=117 », Physical Review Letters, vol. 104, no 14, , article no 142502 (PMID 20481935, DOI 10.1103/PhysRevLett.104.142502, Bibcode 2010PhRvL.104n2502O, lire en ligne).
- (en) Yu. Ts. Oganessian, F. Sh. Abdullin, P. D. Bailey, D. E. Benker, M. E. Bennett, S. N. Dmitriev, J. G. Ezold, J. H. Hamilton, R. A. Henderson, M. G. Itkis, Yu. V. Lobanov, A. N. Mezentsev, K. J. Moody, S. L. Nelson, A. N. Polyakov, C. E. Porter, A. V. Ramayya, F. D. Riley, J. B. Roberto, M. A. Ryabinin, K. P. Rykaczewski, R. N. Sagaidak, D. A. Shaughnessy, I. V. Shirokovsky, M. A. Stoyer, V. G. Subbotin, R. Sudowe, A. M. Sukhov, R. Taylor, Yu. S. Tsyganov, V. K. Utyonkov, A. A. Voinov, G. K. Vostokin et P. A. Wilk, « Eleven new heaviest isotopes of elements », Physical Review C, vol. 83, no 5, (DOI 10.1103/physrevc.83.054315, lire en ligne).
- « Seconde carte postale depuis l'îlot de la stabilité », Courrier CERN, vol. 41, no 5, , p. 26 (lire en ligne).
- (en) « Dubna Gaz-Filled Recoil Separator (DGFRS-I) » (consulté le ).
- (en) Christoph E. Düllmann, « Toward element 117 » [PDF], TASCA 08, 7th Workshop on Recoil Separator for Superheavy Element Chemistry, (consulté le ).
- (en) Pierre de Marcillac, Noël Coron, Gérard Dambier, Jacques Leblanc et Jean-Pierre Moalic, « Experimental detection of alpha-particles from the radioactive decay of natural bismuth », Nature, vol. 422, no 6934, , p. 876-878 (PMID 12712201, DOI 10.1038/nature01541, Bibcode 2003Natur.422..876D, lire en ligne).
- (en) « Element 117 is synthesized », (consulté le ).
- (en) Valeriy Zagrebaev, Alexander Karpov et Walter Greiner, « Future of superheavy element research: Which nuclei could be synthesized within the next few years? », Journal of Physics: Conference Series, vol. 420, no 1, (DOI 10.1088/1742-6596/420/1/012001, Bibcode 2013JPhCS.420a2001Z, arXiv 1207.5700, lire en ligne).
- (en) Feng Zhao-Qing, Jin Gen-Ming, Huang Ming-Hui, Gan Zai-Guo, Wang Nan et Li Jun-Qing, « Possible Way to Synthesize Superheavy Element Z = 117 », Chinese Physics Letters, vol. 24, no 9, (DOI 10.1088/0256-307X/24/9/024, Bibcode 2007ChPhL..24.2551F).
- (en) Zhao-Qing Feng, Gen-Ming Jin, Jun-Qing Li et Werner Scheid, « Production of heavy and superheavy nuclei in massive fusion reactions », Nuclear Physics A, vol. 816, nos 1-4, , p. 33-51 (DOI 10.1016/j.nuclphysa.2008.11.003, Bibcode 2009NuPhA.816...33F, lire en ligne).
- (en) P. Roy Chowdhury, C. Samanta et D. N. Basu, « Search for long lived heaviest nuclei beyond the valley of stability », Physical Review C, vol. 77, no 4, , article no 044603 (DOI 10.1103/PhysRevC.77.044603, Bibcode 2008PhRvC..77d4603C., arXiv 0802.3837, lire en ligne).
- (en) S. B. Duarte, O. A. P. Tavares, M. Gonçalves, O. Rodríguez, F. Guzmán, T. N. Barbosa, F. García et A. Dimarco, « Half-life predictions for decay modes of superheavy nuclei », Journal of Physics G: Nuclear and Particle Physics, vol. 30, no 10, (DOI 10.1088/0954-3899/30/10/014, Bibcode 2004JPhG...30.1487D, lire en ligne).
- (en) Burkhard Fricke, « Superheavy elements: a prediction of their chemical and physical properties », Structure and Bonding, vol. 21, , p. 89-144 (DOI 10.1007/BFb0116498, lire en ligne).
- (en) Cheolbeom Bae, Young-Kyu Han et Yoon Sup Lee, « Spin−Orbit and Relativistic Effects on Structures and Stabilities of Group 17 Fluorides EF3 (E = I, At, and Element 117): Relativity Induced Stability for the D3h Structure of (117)F3 », Journal of Physical Chemistry 1, vol. 107, no 6, , p. 852-858 (DOI 10.1021/jp026531m, lire en ligne).
- (en) Zhiwei Chang, Jiguang Li et Chenzhong Dong, « Ionization Potentials, Electron Affinities, Resonance Excitation Energies, Oscillator Strengths, And Ionic Radii of Element Uus (Z = 117) and Astatine », Journal of Physical Chemistry, vol. 114, no 51, , p. 13388-13394 (PMID 21141866, DOI 10.1021/jp107411s, Bibcode 2010JPCA..11413388C, lire en ligne).
- (en) John S. Thayer, « Relativistic Effects and the Chemistry of the Heavier Main Group Elements », Relativistic Methods for Chemists. Challenges and Advances in Computational Chemistry and Physics, vol. 10, , p. 63-97 (DOI 10.1007/978-1-4020-9975-5_2, lire en ligne).
- (en) Knut Fægri Jr. et Trond Saue, « Diatomic molecules between very heavy elements of group 13 and group 17: A study of relativistic effects on bonding », The Journal of Chemical Physics, vol. 115, no 6, (DOI 10.1063/1.1385366, Bibcode 2001JChPh.115.2456F).
Voir aussi
Articles connexes
Liens externes
- (en) « Technical data for Ununseptium » (consulté le ), avec en sous-pages les données connues pour chaque isotope.
- Communiqué du LLNL américain.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||

