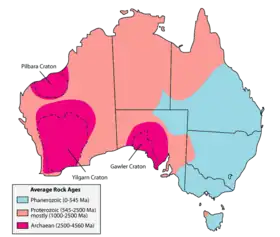
Histoire de la Terre
L'histoire de la Terre couvre approximativement 4,6 milliards d'années, depuis la formation de la Terre à partir de la nébuleuse solaire jusqu'à l'époque actuelle.
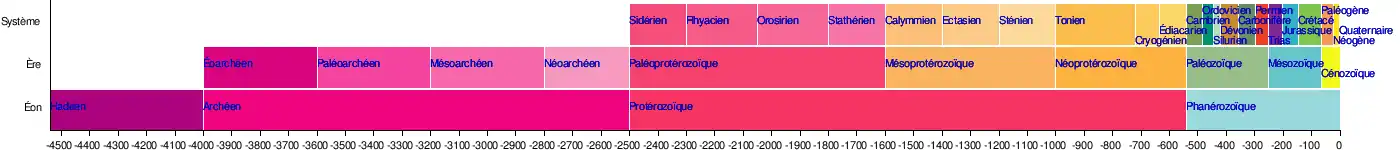
Elle est divisée en quatre périodes chronologiques, les éons, les trois premiers définissant le superéon du Précambrien :
- L'Hadéen dure un demi-milliard d'années. Il n'a guère laissé de roche en place si ce n'est des fragments dans des roches éruptives ultérieures, et est surtout connu à travers la modélisation du système solaire et l'analyse comparative des compositions isotopiques des différents corps célestes ;
- L'Archéen dure un milliard et demi d'années. Il est marqué à la fois par l'apparition des premières croûtes continentales et par l'origine de la vie mettant en place la biosphère. Cet éon est surtout connu par l'analyse des roches qu'il a laissées, de leur âge et des conditions de leur formation ;
- Le Protérozoïque, dure deux milliards d'années. Il est marqué par l'apparition massive de l'oxygène dans l'atmosphère, remplaçant l'atmosphère primitive de gaz carbonique. Comme le précédent, il est surtout connu à travers les roches qui y ont été créées, dans un milieu devenu généralement oxydant ;
- Le Phanérozoïque, littéralement celui des « animaux visibles », organismes multicellulaires, outre les analyses des roches, est connu par les fossiles qu'ont laissés ces organismes animaux et végétaux dans ses différentes strates géologiques. C'est l'âge de la vie, telle qu'on la connaît aujourd'hui, qui n'a commencé qu'il y a 540 millions d'années.
L'histoire de la Terre est également jalonnée de grands épisodes catastrophiques, de basculements chimiques majeurs, comme la Grande Oxydation, ou d'extinctions massives, comme l'extinction Permien-Trias ; séparés inversement par de grandes périodes de stabilité, pendant lesquelles des rétroactions, entre biosphère, atmosphère, hydrosphère et lithosphère, stabilisent les conditions d'existence.


Système solaire

−4,57 Ga : formation du Soleil
L'âge de l'Univers est estimé à 13,799 ± 0,021 milliards d'années[1]. La principale théorie sur la formation de l'Univers est le Big Bang : l'Univers était un point de haute énergie qui est brutalement entré en expansion. En ralentissant et en se refroidissant progressivement, une partie de cette énergie devient de la matière sous forme d'atomes de deutérium, d'hélium 4 et de lithium 7 : c'est la nucléosynthèse primordiale. Des nuages de gaz de dihydrogène se concentrent sous l'impulsion de la gravitation, prenant la forme de galaxies et d'étoiles. Lorsqu'une sphère de gaz atteint une certaine densité, une réaction de fusion nucléaire devient possible, fusionnant quatre atomes d'hydrogène pour former de l'hélium. Lorsque l'étoile devient plus âgée et que la quantité d'hélium produit augmente, la fusion nucléaire produit des atomes plus lourds : carbone, oxygène, etc. Arrivée à un certain âge, une étoile peut s'effondrer sur elle-même puis exploser en une supernova expulsant toute la matière qu'elle a produite depuis son origine.
Cette matière est à l'origine de la nébuleuse solaire, un nuage de gaz (ou disque d'accrétion) à partir duquel le Système solaire s'est formé. Celui-ci est alors un large nuage en rotation, constitué de poussière, de roche et de gaz. La gravité et l'inertie l'aplatissent en un disque protoplanétaire, orienté perpendiculairement par rapport à son axe de rotation, ce qui accélère sa vitesse de rotation. L'essentiel de la masse se concentre alors au centre et commence à s'échauffer, mais de petites perturbations dues aux collisions et au moment cinétique d'autres larges débris créent les conditions pour que des protoplanètes commencent à se former. La chute de matériaux, l'augmentation de la vitesse de rotation et la compression liée à la gravité créent une énorme quantité d'énergie cinétique au centre. L'incapacité à transférer cette énergie suffisamment rapidement à l'extérieur occasionne une montée progressive de la température au centre du disque. Finalement, la fusion nucléaire de l'hydrogène en hélium commence à nouveau et, après contraction, une étoile de type T Tauri devient notre jeune Soleil, il y a 4,57 Ga.
−4,57 à −4,54 Ga : accrétion de la Terre
Pendant ce temps, alors que la gravité pousse la matière à se condenser autour des objets précédemment perturbés, les particules de poussière et le reste du disque protoplanétaire commencent à se séparer en anneaux. Des fragments de plus en plus gros entrent en collision les uns avec les autres et deviennent de plus gros objets, qui deviennent ultimement des protoplanètes. Ceux-ci incluent un groupement situé approximativement à 150 millions de kilomètres du centre : la Terre. C'est ainsi que le système solaire a pu s'établir[2].
La similarité de composition en éléments réfractaires, entre les planètes telluriques, les astéroïdes et le Soleil lui-même est considérée comme une preuve solide de leur origine commune[3]. Par la suite, la Terre perd dans l'espace une grande partie de l'hydrogène et de l'hélium primitifs, qui peuvent dépasser la vitesse de libération du fait de leur agitation thermique. Cependant, il est possible que d'autres éléments volatils puissent être apportés par des épisodes ultérieurs de bombardement météorique[3].
Le Soleil à son début irradie moins qu'à présent. À l'époque de la formation de la Terre, il n'a que 70 % de sa puissance actuelle, et gagne depuis 7 % par milliard d’années[4] - [5].
Au moment de son accrétion, la composante gazeuse de la Terre est largement constituée d'éléments légers, hydrogène et hélium. Le vent solaire de cette nouvelle étoile T Tauri chasse la plus grande partie du gaz et des poussières du disque, qui ne se sont pas déjà condensés en de plus gros corps, d'autant plus facilement que le noyau ne s'étant pas encore différencié, la Terre n'a pas de champ magnétique pour dévier le vent solaire et former la ceinture de Van Allen. Ces éléments légers se trouvent à présent en quantité négligeable dans l'atmosphère terrestre, par comparaison à leur abondance cosmique[6].
Horloge cosmique
Pour aider à appréhender les valeurs relatives d'un million ou d'un milliard d'années, ces durées peuvent être ramenées à un « tour de cadran » de douze heures représentant l'histoire de la Terre, depuis son accrétion à minuit, jusqu'au présent à midi. Dans cette échelle de temps, où les 4,54 milliards d'années sont représentés en douze heures, un million d'années dure un peu moins de dix secondes.
L'Univers s'est ainsi formé un peu plus de 24 heures avant l'accrétion de la Terre. Le Soleil s'est allumé à minuit moins trois. Il met à peu près 230 millions d'années pour faire le tour de notre galaxie, la Voie lactée, ce qui à cette échelle de temps représente à peu près quarante minutes.
L'apparition en Afrique de Homo erectus a lieu dans les dix dernières secondes. Par rapport à l'histoire de la Terre, l'apparition de l'homme est donc à ce jour quantitativement négligeable. L'apparition de la noosphère est en pratique un « présent immédiat ».
Hadéen (de −4,5 à −4 Ga)
Orange : glaciation
Voir aussi : la frise chronologique de l'Univers et Histoire de la Terre
−4,54 Ga : l'origine

L’histoire de la Terre primitive, entre −4,54 et −4 milliards d’années (soit durant le premier éon, l'Hadéen), est très mal connue.
La jeune Terre, durant l'Hadéen, est très différente du monde tel que nous le connaissons aujourd'hui. Elle n'a ni océan, ni oxygène dans son atmosphère. Elle est bombardée par des planétoïdes et des matériaux issus de la formation du système solaire. La Terre se forme pendant plusieurs millions d'années d'impacts et d'accrétion, puis les astéroïdes continuent à entrer en collision avec elle, ce qui a produit un fort échauffement en surface. La Terre est par ailleurs continuellement chauffée par la radioactivité interne.
Ce bombardement, combiné à la chaleur des transformations radioactives, à la chaleur résiduelle et à celle due à la pression de contraction, placent les roches de la planète entière en état de fusion.
Les gaz provenant des roches terrestres en fusion étaient principalement, comme à présent, de l'azote, du dioxyde de carbone, de l'ammoniac, du méthane, de la vapeur d'eau et de plus petites quantités d'autres gaz. Cependant, cette atmosphère anoxique n'a pas de couche d'ozone, et laisse pénétrer le rayonnement ultra-violet qui dissocie les molécules les plus fragiles. Seules s'accumulent en quantité notable les plus robustes : CO2, N2 et H2O.
Le noyau se serait formé en premier, en moins de 15 Ma[7].
Il est essentiellement constitué de fer métallique, mais comporte un peu de nickel et environ 10 % d'éléments plus légers (qui ne sont pas identifiés avec certitude). Les éléments métalliques qui s'y trouvaient (fer et nickel) ont fondu et coulé vers le centre de la planète, ce qui a dégagé encore plus de chaleur, emballant le processus. Le fer liquide contenu dans le noyau crée un véritable champ magnétique autour de celle-ci par un effet dynamo. C'est en fait ce champ qui protège l'atmosphère de la planète du vent solaire.
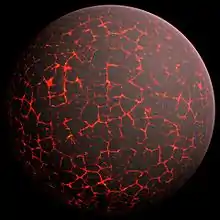
C'est ainsi que le noyau se forme lors des quarante premiers millions d'années de la Terre. Pendant que les éléments les plus lourds s'enfoncent au centre, les plus légers montent à la surface, formant par différenciation les différentes enveloppes de la Terre (voir « structure interne de la Terre ») et produisant ainsi de la chaleur supplémentaire. Cela conduit à l'hypothèse que le modèle de l'océan magmatique lunaire puisse être transposé à la formation initiale de la Terre dont la surface n'est alors qu'un océan de magma généralisé d'environ 2 000 °C[8].
Initialement, la nébuleuse solaire est formée majoritairement d'hydrogène, donc forme un milieu très réducteur. Le carbone tend à se présenter sous forme de méthane (CH4), l'azote sous forme d'ammonium (NH4+), l'oxygène sous forme d'eau (H2O), le soufre sous forme de sulfure d'hydrogène (H2S)...
Mais le fer migrant dans le noyau sous forme réduite, le dégazage des astéroïdes primitifs, qui conduit initialement à une atmosphère fortement réductrice, laisse place à un dégazage plus oxydé, sous forme de dioxyde de carbone CO2 et d'eau. De leur côté, les gaz réduits comme le CH4 ou le monoxyde de carbone CO sont photo-dissociés dans la haute atmosphère et conduisent à la production d'hydrogène, dont la vitesse moyenne, du fait de l'agitation thermique, dépasse la vitesse de libération, si bien qu'il s'échappe dans l'espace[3]. La fuite d'hydrogène gazeux, réduit, sera une cause constante de la montée du degré d'oxydation de la surface terrestre tout au long de son histoire[9]. Avec cette différenciation, une nouvelle atmosphère terrestre est créée à partir du dégazage du magma.
Plusieurs millions d'années plus tard, une collision importante avec une protoplanète appelée Théia ou un astéroïde de la taille d'une planète change la direction de l'axe de la Terre. L'impact mélange, par fusion à haute température, les couches externes des deux planètes, ce qui provoque l'agrandissement de la Terre tandis que le reste des débris forme la Lune. À la suite du chaos des premières années de vie de la planète, les collisions se font plus rares et la Terre peut se refroidir.
−4,5 Ga : formation de la Lune
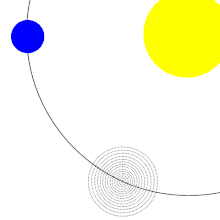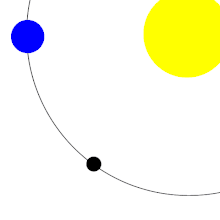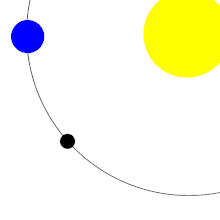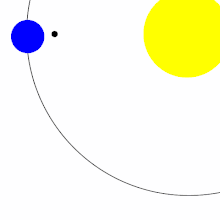


L'origine de la Lune est toujours incertaine, bien que de nombreux indices accréditent la thèse d'une grande collision. La Terre pourrait ne pas avoir été la seule planète à s'être formée à 150 millions de kilomètres du Soleil. Une hypothèse indique qu'un autre amas se serait formé, dessinant un triangle équilatéral avec le Soleil et la Terre, à leur quatrième ou cinquième point de Lagrange. Cette planète, nommée Théia, aurait été plus petite que la Terre, approximativement de la taille et de la masse de Mars. Son orbite, qui aurait pu être stable dans un premier temps, se serait déstabilisée au fur et à mesure que la masse de la Terre augmentait par l'accrétion de matériaux.
Théia oscille par rapport à la Terre jusqu'à approximativement 4,533 milliards d'années[10], date à laquelle elle entre en collision, selon un angle oblique faible. L'angle et la vitesse ne sont pas suffisants pour détruire la Terre, mais une large portion de la croûte est éjectée. La majeure partie des éléments les plus lourds de Théia s'enfoncent au cœur de la Terre, pendant que le reste des matériaux et des éjections se condensent en un seul corps en quelques semaines. Sous l'influence de sa propre gravité, celui-ci devient un corps plus sphérique : la Lune[11].
L'énergie de l'impact vaporise d'importants volumes de roche. Le sommet de cette couche gazeuse incandescente évacue la chaleur dans l'espace, à une température effective de 2 300 K : la Terre est alors une sphère lumineuse orangée rayonnante dont le manteau vaporisé forme une photosphère. Ce refroidissement entraîne des mouvements de convection dans la photosphère et la totalité de la masse du manteau terrestre doit y circuler de manière répétée pour évacuer sa chaleur dans l’espace.

Les composants du manteau se condensent progressivement après refroidissement, retrouvant dans un premier temps une phase liquide. Après un millier d'années, le refroidissement ne laisse dans l'atmosphère que des gaz volatils, quelques centaines de bars de vapeur d'eau et une centaine de bars de CO2[12].
À cette époque, la Lune orbite bien plus rapidement et à une distance 15 fois moindre qu'aujourd'hui[13]. On avance également l'hypothèse que l'impact aurait changé l'axe de la Terre pour produire sa forte inclinaison de l'axe de 23,5°, qui est responsable des saisons sur la Terre — le modèle idéal de l'origine des planètes considère qu'elles auraient des inclinaisons d'axe initiales proches de 0°, donc sans saison reconnaissable. L'impact pourrait aussi avoir accéléré la rotation de la Terre en lui donnant un temps de rotation de 6 h[13] et initié la tectonique des plaques de la planète.
Une conséquence importante de cette collision est que la Terre a capturé le noyau lunaire, la Lune étant beaucoup moins dense que la Terre parce que principalement formée par des roches du manteau. Cet échange a permis à la Terre de disposer d'un noyau plus gros, et donc d'une meilleure protection contre le vent solaire par le champ magnétique terrestre.
−4,5 à −4 Ga : refroidissement



Le flux thermique de l’intérieur de la Terre à ce moment est de 140 W/m2. La surface reste chaude, entre 1 800 et 2 000 K, partiellement fondue avec un peu d’écume solide[12]. La terre cessant d'être incandescente, des nuages d'eau se condensent au sommet de l'atmosphère, limitant ainsi l'évacuation de la chaleur et entraînant un effet de serre, qui ralentit le refroidissement. De plus, la Lune provoque d'importantes marées, dont l'énergie se disperse sous forme de chaleur supplémentaire.
Le CO2 est resté dans l'atmosphère, à une pression de 100 bars, car ce composé est peu soluble dans le magma à cette pression, et les carbonates sont instables à la température de la roche en fusion, de l'ordre de 1 800 K[12].
Une écume de feldspath peut se former et constituer une croûte terrestre primitive de gabbros et d'anorthosites, mais elle doit être constamment recyclée dans la matière fondue[8].
Une croûte terrestre stable semble en place vers 4 400 Ma, comme l'indiquent les cristaux de zircon retrouvés dans l'ouest de l'Australie (datés vers 4 404 ± 8 Ma[14]).
Après 20 millions d'années, la surface de la Terre est suffisamment refroidie et le flux de chaleur a diminué à 0,5 W/m2, soit l'équivalent de la croûte océanique moderne datant d'un million d'années[12].
L'hypothèse d'un océan de magma occupant une fraction non négligeable de la Terre pendant tout l'Hadéen est remise en cause par les études de géochimie (datation par le samarium-néodyme, isotopes de l'hafnium dans les zircons) qui suggèrent qu'une croûte terrestre figée basaltique (constituée de basaltes et de komatiites) ou granitique est bien antérieure aux roches terrestres les plus anciennes (en)[15]. Grâce à l'amélioration de précision du spectromètre de masse, des études de 2005, encore controversées, semblent indiquer que cette croûte primitive se serait formée vers −4,45 Ga et aurait subsisté quelques centaines de millions d'années avant d'être « remélangée » dans le manteau[16].
La Terre s'étant suffisamment refroidie, la croûte terrestre apparaît vraisemblablement il y a 3,8 à 4 Ga, au début de l'Archéen[17], autour de germes à la surface. Des zones entrent à nouveau en fusion à l'occasion de gros impacts, qui interviennent à des intervalles de quelques dizaines ou centaines d'années, et seraient à l'origine de différentiations partielles[18].
−4,2 Ga : formation des océans


La planète continue à se refroidir et les pluies conduisent probablement à la formation des océans il y a 4,2 milliards d'années[19] - [20].
Même si le Soleil ne fonctionne alors qu'à 70 % de sa puissance actuelle, la quantité de CO2 dans l'atmosphère était suffisante pour maintenir une température de surface de l'ordre de 500 K (227 °C) à la surface d’une mer liquide (la pression de vapeur saturante de l'eau est de 26,5 bars à 500 K)[12].
L'eau chargée en CO2 forme de l'acide carbonique, qui attaque les roches volcaniques, et prolonge son action dans les océans également saturés en CO2. L'acide carbonique (CO3H− + H+) est un acide faible, mais au fil des temps géologiques, attaquant le basalte, il ronge le feldspath, par exemple l'anorthite de formule CaSi2Al2O8, les dissociant notamment en ions calcium Ca2+, normalement solubles.
Mais à ce degré de refroidissement, et dans un océan saturé en carbonates et acide carbonique, l'interaction de ce dernier avec le calcium donne du carbonate de calcium (calcaire), pratiquement insoluble[21] :
- Ca2+ + CO3H− ↔ CaCO3 + H+
Les carbonates de calcium et de magnésium sont stables en surface, et peuvent précipiter, en équilibre avec l'érosion des roches basaltiques. Cependant, ils ne sont stables que dans la région la plus froide (500 m) de la croûte océanique[12]. Le volume de carbonates accumulables sur cette épaisseur, sur toute la surface de croûte océanique du globe, correspond à la capture d'une quantité de CO2 permettant de faire baisser sa pression partielle de l'ordre de 50 bars[3].
La capacité de rétention du CO2 par les roches carbonatées est cependant limitée par la masse limitée de CaO et MgO exposée à l'érosion, l'exposition aux intempéries de la surface totale de la croûte océanique ne permettant de faire précipiter que l'équivalent d'une dizaine de bars à la fois[12]. Toute la croûte océanique doit donc passer par de nombreux cycles de subduction avant que les carbonates soient suffisamment transférés dans le manteau terrestre pour faire disparaître la plus grande partie du CO2 atmosphérique, permettre à la surface de refroidir en dessous de 100 °C, et permettre l'apparition de la vie.
Une fois que la majorité du CO2 est éliminé, s'installe un équilibre dynamique entre l'altération des roches en surface et la capture du CO2 sur la croûte océanique pour reformer des carbonates, ce qui entretient une concentration limitée de CO2 dans l’air et dans l’océan[12].
−4,1 Ga : grand bombardement tardif

.jpg.webp)
De -4 à −3,8 Ga, la Terre connaît une période de grand bombardement tardif[22], comme la Lune et les autres corps du Système solaire. Cette phase est probablement due au réarrangement du Système solaire externe.
Ce grand bombardement stérilise périodiquement l'océan par l'énergie qu'il transfère sous forme de chaleur : un astéroïde de ~300 km de diamètre est suffisant pour vaporiser une partie de l'océan et chauffer le reste au-delà de la stérilisation ; un astéroïde de ~450 km de diamètre vaporise l'ensemble des océans ; par la suite, la pluie retombe lentement, de l'ordre d'un mètre par an, et l'océan met quelques milliers d'années pour se reconstituer[12]. Il reste cependant possible que des organismes vivants thermophiles subsistent dans une zone intermédiaire vers mille mètres de profondeur dans la croûte, suffisamment profond pour ne pas être ébouillantés, et suffisamment en surface pour ne pas être cuits par le manteau terrestre[12].
Bien que l'histoire des éléments volatils de la Terre soit dans le détail certainement complexe et en tout cas mal connue, il est assez bien établi qu'une bonne part de la masse apportée par le grand bombardement tardif l'est sous forme d'éléments hydratés et de carbonates réduits, ainsi qu'une fraction significative de métal[3]. L'impact d'astéroïdes métalliques relâche par ailleurs du fer vaporisé ou liquide dans l'atmosphère et l'océan. À haute température, le fer réagit sur l'eau pour s'oxyder, dégageant de l'hydrogène. Cet hydrogène réagit à son tour avec les composants atmosphériques[12], réduisant le CO2 pour former du méthane CH4 et de l'azote N2, qui donnent de l'ammoniac, soluble dans l'océan sous forme d'ammoniaque NH4+. D'une manière générale, le dégazage de cette pluie d'astéroïdes, que ce soit lors de leur impact ou par rejet volcanique ultérieur, conduit à des hétérogénéités dans la croûte terrestre et le manteau terrestre, et produit une atmosphère plus réductrice que précédemment[3].
Cet apport tardif d'éléments réduits en surface a pour conséquence importante de réinjecter de l'azote sous forme de NH4+ directement exploitable par la chimie pré-biotique. D'autre part, les météorites ferreuses sont particulièrement chargées en phosphore, élément indispensable à la vie mais initialement rare sur la croûte terrestre[23] (cet élément sidérophile migre avec le noyau terrestre). De la série d'éléments « CHNOPS » indispensables à la vie et constituant la biosphère, seul le phosphore est un élément naturellement rare.
−4,0 Ga : premières roches datées
Les premières roches se distinguant de la croûte océanique sont des roches magmatiques résultant d'éruptions volcaniques. Les roches les plus anciennes identifiées à ce jour sont datées à −4,03 Ga. Elles marquent la fin de l'Hadéen, éon qui est caractérisé par l'absence de témoins géologiques. Les premières roches sédimentaires sont datées de −3,8 Ga.
Des roches métasédimentaires plus jeunes dans l’ouest de l’Australie (Jack Hills) ont révélé des zircons hadéens datés pour les plus vieux à −4,4 Ga. Le zircon se forme pendant la genèse de roches magmatiques communes, principaux constituants "granitoïdes" de l'écorce terrestre, en particulier les granites et les roches alcalines telles la pegmatite ou la syénite. Il apparaît avec les produits précoces de la cristallisation primaire de ces roches. La présence de ce minéral recyclé dans les roches en question indique qu’il y avait des surfaces soumises à l'érosion dès cette époque ; mais ces surfaces n'ont pas été retrouvées.
Archéen (de −4 à −2,5 Ga)
−3,8 Ga : débuts de la vie microbienne

Au début de l'Archéen, l'activité solaire plus faible était compensée par une atmosphère très chargée en gaz à effet de serre. La température était élevée. L'eau et le gaz carbonique étant transférés dans les océans et les carbonates, l'atmosphère restante devient progressivement constituée majoritairement d'azote. L'effet de serre diminuant avec la perte du CO2, la température de surface baisse progressivement, et atteint des valeurs (70 à 100 °C) où les réactions chimiques des thermophiles deviennent possibles. L'analyse isotopique du silicium montre que la température des océans a décru de 70 °C il y a 3 500 Ma, à 20 °C il y a 800 Ma[24]. Si cette atmosphère s'était maintenue, la Terre ne serait plus habitable aujourd'hui.
La vie microbienne apparaît à cette époque. Qualitativement, un certain milieu disposant d'un gradient chimique a permis la production de composés organiques et de réactions variées. Certaines réactions conduisent à des polymérisations (polynucléotides), et certains composés formés agissent comme catalyseurs à d'autres. Dans un tel système complexe, dès qu'une chaîne de réactions s'auto-catalyse, elle tend à dominer et épuiser les ressources disponibles, et peut alors être à la base de nouvelles complexités.
Dans cette complexification croissante, il n'y a pas de limite franche entre un système autocatalytique et « la vie » ; dans les deux cas la compétition conduit à une sélection naturelle favorisant différentiellement ce qui est le plus efficace en matière de reproduction et d'utilisation efficiente de ressources. Dès que le système devient assez stable et robuste pour assurer une reproduction suffisamment fidèle, dans des conditions environnementales plus variées, il peut être qualifié d'autopoïétique : « la vie » commence et se répand dans tous les environnements connexes, en quelques centaines ou milliers d'années[12].
La voie exacte suivie par les origines de la vie, qui remonteraient à environ 3,5 à 3,8 milliards d'années, demeurent incertaines, et la date d'apparition exacte de la première cellule n'est pas connue par les scientifiques. Mais d'une manière ou d'une autre, la vie a finalement pris la forme d'une « cellule », capable de maintenir l'intégrité d'un « individu » par rapport à l'environnement, capable de maintenir un métabolisme cohérent par des échanges chimiques avec le milieu environnant, et capable de se répliquer en produisant d'autres « individus » identiques.
Ces trois fonctions de base sont essentielles à la vie. La délimitation d'un « individu » par rapport à un environnement « extérieur » renvoie à ce qu'est une membrane plasmique, capable d'assurer une telle séparation. La réplication à l'identique d'un système formel renvoie au codage génétique de l'information nécessaire à cette cellule, probablement d'abord sous forme d'un monde à ARN, puis sous forme stabilisée par l'ADN. Mais c'est le métabolisme de ces cellules qui va s'avérer essentiel pour décrire leur évolution et leur influence sur l'histoire de la terre, à travers l'impact que cette biochimie aura sur l'évolution de la planète.
En dehors de quelques essais de vie en colonie, « la vie » restera unicellulaire pendant tout l'Archéen et le Protérozoïque, pendant lesquels la « soupe primordiale » se transforme simplement en une soupe d'entités répliquantes, progressivement différenciées en virus, archées et bactéries, et enfin eucaryotes. Ce n'est qu'avec l'apparition de ces derniers, trois milliards et demi d'années plus tard, que « la vie » telle que nous la connaissons apparaîtra, inaugurant le Phanérozoïque.
Cycles du carbone et de l'azote
Sur le plan énergétique, la vie est très probablement apparue autour d'un mont hydrothermal diffusant de l'hydrogène réducteur dans un milieu chargé en gaz carbonique[4] - [25] La source d'énergie primaire des cellules primitives aura été la méthanogenèse[9] - [26], réaction d'oxydo-réduction exothermique produisant du méthane à partir d'hydrogène et de gaz carbonique :
- CO2 + 4 H2 → CH4 + 2 H2O + 135 kJ
La fermentation présente l'avantage d'utiliser pratiquement les mêmes processus que ceux du métabolisme méthanogène précédent, et était donc à la portée de ces cellules primitives[25]. Pour la fermentation, le moins efficace des catabolismes, ce sont des composés organiques eux-mêmes qui jouent le rôle d'accepteur d'électron[27]. La fermentation de matière organique notée (CH2O) conduit à rejeter du méthane (et du gaz carbonique) dans une réaction qui peut se décrire schématiquement par[26] :
- 2 (CH2O) → CO2 + CH4
Les cellules primitives consomment du CO2, abondant dans l'environnement de l'époque, mais également de l'hydrogène plus rare, que l'on trouve dans des émissions volcaniques. Cette dépendance à l'hydrogène est un facteur limitant, la production primaire qu'elle permet est nécessairement très limitée[12] - [28]. Le catabolisme des premières cellules ne pouvait pas s'appuyer sur la respiration cellulaire nécessitant de l'oxygène libre alors absent de la planète, ni sur la respiration anaérobie utilisant des composés inorganiques, tels que les ions nitrates (NO3−) ou sulfates (SO42−), moins efficace que la précédente[27].
L'existence d'une voie de catabolisme a pu permettre l'apparition des premières cellules hétérotrophes, dès que l'évolution des cellules leur a permis de capturer et de digérer d'autres cellules sans perdre elles-mêmes leur identité.
Par ailleurs, le début de la vie est également celui du cycle de l'azote.
L'azote est un composant indispensable de la vie, constituant central par exemple des acides aminés. Cependant, l'essentiel de l'azote se présente sous forme de diazote N2, relativement inerte. Dans l'océan primitif, une autre forme stable de l'azote était l'ammonium NH4+[29], apporté par le grand bombardement tardif, ou diffusé autour des dorsales océaniques par des monts hydrothermaux. C'est cette forme qui est pour la biochimie le point d'entrée vers la matière organique. Le besoin en azote fixé est donc initialement passé par un cycle non biologique, dont la biosphère était dépendante[30] - [31], un équilibre se faisant dans l'océan entre l'azote fixé dans la biomasse et celui restitué sous forme de NH4+ par les déchets organiques.
Effet thermostat des méthanogènes
Dans la haute atmosphère, le méthane est dissocié par le rayonnement ultraviolet et l'hydrogène libre s'échappe dans l'espace, contribuant à l'oxydation progressive de la surface de la Terre[9].
Dès que les cellules primitives méthanogènes deviennent suffisamment abondantes pour que leur production puisse excéder la disparition du méthane par photolyse dans la stratosphère, le méthane produit se répand dans l'atmosphère, où il a un effet de serre beaucoup plus efficace que le gaz carbonique. Il devient alors un important contributeur de l'effet de serre[26], et peut, par son accumulation lente, compenser sur le très long terme la baisse du CO2, progressivement transformé en carbonates et immobilisé dans son cycle du carbone au niveau de la lithosphère[21].
Une température trop élevée ou trop faible peut inhiber ce processus de méthanogenèse, qui décroit dès que la température s'éloigne de son optimum. De ce fait, le cycle du méthane a un effet de thermostat maintenant la température effective de la biosphère à un niveau où la production de CH4 compense juste la dissociation de celui-ci par le rayonnement ultra-violet, si bien que son accumulation est auto-régulée. Cette régulation est similaire à celle décrite entre la teneur en CO2 et le climat, mais joue à une échelle de temps beaucoup moins lente[21].
La concentration en méthane est initialement faible. Il apparaît à ce stade une régulation positive entre la disparition géologique du CO2 et l'apparition biologique du CH4, stabilisant dans un premier temps la température à la limite haute de capacité des bactéries méthanogènes : si les températures baissent, la production du CH4 augmente et l'effet de serre avec elle, rétablissant la température haute.
Plus tardivement, la pression atmosphérique en CO2 a pu continuer à baisser jusqu'au point que la fugacité du méthane approche celle du gaz carbonique, ce qui conduit à la formation d'un smog d'hydrocarbones dans l'atmosphère[21] - [26] - [32]. Ce smog a un effet de serre négatif (similaire à celui observable sur Titan), parce que l'énergie solaire est alors absorbée dans la stratosphère et irradie dans l'espace sans atteindre le sol. Dans ce cas, la régulation précédente s'inverse : la température baisse, le CH4 augmente, le smog également, et la température effective de la biosphère chute avec un effet boule de neige. La chute des températures ne dépasse pas cependant la limite basse de capacité des bactéries méthanogènes. En-dessous de cette limite, en effet, la production de CH4 baisse et ne compense plus les pertes, le smog s'éclaircit, et les températures remontent vers leur seconde valeur d'équilibre[21].
Cette seconde régulation ne porte plus directement sur la température, mais sur les conditions de formation du smog. Elle peut donc permettre aux températures de continuer à baisser avec la disparition du gaz carbonique. D'autre part, l'apparition d'une couverture filtrant le rayonnement solaire[26] a pu permettre aux cellules primitives de survivre en surface, ouvrant la voie à la photosynthèse.
−3,7 Ga : apparition de la photosynthèse anoxygénique


La photosynthèse a pu évoluer à partir de réactions photocatalytiques fournissant une voie alternative pour produire les hydrates de carbone (de formule générique CH2O) à partir de sulfures ou d'oxyde de fer.
Avec la fuite constante de l'hydrogène dans l'espace, la surface de la Terre devient progressivement moins réduite, et des substances plus oxydées apparaissent, comme le sulfate ou l'oxyde ferrique. Dans un premier temps, ces substances minérales peuvent être utilisées comme accepteur final d'électron, ouvrant la voie à la respiration anaérobie.
- 2 (CH2O) + SO42− → 2 CO2 + S2− + 2 H2O + énergie
- 2 (CH2O) + 2 Fe2O3 → CO2 + 4 FeO + H2O + énergie
Comme signalé ci-dessus, la fermentation est une voie de catabolisme assez inefficace. L'émergence de voies cataboliques plus efficaces procure donc un avantage sélectif immédiat aux cellules hétérotrophes, ce qui conduit à généraliser le processus.
Les sols schisteux et argileux sont susceptibles de contenir des pyrites (en milieu anoxique), par action de bactéries sur de la matière organique. Le point de départ de cette minéralisation se trouve dans la production d'hydrogène sulfuré par les bactéries protéolytiques qui dégradent les protéines ou par les bactéries sulfato-réductrices qui décomposent les sulfates (produits issus de la décomposition des protéines) en hydrogène sulfuré. D'autres bactéries réduisent les hydroxydes ferriques (hydroxydes issu des roches ou de la matière organique) et libèrent les ions ferreux dans le milieu ambiant. En se combinant avec le fer, l'hydrogène sulfuré conduit à la précipitation de sulfures de fer, précurseurs de la pyrite. Lorsque la pyrite a une origine sédimentaire, elle constitue le minéral authigène caractéristique des environnements marins anoxiques riches en matière organique[33].
La respiration anaérobie est formée d'une chaîne de réactions liées, catalysées par des protéines, permettant d'un côté de consommer de la matière organique pour de l'autre libérer de l'énergie. Inversement, si de l'énergie est fournie à l'autre bout de la chaîne, les équilibres se déplacent dans l'autre sens, vers la synthèse de matière organique. Captant l’énergie du Soleil avec le bon photorécepteur, les bactéries (premières formes de vie) développent un processus nouveau : la photosynthèse, suivant des réactions génériques[12] :
- 2 CO2 + S2− + 2 H2O + hν → 2 (CH2O) + SO42−
- CO2 + 4 FeO + H2O + hν → 2 (CH2O) + 2 Fe2O3
Cette réaction passe par la production d'une coenzyme réductrice, le NADPH, et une coenzyme qui stocke l'énergie chimique, l'ATP. Par ailleurs, les réactions indépendantes de la lumière utilisent le flux de ces deux coenzymes pour absorber et réduire le dioxyde de carbone, utilisant le NADPH comme source d'électron et l'ATP comme source d'énergie.
De même que pour l'origine de la vie, l'invention de la photosynthèse a eu un effet boule de neige. Les premières cellules où ce métabolisme a pu évoluer étaient au départ des cellules méthanogènes, arrivant dans un environnement marin de faible profondeur, suffisamment éclairé pour permettre l'exploitation de ces ions (mais à une profondeur suffisante pour se protéger des rayonnements ultra-violets). Au départ, c'est la faible disponibilité de l'hydrogène H2 qui a mis une pression de sélection en faveur de l'émergence d'un cycle alternatif ; et la disponibilité plus grande du soufre et du fer permettait d'augmenter leur production primaire, constituant un avantage sélectif. La première cellule capable de se dispenser totalement d'hydrogène n'a plus été dépendante de ces sources limitées, et a pu proliférer sur toute la planète[12]. Par rapport aux sources d'énergie précédentes, des estimations quantitatives tendent à montrer que le flux du métabolisme a pu augmenter d'un facteur cent[34].
Cette nouvelle source d'énergie est beaucoup plus disponible que l'hydrogène de la biochimie initiale. Elle reste cependant encore limitée par la disponibilité des accepteurs d'électrons, tels que l'hydrogène sulfuré ou le fer ferrique[28]. L'accès à l'énergie solaire permet néanmoins aux bactéries photosynthétiques de se développer en nombre, au point de laisser des traces significatives et détectables dans la sédimentation :
- les scientifiques pensent avoir retrouvé des micro-organismes fossiles dans les roches d'Isua au Groenland datés de 3,8 milliards d'années. Mais il se pourrait que ce soit des artefacts. L'analyse isotopique des dépôts de fer dans ce même gisement montre une sur-représentation de 56Fe, indice d'une activité photosynthétique[35] ;
- les plus anciens dépôts de fer rubané sont datés de −3,7 Ga. Dans la mesure où ils sont la marque d'un épisode d'oxydation du fer océanique, on peut y voir la signature d'une importante activité de respiration anaérobique, donc de photogénèse[36] ;
- les plus anciens fossiles de cellules connus sont les stromatolithes datés de 3,5 milliards d'années, qui sont formés par des colonies cellulaires en milieu saturé.
Sur ce dernier point, il faut souligner que les stromatolithes sont structurellement formés par des voiles bactériens, mais l'origine de ces voiles peut être variable. De nos jours, ces voiles sont uniquement ceux de cyanobactéries, mais ceci n'implique pas que les stromatolithes fossiles ont de même été créés par ces mêmes cyanobactéries : n'importe quel procaryote susceptible de former une colonie peut tout autant être candidat[37]. Et, en particulier, l'apparition de stromatolithes n'implique donc aucunement une production d'oxygène, dont les effets prouvés sont bien postérieurs. L'apparition de la photosynthèse est distincte de la photosynthèse oxygénique[38].
Si l'azote biodisponible n'était pas nécessairement un facteur limitant des débuts de la vie, il l'est certainement devenu avec l'apparition de la photosynthèse anoxyque[34].
L'accès à l'azote fixé étant un facteur limitant de la biomasse, il a pu exister dès cette époque un avantage sélectif à disposer d'une voie métabolique permettant de fixer l'azote atmosphérique dissout dans la couche océanique superficielle. De fait, la signature de l'enrichissement isotopique de l'azote dans les dépôts de −3,2 à −2,5 Ga tend à montrer qu'une telle voie était déjà en place à cette période[39].
−3,4 Ga (?) : apparition de la photosynthèse oxygénique


Après l'invention de la photosynthèse anoxygénique, les bactéries évoluèrent, et à travers la sélection naturelle, diverses versions de la réaction photosynthétique ont émergé permettant une adaptation optimale à différents milieux colonisés par ces bactéries. Ces versions ont pu être échangées par transfert de gènes horizontaux d'une famille à l'autre, et au hasard de ces croisements, l'ancêtre des cyanobactéries (ou peut-être une bactérie d'une autre famille) a pu hériter de deux jeux de protéines capables de fonctionner en série[40]. Cette mise en série permet d'utiliser l'eau elle-même comme donneur d'électron dans les réactions redox biochimiques :
- 2 H2O → 4 H+ + 4 e− + O2↑
Cette transformation se déroule en deux phases : lors de la première, les réactions dépendantes de la lumière captent l'énergie lumineuse et l'utilisent pour produire une coenzyme réductrice, le NADPH, et une coenzyme qui stocke l'énergie chimique, l'ATP. Ces deux coenzymes vont ensuite alimenter le métabolisme cellulaire, comme précédemment. En notant des « hydrates de carbone » par la formule générique (CH2O), la photosynthèse peut globalement se décrire par :
- CO2 + H2O + énergie lumineuse → (CH2O) + O2↑
L'apparition de la photosynthèse oxygénique modifie radicalement l’économie de la production primaire : pour cette nouvelle source d'énergie, le donneur d'électron qu'est l'eau est à présent inépuisable dans un environnement aquatique[28]. Le point important de ce nouveau cycle est qu'il entraîne la production d'une molécule d'oxygène dans l'environnement.
Diverses études suggèrent que l'apparition de la photosynthèse date de −3,4 Ga[41] - [42] - [43] - [44]. Mais cette date fait l'objet de discussions critiques, la date d'apparition de la photosynthèse oxygénique variant d'un « au plus tôt » associée aux premiers stromatolithes à 3,5, jusqu'à un « au plus tard » marqué par la Grande Oxydation, à −2,4 Ga.
Un indice signalant une production photosynthétique d'oxygène provient de la signature isotopique du carbone dans les dépôts archéens. En effet, la fixation du carbone à travers le cycle de Calvin conduit à une séparation isotopique significative, appauvrissant de plusieurs parties pour mille le 13C par rapport au 12C. L'appauvrissement en masse de la biosphère en 13C conduit symétriquement à un enrichissement de l'hydrosphère et de l'atmosphère, dont le niveau est enregistré lors de la précipitation des carbonates marins[9].
−3,26 Ga : cratère d'impact de Barberton
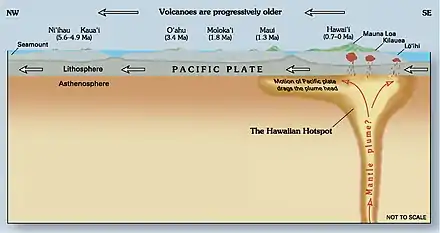
La tectonique des plaques est majoritairement propulsée par l'enfoncement gravitaire de la lithosphère dans des zones de subduction : la croûte océanique de plus de 30 Ma est plus dense (de ~1%) que l'asthénosphère, et y sombre en s'enfonçant dès que possible. Mais cette inversion de densité actuelle n'était pas aussi marquée pendant l'Archéen, parce que la température plus élevée du manteau devait entraîner une lithosphère plus fine[45]. En outre, pour démarrer et entretenir un tel mouvement, il ne suffit pas de l'amorcer par une simple fosse de subduction ; il faut que se mette en place tout un système de dorsales et de failles transformantes, qui une fois en place peut se poursuivre dynamiquement[45]. De plus, pour qu'une subduction s'initie suivant ce modèle, il faut que le mouvement soit tiré par la plaque qui s'enfonce, et donc que la subduction ait déjà commencé[46]
Avant le démarrage de la tectonique des plaques, pendant la plus grande partie de l'Archéen, la surface de la Terre était probablement dans le même état que celle des autres planètes ou planétoïdes telluriques : sous l'hydrosphère océanique, une lithosphère basaltique forme un « couvercle » relativement continu sur l'asthénosphère. Des panaches peuvent occasionnellement percer cette croûte océanique et provoquer un volcanisme en surface, la surcharge étant susceptible de créer un système de fractures[46]. Des morceaux de croûte peuvent s'enfoncer localement et dans l'asthénosphère, puis éventuellement être recyclés ultérieurement par le volcanisme[45]. L'évolution naturelle de ce type de croûte est qu'elle épaissit en bloc avec le refroidissement de la planète[45].
Les premiers éléments de croûte continentale peuvent avoir été formés à partir de grands plateaux basaltiques et leur érosion ultérieure[47]. On ne connaît cependant pas de dépôt sédimentaire carbonaté datant de l'éon Hadéen.
En , les scientifiques ont déclaré avoir trouvé des preuves du plus grand événement d'impact de météore terrestre à ce jour près de la ceinture de roches vertes de Barberton. Ils ont estimé que l'impact a eu lieu il y a environ 3,26 milliards années et que l'impacteur avait un diamètre d'environ 37 à 58 kilomètres, cinq fois plus que l'impact du cratère de Chicxulub dans la péninsule du Yucatan. L'impacteur a heurté la Terre en libérant une quantité énorme d'énergie, déclenchant l'équivalent de tremblements de terre de magnitude 10,8, et de Mégatsunami de milliers de mètres de haut. Le cratère de cet événement (en), s'il existe encore, n'a pas encore été trouvé.
La modélisation montre qu'une tectonique des plaques peut être initialisée par l'impact d'un astéroïde de l'ordre de 500 km de diamètre[45], voire à partir de 100 km[46]. Mais l'impact de Barberton n'est pas de cette classe, même s'il peut avoir été une partie de l'histoire. Il est également possible qu'un panache suffisamment actif puisse créer une province magmatique majeure de plus de 1 000 km de diamètre, dont l'effondrement à la suite de l'inversion de densité est susceptible d'initialiser un mouvement de plaque[45]. Mais même dans ce cas, il n'est pas sûr que ce mouvement perdure jusqu'à présent : une tectonique de plaques a pu être initiée à plusieurs reprises sur la Terre, séparées par des épisodes de couvercle continu[45], conduisant à des traces géologiques alternant présence et absence de subduction[46].
Lente agonie du Protérozoïque

Le dégazement d'oxygène était alors un déchet du cycle, poison pour les organismes anaérobies. Mais la production d'O2 dans l'océan ne signifie pas que sa teneur augmente, car l'oxygène est un corps très réactif ; dans l'environnement réducteur où il est émis, de nombreux « puits » sont capables de le faire réagir et disparaître : en solution, l'ammoniaque, le fer, les sulfures. Pendant plus d'un milliard d'années, l'oxygène dégagé par ces activités photosynthétiques est consommé par des « puits à oxygène », essentiellement l'oxydation des substances réductrices contenues dans les eaux marines (fer et autres métaux, matière organique) et à la surface des terres émergées, et celle du méthane atmosphérique[48].
Il peut sembler paradoxal que l'apparition de l'oxygène dans l'atmosphère, la Grande Oxydation, que l'on date à −2,4 milliards d'années, ne soit survenue que près d'un milliard d'années après l'apparition de la photosynthèse oxygénique[26]. C'est qu'en réalité, l'oxygène est un oxydant redoutable pour l'écologie du Protérozoïque, qui a entraîné une série de catastrophes réduisant presque à néant la biosphère telle qu'elle existait à cette époque :
- celle-ci a été d'abord réduite à famine, par la suppression de l'azote fixé sous forme d'ammoniaque, point d'entrée du cycle de l'azote biologique ;
- quand cet obstacle a pu être levé par la fixation biologique de l'azote, la production a sévèrement réduit la biodisponibilité du fer, indispensable aux enzymes fixant l'azote ou à la photosynthèse, réduisant une fois encore la biomasse ;
- la biosphère a ensuite été massivement intoxiquée, l'oxygène dissout étant un poison pour le métabolisme méthanogène de cette époque, en particulier le fonctionnement de la nitrogénase précédemment mise au point ;
- quand après un milliard d'années de survivance à cette intoxication chronique, ces deux obstacles ont été surmontés, avec la photosynthèse doublée de la respiration aérobie, la biosphère a pu se développer à un point permettant la Grande Oxydation — supprimant l'effet de serre protecteur, et déclenchant une troisième catastrophe sous la forme de la Grande Glaciation, pendant laquelle l'activité biologique a été pratiquement annihilée.
Il faut pour commencer que la production d'oxygène soit plus importante que la production d'éléments réduits par les dorsales océaniques. Au-delà, le carbone réduit que constitue la matière organique est lui-même un « puits ». Que ce soit par respiration aérobie ou par oxydation de matière morte, la réoxydation de matière organique inverse le processus de photosynthèse, consommant l'oxygène pour transformer le carbone réduit en gaz carbonique. Il ne peut y avoir une accumulation significative d'oxygène dans l'atmosphère que si une quantité équivalente de carbone est enfouie pour être soustraite à l'oxydation[38].
−3 Ga : premiers continents

On estime que 80 % de la croûte continentale terrestre s'est formée entre −3,2 et −2,5 Ga[49]. Elle est alors marquée par un changement de régime, passant d'intrusions formées de granitoïdes sodiques à des granites potassiques[50] - [51] - [52].
Cette coïncidence entre les changements observés dans la composition et l'épaisseur de la croûte terrestre et l'oxydation progressive de la surface terrestre due à l'invention de la photosynthèse (anoxygénique puis oxygénique) suggère qu'il y a eu un lien entre les processus géochimiques et la production biologique[53], mais la nature de ce lien reste obscure.
C'est le début de l'importance de la tectonique des plaques. Avec la formation de croûte continentale, les carbonates peuvent y être accumulés dans la lithosphère, qui sert alors de puits dans le cycle du carbone. La croissance continue de la croûte continentale expose de plus en plus de surface à l'érosion de l'acide carbonique, accélérant progressivement la capture du CO2 atmosphérique[26].
Sur le fond des océans, la circulation hydrothermale autour des dorsales océaniques fournit un mécanisme régulateur pour la concentration en CO2 et l'acidité de l'océan. L'eau des océans, plus ou moins chargée de CO2, attaque le basalte et se charge en cations, puis précipite sous forme de carbonates en formant un mont hydrothermal à son retour dans l'océan[54] - [55].
La subduction conduit à la formation d'arcs volcaniques, qui s'accrètent en début de croûte continentale. Les carbonates entraînés par la subduction se décomposent en profondeur, et le volcanisme de l'arc relargue en partie le carbone sous forme de CO2.
Dans le cas de plaques portant beaucoup de sédiments, les arcs insulaires peuvent être doubles :
- un premier arc non-volcanique formé par un prisme d'accrétion sédimentaire proche de la fosse océanique comme la Barbade aux Antilles ou bien les îles Mentawai en Indonésie ;
- un deuxième arc volcanique plus éloigné de la fosse.
Les premiers « continents » sont datés de cette époque. Ils sont hypothétiques, et prennent la forme de « super-cratons » de taille comparable à l'Australie :
−2,9 Ga : crise de l'azote, glaciation de Pongola et nitrogénase
L'oxygène produit réagit immédiatement avec ces composés réducteurs, ce qui capture l'oxygène et limite les possibilités de vie à la prolifération des seuls organismes anaérobies.
Le premier affecté est le cycle de l'azote. Dans l'océan primitif, l'ammoniaque est stable et sert de source d'azote à la biosphère. Tant que le milieu océanique est un milieu réducteur riche en ammoniaque, l'oxygène ne peut pas s'échapper dans l'atmosphère, mais oxyde cet ammoniaque, restituant l'azote sous forme de diazote. La réaction est globalement :
Cet ammoniaque est un puits consommant l'oxygène dissout dans l'océan primitif[29] - [56], mais inversement, cette neutralisation est un puits pour l'azote disponible, parce qu'elle transfère progressivement l'azote, accumulé dans l'océan sous forme d'ammoniaque, vers sa forme inerte de diazote qui s'accumule dans l'atmosphère. La production d'oxygène a donc conduit à une pénurie d'azote biologiquement assimilable.
L'équilibre dans l'océan, entre l'azote fixé dans la biomasse et celui restitué sous forme de NH4+ par les déchets organiques, se déplace alors vers moins d'azote disponible, et donc moins de biomasse. Cette asphyxie progressive déclenche une crise écologique majeure. En l'absence d’ammoniaque dissout, la biomasse n'est alors plus équilibrée que par le flux de NH3 issu des dorsales océaniques (et la production résultant d'une fixation primitive par la biomasse). Inversement, cette réduction de la biomasse limite par conséquent directement le flux d'oxygène, faute de biomasse pour le produire. Il s'établit à ce stade une rétroaction entre le cycle de l'oxygène et le cycle de l'azote, la production d'oxygène s'équilibrant finalement avec celle nécessaire pour consommer celle de l'azote produit, faisant disparaître l'oxygène produit.
La limitation est d'autant plus sévère que le flux des dorsales est en priorité consommé sur place par les organismes métabolisant l'hydrogène, alors que la production d'oxygène se déroule en surface, où la concentration en NH3 est réduite. La biosphère perd de ce fait une partie substantielle de sa capacité à produire du méthane. Il se peut que cette crise ait été à l'origine de la glaciation de Pongola : l'insuffisance de la production de méthane ne lui permet plus de jouer son rôle de « thermostat » ; elle entraîne une diminution de l'effet de serre et une chute des températures moyennes du globe.
L'environnement océanique archéen a donc dû exercer une très forte pression de sélection sur les organismes photosynthétiques par rapport à la dépendance à l'ammoniaque. De ce fait, la capacité à catalyser la réduction du N2 en NH3 a constitué un avantage adaptatif, poussant vers l'émergence d'une nitrogénase de plus en plus performante, et l'avantage sélectif apporté par un métabolisme autotrophe capable de transformer l'azote N2 en ammoniaque assimilable, réalisant la fixation biologique du diazote, a été dans un premier temps immédiat, puisqu'un tel organisme a pu s'étendre sans être lié à une source ammoniaquée[29].
L'analyse des sédiments et de leur enrichissement en azote 15N, par rapport à sa version courante 14N, suggère qu'un cycle métabolique de fixation de l'azote était à l’œuvre entre 3,2 et 2,5 Ga[39].
Avec l'apparition des bactéries fixatrices d'azote, un équilibre s'établit dans les océans entre les concentrations en azote et phosphate assimilable, le ratio [ NO2- ]:[ PO43- ] s'établissant sensiblement à 15 : 1, soit sensiblement la stœchiométrie correspondant à des particules de matière organique en décomposition dans la colonne d'eau[57] (voir Rapport de Redfield). Cette stabilisation provient de la compétition entre les bactéries fixatrices d'azote et les autres formes de la biosphère, et découle du coût métabolique élevé de cette fixation : lorsque l'azote disponible augmente, les bactéries fixatrices d'azote sont handicapées par leur coût métabolique élevé, ce qui fait chuter leur biomasse et de là la fixation d'azote ; inversement, lorsque l'azote est moins disponible que le phosphate, les bactéries fixatrices d'azote peuvent utiliser le phosphate plus efficacement, ce qui augmente leur biomasse et fait remonter la fixation d'azote, puis la disponibilité de l'azote dans les particules en décomposition[57]. Globalement, l'équilibre s'établit autour de la stœchiométrie de la matière organique, avec un léger déficit relatif en NO3- compensant le handicap métabolique des bactéries fixatrices d'azote[57].
Protérozoïque (de −2,5 à −0,54 Ga)
−2,5 Ga : précipitation du fer

L'apparition de la nitrogénase a permis la fixation biologique de l'azote et la production d'oxygène à des niveaux plus importants.
Cependant, une production nette d'oxygène n'est possible que si de la matière organique est capturée dans la lithosphère. En effet, en présence d'oxygène, la matière organique (génériquement notée C(H2O)) est elle-même un puits à oxygène lorsqu'elle s'oxyde en libérant du gaz carbonique[32] :
- C(H2O) + O2 → CO2 ↑ + H2O
Un autre puits à oxygène est la consommation de la pyrite FeS2, formée par la réaction globale[58] :
- 2 Fe2O3 + 8 SO42− + 16 H+ ↔ 15 O2 + 4 FeS2 + 8 H2O
Cette réaction globale est la superposition de trois processus, qui sont la photosynthèse anoxygénique produisant de la matière organique, la réduction anoxique de sulfates en H2S en utilisant cette matière organique comme agent réducteur, et la précipitation de pyrite par réaction de H2S sur Fe2O3.
Dans un deuxième temps, l'oxygène réagit principalement avec les métaux comme le fer ferreux, pour précipiter en hématite et magnétite. La production anaérobie produit de l'oxygène, et cette production détruit la production anaérobie. S'ensuit un cycle d'instabilité : la mort des organismes anaérobies consomme et fixe de l'O2 et en réduit la teneur, rendant les bassins et plateaux continentaux anoxiques et désertifiés. Pendant un événement anoxique océanique, les organismes morts sont enfouis, et le carbone correspondant est transféré vers la lithosphère, avec les oligo-éléments associés. Mais l'érosion apportant de nouveaux oligo-éléments, la disparition du poison permet aux organismes anaérobiques de proliférer à nouveau, déclenchant les conditions de leur nouvelle disparition. Cette instabilité se traduit dans les dépôts par des dépôts de fer rubané, alternativement noirs et rouges. L'oxygène produit a ainsi largement été absorbé par des minéraux et séquestré dans le sol. Ces précipitations, qui reflètent ici des bouffées de production d'oxygène, alternent avec des dépôts de schiste argileux et de carbonates siliceux déposés dans des conditions plus anoxiques, qui sont eux de couleur rougeâtre. C'est l'origine des grands gisements de fer rubanés.
De ce fait, l'oxygène libre n'existait pas dans l'atmosphère jusqu'à il y a environ 2 400 Ma, lorsque, au Paléoprotérozoïque, la plus grande partie de ces formes réduites du fer furent oxydées.
Crise du fer et Grande Oxydation
Le fer biologiquement fixé est un composant essentiel pour la photosynthèse : le photosystème I contient douze atomes de fer. En outre, c'est un composant indispensable à la formation de la nitrogénase, donc à la fixation biologique de l'azote[59]. Mais ce fer n'est disponible biologiquement que lorsqu'il est en solution.
Avec la précipitation des composés ferreux, la disponibilité du fer est devenue un facteur limitant de la biosphère[59].
L'équilibre chimique de la dissolution du fer se déplaçait à la suite de la réduction de la concentration en fer et l'augmentation concomitante de la concentration de O2 dans l'océan, par suite de la photosynthèse, en a progressivement fait un milieu oxydant, alors qu'il était initialement réducteur.
Lorsque, au Paléoprotérozoïque, la plus grande partie des formes réduites du fer ont été oxydées, la sédimentation de gisements de fer rubané s'est raréfiée et la teneur en O2 a alors augmenté dans les océans d'abord, dans l'atmosphère ensuite, pour se révéler hautement toxique pour les organismes anaérobies, au cours de la Grande Oxydation. L'oxygène était en effet toxique pour les organismes anaérobies de l'époque, la biomasse était empoisonnée par ses propres déchets et s'est effondrée une fois encore. En s'accumulant, l'oxygène a fait péricliter les archées méthanogènes pour qui il était un poison[21], mettant pratiquement à l’arrêt la production de méthane.
La transition n'a pris fin qu'à l'apparition de cellules capables de vivre dans un environnement oxygéné. Sont alors apparus, sur le plan géologique, des dépôts rouges, marquage de fer ferrique, et les roches sédimentaires sont passées d'une dominante noire au rouge.
Respiration aérobie
Par ailleurs, l’oxygène est une source d’énergie extrêmement efficace, bien plus que la fermentation, qui ouvre la voie à de nouveaux développements. Le vivant se complexifie. Certaines bactéries apprennent à utiliser l’oxygène : c’est l’apparition de la respiration.
Les cyanobactéries elles-mêmes se sont adaptées à un environnement contenant cet oxygène qu'elles produisent. L'oxygène étant particulièrement réactif, il permet un catabolisme beaucoup plus efficace qu'avec la respiration anaérobique.
Il semble que la capacité d'utiliser l'oxygène dans la respiration aérobie, qui implique une enzyme oxygène-réductase, a pu faire l'objet de transferts de gènes horizontaux d'un groupe à l'autre de bactéries. Le transfert horizontal de gènes semble également répandu parmi les archées[60].
Du fait d'un transfert horizontal de gènes toujours possible, il faut rester prudent devant les analyses de dérive génétique ou de classification phylogénique plaçant l'apparition de telle capacité dans tel groupe ou à telle date.
Bien que tous les métabolismes font usage d'oxygène d'une manière ou d'une autre, certains de ses composés apparaissant dans des cycles métaboliques peuvent être toxiques. Le Dioxygène O2 est paramagnétique et présente deux électrons de spin parallèle. Dans la respiration aérobie, ceci rend délicates les réactions avec l'O2, parce que le donneur d'électron doit pouvoir inverser le spin avant de pouvoir donner un électron. Pour contourner le problème, l'oxygène est combiné à un métal paramagnétique (par exemple du cuivre ou de fer), ou reçoit des électrons supplémentaires. De ce fait, la réduction de O2 en H2O passe par des superoxydes comme ⋅O2−, le peroxyde d'hydrogène H2O2, ou le radical hydroxyle ⋅OH. Ces radicaux libres constituent une menace potentielle pour l'équilibre cellulaire[61]
Multicellularité des cyanobactéries

L'analyse des dérives génétiques des cyanobactéries montre que la multicellularité y a évolué peu avant la grande oxydation[62] - [63].
Initialement, le fait pour des cellules de rester collées ensemble constitue un désavantage, parce que le voisinage d'une autre cellule est nécessairement moins chargé en nutriments et plus chargé en déchets qu'une zone moins peuplée. Mais ce désavantage nutritif est largement compensé en présence de prédateurs capables de capturer et digérer des bactéries libres par phagocytose. Dans ce contexte, la multicellularité constitue un avantage sélectif, parce que le groupe multicellulaire devient trop gros pour être capturé.
Cette production d’oxygène va avoir un impact décisif sur l’évolution de la planète.
L’oxygène des bactéries est produit en si grande quantité que les océans en sont saturés. L’oxygène s’échappe dans l’atmosphère, devenant un de ses composants. C'est ce que l'on appelle la Grande Oxydation.
−2,4 Ga : Grande Oxydation


La production de dioxygène atmosphérique a commencé avec l'apparition de la photosynthèse chez les cyanobactéries, dès −3,5 Ga. Mais des mécanismes divers d'oxydation conduisaient à capturer l'O2 sans qu'il ne puisse réellement s'accumuler dans la couche supérieure de l'océan, ni dans l'atmosphère. L'oxygène a d'abord été consommé par ses réactions sur les éléments réducteurs de l'océan : oxydation du NH4+ puis du Fe2+, limitant ses rejets dans l'atmosphère. Tant que le niveau d'oxygène sortant des eaux de surface reste faible, il est consommé par le méthane présent dans l'atmosphère, dont le niveau est régulé principalement par l'équilibre qu'il créé entre l'effet de serre et la production des bactéries méthanogènes.

Mais à partir du moment où l'océan réducteur a été suffisamment oxydé, le flux d'oxygène vers l'atmosphère a fortement augmenté.
À partir du moment où le flux de sortie devient plus important que celui de la capture de l'O2 par le CH4, la concentration d'O2 devient significative dans l'atmosphère, et il peut commencer à former une couche d'ozone. La formation de cette couche a un effet boule de neige, parce que le blocage du rayonnement ultraviolet par la haute atmosphère diminue la dissociation du méthane présent, et donc inhibe la capture de celui-ci par l'oxygène, qui peut alors renforcer encore plus la couche d'ozone[64].
L'existence de cette oxygénation se lit dans la séparation isotopique des sulfures, qui permet de montrer que jusqu'à −2,45 Ga le niveau d'oxygène étant au plus un cent-millième du présent, alors qu'il monte à 1 à 10 % du niveau présent à partir de −2,33 Ga[64]. On voit de même décliner à cette époque dans les sables sédimentaires les dépôts de minéraux sensibles à l'oxygène comme l'uranite, la pyrite ou la sidérite[37].
Avec la montée de la teneur en oxygène, le méthane reste initialement présent, continuant à jouer son rôle dans l'effet de serre, mais l'oxygène produit s'accumule également dans la couche supérieure de l'océan. Il en résultera, à −2,4 Ga, une crise écologique appelée la « Grande oxydation ». Le modèle océanique de Canfield considère cependant que l'eau des grands fonds marins est demeurée anoxique longtemps après la Grande Oxygénation.
Dans un premier temps, il oxyde les substances réduites pouvant être présentes dans l'atmosphère, les eaux de surface ou les sols altérés[65]. L'oxygène a réagi avec les grandes surfaces oxydables présentes à la surface de la Terre (principalement, le fer).
Le niveau d'oxygène semble avoir initialement atteint des teneurs élevées lors de l'« évènement Lomagundi », qui enregistre un excès de 13C dans des dépôts âgés de 2,2 à 2,3 Ga[28]. L'origine en est peut-être que l'oxygène émis par les cyanobactéries permettait d'oxyder plus complètement des dépôts de matière organique, libérant ainsi l'azote fixé contenu. Cet apport d'azote a pu conduire en retour à une prolifération supplémentaire de cyanobactéries, faisant boule de neige[28]. Ce n'est qu'après avoir épuisé ces ressources fossiles que l'azote est redevenu un facteur limitant, et que la biomasse de cyanobactéries a été lentement réduite, sous l'effet de la dénitrification progressive en milieu anaérobie, et de l'oxydation directe de l'ammoniaque par l'oxygène. Avec cet étouffement des cyanobactéries, l'oxygène n'a plus été produit en quantités significatives, et s'est alors lentement éliminé avec l'oxydation de la surface terrestre et des gaz volcaniques, jusqu'à un niveau permettant le rétablissement du fonctionnement de la nitrogénase, redonnant à la nitrogénase son avantage sélectif.
L'oxygène reste alors à un niveau limité, de l'ordre de 2 à 10 % de la concentration actuelle[66]. La nitrogénase, qui catalyse la séquence complète des réactions au cours desquelles la réduction de diazote N2 conduit à la formation d'ammoniac NH3, est une protéine fer-soufre qui est irréversiblement oxydée et inactivée par le dioxygène (O2)[66] - [56] - [28] De ce fait, le débit d'oxygène généré par la photosynthèse est limité par la capacité des sols à s'oxyder : si la biosphère produit trop d'oxygène, celui-ci détruit trop rapidement la nitrogénase, réduisant la biodisponibilité de l'azote et par là, réduisant l'expansion de la biosphère elle-même.
−2,4 à −2,1 Ga : grande glaciation


Le méthane disparaît progressivement de l'atmosphère, le potentiel réducteur de l'hydrogène le faisant réagir avec l'oxygène nouvellement formé pour former du gaz carbonique et de l'eau. Mais le méthane est un gaz à effet de serre beaucoup plus puissant que le gaz carbonique[26]. Cette substitution entraîne une forte diminution de la température du globe, aggravée par le fait que le Soleil, toujours dans sa première jeunesse, n'émet encore que 85% de sa puissance actuelle[4]. S'ensuit un épisode de glaciation globale, la glaciation huronienne. Le pouvoir réfléchissant de la terre, actuellement d’une valeur de 0,3 passe à des valeurs bien plus élevées, de 0,6 à 0,8, quand la planète prend la forme d'une « terre boule de neige ». Cette montée de l'albédo avec l'apparition des premières calottes glaciaires renforce encore la glaciation, qui finit par s'étendre durablement sur toute la planète[21].
Sous l'effet de la glaciation globale, l'altération des roches par l'acide carbonique ne peut plus avoir lieu, et le cycle du carbone chimique se fige, cessant de consommer le gaz carbonique de l'atmosphère.
Les indicateurs montrent que la biosphère a été pratiquement réduite à néant pendant cette période. L'analyse isotopique du fractionnement entre C12 et C13 reflète l'activité de la biosphère, parce que les vitesses de réaction du métabolisme cellulaire sont légèrement différentes suivant l'isotope concerné, entraînant un fractionnement du carbone à l'entrée dans la biosphère. Or, pour ces périodes, on n'observe plus ce fractionnement, le taux de C13 reste identique à celui de la source volcanique, ce qui montre pour cette époque une quasi-disparition de la biosphère[21]. On observe le même phénomène de fractionnement de soufre dans les dépôts de sulfures[67].
Le méthane n'est plus produit par la biosphère, et le méthane résiduel de l'atmosphère continue à s'échapper, accentuant la glaciation.
Cependant, en amont, le gaz carbonique continue à être produit en faibles quantités par le volcanisme, et s'accumule très progressivement dans l'atmosphère. Après 300 millions d'années, au Rhyacien, l'effet de serre devient suffisant pour déclencher un réchauffement faisant fondre la glace. La perte d'albédo qui en résulte accélère le processus, et la Terre passe assez brutalement d'une glaciation complète à un climat tropical généralisé[4] à l'Orosirien.
Thermostat continental

Au sortir de cette grande glaciation, le retrait des glaciers laisse exposés des continents dénudés et déclenche une érosion massive, qui dissout les silicates, absorbe le CO2 en excès, et le fait précipiter dans les océans sous forme de silicates. Cette élimination du CO2 atténue le fort effet de serre qui avait permis de sortir de la glaciation, et permet le retour à des températures plus modérées.
D'une manière générale, sur le long terme, la teneur de l'atmosphère en CO2, et de là la température et le pH de l'océan, sont contrôlés par le cycle du carbone minéral, par un « thermostat » qui prendra de plus en plus d'importance avec la croissance des continents. La teneur de l'atmosphère en gaz carbonique va être régulée par la capacité des surfaces continentales à consommer ce CO2, la teneur d'équilibre étant d'autant plus faible que la surface de croûte continentale exposée est grande.
- Si la teneur en CO2 augmente au-delà de sa valeur d'équilibre, l'effet de serre augmente, faisant monter la température moyenne du globe.
- Sur la croûte continentale, les températures atmosphériques élevées entraînent une érosion accélérée des silicates, entraînant la capture du CO2 en excès[32] - [54].
- D'autre part, dans l'océan, un réchauffement de la planète conduit à des mers chaudes, où les carbonates précipitent, accélérant le cycle du carbone chimique[21].
Cette régulation est plus aléatoire que celle résultant de l'émission de méthane, parce que l'équilibre découlant du total des surfaces continentales dépend de la disposition géographique effective des différents cratons de croûte continentale :
- Lorsque les cratons forment un supercontinent unique, l'érosion effective ne porte que sur la marge de celui-ci, et non sur le centre généralement désertique. Les surfaces ainsi neutralisées ne peuvent pas participer à l'érosion, conduisant généralement à une hausse des températures par rapport à l'équilibre théorique.
- Lorsqu'une partie de la croûte continentale est couverte par des inlandsis sous l'effet de glaciation ou de latitude polaire, son oxydation est de facto neutralisée, diminuant localement l'effet de l'érosion. Cependant, la formation d'un inlandsis fait baisser le niveau de l'océan, découvrant par ailleurs plus de surface offertes à l'érosion, s'il reste des éléments de croûte continentale à des latitudes clémentes. L'effet peut être positif ou négatif suivant la géographie effective du moment.
- Lorsqu'un supercontinent se désagrège, les surfaces précédemment désertiques contribuent à nouveau à la régulation, ce qui conduit, toutes choses égales par ailleurs, à une baisse des températures. Cette baisse peut être d'autant plus atténuée que tout ou partie de la croûte continentale migre vers des latitudes élevées et se recouvrent alors d'inlandsis : la température est alors régulée par la formation de cet inlandsis : celui-ci bloque l'érosion, qui bloque la capture de CO2, limitant par là la perte d'effet de serre et la baisse de température globale.
Niveau zéro des mers

Un autre aspect de l'érosion est qu'elle tend à ramener la croûte continentale au niveau zéro de ce que marque l'océan mondial : tout ce qui est en relief par rapport au niveau de la mer tend à être érodé, et les alluvions correspondantes se déposent en milieu marin, contribuant aux dépôts sédimentaires.
Inversement, et en négligeant les dépôts sur la croûte océanique profonde, tout ce qui est en-dessous du niveau moyen de la mer tend à être progressivement empâté par des dépôts sédimentaires, qui en font remonter l'altitude.
Globalement, un équilibre (et un non-changement des profils) n'est atteint que lorsque l'épaisseur de la croûte continentale est telle qu'elle compense globalement, par le volume occupé, la perte de surface subie par l'océan global, du fait de l'accumulation des cratons. L'équilibre global de l'époque, entre dépôt et érosion, est atteint quand dans la croûte continentale, la partie émergée est (en gros) équivalente à la partie immergée, aux orogenèses en cours près.
Avec l'accumulation progressive des cratons sur des masses continentales de plus en plus importantes, on assistera donc en parallèle, en moyenne, à un approfondissement progressif des océans. Par ailleurs, on assistera à un équilibre global entre la surface du plateau continental et celle de la croûte continentale exposée à l'érosion.
Cette logique perdure aux temps présents : actuellement nous sommes en fin de glaciation, le niveau des mers est en-dessous de son équilibre, et la remontée naturelle des eaux océaniques recouvrira de nombreuses surfaces considérées géologiquement comme des « plaines océaniques ».
−2,2 à −1,6 Ga : premiers essais pluricellulaires et supercontinent Columbia


À −2,2 Ga, l'augmentation du δ13Corg dans les carbonates s'explique par une fossilisation de matière organique plus importante, notamment dans les stromatolites, des structures en carbonate de calcium probablement édifiées par des cyanobactéries. L'activité photosynthétique a pour effet d'enrichir l'atmosphère en dioxygène.
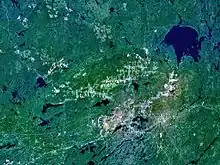
Le groupe fossile de Franceville, daté de −2,1 Ga, montre une vie multicellulaire complexe et organisée au début de l'Orosirien[68]. Cette apparition est restée sans lendemain, en raison peut-être, des impacts de Vredefort (−2,02 Ga) et de Sudbury (1,849 Ga), et de la baisse ultérieure du taux d'oxygène. De tous les cratères d'impact identifiés, ces deux impacts sont en effet les plus importants, nettement supérieurs à celui de Chicxulub dont on pense qu'il mit fin au règne des dinosaures. Des impacts de ce niveau éjectent de la poussière et des cendres, provoquant un hiver d'impact durable, et la chute de la photosynthèse faute de luminosité. Les formes de vie complexes sont dépendantes de la respiration aérobie, et n'auront pas survécu à ces catastrophes.
Columbia est l'un des premiers supercontinents, qui s'est formé tout au long d'une période de collision et d'orogenèse à grande échelle s'étendant de −2,2 à 1,8 Ga, pendant l'ère paléoprotérozoïque. À partir de −1,8 Ga, les paléosols s'enrichissent en fer. La pression partielle de dioxygène est de l'ordre de 15 % de l'actuelle.
À la suite de son assemblage final, au Stathérien, le continent a subi une croissance de longue durée (1,8 à 1,3 Ga) avec des zones de subduction au niveau des marges continentales principales[69], à l'origine d'une large ceinture d'accrétion magmatique.
La fragmentation de Columbia a commencé vers −1,6 Ga, au début du Calymmien, et s'est prolongée jusqu'à la disparition du continent, entre −1,3 et −1,2 Ga, à la fin de l'Ectasien.

Eucaryotes et reproduction sexuée
.svg.png.webp)

Les domaines de protéines spécifiquement associés aux eucaryotes sont datés de −1,5 Ga, sensiblement la date d'apparition des protéines spécifiques aux capsides des virus (−1,6 Ga)[70], ce qui suggère un évènement déclencheur commun dans l'écologie bactérienne.
Le microfossile le plus ancien indiscutablement eucaryote est daté de −1,45 Ga[71].
Vers −1,2 Ga, la présence d'eucaryotes, les algues rouges Bangiomorpha pubescens, est attestée par les micro-fossiles de la formation de Hunting, dans l'île de Somerset, au Canada. C'est le plus ancien organisme multicellulaire complexe connu, capable de reproduction sexuée[72]. La multicellularité complexe est différente de la multicellularité "simple", celle de colonies d'organismes vivant ensemble. Les vrais organismes multicellulaires présentent des cellules spécialisées dans différentes fonctions. C'est une caractéristique essentielle de la reproduction sexuée, car les gamètes mâles et femelles sont elles-mêmes des cellules spécialisées. Les organismes qui se reproduisent sexuellement doivent pouvoir engendrer un organisme entier à partir d'une cellule germinale unique.
La structure des eucaryotes permet par exemple des mouvements d'évitement variés[73]
- The hydrogen hypothesis for the first eukaryote. Martin W, Muller M. Nature 1998, 392(6671):37-41.
- Animals and the invention of the Phanerozoic Earth system. Nicholas J.Butterfield. Trends in Ecology & Evolution. Elsevier, February 2011
−1,1 à −0,75 Ga : supercontinent Rodinia


Le supercontinent Rodinia commence à se former au début du Sténien, à −1,1 Ga. Il y a 750 millions d'années, vers la fin du Tonien, il se scinde en huit continents et leur dérive provoquera sa dislocation.
Les microfossiles du Tonien témoignent de la première radiation évolutive des Acritarches.
La rupture de ce continent serait à l'origine de la période glaciaire du Cryogénien et de la rapide évolution de la vie à l'Édiacarien et au Cambrien.
Les cratères majeurs très anciens sont d'approche difficile sur Terre, parce que l'érosion et la tectonique des plaques brouillent et effacent les traces qu'ils ont pu laisser ; mais l'étude des cratères lunaires et leur datation permet de reconstituer une pluie d'astéroïdes survenue sur le système Terre-Lune vers −0,8 Ga, ce qui sur terre marque l'entrée dans le Cryogénien[74]. L'extrapolation sur la Terre du flux d'astéroïdes relevé sur la Lune donnerait une série d'impacts apportant collectivement l'équivalent d'un astéroïde de 30 à 40 km de diamètre[74].
Outre la possibilité d'un hiver d'impact et une perturbation majeure de la composition et de la température des océans, cet impact aurait pu avoir une influence significative sur le cycle du phosphore. La teneur en phosphore des dépôts à cette fin du Tonien est en effet quatre fois plus élevée que celle des dépôts précédents ; et l'apport d'un tel volume sous forme de Chondrite CI, où le phosphore est présent à un taux de l'ordre de 1‰, aurait entraîné un apport d'un ordre de grandeur supérieur au contenu actuel des océans[74].
−720 à −635 Ma : Terre boule de neige

À la fin du Protérozoïque, il y a 800 millions d'années, le supercontinent Rodinia qui, à l'époque, était centré sur l'équateur et s'étendait du 60e degré de latitude nord au 60e degré de latitude sud, a commencé à se disloquer sous l'effet de points chauds. Cet événement s'est accompagné de l'ouverture d'océans et de bras de mer qui ont permis aux pluies d'atteindre l'ensemble des masses continentales. Le CO2 atmosphérique, présent dans les pluies sous forme d'acide carbonique, reprend son travail d'érosion, solubilisant les roches sous forme de bicarbonates, puis précipitant dans l'océan, piégé dans les sédiments sous forme de carbonates. D'autre part, les énormes écoulements de laves associés à la fracture de Rodinia ont formé de larges surfaces basaltiques à la surface des continents. Or ces surfaces, altérées sous l'effet de l'humidité, consomment huit fois plus de carbone qu'une même surface granitique.
Ces circonstances entraînent une importante diminution du taux de dioxyde de carbone dans l'atmosphère, diminuant l'effet de serre du gaz carbonique, et entraînant une chute des températures. Par ailleurs, le Soleil était plus jeune et diffusait 6 % de chaleur en moins.
En général, quand la Terre se refroidit, le refroidissement ralentit ces réactions d'altération. Mais au Cryogénien, les continents étaient à des latitudes tropicales, ce qui a rendu moins efficace cette régulation, l'érosion continuant à des niveaux élevés même sur une Terre plus froide. Tous ces facteurs ont pu entraîner une période glaciaire particulièrement intense ayant recouvert la surface terrestre de glaciers jusqu'aux latitudes 30°. Une fois ces limites atteintes, l'albédo global est alors tel que cela met en place une boucle auto-amplificatrice qui permet de voir la totalité de la planète se recouvrir de glace. Le début de la glaciation est marqué par une forte baisse de la valeur δ13Corg dans les sédiments, ce qui peut être attribué à la chute de la productivité biologique, en raison des températures froides et des océans recouverts de glace.
Dans le scénario précédent de la grande glaciation huronienne, le « thermostat », initialement assuré essentiellement par le méthane, avait entièrement disparu, et la glaciation avait duré tant que l'accumulation du CO2 atmosphérique ne permettait pas d'atteindre un effet de serre suffisant. Ici, au contraire, le « thermostat » terrestre est dès le départ assuré par le gaz carbonique, dont le niveau initial part de celui permettant le début de la glaciation. La reconstitution par les émissions volcaniques du niveau de CO2 nécessaire pour sortir de la glaciation est donc plus rapide. À la fin d'une période de glaciation, la boucle de rétroaction positive peut faire fondre la glace en très peu de temps à l'échelle géologique, peut-être moins de 1 000 ans. À la fin de la glaciation, la fonte des glaciers libère d'importantes quantités de dépôts glaciaires. Les sédiments résultant fournis à l'océan seraient riches en éléments nutritifs, comme le phosphore, qui, associé à l'abondance de CO2, déclenchent une explosion démographique de cyanobactéries, ce qui entraînerait une réoxygénation accélérée de l'atmosphère. Mais le réapprovisionnement de l'oxygène atmosphérique et l'épuisement du CO2 en excès peut prendre des dizaines ou des centaines de millénaires.
Cette élimination du CO2 a pu conduire ensuite à de nouveaux épisodes glaciaires, tant que les surfaces basaltiques n'ont pas été suffisamment altérées. La fin du néoprotérozoïque est ainsi marquée de trois (ou quatre?) glaciations d'amplitude décroissante.
Une bouffée d'oxygénation a eu lieu entre −0,8 Ga et −0,65 Ga, l'oxygénation du Néoprotérozoïque (Neoproterozoic Oxyenation Event, NOE)[39]. Les océans cessent d'être anoxiques pour devenir riches en sulfates. Cette oxygénation peut avoir contribué à l'apparition de la faune de l'Ediacaran, une concentration plus élevée en oxygène permettant à de grandes formes de vie multicellulaires de se développer.
−600 à −540 Ma : supercontinent Pannotia et faune de l'Édiacarien

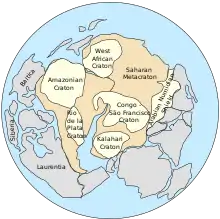 |
 | |
Pannotia (−0,6 Ga, centrée sur le pôle sud). |
Faune de l'Édiacarien. |
La Pannotia ou Pannotie est un ancien supercontinent qui aurait existé à la fin du Précambrien, de -600 à -540 millions d'années (Ma) environ et au début du Cambrien. Ce supercontinent hypothétique s'intègre dans le modèle des cycles de Wilson qui expliqueraient la périodicité des épisodes de formation des chaînes de montagnes, les orogenèses. Il s'est formé à la suite de plusieurs collisions, lors de l'orogenèse panafricaine dont l'orogenèse brésilienne en Amérique du Sud et l'orogenèse cadomienne en Amérique du Nord et en Europe de l'Ouest sont une phase locale.
La faune marine de l'Édiacarien, vieille de 600 Ma, serait une preuve de l'existence de ce supercontinent. On a retrouvé des fossiles de cette faune dans des régions actuellement très éloignées les unes des autres (Australie, Namibie, etc.). Ces animaux ne pouvaient pas parcourir de grandes distances, ils devaient vivre sur les marges continentales d'un seul continent.
Cette faune de l'Édiacarien est apparue de plus en plus énigmatique. Actuellement, le classement de ces espèces est sujet à controverse. Déterminer l'emplacement des organismes de l'Édiacarien dans l'arbre de la vie s'est révélé difficile ; il n'est pas certain qu'il s'agissait d'animaux et ils pourraient être des lichens, des algues, des foraminifères, des champignons, des colonies microbiennes ou des intermédiaires entre les plantes et les animaux. La morphologie de certains taxons suggère un lien de parenté avec les éponges, les cténophores voire les cnidaires[76]. Si certains de ces fossiles, comme Kimberella, Bomakellia et Xenusion, ou même certaines faunes de petits coquillages, peuvent être rattachés à des formes de vie du Cambrien, beaucoup d'autres, par exemple en forme de goutte, de disque, de fronde ou de domino, n'ont pas de relations connues avec une faune postérieure. La plupart des macro-fossiles sont morphologiquement distincts des formes de vie ultérieures : ils ressemblent à des disques, des tubes ou des sacs molletonnés. Du fait des difficultés pour établir des relations entre ces organismes certains paléontologues ont suggéré qu'ils pourraient représenter une forme de vie éteinte ne ressemblant à aucun organisme vivant, une sorte d'« expérience manquée » de la vie multicellulaire[77]. Le paléontologue Adolf Seilacher a proposé un nouveau règne appelé « Vendozoa » pour regrouper ces organismes énigmatiques[78]. Plus récemment beaucoup de ces animaux ont été regroupés dans les Petalonamae, un groupe présentant des affinités avec les cténophores[79].
Les fragments issus de Pannotia forment plus tard la Pangée.
−565 Ma : cristallisation du noyau
Les enregistrements paléomagnétiques de l'Édiacarien relevés à Sept-Îles et datant de ~565 Ma dénotent un champ magnétique terrestre extrêmement faible, dispersé en direction, et un taux d'inversion très élevé[80]. Ce comportement paléomagnétique rappelle celui du Jurassique supérieur (~165 Ma), au cours duquel le champ géomagnétique a subi plus de deix inversions par million d'années, mais ici le champ paraît cinq fois plus faible en force que celui du Jurassique. Avec un champ aussi faible, la magnétopause se serait stabilisée à moins de 4,5 rayons terrestres, moins que la valeur observée pendant une tempête solaire sévère[80].
Cette faiblesse du champ magnétique peut être rapprochée de la modélisation de la dynamo terrestre, pour laquelle le refroidissement progressif du cœur de la planète conduit à une quasi-disparition du champ résultant, avant que le noyau ne cristallise[80]. Si tel est le cas, la nucléation du noyau interne a peut-être eu lieu juste à temps pour recharger la dynamo et restaurer le bouclier magnétique de la Terre[81], donnant la protection nécessaire à l'explosion cambrienne.
Phanérozoïque (depuis −541 Ma)
−541 Ma : explosion cambrienne

Il y a 550 millions d’années a eu lieu l’explosion cambrienne. Les premiers poissons pourvus d’arêtes sont apparus ; ils sont les ancêtres de tous les vertébrés actuels.
Grâce à l’oxygène, la couche d'ozone se forme ; elle protège les êtres vivants des radiations, permettant à ceux-ci de s’aventurer sur la terre ferme : l'extinction de l'Ordovicien-Silurien et celle du Dévonien, marquées par d'importantes crises biologiques qui appauvrissent la vie jusque-là exclusivement marine favorisent la conquête des terres émergées par les plantes chlorophylliennes et plusieurs grands groupes animaux, essentiellement les arthropodes et les vertébrés. Ce processus d'adaptation est appelé la sortie des eaux.
C'est lors de l'Ordovicien supérieur que les plantes non vasculaires s'installent et se développent sur la terre ferme[82]. Cette modification majeure de la biosphère aurait accéléré le processus d'altération des silicates sur les continents. Ce processus, en fixant de très grandes quantités de dioxyde de carbone, aurait conduit à la baisse des températures de la Terre et au développement des calottes polaires[82].
−445 Ma : extinction Ordovicien-Silurien

L'Ordovicien est corrélé à une explosion d'activité volcanique, qui a déposé de nouvelles roches silicatées, lesquelles extraient du CO2 de l'air à mesure qu'elles s'érodent. Il en résulté une baisse du dioxyde de carbone atmosphérique (de 7 000 à 4 400 ppm).
L'apparition et le développement des plantes terrestres et du microphytoplancton, qui consommaient du dioxyde de carbone atmosphérique, a diminué l'effet de serre et favorisé la transition du système climatique vers le mode glaciaire. L'étude d'anciens sédiments marins datant d'environ 444 Ma (fin de l'Ordovicien) montre une grande abondance de dérivés de la chlorophylle, dont la composition isotopique de l'azote coïncide avec celle des algues modernes. En quelques millions d'années seulement les quantités d'algues mortes sédimentées ont plus que quintuplé. Ces algues auraient prospéré aux dépens des autres espèces et notamment des cyanobactéries. Au moins deux fois plus grandes que ces dernières, les algues mortes se seraient rapidement accumulées au fond des océans au lieu de voir leur carbone recyclé, entraînant à la fois une raréfaction des organismes marins (et à cette époque la vie était essentiellement limitée au milieu marin) et une grande glaciation (par diminution de l'effet de serre)[83] - [84].
Le Gondwana était alors situé sur le pôle sud, ce qui a entraîné une glaciation continentale rapide, la glaciation de l'Ordovicien supérieur. La baisse résultante de niveau dans l'océan mondial a fait émerger les plateaux continentaux et les bassins peu profond faisant disparaître la principale niche du biotope ordovicien, et plaçant toute la biosphère en situation de stress.
De même que pour d'autres épisodes d'extinction de masse, cette situation de crise a rencontré des facteurs déclenchant, sous forme d'une grande phase de volcanisme ou d'impact d'astéroïde, obscurcissant l'atmosphère et conduisant à un hiver d'impact. La réduction de la photosynthèse supprime la production primaire et détruit les chaînes alimentaires qui en dépendent.
L'extinction de l'Ordovicien-Silurien aboutit à la disparition de 27 % des familles et de 57 % des genres d'animaux marins[85]. Elle est considérée comme la seconde plus importante des cinq grandes extinctions massives du Phanérozoïque après celle du Permien-Trias qui interviendra environ 200 millions d'années plus tard.
Le taux de disparition de familles d'animaux marins dans la partie supérieure de l'Ordovicien, sur environ 20 millions d'années est le plus élevé jamais enregistré au cours de l'histoire de la Terre, il est de l'ordre de 20 familles par million d'années[86].
−440 Ma : sortie de l'eau et seconde oxygénation
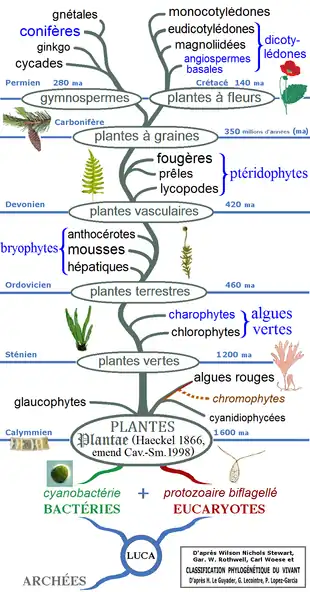
À partir de −440 Ma, au Silurien, les algues sortent de l'eau, et ces formes primitives de plantes multicellulaires envahissent les terres et commencent à y laisser des dépôts organiques. Quelques rares arthropodes migrent vers la terre, et inaugurent des classes d'arthropodes terrestres : arachnides (−435 Ma), myriapodes (−428 Ma).
Les plantes vasculaires sortent de l'eau à leur tour vers −420 Ma, au début du Dévonien. Contrairement aux algues, les plantes vasculaires ont un système de racines avec lesquelles elles puisent des nutriments dans la lithosphère. Les sols résultent de la transformation de la couche superficielle de la roche-mère, dégradée et enrichie en apports organiques par les processus vivants de pédogenèse, constituant progressivement la pédosphère. Les premiers hexapodes apparaissent sur terre vers −395 Ma, et maîtrisent le vol vers −380 Ma.
L'apparition des végétaux terrestres rend caduque la régulation par la nitrogénase de la teneur en oxygène, parce que la production aérienne d'oxygène par ces plantes devient indépendante de la fixation de l'azote dans les sols et les environnements aquatiques[28]. Il en résulte une montée progressive de la teneur atmosphérique en oxygène, entraînant une nouvelle crise dans la biosphère.
En réponse au taux plus élevé d'oxygène, les cyanobactéries qui vivent en colonies cohérentes (en trichomes formant des films, amas ou filaments) fixent l'azote de l'air via des cellules spécialisées dites hétérocystes qui fonctionnent indépendamment des autres cellules, en anaérobiose[28]. Certaines font preuve d'une très bonne résistance au froid, au chaud et aux rayonnements ionisants ou ultraviolets ce qui leur permet notamment de vivre en zone polaire[87]. Quand les nitrates ou l'ammoniac manquent, une partie des cellules de ces cyanobactéries (10 % environ) épaississent leurs parois, excrètent leur pigments et synthétisent une enzyme (nitrogénase) qui fixe l'azote (stocké sous forme de glutamine qui peut être utilisée par d'autres cellules vivant elles en aérobie).
Des variations répétées et significatives du niveau de la mer et du climat, ainsi que l'apparition d'un couvert végétal important sur les continents, pourraient être à l'origine de phénomènes d'anoxie des océans et de crises biologiques majeures, conduisant à l'extinction du Dévonien. Les causes de ces changements sont encore débattues.
Régulation du niveau d'oxygène
L'évolution des plantes terrestres au début du Dévonien entraîna une élévation à long terme du niveau d'oxygène par photosynthèse, construisant des hydrates de carbone génériquement représentés par C(H2O) :
- CO2 + H2O + hν → C(H2O) + O2 ↑
Mais par elle-même, la photosynthèse ne permet pas à l'oxygène de s'accumuler tant que la matière organique reste exposée à l'oxydation chimique ou à la respiration cellulaire, qui consomment cet oxygène et restituent le gaz carbonique :
- C(H2O) + O2 → CO2 ↑ + H2O + énergie
L'oxygène ne peut s'accumuler dans l'atmosphère que si de la matière organique disparaît dans la sédimentation, capturée dans la lithosphère.
Cet enfouissement conduit à une régulation à long terme de la teneur atmosphérique en oxygène, via la fraction de matière organique produite qui reste piégée dans les sédiments. Cette fraction est actuellement très faible (de l'ordre de 0.1%) du fait de l'efficacité de la décomposition aérobique[88] ; cette sédimentation compensant globalement l'oxydation des roches nouvellement exposées, ce qui interdit une accumulation supplémentaire d'oxygène. Une chute dans la teneur atmosphérique diminuerait l'efficacité de la décomposition, permettant une plus grande sédimentation des matières organiques. En particulier, si les fonds océaniques tendent à devenir anoxiques, il ne peuvent plus permettre la décomposition des particules organiques en provenance de la surface.
−359 à −299 Ma : Carbonifère


Le Carbonifère est une période d’orogenèse active: la Pangée est en cours de formation. Après le refroidissement amorcé durant le Dévonien, la température reste tiède, malgré un taux de CO2 estimé à 0,9 % (soit trente fois celui du XIXe siècle) et stable durant la première partie du Carbonifère, pendant la seconde partie du Carbonifère le climat se refroidit à nouveau.
Cette période est caractérisée par les premiers grands arbres. Le fort taux de CO2 de l'atmosphère a certainement favorisé la croissance de la végétation. Les larges dépôts de charbon sont dus à deux facteurs :
- l’apparition d’arbres à écorces et en particulier ceux à écorces ligneuses ;
- le niveau des mers, peu élevé, comparé à celui du Dévonien, qui a permis l’extension de vastes marécages.
On a émis l’hypothèse que l’enfouissement de grandes quantités de bois est dû au fait que les bactéries n’étaient pas encore assez évoluées pour être capables de digérer et de décomposer les nouveaux ligneux. La lignine est en effet difficile à décomposer. Elle n’est pas soluble, et peut rester dans le sol pendant des centaines d’années et inhiber la décomposition d’autres substances végétales[89].
L’enfouissement massif de carbone a pu conduire à un surplus d’oxygène dans l’air allant jusqu’à 35 %[90] mais des modèles révisés considèrent ce chiffre comme irréaliste et estiment que le pourcentage d’oxygène dans l’air devait se situer entre 15 et 25 %[91]. Des taux élevés d’oxygène sont une des causes avancées au gigantisme de certains insectes et amphibiens dont la taille est corrélée à leur capacité à absorber de l’oxygène. De grandes fougères arborescentes, atteignant 20 mètres de hauteur, accompagnées de lycopodes de 30 à 40 mètres, dominaient les forêts du Carbonifère qui prospéraient dans des marais de type équatorial, des Appalaches à la Pologne, puis, plus tard, sur les pentes des monts de l’Oural.
Le charbon a arrêté de se former il y a près de 290 millions d’années (fin du Carbonifère). Selon une étude ayant comparé l’horloge moléculaire et le génome de 31 espèces de basidiomycètes (agaricomycetes : « pourriture blanche », groupe qui contient aussi des champignons ne dégradant pas la lignine — pourriture brune — et des espèces ectomycorrhiziennes), cet arrêt de formation du charbon semble pouvoir être expliqué par l'apparition de nouvelles espèces de champignons lignivores (dits aussi xylophages) capables de dégrader la totalité de la lignine grâce à des enzymes (les lignine peroxydases)[92] - [93].
La haute teneur en oxygène et la haute pression atmosphérique permirent des métabolismes plus énergétiques qui favorisèrent l’émergence des grands vertébrés terrestres et de très grands insectes volants.
−360 à −260 Ma : glaciation du Karoo
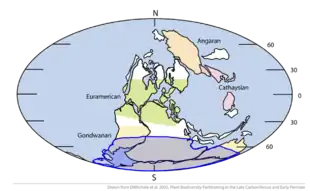
Dès le début de cette ère carbonifère, l'assemblage des plaques tectoniques de la Laurussia et du proto-Gondwana, formant la Pangée, généra une importante masse continentale dans la région Antarctique ; la fermeture de l'océan Rhéique et de l'océan Iapétus perturba la circulation des courants chauds dans la Panthalassa et l'océan Thétys, ce qui entraîna un refroidissement progressif des étés ainsi que des accumulations de neige en hiver, ce qui fit croître la taille des glaciers qui couvrirent la majeure partie du Gondwana. De plus, avec la capture du carbone, le taux global de dioxyde de carbone se réduit. Le Carbonifère est marqué par une tendance au refroidissement et à la formation d'inlandsis sur les continents polaires. Au moins deux épisodes majeures de glaciation ont été identifiés.
La chute de température limita la pousse des plantes, et le niveau élevé d'oxygène favorisa les incendies ; même humides, les plantes pouvaient brûler. Ces deux phénomènes contribuèrent à relâcher du dioxyde de carbone dans l'atmosphère, freinant l'effet « Terre boule de neige » et générant un réchauffement par effet de serre.
−300 à −250 Ma : Pangée

La Pangée, qui apparaît au début du Permien, est formée à la fin du Carbonifère de la collision de la Laurussia et du Protogondwana. Toutes les masses de terre, à l'exception d'une portion de l'Asie du Sud-Est, se sont agglomérées en un seul supercontinent, qui s'étendait de l'équateur aux pôles, entouré par un océan nommé Panthalassa (la « mer universelle »).
Le niveau moyen de la mer est resté assez bas durant le Permien.
La formation du supercontinent Pangée a eu des conséquences importantes sur la vie : la longueur des côtes, et donc la superficie des eaux côtières qui abritent la majorité des espèces marines, ont été considérablement réduites. La réunion de tous les continents en un seul supercontinent fait disparaître les plateaux continentaux, abritant un grand nombre d'espèces, aux niveaux de la collision formant la chaine hercynienne ; puis, le passage de plusieurs continents à un seul, s'il peut conserver la surface totale de terres émergées, diminue nettement la longueur totale des côtes. Les zones côtières, soumises à un climat océanique, sont donc alors plus restreintes. Enfin, sur terre, l'éloignement des terres de la Pangée centrale (Amérique du Nord, Amérique du Sud et Afrique) par rapport à la mer a conduit à une forte baisse des précipitations dans ces régions et, donc, à l'expansion de gigantesques déserts.
La Pangée commence à se fracturer dès la fin du Permien (−252 Ma) mais de manière véritablement intense uniquement à la fin du Trias (~200 millions d'années), par des systèmes de rifts séparant l'Amérique du Nord et l'Afrique. Au Trias, il s'est morcelé en Laurasia au nord et Gondwana au sud.
−252 Ma : extinction Permien-Trias (Grande Extinction)

Une intense activité volcanique continentale (trapps d'Emeishan en Chine, à environ −258 Ma) ; et une activité très importante des dorsales océaniques de l'océan Téthys produisant un volume considérable de laves basaltiques, à l'origine d'une transgression affectant les côtes de la Pangée, sur une dizaine de millions d'années.
L'événement catastrophique est vraisemblablement l'éruption d'un supervolcan en Sibérie[94] - [95] (provoquée par l'arrivée à la surface de la Terre d'un point chaud et dont les trapps de Sibérie sont la trace), qui aurait libéré dans l'atmosphère des quantités phénoménales de gaz sulfureux, et accompagnée d'une forte acidification des océans[96].
D'autres hypothèses envisagent un ou plusieurs impacts de météorites ou la soudaine libération de CO2 et d'hydrates de méthane à partir des océans, ayant comme conséquence une baisse importante de la teneur de l'atmosphère en O2. Le cratère d'impact Bedout, au large de la côte nord-ouest de l'Australie, date de cette époque. C'est le troisième plus grand cratère d'impact sur Terre. Certains scientifiques estiment qu'il pourrait s'agir de l'impact d'une météorite géante qui aurait provoqué cette extinction.
Cette extinction est marquée par la disparition de 95 % des espèces marines (essentiellement des espèces littorales tels les coraux, brachiopodes, échinodermes, etc.) et de 70 % des espèces vivant sur les continents (notamment par la diminution de nombreux groupes de végétaux et d'animaux, y compris des insectes), ce qui en fait la plus grande extinction massive ayant affecté la biosphère. En conséquence, retrouver un niveau de biodiversité équivalent a pris beaucoup plus de temps que pour les autres extinctions massives[97]. Cet événement a été décrit par le paléobiologiste Douglas Erwin (en) comme « la mère de toutes les extinctions de masse »[98].
−201 Ma : extinction Trias-Jurassique

−66 Ma : extinction du Crétacé

Un autre candidat potentiel serait le cratère Shiva, datant de la même époque, un peu antérieur à la formation des trapps du Deccan.
La Terre, qui est progressivement ralentie par l'effet de marée induit par la Lune, tournait plus vite à cette époque, et une année comprenait alors 372 jours[99].
−2,58 Ma : glaciations quaternaires

D'après l'analyse de l'ADN, en particulier l'horloge moléculaire, la branche qui a conduit à l'Homme diverge de celle des primates supérieurs il y a environ 7 millions d'années[100].
Lucy, fossile de l'espèce Australopithecus afarensis date d'environ 3,2 millions d'années.
Homo habilis, hominidé moderne, émerge en Afrique orientale il y a environ 2 millions d'années.
L’Homo sapiens moderne apparaît en Afrique il y a quelque 300 000 ans.
−0,6 Ma : fin de Homo erectus

Il y a 0,079 Ma, un météore percute le sud-Laos[101].
À partir de −10 000 ans environ, les hommes se regroupent en sociétés organisées. C'est également à ce moment que l'agriculture et l'élevage naissent, notamment en Europe et au Proche-Orient. Les premières cités apparaissent dans le Croissant fertile (exemple : Babylone) vers 5000 avant J.C.), puis l'écriture révolutionne l’Humanité vers -3000 et donne naissance aux premiers royaumes (Égypte ancienne…) : c'est le début de l'Antiquité.
Puis les civilisations modernes se développent en Méditerranée et au Proche-Orient avec les cités grecques puis plus tard avec l'empire romain qui durera jusqu'en 476. Les premiers liens entre les civilisations méditerranéennes et les civilisations d'extrême Orient durant l'Antiquité se firent notamment grâce aux conquêtes d'Alexandre le Grand vers -330 et permirent de faire rayonner la culture grecque jusqu'en Iran actuel. Plus tard, c'est Marco Polo puis les grands explorateurs maritimes (Christophe Colomb, Magellan, Vasco de Gama…) qui permirent la découverte (européenne) de l'Asie, des côtes Africaines puis de l'Amérique enclenchant le début de l'époque moderne à partir du XVe siècle.
Notes et références
- (en) Auteur inconnu, « Nine-Year Wilkinson Microwave Anisotropy Probe (WMAP) Observations: Final Maps and Results », ..
- L'Univers et ses mystères, de Tony Long, Flight 33 productions, 2007, ép. 6 (« La Terre, notre vaisseau spatial »).
- (en) George H. Shaw, « Earth's atmosphere – Hadean to early Proterozoic », Geochemistry, vol. 68, no 3, , p. 235-264 (DOI 10.1016/j.chemer.2008.05.001, lire en ligne).
- Quand la Terre était une boule de neige, Anne-Sophie Boutaud, Le journal du CNRS, 05.12.2017
- Étienne Klein, Gilles Ramstein, « La Terre a-t-elle toujours été aussi bleue qu’une orange ? », sur franceculture.fr, (consulté le ).
- (en) James F. Kasting, « Earth's early atmosphere », Science, vol. 259, no 5097, , p. 920–926 (PMID 11536547, DOI 10.1126/science.11536547).
- (en) Asish Basu et Stan Hart, Earth Processes : Reading the Isotopic Code, American Geophysical Union, (lire en ligne), p. 63.
- (en) Alain R. Meunier, La naissance de la Terre. De sa formation à l'apparition de la vie, Dunod, (lire en ligne), p. 101.
- (en) S. T. Petsch, chap. 8.11 « The Global Oxygen Cycle », dans Heinrich D. Holland and Karl K. Turekian, Treatise on Geochemistry, vol. 8 : Biogeochemistry, Elsevier, , 682 p. (ISBN 0-08-043751-6, DOI 10.1016/B0-08-043751-6/08159-7, résumé).
- (en) Carsten Münker, Jörg A. Pfänder, Stefan Weyer, Anette Büchl, Thorsten Kleine, Klaus Mezger, Evolution of Planetary Cores and the Earth-Moon System from Nb/Ta Systematics, Science, 4 juillet 2003, volume 301, no 5629, p. 84–87.
- (en) G. Jeffrey Taylor, Origin of the Earth and Moon, NASA, 26 avril 2004.
- (en)Norman H Sleep, The Hadean-Archaean Environment, Cold Spring Harbor perspectives in biology, juin 2010.
- [vidéo]"La Lune et ses mystères", TV5, 2005 (consulté le 22 décembre 2019).
- (en) Wilde SA, Valley JW, Peck WH et Graham CM, Evidence from detrital zircons for the existence of continental crust and oceans on the Earth 4.4 Gyr ago., Nature, v. 409, 2001, p. 175-178 Lire en ligne, wisc.edu
- Bernard Bourdon, « Sur la piste de l'écorce primitive », La Recherche, no 386, , p. 54 (lire en ligne).
- (en) Guillaume Caro, Bernard Bourdon, Bernard J. Wood & Alexandre Corgne, « Trace-element fractionation in Hadean mantlegenerated by melt segregation from a magma ocean », Nature, no 436, , p. 246-249 (DOI 10.1038/nature03827).
- (en) P. Richard, N. Shimizu, C. Allegre, « 43Nd/146Nd, a natural tracer: an application to oceanic basalts », Earth and Planetary Science Letters, vol. 31, no 2, , p. 269–278 (DOI 10.1016/0012-821X(76)90219-3).
- (en) Alfvén Hannes, Gustaf Arrhenius, Evolution of the Solar System, National Aeronautics and Space Administration, 1976.
- (en) A. J. Cavosie, J. W. Valley, S. A., Wilde, E.I.M.F., Magmatic δ18O in 4400-3900 Ma detrital zircons: A record of the alteration and recycling of crust in the Early Archean, Earth and Planetary Science Letters, volume 235, numéro 3-4, 15 juillet 2005, p. 663-681.
- (en) Edward Young, Executive Summary 2005 « Copie archivée » (version du 14 novembre 2007 sur Internet Archive), 4 juillet 2005.
- Une brève histoire du climat de la Terre, Gilles Ramstein, Reflets de la Physique Numéro 55 (Octobre-Novembre 2017), Revue de la Société Française de Physique
- (en) Robert Roy Britt, Evidence for Ancient Bombardment of Earth, Space.com, 24 juillet 2002.
- Le phosphore des météorites a permis la vie sur Terre, CIRS, Futura Santé, le .
- François Robert and Marc Chaussidon, A palaeotemperature curve for the Precambrian oceans based on silicon isotopes in cherts, Nature, 443, 26 octobre 2006, p. 969-972.
- On the Origin of Heterotrophy. Peter Schönheit, Wolfgang Buckel, William F. Martin. Trends in Microbiology, January 2016, Vol. 24, No. 1.
- A Coupled Ecosystem-Climate Model for Predicting the Methane Concentration in the Archean Atmosphere. James F. Kasting, Alexander A. Pavlov, Janet L. Siefert. Origins of life and evolution of the biosphere, June 2001, Volume 31, Issue 3, pp 271–285.
- L’origine de la vie et les métalloenzymes à fer-soufre. Juan C. Fontecilla-Camps. Exposé au Collège de France, 26 mai 2010.
- (en) John F.Allen, Brenda Thake, William F.Martin, Nitrogenase Inhibition Limited Oxygenation of Earth’s Proterozoic Atmosphere, Trends in Plant Science, Elsevier, novembre 2019.
- (en) Ilana Berman-Frank, Yi-bu Chen, Yuan Gao, Katja Fennel, Mick Follows, Allen J. Milligan, et Paul Falkowski, [PDF] Feedbacks Between the Nitrogen, Carbon and Oxygen Cycles. Nitrogen in the Marine Environment (2d Edition - 2008), Academic Press, pp.1537-1563.
- A reduced, abiotic nitrogen cycle before the rise of oxygen. Ward, Lewis M, James Hemp, and Woodward W. Fischer.
- The Nitrogen Cycle Before the Rise of Oxygen. Ward, L. M.; Hemp, J.; Fischer, W. W. American Geophysical Union, Fall Meeting 2016.
- (en) Earth: Atmospheric Evolution of a Habitable Planet. Stephanie L. Olson, Edward W. Schwieterman, Christopher T. Reinhard, Timothy W. Lyons. arXiv:1803.05967 [astro-ph.EP].
- Jean-François Deconinck, Benjamin Brigaud, Pierre Pellenard, Pétrographie et environnements sédimentaires, Dunod, (lire en ligne), p. 223.
- Donald E. Canfield et al., The Evolution and Future of Earth's Nitrogen Cycle, Science, 2010, 330, 192.
- Quentin Mauguit,La photosynthèse prend de l’âge : elle a 3,8 milliards d’années, Futura, 28/02/2013
- Quentin Mauguit, La photosynthèse prend de l’âge : elle a 3,8 milliards d’années, Futura, 28/02/2013.
- Life: the first two billion years. Andrew H. Knoll, Kristin D. Bergmann, Justin V. Strauss. Philosophical Transactions ofthe Royal Society B: Biological Sciences 371 (1707) (September 26):20150493. doi:10.1098/rstb.2015.0493.
- The Continuing Puzzle of the Great Oxidation Event. Alex L.Sessions, David M.Doughty, Paula V.Welander, Roger E.Summons, Dianne K.Newman. Current Biology, Volume 19, Issue 14, 28 July 2009, Pages R567-R574.
- (en) The evolution of Earth's biogeochemical nitrogen cycle. Eva E. Stüeken, Michael A. Kipp, Matthew C. Koehler, Roger Buick. Earth-Science Reviews, 160, 2016, p. 220–239.
- (en) Tanai Cardona, Thinking twice about the evolution of photosynthesis, Royal Society, 20 mars 2019 DOI 10.1098/rsob.180246.
- (en) Photosynthesis got a really early start, New Scientist, 2 octobre 2004.
- (en) Revealing the dawn of photosynthesis, New Scientist, 19 August 2006
- (en) Tanai Caredona, « Early Archean origin of heterodimeric Photosystem I », Heliyon, vol. 4, no 3, , e00548 (PMID 29560463, PMCID 5857716, DOI 10.1016/j.heliyon.2018.e00548, lire en ligne, consulté le ).
- (en) Victoria Howard, « Photosynthesis Originated A Billion Years Earlier Than We Thought, Study Shows », sur Astrobiology Magazine, (consulté le ).
- The evolution of plate tectonics. Robert J. Stern. One contribution of 14 to a discussion meeting issue ‘Earth dynamics and the development of plate tectonics’. Published by the Royal Society.
- (en) Craig O'Neill, Simon Turner, Tracy Rushmer, The inception of plate tectonics: a record of failure, 1 octobre 2018. One contribution of 14 to a discussion meeting issue ‘Earth dynamics and the development of plate tectonics’. Royal Society.
- The growth of continental crust. FrancisAlbarède. Tectonophysics, Volume 296, Issues 1–2, 30 octobre 1998, Pages 1-14.
- François Ramade, Introduction à l'écochimie, Lavoisier, , p. 41.
- Genèse et Origine de la Croûte Continentale. Christian Nicollet,
- When crust comes of age: on the chemical evolution of Archaean, felsic continental crust by crustal drip tectonics. O. Nebel, F. A. Capitanio, [...], and P. A. Cawood. Phil.Trans. R. Soc. A376: 20180103.http://dx.doi.org/10.1098/rsta.2018.0103.
- The evolving nature of terrestrial crust from the Hadean, through the Archaean, into the Proterozoic. Balz S.Kamber. Precambrian Research, Volume 258, March 2015, Pages 48-82.
- . Ross Taylor, Scott M. McLennan, The Evolution of Continental Crust, Scientific American, 1 juillet 2005.
- Statistical geochemistry reveals disruption in secular lithospheric evolution about 2.5 Gyr ago. Keller, C., Schoene, B. Nature 485, 490–493 (2012) doi:10.1038/nature11024
- (en) [PDF]Constraining the climate and ocean pH of the early Earth with a geological carbon cycle model, Krissansen-Totton et al., PNAS Direct Submission, .
- Carbon dioxide cycling and implications for climate on ancient Earth. Sleep NH, Zahnle K (2001). J Geophys Res Planets 106:1373–1399.
- Electrons, life and the evolution of Earth's oxygen cycle. Paul G Falkowski, Linda V Godfrey. Philos Trans R Soc Lond B Biol Sci. 2008 Aug 27; 363(1504), p. 2705–2716.
- The relative influences of nitrogen and phosphorus on oceanic primary production. Tyrrell, T. Nature, 400, p. 525–531 (1999).
- Phanerozoic atmospheric oxygen, Berner et al., Annual Review of Earth and Planetary Sciences, Vol. 31:105-134 (May 2003).
- (en) Paul G. Falkowski, Richard T. Barber, Victor Smetacek. Biogeochemical Controls and Feedbacks on Ocean Primary Production, Science, 10 juillet 1998, vol. 281, n° 5374, p. 200-206.
- (en) Garcia-Vallvé S, Romeu A, Palau J, « Horizontal gene transfer in bacterial and archaeal complete genomes », Genome research, vol. 10, no 11, , p. 1719-25 (PMID 11076857, lire en ligne).
- Katerina Stamati, Vivek Mudera et Umber Cheema, Evolution of oxygen utilization in multicellular organisms and implications for cell signalling in tissue engineering, J. Tissue Eng., 2011, 2(1).
- Cyanobacteria and the Great Oxidation Event: evidence from genes and fossils. Schirrmeister, Gugger & Donoghue. Palaeontology, the online library, juin 2015.
- Evolution of multicellularity coincided with increased diversification of cyanobacteria and the Great Oxidation Event. Bettina E. Schirrmeister, Jurriaan M. de Vos, Alexandre Antonelli, and Homayoun C. Bagheri. PNAS January 29, 2013 110, 5, p. 1791-1796.
- Colin Goldblatt, Timothy M. Lenton & Andrew J. Watson, Bistability of atmospheric oxygen and the Great Oxidation, Nature volume 443, pages : 683–686 (2006).
- (en) Preston Cloud, Beginnings of Biospheric Evolution and Their Biogeochemical Consequences, Paleobiology, Vol. 2, No. 4 (Autumn, 1976), pp. 351-387.
- Sarah Derouin, Did Bacterial Enzymes Cap the Oxygen in Early Earth’s Atmosphere?, Earth & Space Science News, 25 septembre 2019.
- Timothy W. Lyons, Christopher T. Reinhard, & Noah J. Planavsky., The rise of oxygen in Earth’s early ocean and atmosphere, Nature, Vol 506, Février 2014.
- Une vie complexe il y a 2 milliards d’années : l’hypothèse se confirme ! futura-sciences.com, 26 Juin 2014.
- (en) Guochun Zhao, M. Sun, Simon A. Wilde et S.Z. Li, « A Paleo-Mesoproterozoic supercontinent: assembly, growth and breakup », Earth-Science Reviews, vol. 67, , p. 91-123.
- Viral evolution : Primordial cellular origins and late adaptation to parasitism. Arshan Nasir, Kyung Mo Kim & Gustavo Caetano-Anollés (2012), Mobile Genetic Elements, 2:5, 247-252, DOI: 10.4161/mge.22797.
- The Origin of Mitochondria. William F. Martin, Ph.D. Nature Education 3(9):58.
- (en) Nicholas J. Butterfield, « Bangiomorpha pubescens n. gen., n. sp.: implications for the evolution of sex, multicellularity, and the Mesoproterozoic/Neoproterozoic radiation of eukaryotes », Paleobiology, vol. 26, no 3, , p. 386-404 (DOI 10.1666/0094-8373(2000)026<0386:BPNGNS>2.0.CO;2).
- A Complex Hierarchy of Avoidance Behaviors in a Single-Cell Eukaryote.
- Asteroid shower on the Earth-Moon system immediately before the Cryogenian period revealed by KAGUYA. Terada, K., Morota, T. & Kato, M. Nat Commun 11, 3453 (2020).
- (en) A.G. Smith, « Neoproterozoic timescales and stratigraphy », Geological Society, London, Special Publications, vol. 326, , p. 27–54 (DOI 10.1144/SP326.2, Bibcode 2009GSLSP.326...27S).
- (en) M. L. Droser et J. G. Gehling, « Synchronous Aggregate Growth in an Abundant New Ediacaran Tubular Organism », Science, vol. 319, no 5870, , p. 1660–1662 (PMID 18356525, DOI 10.1126/science.1152595, Bibcode 2008Sci...319.1660D, lire en ligne).
- (en) Guy Narbonne, « The Origin and Early Evolution of Animals », Department of Geological Sciences and Geological Engineering, Queen's University, (consulté le ).
- (en) Adolf Seilacher, « Vendobionta and Psammocorallia: lost constructions of Precambrian evolution », Journal of the Geological Society, Londres, vol. 149, no 4, , p. 607–613 (DOI 10.1144/gsjgs.149.4.0607, lire en ligne, consulté le ).
- Jennifer F. Hoyal Cuthill et Jian Han, Cambrian petalonamid Stromatoveris phylogenetically links Ediacaran biota to later animals, 2018. DOI 10.1111/pala.12393.
- (en) Richard K. Bono, John A. Tarduno, Francis Nimmo et Rory D. Cottrell, « Young inner core inferred from Ediacaran ultra-low geomagnetic field intensity », Nature Geoscience, vol. 12, no 2, , p. 143–147 (ISSN 1752-0908, DOI 10.1038/s41561-018-0288-0, lire en ligne [PDF], consulté le ).
- (en) Peter Driscoll, « Geodynamo recharged », Nature Geoscience, vol. 12, no 2, , p. 83–84 (ISSN 1752-0908, DOI 10.1038/s41561-019-0301-2, lire en ligne, consulté le ).
- (en) Timothy M. Lenton, Michael Crouch Martin Johnson, Nuno Pires, Liam Dolan, First plants cooled the Ordovician., Nature Geoscience. Band 5, 2012, S. 86–89, doi:10.1038/ngeo1390,
- (en) « Tiny Algae May Have Prompted a Mass Extinction », sur Eos (consulté le ).
- (en) Jiaheng Shen, Ann Pearson, Gregory A. Henkes, Yi Ge Zhang, Kefan Chen et al., « Improved efficiency of the biological pump as a trigger for the Late Ordovician glaciation », Nature Geoscience, vol. 11, , p. 510-514 (DOI 10.1038/s41561-018-0141-5).
- (en) J. John Sepkoski Jr., A factor analytical description of the Phanerozoic marine fossil record, Paleobiology, v. 7, 1981, p. 36–53
- (en)Raup, D. M. and J. John Sepkoski Jr., Mass extinctions in the marine fossil record, Science, 215, 1982, [PDF] p. 1501-1503.
- (en) Antonio Quesada, Warwick F. Vincent, David R. S. Lean, Community and pigment structure of Arctic cyanobacterial assemblages: the occurrence and distribution of UV-absorbing compounds ; FEMS Microbiology Ecology, volume 28, no 4, avril 1999, pages 315-323 (résumé)
- The Proterozoic Biosphere: A Multidisciplinary Study. J. William Schopf, Cornelis Klein. Cambridge University Press, juin 1992.
- (en) Jennifer M. Robinson, « Lignin, land plants, and fungi: Biological evolution affecting Phanerozoic oxygen balance », Geology, vol. 18, no 7, , p. 607-610 (DOI 10.1130/0091-7613(1990)018<0607:LLPAFB>2.3.CO;2, résumé).
- (en) Robert A. Berner, « Atmospheric oxygen over Phanerozoic time », PNAS, vol. 96, no 20, , p. 10955-10957 (lire en ligne).
- (en) Timothy M. Lenton, « The role of land plants, phosphorus weathering and fire in the rise and regulation of atmospheric oxygen », Global Change Biology, vol. 7, no 6, , p. 613-629 (DOI 10.1046/j.1354-1013.2001.00429.x).
- (en) D. Floudas et al., The Paleozoic Origin of Enzymatic Lignin Decomposition Reconstructed from 31 Fungal Genomes Science, 336, 2012, 1715, (résumé).
- David Garon et Jean-Christophe Guéguen, Biodiversité et évolution du monde végétal, EDP Sciences, , p. 166.
- Pauline Gravel, « Sciences - Le mystère de la grande extinction enfin élucidé », Le Devoir, .
- (en) Stephen E. Grasby, Hamed Sanei et Benoit Beauchamp, « Catastrophic dispersion of coal fly ash into oceans during the latest Permian extinction », Nature Geoscience, vol. 4, , p. 104–107 (DOI 10.1038/ngeo1069, lire en ligne).
- (en) Alexandra Witze, « Acidic oceans linked to greatest extinction ever : Rocks from 252 million years ago suggest that carbon dioxide from volcanoes made sea water lethal », Nature, (lire en ligne).
- (en) M. J. Benton, When Life Nearly Died : The Greatest Mass Extinction of All Time, Thames & Hudson, , 336 p. (ISBN 978-0-500-28573-2).
- (en) D. H. Erwin, The great Paleozoic crisis; Life and death in the Permian, Columbia University Press, (ISBN 0-231-07467-0).
- Ancient shell shows days were half-hour shorter 70 million years ago. AGU 100 news, 9 March 2020.
- Jared Diamond, Le troisième chimpanzé, Folio Essais, p.40-45, (ISBN 978-2-07-044133-4).
- (en) Kerry Sieh et al, {https://www.pnas.org/content/early/2019/12/24/1904368116 Australasian impact crater buried under the Bolaven volcanic field, Southern Laos], PNAS, 30 décembre 2019.
Voir aussi
Bibliographie
- Christian Grataloup, Atlas historique de la Terre et de son usage par les Humains, Les Arènes, 2022, 340 p. (ISBN 979-10-375-0718-1)
- Vera M. Kolb, Handbook of Astrobiology. CRC Press, .