Grande Oxydation
La Grande Oxydation ou Grande Oxygénation[1] (Great Oxygenation Event en anglais, ou GOE), également appelée catastrophe de l'oxygène ou crise de l'oxygène, est un événement majeur qui s'est produit dans l'atmosphère terrestre, les eaux de surface et la biosphère il y a environ 2,4 à 2 milliards d'années (Ga), au Paléoprotérozoïque : le dioxygène, ou oxygène libre (non combiné à d'autres éléments comme dans CO2), est devenu un constituant notable de l'atmosphère, il s'est accumulé à l'état dissous dans les eaux, une majeure partie des sols se sont oxydés, et les organismes vivants ont dû s'adapter à ces nouvelles conditions[2] - [3].
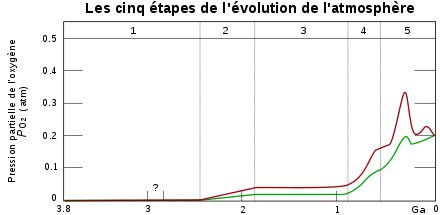 Évolution de la concentration en dioxygène de l'atmosphère terrestre (limite haute en rouge, basse en vert). Échelle horizontale : âge en milliards d'années. | ||
| Phase | Période (Ga) | Caractéristiques |
| 1 | 3,85–2,45 | Pas de production de dioxygène. |
| 2 | 2,45–1,85 | La production de dioxygène est absorbée par les océans et les fonds marins. |
| 3 | 1,85–0,85 | Les océans dégagent du dioxygène mais il est absorbé par les terres. Constitution de la couche d'ozone. |
| 4 et 5 | 0,85–0,54 0,54–présent | Les puits d'oxygène sont saturés et le dioxygène s'accumule dans l'atmosphère. |
Le dioxygène, libéré dans l'eau de mer par le métabolisme des organismes photosynthétiques (principalement les cyanobactéries), a d'abord réagi avec les composés réducteurs présents en surface (méthane CH4, sels et minéraux ferreux). Il a commencé à s'accumuler quand ces « puits de l'oxygène » sont venus à saturation. L'oxygène libre était probablement un poison pour les premiers organismes vivants, comme il l'est encore aujourd'hui pour une majeure partie des organismes anaérobies : ils ont d'abord dû développer des mécanismes pour s'en protéger, ensuite sont apparus des organismes aérobies — aujourd'hui majoritaires — pour lesquels le dioxygène est devenu indispensable (respiration). Les organismes photosynthétiques ont également dû adapter leur métabolisme car le dioxygène diminue l'efficacité de la Rubisco, l'enzyme-clé de la photosynthèse. La Grande Oxydation n'est donc pas qu'un événement chimique affectant la surface terrestre, c'est aussi une crise écologique majeure, sans doute la première de l'histoire du vivant.
Évolution du cycle de l'oxygène
Orange : glaciation
Voir aussi : la frise chronologique de l'Univers et Histoire de la Terre
La compréhension de ces évènements nécessite de connaître certaines bases de physiologie : les êtres vivants élaborent des structures basées sur le carbone — qu'il s'agisse de courtes chaînes cycliques (glucides = sucres), ou de longues chaînes plus ou moins complexes (lipides = graisses), ou encore des composés carbonés comportant un groupe azoté (protéines, formées de chaînes d'acides aminés). Dans tous les cas, il s'agit d'assemblages d'atomes de carbone. Les organismes responsables de l'oxygénation tirent leur carbone des molécules de dioxyde de carbone (CO2) extraites de l'atmosphère, l'énergie nécessaire provenant de la lumière solaire (photosynthèse). Chaque réaction de fixation d'un atome de carbone supplémentaire libère une molécule de dioxygène (O2), qui n'est donc pour ces organismes vivants (cyanobactéries) qu'un déchet toxique.
Ces organismes primitifs éliminaient ce dioxygène dans les océans, celui-ci réagissait avec les composés de l'océan, principalement avec les métaux comme le fer ferreux pour précipiter en hématite et magnétite, ce qui limitait les possibilités de vie à la prolifération des seuls organismes anaérobies. Ce n'est plus le cas vers −2,4 Ga : après l'épuisement du fer ferreux marin, le dioxygène s'est alors répandu des océans à l'atmosphère, déclenchant une crise écologique en raison de sa toxicité pour les organismes anaérobies de l'époque qui le produisent.
La fluctuation de la teneur d'un autre métal dissous dans l'eau de mer pourrait être à l'origine de la Grande Oxydation. Une étude de 2009 montre une chute brutale des teneurs en nickel dissous dans l'eau de mer à une période estimée entre 2,7 et 2,4 Ga[4]. L'origine de cette baisse considérable — la teneur était alors 400 fois supérieure à ce qu'elle est aujourd'hui — n'est pas bien expliquée, peut-être liée au refroidissement et à la solidification du manteau terrestre. Cette chute des teneurs en nickel serait responsable de la quasi-disparition de micro-organismes (archéobactéries) méthanogènes qui proliféraient dans ces eaux enrichies en nickel (épisode surnommé la « famine du nickel »). Leur quasi-disparition a laissé la place à des algues et autres organismes producteurs d'oxygène par photosynthèse, responsables de la Grande Oxydation[4] - [5].
De plus, l'oxygène libre réagit avec le méthane atmosphérique (ce gaz étant à cette époque, avec le dioxyde de carbone, à l'origine de l'effet de serre), déclenchant ainsi la glaciation huronienne entre 2,4 et 2,1 Ga, probablement le plus long épisode boule de neige de la Terre. Après cette glaciation, la fonte des glaces provoque un lessivage des continents, ce qui apporte des éléments nutritifs dans les océans, favorisant le développement des cyanobactéries photosynthétiques à l'origine de l'accélération considérable de l'augmentation de la concentration d’oxygène dans l'atmosphère terrestre : la concentration en oxygène de l’air augmente rapidement, en deux cents millions d'années, pour atteindre vers −2,1 Ga d'années un seuil de 4 % qui voit l'émergence de la vie multicellulaire aérobie.
De plus, cet oxygène libre est à l'origine de la formation de la couche d'ozone qui a pour effet d'absorber la plus grande partie du rayonnement solaire ultraviolet, autorisant l'accroissement de la biodiversité.
Ainsi, la vie aérobie (utilisant l'oxygène atmosphérique libre), actuellement majoritaire, résulte de l'adaptation de la vie primitivement anaérobie à un environnement qu'elle a rendu toxique.
Modèles et théories
Ce modèle a été précisé en 2013 : la concentration d’oxygène dans l'atmosphère terrestre montre des fluctuations et une dynamique « en yoyo » entre 2,3 et 1,8 Ga pour chuter au cours du Mésoprotérozoïque 1,8 et 1,6 Ga à un taux de 0,1 % de la teneur actuelle[6] - [7], qui perdure pendant un milliard d'années, cette période voyant le développement uniquement de bactéries qui laissent peu de traces fossiles. Ce milliard (d'années) est nommé par les scientifiques britanniques « le milliard ennuyeux » (the boring billion, par l'absence de fossiles) et après cette période vers 600-700 millions d’années (glaciation Varanger à l'époque du Cryogénien), l'atmosphère terrestre connaît à nouveau une importante augmentation d'oxygène jusqu'à nos jours[8], où le taux est de 20,9 %.
Notes et références
Références
- « L'histoire de l'univers », sur Futura (consulté le ).
- Yves Sciama, « Elles ont façonné la Terre », Science et Vie, hors-série no 261, , p. 21 (ISSN 0151-0282).
- Christian de Duve (trad. Anne Bucher et Jean-Mathieu Luccioni), Poussière de vie : Une histoire du vivant, Paris, Fayard, , 588 p. (ISBN 978-2-213-59560-3).
- (en) Kurt O. Konhauser et al., « Oceanic nickel depletion and a methanogen famine before the Great Oxidation Event », Nature, vol. 458, no 7239, , p. 750–753 (PMID 19360085, DOI 10.1038/nature07858, Bibcode 2009Natur.458..750K)
- (en) Cynthia Graber, « Breathing Easy Thanks to the Great Oxidation Event », sur Scientific American (consulté le ).
- « L’effet « yoyo » de l’oxygène atmosphérique il y a 2,3 à 2 milliards d’années, décisif pour la vie sur Terre », sur INSU (consulté le )
- « Découverte scientifique majeure par l’analyse des sédiments du bassin de Franceville au Gabon », sur La France au Gabon et à São Tomé et Principe (consulté le )
- (en) Donald E. Canfielda, Lauriss Ngombi-Pembab, Emma U. Hammarlunda, Stefan Bengtsonc, Marc Chaussidond, François Gauthier-Lafayee, Alain Meunierb, Armelle Riboulleauf, Claire Rollion-Bardd, Olivier Rouxelg, Dan Asaelg, Anne-Catherine Pierson-Wickmannh et Abderrazak El Albani, « Oxygen dynamics in the aftermath of the Great Oxidation of the Earth’s atmosphere », Proceedings of the National Academy of Sciences, vol. 110, no 42, , p. 16736-16741 (DOI 10.1073/pnas.1315570110)