Réducteur (chimie)
En chimie, un réducteur est un corps simple, un composé ou un ion qui cède au moins un électron à une autre espèce chimique lors d'une réaction d'oxydoréduction[1]. Le réducteur ayant perdu au moins un électron au cours de cette réaction est dit oxydé, tandis que l'espèce chimique qui a reçu au moins un électron est dite réduite[2]. Un réducteur est généralement proche de son état d'oxydation le plus faible — historiquement, la réduction correspondait à l'élimination de l'oxygène d'une substance — et se comporte par conséquent comme un donneur d'électron.
Exemples
Les substances suivantes sont des exemples de réducteurs :
- les non-métaux tels que l'hydrogène et le carbone ;
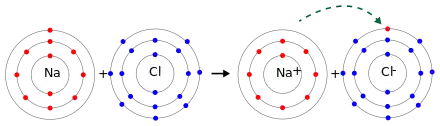
- les métaux tels que les métaux alcalins (lithium, le sodium ou le potassium), le magnésium, l'aluminium ou le zinc ;
- les hydrures tels que le borohydrure de lithium LiBH4, le tétrahydruroborate de sodium NaBH4, l'hydrure de sodium NaH ou l'hydrure de calcium CaH2 ;
- les sels et les composés moléculaires tels que le sulfite de sodium Na2SO3, le dithionite de sodium Na2S2O4, le thiosulfate de sodium Na2S2O3 ou l'hydrazine N2H4 ;
- les aldéhydes.
Ainsi, dans la réaction globale de la respiration cellulaire aérobie :
l'oxygène O2 est réduit, et est l'oxydant de cette réaction ; le glucose C6H12O6 est quant à lui oxydé, c'est le réducteur de cette réaction.
En chimie minérale, la réduction désigne plus spécifiquement l'addition d'hydrogène à une molécule ; ainsi, le benzène peut être réduit en cyclohexane en présence d'un catalyseur de platine :
En chimie organique, un bon réducteur est un réactif qui fournit de l'hydrogène. Les oses qui possèdent une fonction aldéhyde –CHO, sont appelés aldoses et sont des oses réducteurs, de même que certains diholosides et polyholosides qui en contiennent ; le ribose, le glucose, le maltose sont ainsi des composés réducteurs, contrairement par exemple au saccharose ou au tréhalose.
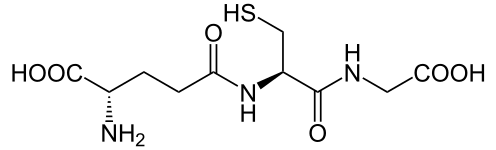
En biochimie, les biosynthèses utilisent comme cofacteurs des réducteurs tels que le NADH, le NADPH, le FADH2 ou encore la coenzyme QH2. Les antioxydants sont souvent des réducteurs qui neutralisent les effets des substances les plus oxydantes susceptibles d'endommager les cellules, par exemple au cours du stress oxydant ; les thiols tels que le glutathion, ou encore l'acide ascorbique (vitamine C), la vitamine A et les vitamines E sont des exemples d'antioxydants agissant comme réducteurs au sein des cellules vivantes.
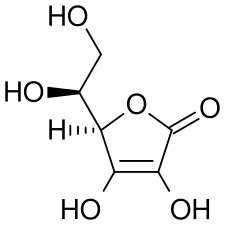 Acide ascorbique
Acide ascorbique
(réducteur).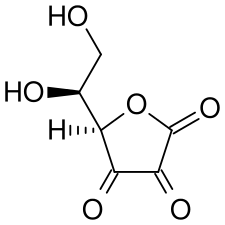 Acide déshydroascorbique
Acide déshydroascorbique
(forme oxydée).
Références
- « La réaction d'oxydoréduction », sur alloprof.qc.ca (consulté le ).
- « Oxydant et réducteur », sur StudySmarter (consulté le ).