Ammoniac
L'ammoniac est un composé chimique de formule NH3 (du groupe générique des nitrures d'hydrogène). Dans les conditions normales de température et de pression, c'est un gaz noté NH3 gaz[22]. Il est incolore et irritant, d'odeur piquante à faible dose ; il brûle les yeux et les poumons en concentration plus élevée.
| Ammoniac | |
  Molécule d'ammoniac. |
|
| Identification | |
|---|---|
| Nom UICPA | azane |
| Synonymes |
nitrure d'hydrogène |
| No CAS | |
| No ECHA | 100.028.760 |
| No CE | 231-635-3 |
| No RTECS | BO0875000 |
| PubChem | |
| ChEBI | 16134 |
| FEMA | 4494 |
| SMILES | |
| InChI | |
| Apparence | gaz comprimé liquéfié, incolore à légèrement coloré, d'odeur âcre, intense, suffocante, irritante[2]. |
| Propriétés chimiques | |
| Formule | NH3 |
| Masse molaire[3] | 17,030 5 ± 0,000 4 g/mol H 17,76 %, N 82,25 %, |
| pKa | 9,23 |
| Moment dipolaire | 1,471 8 ± 0,000 2 D[4] |
| Diamètre moléculaire | 0,310 nm[5] |
| Propriétés physiques | |
| T° fusion | −77,7 °C[6], −77,74 °C |
| T° ébullition | −33,35 °C[6] |
| Solubilité | dans l'eau à 20 °C : 540 g l−1[2], dans l'alcool soit 14,8 g pour 100 g d'alcool à 95° à 20 °C, l'éther éthylique et les solvants organiques |
| Paramètre de solubilité δ | 33,4 MPa1/2 (25 °C)[7]; 29,2 J1/2 cm−3/2 (25 °C)[5] |
| Masse volumique | 0,86 kg/m3 (1,013 bar, point d'ébullition) 0,769 kg/m3 (CNTP)[8] |
| T° d'auto-inflammation | 651 °C[2] |
| Limites d’explosivité dans l’air | Inférieure : 15,5 (Weiss, 1985) Supérieure : 27 (Weiss, 1985) |
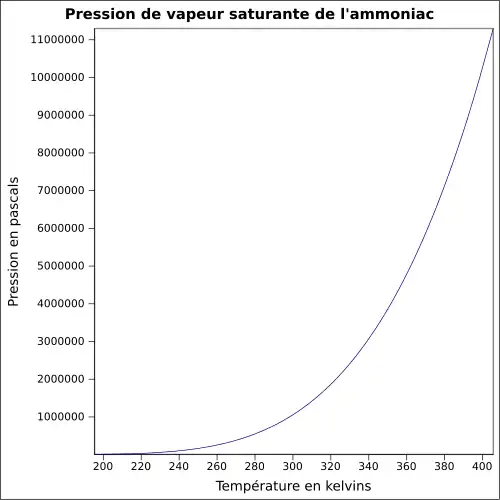
| Pression de vapeur saturante | à 26 °C : 1 013 kPa[2]
|
| Point critique | 112,8 bar, 132,35 °C[12] |
| Thermochimie | |
| S0gaz, 1 bar | 192,77 J mol−1 K−1 |
| ΔfH0gaz | −39,222 kJ·mol-1 (−273,15 °C) −46,222 kJ·mol-1 (24,85 °C)[6] |
| ΔfH0liquide | −40,2 kJ/mol |
| ΔvapH° | 23,33 kJ mol−1 (1 atm, −33,33 °C) 19,86 kJ mol−1 (1 atm, 25 °C)[13] |
| Cp | 2 097,2 J·kg-1·K-1 (0 °C) 2 226,2 J·kg-1·K-1 (100 °C) |
| PCS | 382,8 kJ·mol-1 (25 °C, gaz)[14] |
| PCI | 317,1 kJ mol−1[15] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 10,070 ± 0,020 eV (gaz)[16] |
| Cristallographie | |
| Symbole de Pearson | [17] |
| Classe cristalline ou groupe d’espace | P213 (n° 198)[17] |
| Strukturbericht | D1[17] |
| Structure type | NH3[17] |
| Propriétés optiques | |
| Indice de réfraction | 1,325[5], même valeur pour l'ammoniac liquide à 16,5 °C sous pression |
| Précautions | |
| SGH[18] - [19] | |
     Danger |
|
| SIMDUT[20] | |
    A, B1, D1A, E, |
|
| NFPA 704 | |
| Transport | |
| Inhalation | Les vapeurs sont très irritantes et corrosives. |
| Peau | Les solutions concentrées peuvent provoquer des brûlures. |
| Yeux | Dangereux, Irritation |
| Ingestion | L'ingestion peut provoquer des brûlures de la bouche, langue, œsophage. |
| Écotoxicologie | |
| Seuil de l’odorat | bas : 0,04 ppm haut : 53 ppm[21] |
| Unités du SI et CNTP, sauf indication contraire. | |
Il est industriellement produit par le procédé Haber-Bosch à partir de diazote et de dihydrogène. C'est l'un des composés les plus synthétisés au monde, utilisé comme réfrigérant, et pour la synthèse de nombreux autres composés (dont un grand tonnage d'engrais). C'est aussi un solvant liquide en usage pur, à 20 °C et 8 bar, soit NH3 liquide.
L'auto-ionisation de l'ammoniac liquide est très faible, caractérisée par une constante de dissociation ionique Ki = [NH4+] [NH2−] qui vaut environ 10−33 mol2 l−2 à −50 °C.
Dans le solvant protique NH3 liquide, le cation ammonium NH4+ est l'acide le plus fort alors que l'anion amide NH2− est la base la plus forte.
Son doublet électronique en fait à la fois une base, un nucléophile, un ligand et un réducteur[23]. Sa propriété basique le rend utile pour divers sels d'ammonium. Ses propriétés de nucléophile en font un réactif de base en chimie organique pour la préparation des amides, des imides, etc. Ses propriétés de ligand sont connues depuis le début de la chimie de coordination et le fameux débat scientifique entre Sophus Mads Jørgensen et Alfred Werner, qui attira l'attention du jury du prix Nobel, décerné à ce dernier en 1913. Enfin, sa propriété de réducteur lui permet d'être industriellement oxydé en acide nitrique et en hydrazine notamment, deux produits industriels de fort tonnage.
En génie chimique, le système (air - NH3 - eau) constitue un modèle très étudié de phases liquide-gaz, puisque l'ammoniac est un gaz très soluble dans l'eau, avec une solubilité de 89,9 g pour 100 g d'eau à 0 °C et seulement 7,4 g à 96 °C. Le gaz est soluble dans l'eau, sous forme de NH3 aqueux faiblement dissocié en cations ammonium et anions hydroxyle, cette solution aqueuse est nommée ammoniaque[24].
Physiologiquement, il joue un rôle majeur en agriculture ; c'est via l'ammoniac que l'azote est artificiellement incorporé par les plantes. Chez l'animal, il est impliqué dans l'élimination de l'azote du corps et la régulation du pH sanguin.
Sur terre il est essentiellement piégé dans l'écorce terrestre (sels ammoniacaux minéraux tels que bicarbonates, nitrates, nitrites, chlorures, phosphates, etc.) ou dans la matière organique (charbon, tourbe, pétrole)… En excès dans l'air, c'est un polluant acidifiant et eutrophisant de l'environnement. Après une amélioration de 1990 à 2011[25], ses teneurs dans l'air, maintenant suivies par satellite, sont reparties à la hausse en Europe et en France, en raison essentiellement des pratiques agricoles plus industrielles (donnée 2016)[26]. En ville et sur les axes de transport il est issu du trafic routier pour 40 à 60 %[27], mais à échelle du pays, en 2011, il provient à 94 % des émissions de NH3[28] d'origine agricole. L'élevage via les fumiers et lisiers en est la 1re source[29] - [30]. Sa teneur dans l'air devrait être infime (hormis en présence d'excréments ou urines en décomposition, d'une fermentation par des micro-organismes en milieu confiné ou d'une putréfaction en milieu anaérobie).
Histoire
Le mot ammoniac, attesté au XIVe siècle, vient du latin ammoniacum, lui-même issu du grec ancien : ἀμμωνιακόν, « sel ammoniac ou gomme ammoniaque »[31], qui évoquait le nom du dieu égyptien Amon (car en Libye, c'est près du temple de Jupiter Ammon qu'on extrayait un minéral[32] (salmiac) pouvant libérer de l'ammoniac). Cet alcali était en outre, dans l'Antiquité, produit en chauffant des excréments frais ou un mélange de sel et d'urines. On pouvait le sentir et on savait utiliser son action alcaline sur d'autres matières (au moins dès la XIIe dynastie égyptienne soit 2 000 ans av. J.-C.). Mais comme toute matière gazeuse, il est resté longtemps mal compris.
Au Moyen Âge, les forgerons obtenaient cet alcali d'Amôn par distillation de cornes et de sabots de bœufs (matières riches en azote).
Le chimiste britannique Robert Boyle invente des tests de détection de cet alcali gazeux (teinture de tournesol ou sirop de violette virant au bleu en présence de ce gaz)[33].
Un siècle plus tard environ, avec l'essor de la pneumochimie à cuve à mercure, sa préparation et son isolement sont facilités par Joseph Priestley en 1774, par simple chauffage de sels d'ammonium avec de la chaux CaO ou du calcaire comme pierre à chaux ; avec une cuve à eau, on obtient, par piégeage dans l'eau de la cuve, de l'ammoniaque ou eau ammoniaquée.
En 1785, le chimiste Berthollet confère à ce corps chimique une formule de un azote pour trois hydrogènes.
À partir des années 1850, le cycle de l'azote commence à être perçu : on comprend notamment que l'ammoniac atmosphérique peut être directement absorbé et utilisé par les plantes : De Ville (1850) et Schlösing (1874) exposent des plantes jusque-là maintenues en déficit d'azote à un air enrichi en ammoniac et ils montrent qu'elles peuvent l'absorber et le métaboliser[34] - [35]. À la même époque, Boussingault (1856) montre le rôle fondamental des nitrates[36] alors que l'on commence à mesurer les dépôts d'ammonium (NH4+) dans les précipitations (environ 5 kg N-NH4+ par hectare et par an selon Lawes et Gilbert au milieu du XIXe siècle (1851)[37]. Peu après, Bineau (1854) piège (dans un « piège acide ») et mesure les dépôts secs d'ammoniac à partir de l'air ambiant de Caluire et à Lyon : 15 à 50 kg N-NH3 par hectare et par an[38]. De la même manière, Heinrich (1881) à Rostock[39] (Allemagne), Kellner et al. (1886) à Tokyo[40], mesurent respectivement des dépôts de 31 et 12 kg N-NH3 par hectare et par an. Puis Hall et Miller (1911) ont l'idée de protéger leur piège à ammoniac des poussières et insectes par une fine grille (ce qui a pu leur faire sous-estimer les dépôts secs, note Loubet dans sa thèse en 2000[41]) et de disposer de tels pièges à différentes hauteurs, ce qui leur a permis de mettre en évidence des gradients de « concentration » au-dessus de la végétation et de repérer des zones « puits » (non fertilisées) et des zones sources (émissions probablement au-dessus de zones fertilisées)[42].
Plus tard, les physiciens constateront le mouvement d'oscillation de la molécule NH3 gaz, où l'azote passe entre la base triangulaire formée par les trois H pour atteindre sa double position en sommet de l'agencement pyramidal[43]. Ce mouvement oscillant régulier de la molécule d'ammoniac est à l'origine de la première horloge atomique, du Bureau of stantards aux États-Unis en 1948.
Après la Seconde Guerre mondiale, le développement de l'agriculture industrielle et productiviste relance les études sur la perte d'azote à partir d'engrais organiques (minéralisation) et d'engrais chimiques (lessivage des nitrates, perte qui est source d'un coûteux gaspillage d'engrais, et d'une pollution croissante et générale des nappes phréatiques ainsi que d'une eutrophisation des eaux de surface dont on ne s'alarmera que bien plus tard). Allison (1955) démontre que la volatilisation de nitrates a par le passé été sous-estimée. Ces pertes font encore l'objet de recherche (ex. : Whitehead et Raistrick, 1990[44]).
Histoire sémantique
Le terme d'origine adjectivale ammoniac qualifiait autrefois[45] une substance médicinale, la gomme ammoniaque, utilisée par les apothicaires, présentée comme suit en 1752 par le Dictionnaire français-latin de Trévoux :
« Ammoniac ; une gomme dont on se sert en Pharmacie. Gummi ammoniacum. On nous l'apporte des Indes Orientales, & on croit qu'elle découle d'une plante umbellifére. Elle doit être en larmes séches, blanchâtres en dedans, un peu roussâtres en dehors, faciles à se fondre, gommeuses & résineuses, un peu amères, d'une odeur & d'un goût acre, tenant de l'ail. On en apporte aussi en masses remplies de petites larmes bien nettes & bien blanches. Cette gomme roussit en vieillissant ; Dioscoride & Pline en font mention. Dioscoride dit que l'ammoniac est le jus d'une espèce de férule qui croît en Afrique auprès de Cirène de Barbarie. La plante qui le porte, & sa racine, s'appellent Agafillis. Le bon ammoniac est haut en couleur, & n'est brouillé ni de raclure de bois, ni de sable, ni de pierres. Il a force petits grains comme l'encens, retire à l'odeur du castoreum, & est amer au goût (…) Pline appelle l'arbre dont il découle Métopion (…) L'ammoniac des Apoticaires est réduit en masse comme poix résine, au lieu d'être fraisé & menu comme de l'encens. On prétend qu'il servoit d'encens aux Anciens dans leurs sacrifices. Cette gomme entre dans plusieurs compositions ; elle est purgative, fondante, & résolutive, étant appliquée extérieurement. Gafer en tire un esprit & une huile, qui ont, à ce qu'il dit, de grandes vertus, lesquelles ne procèdent que du sel volatile qu'elle contient. Mais comme il est mêlé d'un acide qui empêche son activité, il donne le moyen de séparer ces deux esprits, lesquels sont capables, selon lui, de produire des effets tout différens (…) Il y a un sel qu'on appelle aussi armoniac, ou ammoniac. »
L'adjectif ammoniacque, attesté en 1575 dans les écrits français d'André Thevet, qualifie une gomme ou un sel ammoniac recueillis près du temple d'Amon en Libye[46]. Le « sal ammoniac » est simplement le salmiac purifié, facilement sublimable. La gomme est probablement un mélange de substance végétale molle ou pâteuse contenant du salmiac.
En 1787, Guyton de Morveau introduit dans la nomenclature chimique française le substantif ammoniac, définissant le corps chimique. Le terme ammoniacal, caractérisant les solutions aqueuses d'ammoniac ou ammoniaque, est attesté toutefois vers 1748. Le mot ammonisation, désignant la transformation d'azote organique en azote ammoniacal, est attesté dans le vocabulaire commun par le Grand Larousse de 1933. Aujourd'hui selon la nomenclature IUPAC, l'ammoniac est le plus simple des azanes[47], ou hydrures d'azote acycliques.
Production industrielle


.jpg.webp)

La production industrielle de l'ammoniac se fait essentiellement par synthèse directe à partir de dihydrogène et de diazote. L'hydrogène peut venir du méthane et l'azote de l'air. La mise au point du premier réacteur est l'œuvre de chimistes allemands et est encore secrète lorsqu'elle aboutit en 1913 avec le procédé Haber-Bosch, portant le nom de ses chimistes développeurs du catalyseur à base de fer (Fe) et nickel (Ni) et du procédé en réacteur-tube à une température de 550 °C.
La synthèse de l'ammoniac est exothermique, dégageant 12,9 calories par mole à la pression atmosphérique. Elle implique deux gaz, l'azote et l'hydrogène. Dans les conditions « ambiantes », le produit final se présente sous la forme d'un gaz incolore (produisant une fumée de condensation à haute concentration) et dégageant une très désagréable odeur putride.
La production industrielle d'ammoniac, appelée banalement pour les besoins en engrais, était alors stratégique, car elle était capitale pour l'industrie d'armement et celle conjointe des explosifs, et dépendant alors essentiellement des exportations de nitrates du chili, de facto contrôlées par l'empire maritime britannique[48]. En 1901, la réaction avait été étudié par le chimiste français Le Chatelier, avec un catalyseur à base de Fe, K sur support d'alumine.
Le procédé Haber-Bosch, déjà amélioré au niveau cinétique par une pression modulée jusqu'à plus de 200 atm pendant les années du conflit mondial, est récupéré par les nations alliées victorieuse, en particulier le groupe ONIA à Toulouse[49]. Les groupes chimiques français et italien peuvent investir afin de le modifier et perfectionner sur le continent. Ainsi apparaissent au moins quatre procédés dans l'entre-deux-guerres, attestant la vitalité du secteur des gaz industriels en France :
- le procédé ONIA, fondé sur le procédé Haber-Bosch récupéré mais modifié en un process avec tube à catalyse à 500 °C et 300 atm, en matière réfractaire et avec échangeur-récupérateur de chaleur. Il est à l'origine du procédé NEC des usines Kulhmann, au cours des années 1960 à La Madeleine-lès-Lille[50] ;
- le procédé Georges Claude, ainsi nommé en l'honneur de grand spécialiste français des gaz. Georges Claude perfectionne en 1918 la rentabilité du procédé allemand d'un facteur 15 et comprime le mélange gazeux de 800 à 1 000 bar. De l'usine pionnière de Montereau le procédé sera adapté sur les sites de Saint-Étienne, Béthune, Grand-Quevilly, Mazingarbe. Le mélange est comprimé à 1 000 atm ou 1 000 bar à une température entre 500 °C et 600 °C. Si la rentabilité est excellente, la dépense d'énergie est jugée importante ;
- le procédé Casale, à partir d'une température de mélange réactif abaissée à 460 °C et d'une pression de 400–450 atm, promu dans les années 1960. Il était en vigueur en 1990 à Lens, Hénin-Liétard, Anzin ou Saint-Auban, et son évolution moins gourmande en énergie influence les installations récentes[51] ;
- le procédé Fauser, mis au point en Italie, adopté tardivement par ONIA dans son usine de Soulon, qui se fonde à partir d'un mélange à 250 atm et 550 °C[52].
Le procédé basse pression du Mont-Cenis se caractérise par une pression plus faible de 100 à 150 bar à une température avoisinant 430 °C.
Dès les années 1960, le gaz industriel ammoniac est vendu dans des récipients en acier calibrés à une pression de 12 atm. Par sa chaleur d'évaporation élevée à la température normale de 0 °C, il est nécessaire à l'industrie de la réfrigération.
Depuis les années 1990, la géographie de la synthèse industrielle d'ammoniac est chamboulée par la multiplication de nouvelles unités de productions des dérivés d'ammoniac et d'urée, stimulée par une demande croissante d'engrais chimiques et la volonté de pays producteurs de gaz naturel de l'utiliser, notamment sous forme de production d'ammoniac. En 2000, Trinité-et-Tobago avaient l'unité la plus grosse au monde, mais dès 1998, le golfe Persique, bien placé pour livrer le marché asiatique qui absorbe plus du tiers de la productions mondiale d'ammoniac de l'époque, se dote d'unités à Abu Dhabi de 400 000 tonnes par an, le Qatar de 300 000 tonnes par an, suvi par Oman, etc.
En pratique, le diazote vient de l'air et le dihydrogène du vaporeformage du méthane (gaz naturel), procédé le plus utilisé pour la production d'hydrogène selon les réactions :
Le bilan des réactions est alors :
Production mondiale à partir de H2 et N2 : elle a été estimée à 122 millions de tonnes en 2006. Exprimée le plus souvent en millions de tonnes d'azote N, elle approcherait de 136,5 en 2012[53].
Anciennes méthodes de fabrication modernes
Il a été fabriqué par synthèses indirectes, à partir d'eaux ammoniacales. Ainsi pouvait-il être obtenu par distillation du purin et du fumier. Mais il l'était plus communément à partir de minerai, lors de carbonisation de la houille, voire du coke après 1880 (sous-produit du traitement des gaz de fours à coke).
Au début du XXe siècle, différents procédés de synthèse ont été imaginés.
L'un d'entre eux se base sur l'hydrolyse de la cyanamide calcique, elle-même obtenue à partir du carbure de calcium.
L'autre utilise l'hydrolyse du nitrure d'aluminium, lui-même produit par nitruration à haute température de l'alumine.
Il faudra attendre 1913 pour voir apparaître le procédé Haber-Bosch encore employé au XXIe siècle.
Méthode de fabrication pour l'avenir
L'ammoniac apparait comme un produit qui restera important, et la recherche est active pour de nouveaux procédés. Tous se heurtent à la grande stabilité chimique de la molécule de diazote, qu'il faut activer d'une manière ou d'une autre.
On sait qu'il est possible de réaliser cela sans recourir à des pressions et des températures extrêmes comme dans le procédé Haber-Bosch, puisque des bactéries le font : leurs enzymes nitrogénases catalysent la réduction de N2 en NH3 dans les conditions usuelles de température et de pression. Une des voie de recherche est donc le biomimétisme : la création de catalyseurs reproduisant le fonctionnement des nitrogénases, mais d'une façon industrialisable, par exemple à l'université de Tokyo qui utilise l'iode, le samarium et le molybdène[54] - [55].
Statistiques de production
Production mondiale en millions tonnes en 2021 [56]:
| Pays | Production | % mondial | |
|---|---|---|---|
| 1 | Chine | 39 | 26,0 |
| 2 | Russie | 16 | 10,7 |
| 3 | États-Unis | 15 | 10,0 |
| 4 | Inde | 12 | 8,0 |
| 5 | Indonésie | 5,9 | 4,0 |
| 6 | Arabie saoudite | 4,3 | 2,9 |
| 7 | Trinité-et-Tobago | 4,2 | 2,8 |
| 8 | Égypte | 4,2 | 2,8 |
| 9 | Canada | 3,9 | 2,6 |
| 10 | Iran | 3,6 | 2,4 |
| 11 | Qatar | 3,3 | 2,2 |
| 12 | Pakistan | 3,3 | 2,2 |
| 13 | Ukraine | 2,3 | 1,5 |
| 14 | Allemagne | 2,2 | 1,5 |
| 15 | Algérie | 2,2 | 1,5 |
| ... | Reste du monde | 28,6 | 19,1 |
| TOTAL MONDE | 150 | 100 | |
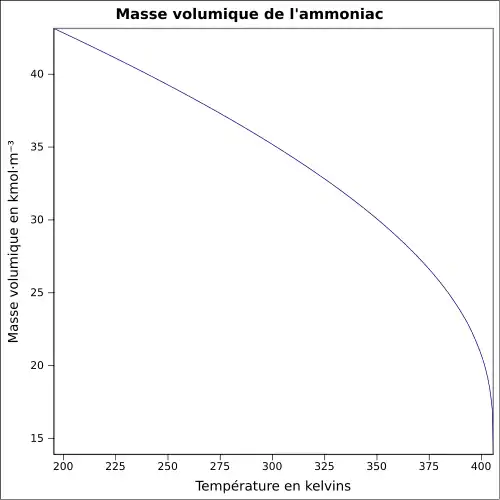
Propriétés physico-chimiques
- Aspects moléculaires et atomiques : l'ammoniac est une molécule pyramidale à base trigonale : l'atome d'azote (N) est au sommet et les trois atomes d'hydrogène (H) occupent les trois coins (sommets) de la base triangulaire équilatérale. Plus précisément, l'atome d'azote « monte » et « descend » entre ce « sommet » de la pyramide et celui de la pyramide opposée, traversant ainsi la base triangulaire des atomes d'hydrogène. Cette « oscillation » s'effectue à une fréquence fondamentale de 24 GHz et a été mise à contribution dans les premières horloges atomiques.
- Transitions de phase : à pression atmosphérique, l'ammoniac se liquéfie à −33,35 °C et se solidifie à −77,7 °C[6]. À haute pression on connaît une phase dite « superionique », dont la courbe de fusion a été déterminée en 2023 : au-dessus de 100 GPa l'ammoniac (superionique) fond à plus basse température que l'eau et sa conductivité électrique est supérieure, ce qui a des implications pour la génération du champ magnétique à l'intérieur d'Uranus et de Neptune[57] - [58].
- Odeur : très âcre et facilement reconnaissable, nocif par inhalation (mortel à hautes doses).
- Inflammabilité et explosibilité : sous forte pression, l'ammoniac peut former un mélange explosif avec les huiles de lubrification, le mélange air-ammoniac s'enflamme et explose violemment, mais la source d'ignition doit être énergétiquement importante.
- Surchauffe de compression : la valeur élevée du rapport α=Cp/Cv = 1,335 à 0 °C limite rapidement le taux de compression admissible du fait des hautes températures des vapeurs de refoulement, températures qui risqueraient au-delà d'une température de 120 °C une altération des huiles de lubrification et la formation d'un mélange détonant.
- Corrosion des métaux, joints et lubrifiants : attaque le cuivre et tous ses alliages, ce pourquoi les installations frigorifiques fonctionnant à l'ammoniac sont réalisées avec des tuyauteries en acier.
- Miscibilité et solubilité : non miscible avec les huiles naphténiques et les huiles de synthèse. Très soluble dans l'eau, il y forme une solution aqueuse dénommée ammoniaque dont l'équilibre chimique est peu dissocié. L'ion ammonium NH4+ en solution comporte alors un atome d'hydrogène aux quatre sommets du tétraèdre. En milieu aqueux, l'acide conjugué de l'ammoniac est l'ion ammonium, ce qui peut s'expliquer par le fait qu'une molécule d'ammoniac ait bien fixé ou capté un proton, dans le cadre de la théorie acide-base de Thomas Lowry et Joannes Brønsted.
- Ammoniac base de Lewis : en 1923, à peine trois années après l'exposition des théories Lowry-Brønsted, le cas particulier de l'ammoniac, muni de son doublet électronique si caractéristique, a motivé les travaux de Gilbert Lewis.
- Ammoniac soluté donneur de proton : en absence d'espèces chimiques comportant des hydrogènes acides (l'eau et les alcools inclus), l'ammoniac peut également perdre un proton, H+, et donner l'ion amidure, NH2−, qui est une base forte.
- Ammoniac liquide, un solvant protique : la gamme de pH mesurable dans l'ammoniac liquide oscille entre 0 et 29. Dans ce solvant spécifique où l'ion amidure est la base la plus forte et l'ion ammonium l'acide le plus fort, l'acide acétique est dissocié totalement, et se comporte comme un acide fort.
L'ammoniac dans l'environnement
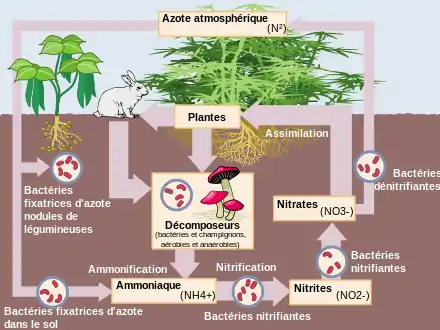

Dans la nature
L'azote est un élément essentiel des acides aminés constitutifs des protéines. Il est donc indispensables à tout être vivant. Bien que constituant 75 % du volume de l'atmosphère, très peu d'êtres vivants savent l'utiliser directement pour biosynthétiser leurs acides aminés. Seuls quelques microbes l'extraient directement de l'air grâce à un enzyme (nitrogénase) ; ce sont notamment des cyanobactéries ou des protéobactéries (ex. : Azotobacter). La plupart des légumineuses, telles que les haricots, trèfles et lupins ont développé des symbioses avec certaines de ces bactéries, qui leur permettent de plus facilement produire des acides aminés et de jouer un rôle de puits d'ammoniac et d'engrais vert. Inversement il existe des puits d'ammoniac, principalement liés à l'absorption d'ammoniac par des bactéries et des plantes et liés à la conversion d'ammoniac en nitrites par des bactéries du genre Nitrosomonas.
Dans l'environnement il est essentiellement présent sous sa forme acide, l'ion ammonium (NH4+), qui est une source d'azote directement assimilable par les plantes. En temps normal il est transformé en nitrites puis en nitrates dans le cycle de l'azote, ce dernier étant la principale voie d'assimilation de l'azote par les plantes. Mais en excès l'azote est source de dystrophisation.
Ammoniac naturel
Il provient essentiellement de la décomposition de l'urée CO(NH2)2 et de l'acide urique qui en dérive (l'urée est le produit ultime de déjection azotée du métabolisme cellulaire animal, par exemple des mammifères, il est produit par des bactéries et des levures, et aussi par certaines plantes via un enzyme : l'uréase. L'ammoniac est ainsi le gaz piquant qui caractérise les caves d'affinage de fromages, notamment les pâtes molles lavées à l'eau salée que sont le maroilles, le munster ou le géromé, soumises à l'action de fermentation bactérienne et à certains enzymes.
Dans la nature, les réactions produisant l'ammoniac se déroulent de manière diffuse dans les eaux douces et marines sur et dans les sols. Dans le monde en volume, 25 à 30 % de tout l'ammoniac naturel proviendrait de l'océan (première source d'ammoniac atmosphérique) puis de la décomposition des urines, excréments et cadavres d'animaux sauvages terrestres, de divers excrétats, phanères, etc. et un peu de certains végétaux). La part des émissions naturelles a fortement diminué dans les pays et régions d'agriculture intensive. Tout comme dans les stations d'épuration et les élevages, l'ammoniac naît de la décomposition de l'urée et de l'acide urique (contenu en grande quantité dans ces excrétats) en ion ammonium NH4++, sous l'action hydrolysante de l'enzyme uréase (aussi présente dans les faeces) ; selon la réaction :
- CO(NH2)2 + 3 H2O → 2 NH4+ + HCO3− + OH−.
En solution (phase liquide), l'ion ammonium est en équilibre avec NH3 (sa base conjuguée, elle-même en équilibre avec NH3 en phase gazeuse). Ces réactions contribuent à une volatilisation de l'ammoniac vers l'atmosphère, plus ou moins rapide selon la température (plus rapide quand il fait chaud et donc en climat tropical) et selon le pH de la solution.
Dans l'atmosphère, après le diazote (N2), la forme la plus présente de l'azote est le gaz NH3 (ammoniac). Il provient aujourd'hui d'abord des engrais chimiques et des parcs d'engraissement de l'élevage industriel, suivis de la combustion de la biomasse fossile (charbon, pétrole, gaz naturel) ou de biomasse parfois (dont via les incendies de forêt)[59]. Il est possible que des sols dégradés et réchauffés libèrent aussi un peu d'ammoniac[60]. Il est rabattu au sol par les pluies qu'indirectement il acidifie et rend eutrophisantes[61]. Il acidifie secondairement le sol et contribue ainsi également à l'eutrophisation des milieux. Alors que la pollution soufrée des années 1970-1980 a diminué, il est devenu la cause principale des pluies acides et de l'acidification des eaux douces.
Dans les océans, Bouwman et al. estimaient en 1997 que les mers sont la première source naturelle d'ammoniac[62], mais aussi la plus incertaine et mal comprise (ex. : plus l'eau est froide, plus elle peut dissoudre d'ammoniac, mais bien d'autres facteurs interviennent et une même mer est à la fois un puits et une source d'ammoniac : quand la concentration d'ammoniac de l'eau de surface dépasse celle de l'air il y a émission de l'océan vers l'atmosphère, et inversement. Asman et al. ont montré en 1994 que les zones polluées de la mer du Nord émettent l'ammoniac alors qu'ailleurs elle est un puits. La présence d'ammoniac (naturel ou anthropique) dans les eaux de surface est liée aux apports terrigènes (dépôts secs et pluviaux, apports par les fleuves et estuaires), mais aussi liée à l'activité zooplanctonique et à la décomposition de phytoplancton ou de zooplancton ou d'autres organismes marins. Les apports d'ammoniac dépendent aussi des courants marins, d'upwellings ou d'endo-upwellings et encore de la photochimie et du degré d'intensité des puits chimiques de NH3 dans la troposphère située au-dessus de la mer, laquelle intensité dépend de l'éventuelle formation d'aérosols sulfatés (NH4)2SO4 où le sulfate provient d'une oxydation par les radicaux OH° et NO3 du diméthylsulfide (DMS), un composé organosulfuré de formule (CH3)2S massivement produit par le phytoplancton et nébulisé ou évaporé dans l'air. Un autre puits chimique d'ammoniac est l'oxydation d'NH3 par les radicaux hydroxyde.
Ammoniac anthropique
Il a trois grandes origines : l'industrie chimique, la décomposition de nos urines et excréments, et des urines, fientes et excréments émis par les animaux vivant en condition d'élevage.
À titre indicatif, en 1987, Buijsman et al. ont estimé[63] que dans les élevages européens, les animaux qui émettent le plus d'ammoniac sont les bovins (18 kg NH3 par tête en moyenne par an), devant les chevaux (9,4 kg), les moutons (3,1 kg), les porcs (2,8 kg) puis les volailles (0,26 kg), chiffres variant selon le type d'élevage, et à rapporter au nombre de têtes par élevage ou par hectare, et qui ne peut être dupliqué aux régions tropicales.
Son seuil de toxicité varie selon les espèces, la durée et le niveau d'exposition et leur environnement, mais l'excès d'ammoniac dans l'air ou dans un milieu est toxique et écotoxique.
Le gaz ammoniac (NH3) est source d'ammonium dans les précipitations (pluies, neiges, mais aussi rosée, brumes). De 1980 à 2008, les émissions de NH3 françaises n'ont diminué que de 4 % (source Citepa[64]). Le dépôt d’ammonium est indirectement acidifiant quand dans le sol il libère des ions H+ par transformation en nitrites (NO2−) ou nitrates (NO3−), tout en eutrophisant le milieu où il s'est déposé[64] ; l'ammoniac n'étant pas la seule forme de l'azote en cause, l'étude de la pollution ammoniacale doit être faite dans le cadre d'une approche plus globale faisant le bilan des effets environnementaux en termes d'azote total.
Chez la plante
La plupart des plantes terrestres exploitent l'ammoniac et d'autres déchets azotés incorporés dans le sol par les matières en décomposition. Quelques-unes sont parasites ou hémiparasites d'autres plantes. D'autres, comme les légumineuses fixatrices d'azote, bénéficient de relations symbiotiques avec les rhizobiums qui créent ammoniac à partir de l'azote atmosphérique[65], mais un excès d'ammoniac dans le sol ou même dans l'air peut en revanche avoir des effets négatifs sur de nombreuses espèces végétales[59], dès que les effets toxiques du NH3 dépassent la vitesse et capacité de désintoxication in vivo des plantes qui y sont exposées.
À partir des sources agricoles ou industrielles, l'ammoniac se dépose en moyenne assez rapidement (dans les premiers quatre à cinq kilomètres après avoir été émis par sa source[59]). En contact avec les feuilles, le NH3 peut entraîner :
- des dommages foliaires visibles ;
- une croissance réduite ;
- une productivité moindre ;
- la formation de composés toxiques dans les tissus ;
- une moindre tolérance et résilience face à la sécheresse et au gel ;
- une moindre résistance aux parasites et insectes nuisibles ainsi qu'aux maladies causées par des micro-organismes (pathogènes) ;
- une dégradation des associations symbiotiques ou mycorhizienne ;
- une concurrence faussée entre espèces au détriment de la biodiversité et en faveur de quelques espèces ubiquistes ou résistantes.
Avant de retomber au sol, une partie du NH3 anthropique ou naturel aura déjà été convertie dans l'atmosphère en nanoparticules et en aérosols de NH4+ (ammonium) qui eux posent un problème à des échelles au moins régionales. En effet, selon les données scientifiques disponibles, la charge critique à ne pas dépasser pour les milieux les plus vulnérables (landes, tourbières, zones humides oligotrophes, et certains milieux abritant des cryptogames) serait de 5 à 10 kg d'azote total par hectare (charge par an en dépôt sec et/ou humide combinée de toutes les formes de l'azote atmosphérique). Les plantes autochtones sont les plus vulnérables ; les forêts semblent pouvoir supporter des charges plus élevées (de 10-20 kg/ha et par an), plus ou moins selon les conditions édaphiques, mais la plupart des cryptogames (lichens, bryophytes, hépatiques) qu'elles hébergent y sont néanmoins très vulnérables au NH3 ainsi qu'à d'autres eutrophisants azotés. Sans doute parce que sélectionnées depuis des milliers d'années pour supporter les apports de fumiers et lisiers, les plantes cultivées sont celles qui supportent le mieux les retombées de NH3[59]. Ces seuils critiques sont très fréquemment dépassés dans les régions industrielles et d'agriculture intensive (un hectare cultivé peut perdre jusqu'à 40 kg/an d'azote sous forme d'ammoniac[66]).
Des synergies ou effets additionnels conjoints avec d'autres polluants (ozone et CO2 notamment qui semblent en augmentation presque partout) sont fortement suspectés mais avec des mécanismes toxicologiques et écotoxicologiques encore mal compris.
Chez l'animal
Chez l'animal, l'ammoniac joue un rôle à la fois dans la physiologie normale et anormale. En tant que polluant de l'air il affecte les animaux, plus ou moins selon les espèces et selon la durée d'exposition. À l'intérieur de la cellule, en tant que déchet du métabolisme des acides aminés, il est rapidement toxique, pour la cellule puis pour l'organisme[67]. L'organisme doit donc le gérer et l'éliminer.
- Les animaux aquatiques vivants l'évacuent facilement dans leur milieu ambiant (ammoniotélisme) car l'ammoniac est très soluble dans l'eau ; ils n'ont donc pas besoin de produire de le transformer en complexes non-toxiques pour le stocker avant de l'évacuer.
- Les animaux terrestres le convertissent, eux, en intermédiaires non-toxiques avant de l’excréter (via l'urine et/ou les excréments secs).
Les deux intermédiaires les plus utilisés dans le monde animal sont :
- L'acide urique insoluble dans l'eau (chez les insectes, oiseaux et reptiles dits uricotéliques) qui l'excrétent sous forme de solide (uricotelia) ce qui est intéressant pour les espèces vivant en milieux arides et ne disposant que de peu d'eau, ou pour les oiseaux qui doivent rester légers pour consommer moins d'énergie[68] ;
- L'urée relativement non-toxique et hydrosoluble (ureotelia) qui peut ensuite être évacuée dans l'urine. C'est le cas pour tous les mammifères qui doivent convertir l'ammonium (transporté dans le foie) en urée puis l'évacuer. L'ensemble des réactions permettant cette détoxication est dite cycle de l'urée[69]. Un dysfonctionnement hépatique, tel que celui observé chez l'homme avec la cirrhose, peut conduire à un empoisonnement du sang par de l'ammoniac (hyperammoniémie). De même, le fonctionnement défectueux des enzymes responsables de cycle de l'urée, tels que l'ornithine transcarbamylase, conduit à une hyperammoniémie. Cette dernière contribue à la confusion mentale et peut conduire au coma de l'encéphalopathie hépatique, ainsi qu'à des maladies neurologiques (fréquentes chez les personnes présentant des anomalies du cycle de l'urée et des aciduries organiques[70]).
Remarque : l'urée peut être ensuite (re)fractionnée en ammoniac et en dioxyde de carbone par l'enzyme uréase présente dans certaines plantes (soja, haricot), certains invertébrés et dans certaines bactéries (notamment retrouvées dans le rumen des ruminants ce qui explique que leurs bouses et fumiers sont plus ammoniacaux que chez d'autres espèces (première source anthropique d'ammoniac dans l'environnement)[71].
L'ammoniac participe chez les animaux aux équilibres acide-base normaux. Après la formation d'ammonium à partir de glutamine, l'α-cétoglutarate peut être décomposé en produisant deux molécules de bicarbonate qui deviennent disponibles comme « tampon » pour les acides alimentaires. L'ammonium est excrété dans les urines, entraînant une perte nette d'acide.
L'ammoniac peut en outre se diffuser à travers les tubules rénaux et s'y combiner avec un ion hydrogène, permettant ainsi l'excrétion supplémentaire d'acide[72].
Chez l'Homme
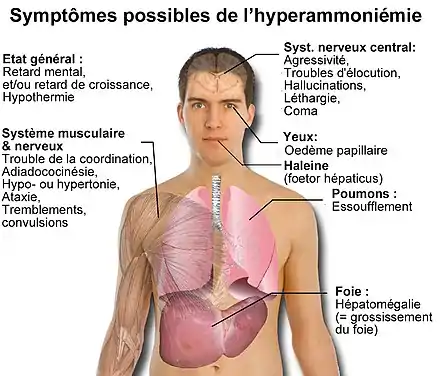
L'ammoniac peut passer dans l'organisme humain, principalement par inhalation, ou parfois il y est issu d'une production pathologique par l'organisme lui-même (« intoxication endogène » ) à la suite d'un dysfonctionnement du rein, du foie, des muscles, ou de l'intestin)[73]. C'est « un gaz particulièrement toxique. À une concentration de 500 ppm pour une exposition de 30 min, il produit des effets irréversibles. À une concentration de 3 400 ppm, il est mortel en 60 minutes »[74]. Les expositions aux fortes doses sont cependant rares (liées à un contexte industriel ou accidentel).
L'exposition chronique à de faibles doses touche par contre une grande partie du monde ; dans les régions cultivées, sa première source de NH3 est l'engrais azoté (« de 0 à 90 % de la quantité totale d'azote ammoniacal apportée peut s'évaporer » sous forme d'ammoniac)[66] et ses usines de fabrication. En Europe, l'ammoniac volatilisé perdu par les engrais agricole (minéraux et organiques) est après la lixiviation le second poste de pertes d’azote. Jusqu'à 20 % des apports d’engrais minéraux (selon les formes, le sol et conditions d'apport) et jusqu'à 70 % de la fraction ammoniacale des lisiers peuvent être perdus dans l'atmosphère, en quelques jours à quelques semaines après épandage[75], avec jusqu'à 40 kg/ha et par an[66].
En pathologie humaine et vétérinaire, une augmentation du taux d'ammoniac sanguin est signe de dysfonctionnement du foie. Du NH3 est naturellement issu de la dégradation des acides aminés. Il est transformé en urée dans le foie, pour être éliminé de l'organisme (détoxication) via l'urine ; toute dégradation de fonctionnement du foie entraîne donc une augmentation du taux d'ammoniac dans le sang. Et l'excès d'ammoniac sanguin peut notamment entraîner une encéphalopathie, avec divers symptômes :
L'ammoniac absorbé (ou anormalement produit) par l'organisme induit[73] :
- un altération des astrocytes, en modifiant les protéines astrocytaires (Glial fibrillary acidic protein) ;
- une altération des échanges ioniques cellulaires ;
- une altération des sécrétions des NT.
L'origine d'une hyperammoniémie peut être directe (éventuellement génétiquement acquise) :
- une acidose (le plus souvent, production de NH4+ associée à un défaut d'élimination rénale) ;
- une insuffisance hépatique sévère ;
- une toxicose médicamenteuse (ex. : valproate) ;
- une prématurité, avec défaut de perfusion, liée à une immaturité hépatique (chez le bébé, dans les 24 à 72 heures suivant la naissance, se traduisant par des vomissements, une hypothermie, hyperventilation et conduisant au coma).
L'origine peut aussi être indirecte[73], avec :
- une acidurie organique ;
- un déficit de la B oxydation des AG ;
- un déficit de la chaîne respiratoire.
Le taux sanguin normal d'ammoniac est 11 à 45 µmol l−1. Au-delà de 50 µmol l−1, on peut parler d'hyperammoniémie (quelques centaines à plus de 1 000 µmol l−1) qui peut être déclenchée par un changement important dans l'alimentation, un stress important, une infection.
Les symptômes en sont : des douleurs abdominales, une hépatomégalie, cytolyse, IHC avec troubles digestifs (anorexie, un dégoût pour les mets protéinés en particulier viande et poisson), troubles neuropsychologiques (asthénie, somnolence, etc.), troubles de l'humeur, troubles du comportement et de la personnalité (irritabilité…), de l'élocution, hallucinations, crises ataxiques ou convulsives puis « coma hyperammoniémique »). Ces symptômes n'étant pas spécifiques, le diagnostic peut être difficile à poser. Chez l'adulte, il peut être suggéré par un retard mental et/ou psychomoteur, des troubles du comportement, une microcéphalie avec atrophie cérébrale, un régime végétarien lié à une aversion pour les protéines, un syndrome de Reye[73].
L’ammoniac étant labile, le prélèvement sanguin (au moins 1 ml de sérum en tube hépariné ou avec EDTA) doit être fait si possible lors d'une crise et rapidement transporté dans de la glace (en moins de 15 min) puis centrifugé et décanté le plus vite possible par un laboratoire prévenu de son arrivée. Il peut être conservé 2 heures à 4 °C ou 48 heures à −20 °C[73]. Le sang veineux en contient naturellement près de deux fois plus que le sang artériel ou capillaire, et le nouveau-né en produit naturellement plus (34–102 µmol l−1 pour le sang veineux, et 50 à 128 µmol/l pour le sang artériel pour un nouveau-né de trois jours) que l'enfant ou l'adulte[73].
Diagnostic différentiel
Il doit faire éliminer[73] :
- d'autres formes d'encéphalite ;
- l'épilepsie ;
- une intoxication alimentaire ;
- une porphyrie ;
- la thrombose veineuse cérébrale ;
- une tumeur cérébrale ;
- etc.
Santé environnementale, santé au travail
Les adsorbants commerciaux utilisés dans les masques à gaz sont des charbons actifs, parfois imprégnés d’oxydes de cuivre. En 2017, ils sont encore moyennement efficaces pour l'ammoniac. Des adsorbants microporeux divers sont étudiés pour mieux adsorber le NH3 : ce sont des charbons, zéolithes et metal–organic frameworks (MOF) ; certains MOF de type UiO-66 se sont montrés efficaces en conditions sèches et humides)[74].
Seuils à ne pas dépasser au travail : une directive européenne a fixé des seuils d'émission à ne pas dépasser (plafonds) pour réduire les émissions européennes de NH3 à horizon 2010 puis 2020. Le NH3 est l'un des principaux précurseurs de particules fines dont les effets sanitaires négatifs sont largement démontrés[66].
Pour l'exposition des ouvriers et autres employés de l'Industrie, l'American Conference of Governmental Industrial Hygienists (ACGIH), et le Canada recommandent de ne pas dépasser :
Utilisations
Engrais
Le NH3 est principalement utilisé dans la production d'engrais ; De l'ammoniac (contenant 82 % d'azote) sert parfois aussi d'engrais azoté gazeux ; il est alors injecté directement dans le sol sous forme d'ammoniac liquéfié sous pression. Étant très soluble dans l'eau, une grande partie du gaz se dissout dans l'eau du sol.
Explosifs
Sous forme gazeuse, l'ammoniac est aussi utilisé par l'industrie pour la fabrication d'explosifs.
Polymères
L'ammoniac est un ingrédient de la fabrication de divers polymères (plastiques, fibre synthétique, etc.).
Tabac
On le trouve aussi dans la cigarette ou le tabac de pipe. Les fabricants l'ajoutent lors de la préparation du tabac, car en réagissant avec la nicotine (alcaloïde) l'ammoniac produit un composé nicotinique basique libre, encore plus assimilable par l’organisme que sous sa forme acide. Ceci multipliant très fortement l’effet addictif de la nicotine sur le cerveau ; le fumeur est ainsi prisonnier de son addiction et fortement poussé à consommer toujours plus de tabac[77] - [78] - [79].
Réfrigération
L'ammoniac est un fluide frigorigène aux capacités thermodynamiques et thermiques excellentes, malgré les contraintes qu'il implique ; alors désigné par la référence R717.
- La lettre « R » signifie réfrigérant ;
- 7 : les fluides frigorigènes d'origine inorganique sont répertoriés dans la série des 700. Le chiffre des centaines est donc un 7 ;
- 17 : le chiffre des dizaines et celui des unités ici représentent la masse molaire de la molécule, à savoir M(NH3=17,0 g/mol ;
L'ammoniac est très utilisé dans le secteur du froid industriel dans les installations à puissance importante (plusieurs centaines de kW). En Suisse, plus de 90 % des équipements industriels y ont recours. Son utilisation devrait augmenter avec le bannissement des gaz nocifs pour l'environnement comme les HFC[80]. En raison de sa toxicité, il doit être confiné en salle des machines.
Carburant

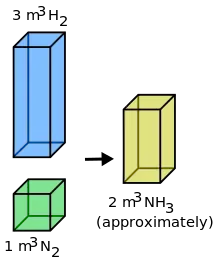
L'ammoniac est un vecteur énergétique car il permet de transporter de l'hydrogène sous une forme dont le stockage est relativement simple[81]. Il brûle difficilement dans l'air mais la combustion est facilitée par une décomposition partielle par passage sur un catalyseur. Il peut être utilisé comme carburant dans des moteurs adaptés, avec toutefois des problèmes encore à résoudre de corrosion, de catalyseur, d'additifs, d'émissions d'imbrûlés et une contribution à l'émission de NOx polluants.
En 1872, le docteur Émile Lamm, dentiste français émigré aux États-Unis, dépose plusieurs brevets pour un moteur à ammoniac et met ce système en application sur une des lignes de tramways de La Nouvelle-Orléans.
Pendant la Seconde Guerre mondiale, des véhicules (notamment des autocars en Belgique) ont fonctionné avec de l'ammoniac. Dans les années 1960, l'armée américaine s'y est intéressée dans le cadre du concept MED (Mobile Energy Depot) qui visait à produire directement les carburants sur le champ de bataille à partir de réacteurs nucléaires transportables[82] - [83].
Au XXIe siècle, l'ammoniac fait l'objet de nouvelles études pour des moteurs classiques sans émissions de CO2 et pour le fonctionnement de piles à combustible. Il est particulièrement étudié pour le transport maritime[84] - [85] - [86] - [87] - [88].
Détection des fuites
Son odeur particulière rend une fuite d'ammoniac facilement signalée, mais la recherche du point de fuite sur une installation ammoniac ne doit toujours se faire qu'à l'aide d'un appareil respiratoire isolant du fait de sa très forte toxicité. On utilisait autrefois une baguette soufrée, qui enflammée au voisinage d'émanation d'ammoniac produit une fumée blanche dense permettant ainsi de localiser l'origine de la fuite ; technique aujourd'hui interdite en raison de sa dangerosité. La recherche de fuite se fait, le plus souvent, à l'aide de détecteurs électroniques ou de papiers imbibés de phénolphtaléine.
En tant que polluant
.JPG.webp)

Caractéristiques et cinétique environnementale
Hormis à faible dose, l'ammoniac est un gaz écotoxique, acidifiant et eutrophisant. Autour de ses sources (agricoles le plus souvent[41]), sous forme de dépôts humides ou secs, et à des distances plus ou moins grandes selon la quantité de gaz émise, et selon l'humidité environnante, la force et direction du vent, il contribue à l'acidification des pluies, brumes, brouillards, rosées (car très soluble dans l'eau) et de l'environnement.
Dans les eaux douces ou marines, il contribue notamment aux efflorescences algales[89], contribue au réchauffement[90].
Il se dépose rapidement sur les cuticules des feuilles dans lesquelles il peut aussi entrer via les stomates, et sur le sol où il est un puissant eutrophisant[91] - [92].
Il est aussi indirectement source de particules fines (de type PM2.5 (les plus dangereuses car pénétrant profondément les voies respiratoires), ce qui explique que y être chroniquement exposé diminue l’espérance de vie[93]. Il peut s'adsorber sur des poussières en suspension[41].
Concernant les bâtiments d'élevage, ils sont souvent bas, ce qui encourage des retombées à leur proximité plutôt que très loin, ce que confirme l'observation des plantes nitrophiles (orties, gaillet et herbacées telles que Deschampsia flexuosa et Holcus lanatus), qui sont plus densément présentes à proximité d'un poulailler (dans ce cas situé en zone tempérée proche d'une forêt de résineux) dont les émissions de NH3 atteignaient 50 μg d'ammoniac par mètre cube d'air et près duquel les dépôts d'azote dépassaient 40 kg de N-NH3 par hectare et par an)[94]. Les feuilles d'arbres et plus encore de bryophytes voient aussi leur teneur en azote croitre dans les centaines ou dizaines de mètres situés autour du bâtiment, surtout sous le vent dominant (la teneur en azote des feuilles de bryophytes grimpe jusqu'à environ 3 % du poids sec de la feuille quand le taux d'ammoniac de l'air dépasse 20 à 40 μg/m3 d'air[95]. Ces modifications floristiques (nitrophiles surfavorisées) sont cependant moins visibles dès que l'on s'éloignait d'un élevage (en moyenne 90 % de la flore était à nouveau normale à une cinquantaine de mètres en moyenne autour du poulailler Cependant les espèces très vulnérables à l'eutrophisation étaient en régression visible jusqu'à environ 300 m autour des mêmes élevages[95].
Il a été montré que les élevages émettent aussi de l'ammoniac la nuit, mais qu'il est alors moins dispersé (en moyenne il y a moins de vent et de turbulence d'air la nuit[96]). La chaleur et l'humidité de l'air, qui varient beaucoup selon les régions du monde sont aussi des facteurs entrant en jeu.
Des modèles mécanistes de dispersion et de dépôt d'NH3 ont été mis au point[41] ; ils montrent tous, comme les observations de terrain, que les dépôts secs cumulés peuvent varier de quelques dixièmes de % à près de 20 % de la quantité émise à 400 m en aval d'une source (ces paramètres variant principalement en fonction de la hauteur de la source par rapport au couvert végétal, mais aussi selon la stratification thermique, la force et direction du vent)[41].
Le degré de « contamination » des plantes dépend des conditions météo et d'interactions avec les résistances stomatiques et cuticulaires des feuilles : quand il fait chaud et sec, c'est par les stomates que l'ammoniac pénètre dans la plante. Quand il fait frais/humide c'est la voie cuticulaire qui prédomine (et elle est encore mal comprise)[41].
Sources d'émissions polluantes
Dans le monde, les principales sources diffuses d'ammoniac sont devenues (à une écrasante majorité) l'agriculture intensive (élevage intensif, engrais azotés, épandages), loin devant les transports (les véhicules équipés de pots catalytiques sont sources d'ammoniac rappelle le CITEPA[97]). Une pollution diffuse mal mesurée est liée aux brûlis (en France métropolitaine, l'écobuage est jugé responsable de 0,2 % des émissions) et incendies de forêt, aux égouts, aux sols et eaux réchauffés qui perdent de l'ammoniac[98]. Les données satellitales récentes montrent que les usines d'engrais sont souvent encore des hotspots d'émissions intenses, et plus localement certaines stations d'épuration, certains lieux de stockages de matières organiques (lisiers, fumiers, déchets organiques) ou très localement et ponctuellement certains postes d'unités de méthanisation[99].
Selon les études disponibles, à la fin du XXe siècle l'agriculture est devenue la source de 80 à 96 % de l'ammoniac anthropique[100]. L'utilisation d'engrais minéraux azotés pour la fertilisation (nitrate et/ou ammonium) entraîne la volatilisation d'une partie de l'ammoniac responsable selon les auteurs scientifiques de 15 à 20 % de toutes les émissions, principalement en zones tropicales où les conditions climatiques favorisent ce phénomène. Les pays en développement sont donc les plus concernés (80 % des émissions en provenaient à la fin des années 1990 selon Bouwman et van der Hoek en 1997, ce qui a été ensuite confirmé par les données satellitales).
Remarque : selon le climat, l'époque de l'année et selon le type de pratiques agricoles qui y sont appliquées, un champ ou une prairie peuvent être « puits » ou « source » d'ammoniac pour l'air et le sol et l'eau[101].
Quantités
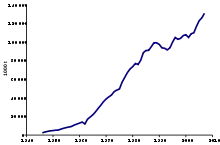
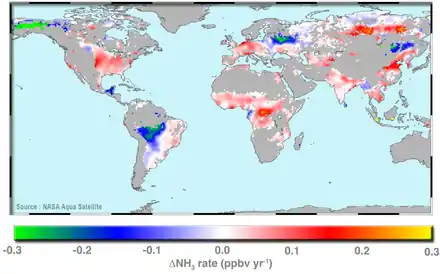
En tant que polluant environnemental, l'ammoniac a été longtemps méconnu car ses sources agricoles en sont très dispersées et donnaient l'impression d'être éloignées voire sans effets sur les zones peuplées. Mais il est maintenant planétairement suivi à distance, sur toute la planète, dans la colonne d'air, grâce à l'interféromètre atmosphérique de sondage dans l'infrarouge (IASI, un capteur interférométrique ultrasensible, mis au point par le Centre national d’études spatiales (CNES) et EUMETSAT) embarqué sur les satellites météorologiques européens MetOp et grâce à un satellite de la NASA (Nasa Aqua) quantifiant à grande échelle le NH3 dans l'atmosphère, montrant une hausse constante des taux d'ammoniac de 2002 à 2016 à partir des centres agricoles des États-Unis, de Chine et d’Inde et un peu moins de l'Europe ; selon la NASA, une petite partie de cette augmentation pourrait être due à la chimie atmosphérique (la lutte contre les pluies acides a efficacement réduite le taux de SOx de l'air, or ces derniers retiraient de l'atmosphère une partie de l'ammoniac anthropique) et au réchauffement des sols (qui retiennent alors moins d’ammoniac)[102]
Huit ans de données accumulées (2008-2016) ont permis au CNRS et à l'Université libre de Bruxelles de publier en 2018 la première cartographie mondiale de l’ammoniac atmosphérique avec un détail sans précédent (maille au km2).
En 2018, dans la revue Nature[103] Van Damme et al. confirmaient que la pollution azotée par l'élevage intensif avait été très sous-estimée par les inventaires et cartographies de la pollution de l'air, à échelle planétaire ; Cette pollution est en outre devenue chronique et catastrophique (à des échelles presque continentale) en Inde du Nord et au sud de l’Afrique de l’Ouest (où le nuage de pollution azotée s'étend largement au-dessus de l'océan Atlantique). Ailleurs, dans les pays riches les zones très polluées par l'ammoniac sont plus petites et centrées sur des usines chimiques ou des élevages industriels particulièrement intensifs. Ce travail confirme la responsabilité majeure l’élevage intensif et la production industrielle d’engrais (à partir de pétrole). Il montre aussi que de très nombreuses sources n’avaient pas été auparavant identifiées, fautes de mesures in situ. Sur 248 grandes sources de NH3 très nettement visibles de satellite (de diamètre de moins de 50 km) les deux tiers n’avaient pas encore été repérées par les États ou les autorités environnementales. 83 étaient des fermes d’élevage intensif et 130 des usines d’engrais. La région la plus émissive au monde (sources agro-industrielles principalement) est la vallée du Gange qui émet 475 kg de NH3 par seconde, soit 1,1 × 1017 molécules par centimètre carré (Pakistan et Inde du Nord). Pour les élevages, le record est une émission moyenne de 0,81 kg/s, observé dans les fermes géantes de Bakersfield et Tulare (Californie) qui abritent des centaines de milliers de vaches[103]. Quant à l’usine la plus polluante (0,75 kg/s), il s’agit d’un complexe chimique d'Ouzbékistan, de la vallée de Ferghana, fabriquant des engrais dans une région par ailleurs d’agriculture intensive[103]. La cartographie par satellite n'a permis de détecter qu'un unique foyer naturel, en Tanzanie[103].
Impact environnemental
Les impacts toxicologiques de l'ammoniac semblent assez bien connus, mais ses impacts écotoxicologiques, autres que liés à son caractère basique ou eutrophisant sont moins bien étudiés.
On sait que :
- les quantités d'ammoniac rejetées dans l'atmosphère en font l'un des principaux responsables de l'acidification de l'eau et des sols[104], ainsi qu'un facteur favorisant les pluies acides[105]. En France et en Europe, le secteur de l'agriculture est à l'origine de 95 % des émissions d'ammoniac[106]. 80 % des émissions proviennent de la volatilisation des déjections animales ; les 20 % restants sont principalement liés à la production des engrais azotés et à leur épandage, difficile à adapter aux aléas climatiques[106] ;
- il s'agit du principal responsable de l'eutrophisation des milieux aquatiques[104] ;
- avec un GWP (global warming potential) de 0[107], l’ammoniac est un fluide frigorigène sans effet sur le réchauffement climatique, contrairement aux fluides frigorigènes type HFC couramment utilisés dans les climatiseurs et pompes à chaleur dont le GWP peut varier de 1 430 (R134a)[107] à 3 900 (R404A)[107] ;
- de même, avec un ODP (potentiel de déplétion ozonique) de 0[108], l'ammoniac est un fluide frigorigène sans effet sur la couche d'ozone, contrairement aux fluides frigorigènes type HCFC dont le plus connu est le R22 encore courant dans les systèmes de climatisations anciens ;
- la production d'ammoniac est une grande consommatrice d'électricité, représentant jusqu'à 2 % de la production mondiale[109] ;
- dans l'eau, bien que considéré comme non toxique aux doses où il est aujourd'hui présent, il semble discrètement affecter le métabolisme de tous téléostéens (l'infra-classe des Teleostei qui regroupe l'écrasante majorité des espèces de poissons actuels, soit environ 23 600 espèces actuellement connues), par exemple en diminuant les réflexes de ces poissons[110] - [111] ;
- une certaine toxicité est également constatée chez des animaux primitifs comme les amphipodes[112].
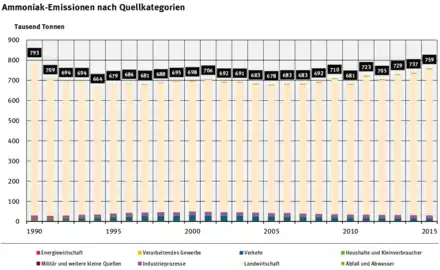
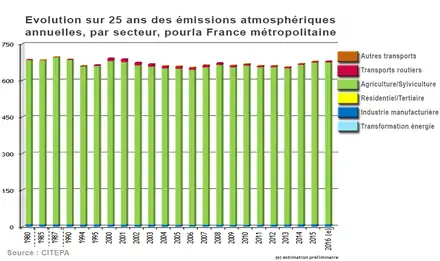
En France, selon le CITEPA, les émissions d’ammoniac atmosphérique ont légèrement baissé en trente ans (de 1980 à 2012 ; en moyenne de 0,5 % par an sur cette période pour arriver à 636 000 tonnes/an en 2012)[113]. Le protocole de Göteborg fixe une nouvelle diminution : –4 % de 2005 à 2020, soit 636 000 tonnes par an[113].
Polluant transfrontalier : en Europe, avec l'EMEP (European Monitoring and Evaluation Programme) et en application de la convention de Genève dite convention sur la pollution atmosphérique transfrontière à longue distance et de son « protocole »[114] sur l'acidification, l'eutrophisation et l'ozone, l'acidité des pluies fait l'objet d'un suivi, centralisé pour la partie française par EcoLab (Laboratoire écologie fonctionnelle et environnement), accueille le point focal national chargé de la modélisation des charges critiques atmosphériques)[115].
En France, l'acidité des pluies a diminué grâce à une forte diminution des émissions de dioxyde de soufre (SO2), mais leur teneur en ammoniac n'a pas diminué, alertait le ministère de l'Environnement en 2011[64], alors que le protocole de la convention demande aux États signataires d'appliquer « les meilleures techniques disponibles pour prévenir et réduire les émissions d'ammoniac énumérées dans le document d'orientation V adopté par l'Organe exécutif à sa dix-septième session (décision 1999/1) et tous amendements y relatifs » notamment par de « bonnes pratiques agricoles respectueuses de l'environnement »[114]. Son article 8 stipule que les parties doivent élaborer des « stratégies visant à réduire davantage les émissions de soufre, d'oxydes d'azote, d'ammoniac et de composés organiques volatils en se fondant sur les charges critiques et les niveaux critiques ainsi que sur les progrès techniques, et amélioration de la modélisation de l'évaluation intégrée pour calculer la répartition optimisée au niveau international des réductions des émissions compte tenu de la nécessité d'éviter des coûts excessifs pour quelque Partie que ce soit. Une importance particulière devrait être accordée aux émissions imputables à l'agriculture et aux transports »[114].
Pour la France, second pays européen le plus émetteur d’ammoniac derrière la fédération de Russie, le niveau de 1990 avait été évalué à 814 000 t de gaz NH3 par an, et la convention de Genève imposait de descendre sous un « plafond » de 780 000 t/an, soit un effort de -4 %[116] alors qu'on demandait à la Slovaquie qui émettait 62 000 t/an de réduire ses émissions de 37 %.
Écotoxicologie
Peu de données sont disponibles à ce sujet dans les écosystèmes car l'ammoniac ne semble pas être un produit très présent dans un écosystème normal. Il est cependant démontré que :
- il endommage le système respiratoire des animaux d'élevages intensifs qui y sont parfois fortement et souvent fréquemment ou chroniquement exposés[117]. Ainsi chez le porc adulte, 25 ppm peuvent après six jours d'exposition causer une inflammation nasale, une hyper-réactivité trachéale et réduire la croissance corporelle[117]. Et à partir de 50 ppm, des dommages pulmonaires apparaissent, qui probablement peuvent favoriser diverses maladies pulmonaires[117] ;
- dans l'eau, sa toxicité pour les amphipodes[118] et les amphibiens notamment, varie aussi selon le pH du milieu[119] ;
- il se montre très toxique pour certaines espèces de crustacés du zooplancton marin (copépodes par exemple)[120] ;
- au moins pour certaines espèces, sa toxicité varie considérablement selon la température de l'eau : ainsi le NH3 est beaucoup plus toxique à 10 °C qu'à 20 °C pour le copépode Acartia pacifica, mais cette toxicité ne varie pas de manière non linéaire avec la température ; dans ce dernier cas, la toxicité de l'ammoniac « tend à diminuer avec l'augmentation de la température jusqu'à un certain point, au delà duquel elle augmente considérablement avec l'augmentation de la température »[121].).
Phrases de risque et conseils de prudence selon l'INRS


- R10 – Inflammable (relativement peu)
- R23 – Toxique par inhalation
- R34 – Provoque des brûlures
- R50 – Très toxique pour les organismes aquatiques
- S9 – Conserver le récipient dans un endroit bien ventilé
- S16 – Conserver à l’écart de toute flamme ou source d’étincelle. Ne pas fumer
- S26 – En cas de contact avec les yeux laver immédiatement et abondamment avec de l’eau et consulter un spécialiste
- S36/37/39 – Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage
- S45 – En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible lui montrer l’étiquette)
- S61 – Ne pas rejeter dans l’environnement. Consulter les instructions spéciales / la fiche de données de sécurité
Référence ONU pour le transport des matières dangereuses
- Classe 2
- numéros :
- 1005 (ammoniac anhydride)
- 3318 (ammoniac en solution aqueuse de densité inférieure à 0,880 à 15 °C contenant plus de 50 % d'ammoniac)
- 2073 (ammoniac en solution aqueuse de densité inférieure à 0,880 à 15 °C contenant plus de 35 % mais au maximum 50 % d'ammoniac)
- numéros :
- Classe 8
- numéro 2672 (ammoniac en solution aqueuse de densité comprise entre 0,880 et 0,957 à 15 °C contenant plus de 10 % mais au maximum 35 % d'ammoniac)
Notes et références
- P.H. Nysten, Dictionnaire de médecine, de chirurgie, de pharmacie, des sciences accessoires et de l'art vétérinaire, Société typographique belge, , p. 345.
- AMMONIAC (ANHYDRE), Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 9-50.
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1)
- (en) T.A. Czuppon et al., Kirk-Othmer encyclopedia of chemical technology 4th ed. : Ammonia, vol. 2, John Wiley & Sons
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- « Gases – Densities » (consulté le ).
- Yost, Don M., Systematic Inorganic Chemistry, READ BOOKS, , 440 p. (ISBN 978-1-4067-7302-6, lire en ligne), « Ammonia and Liquid Ammonia Solutions », p. 132
- Blum, Alexander, « On crystalline character of transparent solid ammonia », Radiation Effects and Defects in Solids, vol. 24, no 4, , p. 277 (DOI 10.1080/00337577508240819)
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne).
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89
- Magalie Roy-Auberger, Pierre Marion et Nicolas Boudet, Gazéification du charbon, éd. Techniques de l'ingénieur, réf. J5200, 10 décembre 2009, p. 4
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205.
- « The Ammonia (NH3, D1) Structure », sur cst-www.nrl.navy.mil (consulté le )
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008, 16 décembre 2008
- « Ammoniac » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Ammonia », sur hazmap.nlm.nih.gov (consulté le )
- La structure électronique de l'azote satisfait la règle de l'octet, soit cinq électrons sur les couches orbitales de l'azote externe et trois électrons entrant dans les liaisons moléculaires azote-hydrogène, donc associés aux trois atomes d'hydrogène. Cette simple donnée quantique rend compréhensible sa réalité physique gazeuse. Sa densité par rapport à celle de l'air prise pour 1, est 0,5971, soit une masse volumique de 0,77 × 10−3 g/cm3.
- Le doublet électronique explique facilement sa réactivité, notamment son comportement de base faible ou de réducteur, sa polarisabilité ou son rôle de ligand en chimie générale ou minérale, voire de nucléophile en chimie organique.
- NH3 aqueux est une base faible, pKa= 9,23.
- Eurostat Agriculture - ammonia emission statistics, données extraites en juin 2015.
- Jobert Marine (2016) Air: l’ammoniac repart à la hausse Le publié 08 juillet 2016
- Source : programme de recherche NUAGE, Coordonné par AgroParistech, et financé par l'Ademe : voir CORTEA Connaissance et réduction des émissions de polluants dans l'air - 5ème restitution du programme CORTEA Synthèse et recueil des résumés des projets CORTEA achevés en 2020 https://librairie.ademe.fr/cadic/5135/CORTEA_Connaissance_et_r__duction_des___missions_de_polluants_dans_l_air_-_5__me_restitution_du_programme_.zip (voir chapitre Mesure des émissions d’ammoniac)
- Agence européenne de l'environnement Ammonia (NH3) emissions
- Webb J, Chadwick D et Ellis, S (2004), Emissions of ammonia and nitrous oxide following rapid incorporation of farmyard manures stored at different densities, Nutrient Cycling in Agroecosystems, 70, 67-76
- Webb J, Henderson D et Anthony SA (2001), Optimising livestock manure applications to reduce nitrate and ammonia pollution: scenario analysis using the MANNER model, Soil Use and Management, 17, 188-94.
- Dioscoride, 3, 98.
- Oscar Bloch et Walther von Wartburg (préf. Antoine Meillet), Dictionnaire étymologique de la langue française, P.U.F., (1re éd. 1932), p. 23, s.v.
- Robert Boyle, Experiments and considerations touching colors, 1664.
- De Ville G., 1850, Note sur l'assimilation de l'azote de l'air par les plantes, et sur l'influence qu'exerce l'ammoniaque dans la végétation, Compte Rendus de l'Acad. Sci., Paris, 31:578-580
- Schlösing Th (1874), Sur l'absorption de l'ammoniaque de l'air par les végétaux, Compte Rendus de l'Acad. Sci., Paris, 78: 1700-1703
- Boussingault J.B (1856), Recherches sur la végétation, Troisième mémoire, De l'action du salpêtre sur le développement des plantes, Ann. Chim. Phys. Ser., 3, 46: 5-41
- Lawes J.B, Gilbert J.H (1851), On agricultural chemistry, J. R. Agr. Soc., 12: 1-40.
- Bineau A (1854), Études chimiques sur les eaux pluviales et sur l'atmosphère de Lyon et de quelques points des environs, Lyon (Cité dans Hall et Miller, 1911).
- Heinrich R (1881), Über die Ammoniakmengenwelche der Atmosphäre im Lauf eines Jahres durch Salzeure entzogen werden, Wollnys Forschungen, 4:446-452
- Kellner (1986), Über das Maximum auf gebundenen Stickstoff Welches des Ackerboden der Atmosphäre zuenziehen vermag, Landwirtschaftliche Jahrb., 15 : 701-711.
- Benjamin Loubet (2000), Modélisation du dépôt sec d’ammoniac atmosphérique à proximité des sources, université Paul-Sabatier, URL : https://tel.archives-ouvertes.fr/tel-00003250/document
- Hall A.D et Miller N.H.J (1911), On the absorption of ammonia from the atmosphere, J. Agric. Sci., 4:56-68
- L'agencement de la molécule est pyramidale, avec distance N-H équivalant à 1 Å, et angle HNH de l'ordre de 107°.
- Whitehead D.C et Raistrick N (1990), Ammonia volatilisation from five nitrogen compounds used as fertilizers following surface application to soils of differing characteristics, J. Soil Sci., 41:387-394.
- Dictionnaire français-latin de Trévoux ; Dictionnaire universel francois et latin : Contenant La Signification Et La Definition tant des mots de l'une & de l'autre Langue, avec leurs differens usages, que des termes propres de chaque État & de chaque Profession, édité à Paris, par la compagnie des libraires associés en 1752 (numérisé en livre numérique Google)
- Il vient du mot latin ammoniacum, emprunté au grec ammôniakon, de même emploi. L'évolution médiévale a parfois engendré les termes synonymes armoniac ou armognac, voire armagnac.
- (en) « azanes », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8)
- La production industrielle de l'ammoniac a ouvert la voie à une filière industrielle, qui se déploie vers les composés nitrés, par exemple par le biais de la fabrication d'acide nitrique via le procédé Ostwald. L'adsorption alcaline terminale de ce procédé pour récupérer les restes d'acide nitrique peut s'opérer avec une solution d'ammoniaque, pour obtenir du nitrate d'ammonium, à l'origine des engrais ammonitrates.
- Selon le formulaire Chimie technique rédigé par H. Ibert et traduit par Francis Pichon, pour les éditions Mac-Graw Hill, opus cité, le procédé Haber-Bosch classique se caractérise par une pression du mélange gazeux initial à proportions stœchiométriques, comprise entre 200 et 250 bar et une température optimale de 550 °C. Tant que les catalyseurs sont à base de Ni et de Fe, sur des supports d'oxydes d'aluminium et de silicates, et même si les températures et pressions des gaz sont modifiés largement, il est possible de classer l'ensemble de ces procédés dans la famille des procédés Haber-Bosch. Peu importe l'origine des gaz, le (di)azote N2 issus du gaz à l'air ou de procédés de fabrication d'azote liquide Linde, le gaz hydrogène H2 du gaz à l'eau ou par voies électrolytiques en milieu aqueux. Notons les progrès remarquables au cours du XXe siècle, mais à l'époque assez bien tenus secrets, pour l'obtention de support à grandes surfaces spécifiques. Ce qui permet des gains en termes de temps de passage et même d'énergie.
- Selon H. Ibert, opus cité, le procédé Haber Bosch modifié opte pour une pression plus élevée de 325 bar sans modifier la température. Le procédé de la Nitrogen Engineering Corporation, entreprise américaine, serait optimum à 300 bar et 550 °C.
- Selon H. Ibert, cité supra, le procédé italien Casale serait resté à des pressions de 600 bar pour 500 °C.
- Selon Ibert, cité supra, 250 bar et 550 °C.
- Pour une présentation actualisée des entreprises productrices et des pays producteurs, lire la fiche ammoniac de la Société chimique de France SCF, mise à jour par Jean-louis Vigne en 2014, lien externe cité.
- (en) « Cleaner, cheaper ammonia UTokyo researchers dramatically clean up ammonia production and cut costs », sur u-tokyo.ac.jp, .
- Daphné Lecellier, « Synthèse d’ammoniac à partir d’azote et d’eau », sur France diplomatie, (consulté le ).
- (en) U.S. Geological Survey, « NITROGEN (FIXED)—AMMONIA, », Mineral Commodity Summaries, (lire en ligne [PDF])
- « De l'ammoniac superionique créé et analysé en laboratoire », sur CNRS, (consulté le ).
- (en) J.-A. Hernandez, M. Bethkenhagen, S. Ninet, M. French, A. Benuzzi-Mounaix et al., « Melting curve of superionic ammonia at planetary interior conditions », Nature Physics, (DOI 10.1038/s41567-023-02074-8) (correction le ).
- Krupa S.V. (2003), Effects of atmospheric ammonia (NH3) on terrestrial vegetation: a review, Environmental Pollution, 124: 179–221 (résumé)
- NASA NASA Satellite Identifies Global Ammonia ‘Hotspots’, 16 mars 2017
- Houdijk A, Smolders A et Roelofs J (1993), The effects of atmospheric nitrogen deposition on the soil chemistry of coniferous forests in the Netherlands, Environmental Pollution, 80, 73-78.
- Tableau I.3 dans Loubet B. (2000), Modélisation du dépôt sec d’ammoniac atmosphérique à proximité des sources [PDF], thèse de physique, université Paul-Sabatier, 361 p.
- Buisman E, Maas H.F et Asma W (1987), Anthropogenic NH3 emissions in Europe, Atmospheric Environment, 21(5), 1009-1022.
- CGDD (2011), La qualité des eaux de pluie : acidité en baisse mais pas de progrès pour les dépôts d’azote [PDF], ministère de l'Écologie, du Développement durable, des Transports et du Logement, Service de l'Observation et des statistiques, Le point sur, no 88, juin 2011, 4 p.
- Adjei, M.B. ; Quesenberry, K.H. et Chamblis, C.G. (juin 2002), Nitrogen Fixation and Inoculation of Forage Legumes, University of Florida IFAS Extension
- Comifer/Groupe Azote Calcul de la fertilisation azotée [PDF], Groupe azote Comifer, avril 2011, 92 p.
- PubChem Substance Summary (consulté le 7 juillet 2009).
- (de) Stickstoff-Exkretion. Dans Römpp Online, Georg Thieme Verlag, 13 juin 2014
- (de) (Harnstoff-Cyclus, Cycle de l'urée). Dans Römpp Online, Georg Thieme Verlag, 13 juin 2014.
- Zschocke, Johannes, et Georg Hoffman (2004), Vademecum Metabolism. Friedrichsdorf, Allemagne, Milupa GmbH.
- (de) Urease. Dans Römpp Online, Georg Thieme Verlag, 13 juin 2014.
- Rose Burton, Renal pathophysiology : the essentials, Baltimore, Williams & Wilkins, , 351 p. (ISBN 978-0-683-07354-6, OCLC 424442230).
- Gaspard Beaune, Les hyperammoniémies [ppt], Laboratoire de biochimie CHRA, 26 septembre 2002 (consulté le 4 octobre 2011)
- Khabzina Y et Farrusseng D (2017), Application des MOFs à l’adsorption de gaz toxiques industriels. Dans 33e réunion annuelle du Groupe francais des zéolithes, mars, résumé
- Nicolardot B., Mary B., Houots S. et Recous S. (1997), La dynamique de l'azote dans les sols cultivés. In Maîtrise de l'azote dans les agrosystèmes, Annales colloques INRA 83, Reims (France), 19-20 novembre 1996, INRA Éd., 87-103.
- CCHST, Fiche Ammoniac, centre canadien d'hygiène et de sécurité au travail (consulté le 9 décembre 2018)
- Revue médicale suisse ; Modification de la composition des cigarettes durant le XXe siècle : rôle de l’industrie du tabac et effet sur la dépendance tabagique
- « Dis pourquoi Papa : Pourquoi l'ammoniac rend dépendant du tabac ? », sur ww3.ac-poitiers.fr (consulté le )
- « Composants du tabac », sur Quebec sans tabac (consulté le )
- « Installations de réfrigération: Prudence avec l’ammoniac », sur bafu.admin.ch, (consulté le ).
- Feuillade G. (1984), Le stockage chimique de l'énergie, IV. Utilisation des nouveaux vecteurs d'hydrogène dans les moteurs thermiques. Élaboration d'un programme prospectif général, Entropie, 20(119), 57-68 (Notice Inist-CNRS/résumé)
- (en) Burwell, S. B., Carlson, J. A. et Clark, R. G., « Mobile energy depot feasibility study : summary report », sur osti.gov, (consulté le ).
- C.G. Garabedian et J.H. Johnson, The theory of operation of an ammonia burning internal combustion engine, US Army tank automotive center, Warren Michigan, 1963
- Adeline Descamps, « Transport maritime : le grand consensus autour de l'ammoniac », sur journalmarinemarchande.eu, .
- Cédric Philibert, « Des cargos écolos grâce à l’ammoniac vert », sur revolution-energetique.com, .
- Japanese firms working on ammonia-fueled engines
- Stockage de l’énergie via l’ammoniac
- Ammonia-fueled vessel gets approval
- Paerl H.W., Gardner W.S., McCarthy M.J., Peierls B.L. et Wilhelm S.W. (2014), Algal blooms: noteworthy nitrogen, Science, 346, 175
- Shindell D.T. et al. (2009), Improved attribution of climate forcing to emissions, Science, 326, 716–718
- Galloway J. et al. (2003), The nitrogen cascade, Bioscience, 53, 341–356 (2003)
- Bobbink, R. et al., Global assessment of nitrogen deposition effects on terrestrial plant diversity: a synthesis, Ecol. Appl., 20, 30–59 (2010)
- Lelieveld J, Evans J.S, Fnais M, Giannadaki D et Pozzer A (2015), « The contribution of outdoor air pollution sources to premature mortality on a global scale », Nature, 525, 367–371
- Kaupenjohann M, Döhler H et Bauer M (1989), Effects of N-immissions on nutrients status and vitality of Pinus sylvestris near a hen-house. Plant Soil, 113:279-282
- Pitcairn C.E.R., Leith I.D., Sheppard L.J., Sutton M.A., Fowler D., Munro R.C., Tang S. et Wilson D., 1998, The relationship between nitrogen deposition, species composition and foliar nitrogen concentrations in woodland flora in the vicinity of livestock farms, Environ. Pollut., 102(S1): 41-48
- Jacobs A.F, van Boxel J.H et El-Kilani R.M (1994), Night-time free convection characteristics within a plant canopy, Boundary-Layer Meteorol., 71:375-391.
- https://www.citepa.org/fr/air-et-climat/polluants/aep-item/ammoniac consulté le 28 juin 2019
- « NASA Satellite Identifies Global Ammonia ‘Hotspots’ », sur NASA (consulté le ).
- Dirrenberger P, Nicot T, Mont N., Kunz-Iffli J, Grosjean, J, Galland B, … et Bruant D (2018), Évaluation des niveaux d’exposition à différents composés délétères dans les unités de méthanisation, Archives des Maladies Professionnelles et de l'Environnement, 79(3), 373.
- Tableau I.2 : Exemple d'émissions d'ammoniac liée à l'activité anthropique, à l'échelle globale ; d'après Schlesinger et Hartley (1992), Dentener et Crutzen (1994), et Bouwman et al. (1997), cités par Benamin Loubet in Modélisation du dépôt sec d’ammoniac atmosphérique à proximité des sources, Physique, université Paul-Sabatier, 2000, p. 38/361
- David M. (2002), Échange d'ammoniac entre une prairie et l'atmosphère : sources et puits à l'échelle du couvert prairial et influence des pratiques agronomiques (Doctoral dissertation, Paris 11) (résumé)
- NASA (2017), NASA Satellite Identifies Global Ammonia ‘Hotspots’, 16 mars 2017, résume notamment une étude publiée dans Geophysical Research Letters.
- Van Damme, M., Clarisse, L., Whitburn, S., Hadji-Lazaro, J., Hurtmans, D., Clerbaux, C. et Coheur, P.-F (2018), Industrial and agricultural ammonia point sources exposed, Nature, 564, 99-103, DOI 10.1038/s41586-018-0747-1
- Ifen
- Ademe
- Commission européenne
- International Institute of refrigeration, Ammonia as a Refrigerant, 3e éd., Dr A.B. Pearson, 2008
- Michèle Mondot, Ahmed Bensafi et Christophe Marvillet, L'après R22 - Guide des fluides frigorigènes pour la climatisation, Publications du CETIAT, 2002
- (en) « Water and air are all you need to make one of world’s most important chemicals », sur theconversation.com
- McKenzie, D.J., Shingle, A., Claireaux, G. et Domenici, P.(2009), Sub-lethal concentrations of ammonia impair performance of the teleost fast-escape response, Physiol.Biochem. Zool., 82, 353–362
- McKenzie, D.J., de bardeaux, A., Claireaux, G. et Domenici, P.(2009)
- Prenter, J., MacNeil, C., Dicka, J.T.A., Riddella, G.E. et Dunn, A.M. (2004), Lethal and sublethal toxicity of ammoniato native, invasive, and parasitised freshwater amphipods, Water Res., 38, 2847–2850.
- Ammoniac, Centre interprofessionnel technique d'études de la pollution atmosphérique (CITEPA)
- ONU (2000), Protocole à la convention de 1979 sur la pollution atmosphérique transfrontière à longue distance, relatif à la réduction de l'acidification, de l'eutrophisation et de l'ozone troposphérique [PDF], 74 p.
- ECOLAB Ecolab
- Tableau p. 24/74 du protocole de Genève de 2000
- Gustin, P., Urbain, B., Prouvost, J. et Ansay, M. (1999), Impact de l'ammoniac sur le système respiratoire du porc, Bulletin et mémoire, Académie royale de médecine de Belgique, 154 (6, SPI), 371-376.
- Ankley G.T, Schubauer-Berigan M.K et Monson P.D (1995), Influence of pH and hardness on toxicity of ammonia to the amphipod Hyalella azteca, Canadian Journal of Fisheries and Aquatic Sciences, 52(10), 2078-2083 (résumé).
- Dejours P, Armand J et Beekenkamp H (1989), La toxicité de l'ammoniac est fonction du pH de l'eau. Étude chez la salamandre Pleurodeles waltl. Comptes rendus de l'Académie des sciences, série 3, Sciences de la vie, 308(2), 55-60.
- Shang J. Lu M et Yu Q (2018), Acute Effects of Ammoniac Nitrogen on Marine Copepod Acartia pacifica When Exposed to Different Temperature Conditions, Aquatic Science and Technology, 6(2), 6-11
- Shang, J., Lu, M. et Yu, Q. (2018), Acute Effects of Ammoniac Nitrogen on Marine Copepod Acartia pacifica When Exposed to Different Temperature Conditions, Aquatic Science and Technology, 6(2), 6-11 (résumé)
Voir aussi
Articles connexes
Liens externes
- Fiche ammoniac de la SCF mise à jour par Jean-louis Vigne en 2014
- Expérience du jet d'eau : solubilité de l'ammoniac dans l'eau
- Analyse documentaire avec questions sur La synthèse industrielle de l'ammoniac, académie de Paris
- Un cours lorrain sur l'ammoniac et l'acide nitrique
- Robert Nardone, La chimie de la guerre, épisode de la série Savants et Militaires, Universcience, France Télévisions, Enfin Bref production, 2012 : un aperçu de la vie de Carl Bosch en 3 min 22 s.
- Fiche toxicologique de l'INRS
- Fiche internationale de sécurité
- Fiche Aria retour d'expérience, no 31821 Incendie et explosion de gaz de synthèse d’ammoniac, , Billingham, Grande-Bretagne
- Développement en cours chez un constructeur de moteurs marins(en anglais)
- L'ammoniac un carburant fabriqué à partir du soleil
Bibliographie
- Iñaki de Aguirre et Marie-Anne Van de Wiel, Introduction à la chimie générale, édition De Boeck Supérieur, 1995, vol. 2, 518 p., p. 298-310 sur l'ammoniac (ISBN 9782804107208).
- Gérard Emptoz, Les chimistes, leurs institutions et leurs sociétés savantes entre les deux guerres. II - La nouvelle chimie de l’azote dans l’entre-deux-guerres, L'Actualité chimique, Journal de la Société chimique de France, no 381, janvier 2014, 60 p., p. 40-47.
- Victor Kaiser, Ermanno Filippi, Henri Dominique Léger et Pierre Lesur, Calcul des réacteurs catalytiques - Synthèse d’ammoniac - Aspects fondamentaux de la réaction de synthèse, Techniques de l'ingénieur, J 4040, 10 juin 1999.
- Paul Pascal, Nouveau traité de chimie minérale, vol. 10, t. 10 : Azote et phoshore, Paris, Masson, (réimpr. 1966), 32 vol.
- Arkan Simaan, Grandeur et décadence de Fritz Haber, dans Bulletin de l'Union des professeurs de physique-chimie, vol. 99, no 874, mai 2005, p. 613-626.
- H. Ebert (trad. Francis Pichon), Chimie technique, Auckland, Bogota, Paris, McGraw-Hill, coll. « Formulaire de poche », (ISBN 978-2-7042-1108-1, OCLC 25322022, BNF 34839286).