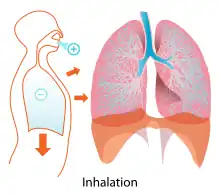
Inhalation
En physiologie et médecine, le mot inhalation désigne de manière générale l'absorption par le nez et les voies respiratoires d'une substance (air, autre gaz, aérosol…).
Le terme peut désigner plusieurs choses :
- Une méthode d'absorption — à fin thérapeutique — de certaines substances sous forme de gaz, de liquide nébulisé en micro-gouttelettes ou de poudre en suspension[1] (anesthésiques[2], désinfectants, bronchodilatateur…)[3]. L'inhalation est aussi très utilisée en médecine traditionnelle (infusions de plantes, fumées).
Le traitement des maladies respiratoires par inhalation a été recommandé à la fin du XVIIIe siècle par le pneumologue anglais Thomas Beddoes[4] - [5] ; - Une inhalation pulmonaire du contenu gastrique, pouvant provoquer une « pneumopathie d'inhalation » ;
- L'absorption de drogue par voie nasale, sous forme de poudre (cocaïne, prise de tabac), ou de fumée de tabac ou de haschisch…).
C'est une des voies de pénétration de certains allergènes et polluants aéroportés dans l'organisme. Chez les grands brûlés l'inhalation peut être altérée[6]. Le lavage broncho-alvéolaire permet l'étude des territoires alvéolaires (« poumon profond »).
Inhalations thérapeutiques
- Selon une revue Cochrane récemment mise à jour (2017)[7] : l'inhalation d'une solution saline hypertonique - faite avant, pendant ou après les techniques de dégagement des voies aériennes - améliore la rhéologie (fluidité) des expectorations, accélère la clairance mucociliaire et améliore cliniquement l'état des personnes atteintes de fibrose kystique (mucoviscidose), sans effets négatifs sur la qualité de vie du patient. Mais aucune étude n'a porté sur le long, ce qui ne permet pas de savoir si le moment du traitement dans la journée pourrait le rendre encore plus performant[7].
- Le poumon est déjà une porte d'entrée pour quelques médicaments inhalés[8], mais la nanomédecine espère pouvoir utiliser l'inhalation de nanoparticules par exemple utiles pour l'imagerie ou comme médicaments contre l'arythmie ou l'insuffisance cardiaque en évitant la délivrance intraveineuse ; avec plus d'efficacité ou de rapidité[9] - [10] - [11]. Miragoli et al. (2013) ont par exemple testé chez la souris (modèle murin de cardiomyopathie diabétique) l'inhalation de nanoparticules destinées à transporter des peptides améliorant la contraction cardiaque vers le cœur (au lieu de l'injection classique)[12]. Ces particules ont effectivement pénétré les tissus du cœur, plus vite que celles injectées. De même, chez des porcs (en bonne santé) ces nanoparticules inhalées ont aussi pénétré le tissu cardiaque. Des nanoparticules de phosphate de calcium (<50 nm) sont des vecteurs biocompatibles et biodégradables qui passent rapidement du poumon au sang puis au myocarde où ils peuvent libérer leur cargaison est rapidement libérée[13]. Ces expériences montrent aussi combien certains nanopolluants pourraient rapidement passer de l'air à des organes du corps humain.
Lésions acquises par inhalation
Ce sont souvent des lésions de la partie profondes de l'arbre respiratoire induites par des infections ou qui accompagnent des hypoxies ou des intoxications induites par l'inhalation de monoxyde de carbone et/ou de fumée[14] - [15].
Les blessures par inhalation auront des symptômes, conséquences et traitements différents selon leurs origines et gravité :
- brûlures thermiques par inhalation ; elles affectent plutôt les voies respiratoires supérieures et sont constatées chez environ un tiers des grands brûlés. Elles se manifestent et se détectent en général dans les 48 heures qui suivent l'exposition, avec un risque d'infection bactérienne secondaire[16]. Le patient est sous oxygène humidifié, subi des toilettes pulmonaires attentives, est si nécessaire il est traité par un bronchodilatateur et une intubation endotrachéale prophylactique. Le poumon cicatrise en général en quelques jours mais les brûlures internes graves restent une cause importante de décès chez les grands brûlés[14]. Le risque de mortalité augmente avec l'âge, avec le pourcentage du corps brûlé ou TBSA (percentage of the total body surface area[17]) et l'importance de la lésion respiratoire pulmonaire[18]. Le risque de mortalité semble moindre chez les 5-14 ans et plus élevée après 59 ans[18] ;
- empoisonnement au monoxyde de carbone (CO) ; le degré d'intoxication est évalué via l'analyse des gaz du sang artériel. Le traitement utilise le fait que la dissociation du monoxyde de carbone se fait beaucoup plus vite quand le patient est placé sous 100% d'oxygène, mais les symptômes persistent parfois (voire s'aggravent) malgré un traitement adéquat[14] ;
- inhalation de fumée, allergènes ou de gaz ou aérosols toxiques (dont armes chimiques…) ou mauvaise utilisation d'inhalateurs (source fréquente (retrouvée chez 50 % des usagers) d’exacerbation sévère de BPCO)[19]. Ces lésions dégradent la physiologie de la respiration et provoquent des lésions dont les conséquences sont (selon la gravité et le type d'exposition) l'insuffisance respiratoire aiguë, et parfois l'œdème pulmonaire ou la bronchopneumonie. Le diagnostic est basé sur l'histoire de l'exposition et des résultats cliniques ou analytiques (gaz du sang artériel, bronchoscopie à fibres optiques…)[14].
Depuis deux siècles, une meilleure compréhension de la physiopathologie des brûlures et des autres lésions de l'arbre respiratoire, associé à une prise en charge souvent plus précoce et agressive[20] ont nettement amélioré le taux de survie des blessures par inhalation[14]. Mais on sait que l'exposition chronique aux fumées et aux micro- et nanoparticules sont une source importante voire croissante d'autres pathologies.
Notes et références
- de Boer A.H & al. (2017) Dry powder inhalation: past, present and future. Expert opinion on drug delivery, 14(4), 499-512.
- Steffey E.P, Mama K.R & Brosnan R.J (2015) Inhalation anesthetics. Lumb & Jones' veterinary anesthesia, 3, 297-323 (résumé).
- Hickey A.J & Mansour H M. (Eds.) (2019) Inhalation aerosols: physical and biological basis for therapy (Vol. 1). CRC press.
- (en) D. P. Miller et T. H. Levere, « "Inhale it and see?" the collaboration between Thomas Beddoes and James Watt in pneumatic medicine », Ambix, vol. 55, no 1, , p. 5–28 (PMID 18831152)
- (en) D. A. Stansfield et R. G. Stansfield, « Dr Thomas Beddoes and James Watt: Preparatory work 1794-96 for the Bristol Pneumatic Institute », Medical History, vol. 30, no 3, , p. 276–302 (PMID 3523076, PMCID 1139651, DOI 10.1017/s0025727300045713)
- Thompson P.B, Herndon D.N, Traber D.L & Abston S (1986) Effect on mortality of inhalation injury. Journal of Trauma and Acute Care Surgery, 26(2), 163-165.
- Elkins M & Dentice R (2020) Timing of hypertonic saline inhalation for cystic fibrosis. Cochrane Database of Systematic Reviews, (2). Intervention Version ; publié le 28 février 2020 | https://doi.org/10.1002/14651858.CD008816.pub4 (résumé)
- J.S Patton, C.S Fishburn, J.G Weers (2004) The lungs as a portal of entry for systemic drug delivery. Proc. Am. Thorac. Soc. 1, 338–344.
- M Giardiello, N J Liptrott, T.O McDonald, D Moss, M Siccardi, P Martin, D Smith, R Gurjar, S.P Rannard, A Owen, (2016) Accelerated oral nanomedicine discovery from miniaturized screening to clinical production exemplified by paediatric HIV nanotherapies. Nat. Commun. 7, 13184.
- B.Y.S Kim, J.T Rutka, W.C.W Chan (2010) Nanomedicine. N. Engl. J. Med. 363, 2434–2443
- M.E Davis, J.E Zuckerman, C.H.J Choi, D Seligson, A Tolcher, C.A Alabi, Y Yen, J.D Heidel, A Ribas, (2010) Evidence of RNAi in humans from systemically administered siRNA via targeted nanoparticles. Nature 464, 1067–1070
- M Miragoli, P Novak, P Ruenraroengsak, A.I Shevchuk, Y.E Korchev, M.J Lab, T.D Tetley, J Gorelik (2013) Functional interaction between charged nanoparticles and cardiac tissue: A new paradigm for cardiac arrhythmia? Nanomedicine 8, 725–737.
- Miragoli M & al. (2018) Inhalation of peptide-loaded nanoparticles improves heart failure. Science translational medicine, 10(424), eaan6205.
- Heimbach D.M & Waeckerle J.F (1988) Inhalation injuries. Annals of emergency medicine, 17(12), 1316-1320.
- Thompson P.B, Herndon D.N, Traber D.L & Abston S (1986) Effect on mortality of inhalation injury. The Journal of trauma, 26(2), 163-165 (résumé)
- Sheridan R.L (2016) Fire-related inhalation injury. New England journal of medicine, 375(5), 464-469 (résumé).
- TBSA Burn Estimation Chart
- Thompson, P. B., Herndon, D. N., Traber, D. L., & Abston, S. (1986) Effect on mortality of inhalation injury. The Journal of trauma, 26(2), 163-165.
- Molimard M, Raherison C, Lignot S, Lamarque S, Balestra A, Chartier A, … & Girodet P.O (2017) La mauvaise utilisation des systèmes d’inhalation est associée à la survenue d’exacerbations sévères de BPCO: évaluation en vie réelle de 2935 patients. Revue des Maladies Respiratoires, 34, A6-A7 (résumé).
- Mlcak R.P, Suman O.E & Herndon D.N (2007) Respiratory management of inhalation injury. burns, 33(1), 2-13
Voir aussi
Articles connexes
Liens externes
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Ressources relatives à la santé :
- (en) Medical Subject Headings
- (en) NCI Thesaurus
- (no + nn + nb) Store medisinske leksikon