Acide acétylsalicylique
L’acide acétylsalicylique (AAS), plus connu sous le nom commercial d’aspirine, est un anti-inflammatoire non stéroïdien. C’est la substance active de nombreux médicaments aux propriétés antalgiques, antipyrétiques et anti-inflammatoires. Il est surtout utilisé comme antiagrégant plaquettaire.
| Acide acétylsalicylique | |
| |
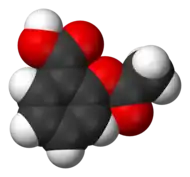
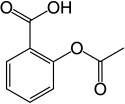 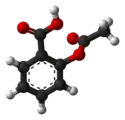 Molécule d'acide acétylsalicylique. |
|
| Identification | |
|---|---|
| Nom UICPA | acide 2-acétyloxybenzoïque |
| Synonymes |
Aspirine |
| No CAS | |
| No ECHA | 100.000.059 |
| No CE | 200-064-1 |
| No RTECS | VO0700000 |
| Code ATC | A01, B01, N02 |
| DrugBank | DB00945 |
| PubChem | 2244 |
| ChEBI | 15365 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores à blancs ou poudre cristalline blanche, d'odeur caractéristique[1] |
| Propriétés chimiques | |
| Formule | C9H8O4 [Isomères] |
| Masse molaire[2] | 180,157 4 ± 0,009 g/mol C 60 %, H 4,48 %, O 35,52 %, |
| pKa | 3,5 |
| Propriétés physiques | |
| T° fusion | 135 °C[1] |
| T° ébullition | Se décompose au-dessous du point d'ébullition à 140 °C[1] |
| Solubilité | 2,5 g·l-1 (eau, 15 °C)[1], 4,6 g·l-1 (eau, 25 °C), |
| Masse volumique | 1,4 g·cm-3[1] |
| Point d’éclair | 131,2 °C |
| Pression de vapeur saturante | 0,016 5 Pa à 25 °C |
| Cristallographie | |
| Classe cristalline ou groupe d’espace | P21/c[5] |
| Paramètres de maille | a = 11,430 Å b = 6,591 Å |
| Volume | 854,23 Å3[5] |
| Propriétés optiques | |
| Indice de réfraction | 1,55 |
| Précautions | |
| SGH[6] - [7] | |
 Attention |
|
| SIMDUT[8] | |
 D2A, |
|
| Écotoxicologie | |
| LogP | 1,19[1] |
| Données pharmacocinétiques | |
| Biodisponibilité | 60 - 90 % selon la dose[9] |
| Liaison protéique | 99,6 % |
| Métabolisme | Hépatique |
| Demi-vie d’élim. | 3,1 h (dose < 650 mg) 5 h (dose = 1 g) 9 h (dose = 2 g) |
| Excrétion | |
| Considérations thérapeutiques | |
| Classe thérapeutique | Antalgique • Antipyrétique • Anti-inflammatoire • Antiagrégant plaquettaire |
| Voie d’administration | Orale, IV |
| Grossesse | Contre-indiqué au 3e trimestre |
| Enfants | Déconseillé aux enfants de 3 à 12 ans (risque de syndrome de Reye) |
| Précautions | Toxicité gastrique |
| Composés apparentés | |
| Isomère(s) | Acide caféique |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
C’est un acide faible, dont la base conjuguée est l’anion acétylsalicylate.
C’est un des médicaments les plus consommés au monde.
Étymologie
L’acide acétylsalicylique est obtenu par acétylation de l’acide salicylique. Son nom vient du latin salix, « saule », cet acide ayant été isolé pour la première fois dans l’écorce de cette essence d’arbre.
L’appellation aspirine vient d'Aspirin enregistrée comme nom de marque le par la société Bayer à Berlin[10] - [11]. Le nom de marque a été formé à partir des éléments suivants[12] :
- Le préfixe A pour Acétyl, l'acétylation rendant ce métabolite secondaire de plantes toxique (son activité allélopathique leur sert de défense chimique contre les herbivores) moins irritant dans le tube digestif ;
- Le radical spir- (issu de l'allemand Spirsäure, « acide spirique », molécule issue de la spirée ulmaire et identique à l'acide salicylique[13]) ;
- Le suffixe -in(e) (suffixe classique employé en chimie industrielle pour la désignation des alcaloïdes).
Le brevet américain demandé le est accordé le (US Patent no 644 077) pour une durée de validité de 17 ans avec une date d'expiration le [14].
Histoire

L’écorce de saule est connue au moins depuis l’Antiquité pour ses vertus curatives. On a trouvé la mention de décoctions de feuilles de saule dans un papyrus égyptien dès 1550 av. J.-C. (papyrus Ebers)[15]. Le médecin grec Hippocrate (460-377 av. J.-C.) conseillait déjà une préparation à partir d’écorce de saule blanc pour soulager les douleurs et les fièvres[16] - [17]. De même, le médecin et pharmacologue grec Dioscoride (25 - 90 ap. J.-C.) en conseillait l'usage pour les douleurs auriculaires, dans sa Matière médicale (De materia medica) au premier siècle[18].
En , le pasteur Edward Stone présente un mémoire devant la Royal Society of Medicine sur l'utilisation thérapeutique de décoctions de l'écorce du saule blanc contre la fièvre malarienne[19].
En 1824 Bartolomeo Rigatelli utilise un extrait d’écorce de saule comme agent thérapeutique, le dénommant salino amarissimo antifebbrile (sel antipyrétique très amer). En 1825 le pharmacien-chimiste Francesco Fontana (1794-1867) isole l'acide salicylique des feuilles de saules lui donnant le nom de salicina (salicine)[20].
En 1828, le pharmacologue allemand Johann Andreas Buchner l'extrait de l'écorce du saule (Salix alba) . En , Pierre-Joseph Leroux, un pharmacien français, tente, après avoir fait bouillir de la poudre d’écorce de saule blanc dans de l’eau, de concentrer sa préparation ; il en résulte des cristaux solubles qu’il nomme salicyline (de salix)[21].
Puis, des scientifiques allemands purifient cette substance active, un des dérivés est identifié comme la substance active. Ce dérivé prend le nom d’acide salicylique. Parmi les dérivés de la salicyline, d'autres médicaments de la famille des salicylacés voient le jour à cette époque.

En , Carl Löwig montre que l’acide spirique, extrait de la reine-des-prés, est chimiquement identique à l’acide salicylique. À partir des extraits naturels, on isole le salicylate de sodium, qui devient alors le médicament couramment employé contre la douleur et l’inflammation. Cette préparation permet de faire tomber la fièvre et de soulager les douleurs et les rhumatismes articulaires, mais provoque de graves brûlures d’estomac. En , à partir de la salicyline, l'Italien Raffaele Piria prépare l'acide salicylique, dont il préconise l'emploi comme désinfectant de la lumière intestinale, notamment dans la fièvre typhoïde.
En , le chimiste strasbourgeois Charles Frédéric Gerhardt effectue la synthèse de l’acide acétylsalicylique (en traitant le salicylate de sodium avec le chlorure d'acétyle), qu’il nomme acide acétosalicylique[22], et dépose un brevet. Cependant, son composé est impur et thermolabile. Le savant meurt trois ans plus tard et ses travaux tombent dans l’oubli.
En , Adolph Wilhelm Hermann Kolbe réussit la synthèse totale de l'acide salicylique. Les propriétés antipyrétiques de l'acide salicylique sont mises en évidence par le Suisse Carl Buss en . Utilisé largement mais surtout comme antirhumatismal dans les années 1890, il a très mauvais goût. En , Germain Sée propose le salicylate de soude comme antipyrétique. Marceli Nencki prépare à partir de un dérivé de l’acide salicylique et du phénol appelé Salol, qui, sans présenter de propriétés pharmacologiques supérieures aux médicaments alors existants, a toutefois un goût plus agréable. Ce produit fait l’objet d’un grand engouement populaire[23].
Felix Hoffmann, chimiste allemand ayant obtenu un doctorat en pharmacie à Munich en 1890, puis un doctorat en chimie le , entre en tant qu'assistant de laboratoire au service des laboratoires Bayer à Elberfeld (Allemagne) en .
Le à Leverkusen, reprenant les travaux antérieurs de Gerhardt, il trouve le moyen de synthétiser l'acide acétylsalicylique sous une forme stable utilisable pour des applications médicales. Il transmet ses résultats à son patron Heinrich Dreser, le responsable du département pharmaceutique et chimique chez Bayer depuis 1896[24]. Ce dernier teste le produit sur le cœur de grenouille, son animal de laboratoire favori, et n'obtient aucun résultat probant. Hoffmann est persuadé de l'intérêt de la molécule (il y a une légende qui indique qu'Hoffmann s'en serait servi pour soigner son père, qui souffrait de rhumatisme chronique et prenait jusque-là du salicylate de sodium, médicament antirhumatismal selon le corps médical de la Belle Époque)[25]. Hoffmann donne le médicament à des amis médecins et dentistes, qui le testent avec succès sur leurs patients pendant deux ans : les tests révèlent un effet antalgique et moins toxique pour l'estomac que le salicylate de sodium, lorsque Hoffmann a acétylé l'acide salicylique pour produire de l'acide acétylsalicylique.
 Protocole de laboratoire de Felix Hoffmann du 10 août 1897.
Protocole de laboratoire de Felix Hoffmann du 10 août 1897.
En 1898, le Dr Dreser fait tester la substance sur un groupe de 50 patients dans un hôpital de Halle (Saxe-Anhalt).
Commence alors la production industrielle du médicament de l'acide acétylsalicylique par Bayer, qui met au point une nouvelle voie de synthèse de la molécule, et observe que l'acétylation de la molécule rend celle-ci moins irritante dans le tube digestif[26]. Le brevet et la marque de l'aspirine sont déposés le par la société Bayer sous la dénomination d'Aspirin[27].
C'est le Dr Kurt Witthauer (de), médecin-chef interniste au Diakoniewerk Halle (de), qui publie les résultats du premier essai clinique de l'aspirine en .
Initialement, l'Aspirin est disponible sous forme de poudre dans les pharmacies : de petits sacs en papier sont remplis de 500 mg de poudre chacun et remis au patient. Dès l'année suivante, le comprimé Aspirin contenant 500 mg d'acide acétylsalicylique est lancé, ce qui en fait l'une des premières préparations sous forme de comprimé au monde[11]. La préparation arrive en France en 1908 et est commercialisée par la Société chimique des usines du Rhône.
 Aspirin Bayer (1899)
Aspirin Bayer (1899) Couverture du premier rapport clinique du Dr Kurt Witthauer sur l'Aspirine (1899)
Couverture du premier rapport clinique du Dr Kurt Witthauer sur l'Aspirine (1899) Présentation pharmacologique de l'Aspirine, par le Dr Heinrich Dreser (1899)
Présentation pharmacologique de l'Aspirine, par le Dr Heinrich Dreser (1899) Réclame de 1923 en France (L'Illustration)
Réclame de 1923 en France (L'Illustration)
En , le supérieur hiérarchique direct d'Hoffmann, Arthur Eichengrün (en), publie un article revendiquant la paternité de la découverte[28]. Cette revendication est ignorée par les historiens des sciences jusqu'en , date à laquelle les recherches de Walter Sneader de l'université de Strathclyde, à Glasgow, concluent que c'est bien Eichengrün qui a eu l'idée de synthétiser l'acide acétylsalicylique[29]. Bayer, dans un communiqué de presse, réfute cette théorie, mais la controverse reste ouverte.
Le mécanisme d'action de la molécule n'est élucidé que bien plus tard. En , John Vane et Priscilla Piper découvrent l'action inhibitrice de l'aspirine sur les prostaglandines[30]. Vane et les biochimistes suédois Bengt Samuelsson et Sune Karl Bergström sont récompensés par le prix Nobel de médecine en pour cette découverte. La cible précise de la molécule, la cyclooxygénase, a été isolée en [31].
Ce n'est qu'en que les propriétés antiagrégantes plaquettaires de l'acide acétylsalicylique ont été mises en évidence[32]. La première étude clinique démontrant une efficacité dans les maladies cardiovasculaires date de [33].
Le brevet Bayer
Après la Première Guerre mondiale, le traité de Versailles stipule que la marque et le procédé de fabrication entrent dans le domaine public dans un certain nombre de pays (France, États-Unis, etc.) mais pas dans d'autres (comme le Canada).
Après l’entrée en guerre des États-Unis contre l’Allemagne en , le Bureau d'administration des biens étrangers (en) a saisi les biens américains de Bayer. Deux ans plus tard, le nom de la société Bayer et les marques commerciales aux États-Unis et au Canada ont été vendus aux enchères et achetés par le laboratoire pharmaceutique Sterling Products Company (en), devenu plus tard Sterling Winthrop, pour un montant de 5,3 millions de dollars.
Aux États-Unis la marque a été partiellement annulée par une décision de justice de 1921 car Bayer n'avait pas utilisé correctement le nom de son propre produit et avait autorisé pendant des années l'utilisation de la mention « aspirine » par d'autres fabricants sans défendre ses droits de propriété intellectuelle[34]. Une mention en rouge « Authentique » (Genuine), figurait sur les boîtes et apparaissait dans la publicité des comprimés d'aspirine de Bayer peu de temps après la décision de 1921[35].
La société Bayer n'a récupéré ses droits aux États-Unis qu'en en rachetant l'activité de vente libre de Sterling Winthrop[36]. Bayer a repris à compter de cette date les droits sur le nom et le logo de Bayer et a permis à l’entreprise de profiter à nouveau des ventes américaines de son produit le plus célèbre[10].
Aujourd'hui, l'aspirine est une marque générique dans de nombreux pays. L'aspirine, avec un A majuscule, reste une marque déposée de Bayer en Allemagne, au Canada, au Mexique et dans plus de 80 pays, pour l'acide acétylsalicylique sur tous les marchés, mais en utilisant des emballages et des aspects physiques différents pour chaque[37].
Propriétés pharmacologiques
L'aspirine possède les propriétés pharmacologiques suivantes :
- antalgique (diminution de la douleur) ;
- antipyrétique (diminution de la fièvre) ;
- anti-inflammatoire non stéroïdien ;
- antiagrégant plaquettaire (empêche la coagulation du sang).
Mécanisme d'action
L'aspirine inhibe la production de prostaglandines et de thromboxanes. L'aspirine par une réaction chimique d'acétylation inhibe de façon irréversible les enzymes cyclooxygénase (COX1 et COX2), des enzymes participant à la production de prostaglandines et de thromboxanes. L'aspirine est différente des autres anti-inflammatoires non stéroïdiens (AINS) qui inhibent de façon réversible cette enzyme.
L'aspirine fait baisser la fièvre (antipyrétique), en réduisant la production de prostaglandines dans l'hypothalamus, thermostat de la température corporelle.
Elle réduit la douleur (analgésique) en bloquant la production des hormones responsables des messages transmis aux récepteurs de la douleur dans le cerveau, d'où son efficacité sur les migraines et les douleurs d'origines diverses. Par le même mode d'action, elle réduit les inflammations (AINS) résultant d'une dilatation vasculaire, comme les coups de chaleur, qui ne s'accompagnent pas forcément de coups de soleil.
L'aspirine agit sur les plaquettes sanguines, en inhibant la cyclooxygénase, une enzyme ayant un rôle important dans l'agrégation des plaquettes, et ce, de manière permanente, c'est-à-dire durant toute la durée de vie de la plaquette jusqu'à ce qu'elle soit détruite par la rate (entre sept et dix jours). Elle favorise par ce biais la circulation et peut servir pour prévenir les infarctus (du myocarde ou d'autres organes), en évitant la formation de caillots (thrombose)[38].
L'acide acétylsalicylique pourrait avoir une action sur le système immunitaire[39] en stimulant légèrement (à faible dose) ou au contraire en inhibant (à forte dose) la production des cytokines[40].
Pharmacocinétique
L'aspirine est absorbée au niveau de l'estomac et du duodénum. Le facteur de biodisponibilité dépend de la dose : de 60 % pour moins de 500 mg à 90 % pour 1 g ou plus par saturation de l’hydrolyse hépatique[9]. La prise de certains aliments épicés semble réduire le taux d'absorption[41].
Pour les formes pharmaceutiques immédiates, le pic de concentration est atteint de 25 à 60 minutes après la prise[9]. Il peut être atteint plusieurs heures après pour une forme gastro-résistante ou à libération modifiée. L’absorption peut être fortement perturbée dans ces dernières formes, en particulier chez le patient diabétique[42].
Sa demi-vie dans le sang n'est que de 15 à 20 minutes et de 2 à 4 heures pour l'acide salicylique qui est un métabolite actif obtenu par hydrolyse[9].
Douleur, fièvre et inflammation
L'aspirine est utilisée depuis plus de cent ans pour soulager la douleur, faire baisser la fièvre et traiter l'inflammation.
Elle n'est plus indiquée pour traiter ces symptômes, on préfèrera utiliser d'autre AINS comme l'ibuprofène ou des antalgiques/antipyrétique comme le paracétamol.
Maladies cardiovasculaires
À petite dose (entre 75 et 300 mg/jour suivant les études), les propriétés antiagrégantes de l'aspirine préviennent efficacement la formation de caillots de sang dans les vaisseaux sans causer de dommages significatifs à l'organisme. Le bénéfice de cette prise a été prouvé en prévention secondaire[43], c'est-à-dire après un premier accident vasculaire (syndrome coronarien aigu, AVC, AOMI...) et elle est indiquée à vie. Le bénéfice excède significativement le risque majoré d'hémorragie dans ce cas.
Les recommandations médicales de la HAS[44] préconisent l'emploi de l'aspirine en prévention primaire (c'est-à-dire avant même l'apparition d'une maladie vasculaire) chez les patients à haut risque cardio-vasculaire (SCORE>5). L'efficacité semble être partielle (diminution des infarctus du myocarde mais tendance à l'augmentation des accidents vasculaires cérébraux de type hémorragique) et n'a été testée que sur des populations bien ciblées (médecins)[45] ou femmes de plus de 45 ans avec une diminution modérée des accidents vasculaires cérébraux mais un effet sur la mortalité et la morbidité cardiovasculaire non significatif[46]. Une plus grande efficacité chez la femme que chez l'homme a aussi été constatée[47]. Les résultats sont plus mitigés pour d'autres études, bien qu'elles soient faites chez des personnes dites « à hauts risques »[48] - [49]. En particulier, il n' y a pas de diminution de la mortalité cardiovasculaire, avec une augmentation du risque d'hémorragies[50].
Une « résistance à l'aspirine » est décrite chez certains patients, conduisant à une antiagrégation plaquettaire insuffisante[51] et concernerait environ 5 % des patients[52], avec un risque théorique supérieur d'accidents cardiaques. Cette résistance serait plus liée avec la forme gastro résistante de la présentation de l'aspirine, conduisant à une absorption différée ou réduite qu'avec la molécule elle-même[53].
Réduction du risque de cancer
Un grand nombre de données expérimentales, ainsi que plusieurs études épidémiologiques rétrospectives, ont conclu que de petites doses d'aspirine en chimioprévention pouvaient diminuer le risque de contracter certains types de cancers, dont ceux du foie[54]. Les études expérimentales le montrent pour divers cancers, comme celui du côlon, du sein, de la prostate, de la bouche, de la gorge, de l'œsophage, de l'estomac et du poumon (non à petites cellules). Les études épidémiologiques montrent que c'est la mortalité par cancers digestifs qui diminuerait le plus[55].
Une vingtaine d'études de cancérogenèse chez rats et souris étayent cet effet protecteur[56]. Plusieurs essais cliniques montrent que de petites doses d'aspirine diminuent, modestement, la récurrence des polypes intestinaux et la survenue des cancers du côlon[57], essentiellement si ces derniers expriment l'enzyme cyclooxygénase de type 2 (ce qui représente environ deux tiers desdits cancers)[58]. Les doses indiquées étant cependant susceptibles de provoquer des saignements gastriques ou intestinaux, l'utilisation de l'aspirine n'est pas actuellement recommandée pour la prévention des cancers[59].
Grossesse
A petites doses, chez la femme enceinte, la prise d'aspirine diminue le risque de prématurité, du moins, dans les pays avec accès limités aux soins[60].
La prise d'aspirine à 75 mg/jour augmenterait l'efficacité de la fécondation in vitro en améliorant la vascularisation de l'utérus[61].
La prise quotidienne d'aspirine à faible dose (entre 100 et 150 mg selon les études) permettrait de réduire significativement le risque de développer une pré-éclampsie au cours de la grossesse pour les femmes à risque[62]. Cette maladie, également appelée toxémie gravidique, est une des principales causes des décès maternels, jusqu'à 20 %. L'aspirine ayant pour effet de fluidifier le sang permet de diminuer l'hypertension et les dangers qui y sont liés. Toutefois il semble que la prise d'aspirine doive commencer tôt dans la grossesse afin d'empêcher la formation d'anomalies au niveau des artères intra-utérines qui seront la cause de la pré-éclampsie.
Effets secondaires
Ses effets secondaires sont essentiellement des troubles gastriques (exemple : gastrite voire hémorragie digestive en cas de dose élevée) et des allergies (pouvant provoquer l'œdème de Quincke). Certaines présentations de l'aspirine, dites « entériques » diminuent l’absorption de la molécule au niveau de l'estomac, alléguant une protection de ce dernier, mais qui n'est pas du tout démontrée[63].
De manière générale, l'aspirine inhibe l'agrégation plaquettaire. Par conséquent, le risque d'hémorragie est à prendre en compte, surtout s'il y a déjà prescription d'anticoagulants.
Contre-indications et précautions
Elle est ainsi totalement contre-indiquée chez les personnes souffrant d'hémophilie. Elle est évidemment déconseillée en cas de plaie en début de cicatrisation.
Elle est déconseillée en tant que prévention primaire de maladies cardiovasculaires, la balance bénéfice-risque n'étant pas favorable.
L'aspirine doit être utilisée avec prudence chez le nourrisson et l'enfant, car en cas de surdosage (au-dessus de 50 mg par kg et par jour), elle est neurotoxique. En outre, elle peut entraîner l'apparition du syndrome de Reye en cas de varicelle ou de grippe. En effet, l'aspirine peut aussi provoquer un syndrome de Lyell (syndrome d'origine médicamenteuse) à l'origine d'une destruction des kératinocytes, décollement dermique et atteinte des muqueuses.
Les cardiaques, sous traitement au long cours à petites doses en raison de son effet antiagrégant, peuvent être exposés à ses effets secondaires. Le bénéfice du traitement reste cependant de loin supérieur au risque, ce qui justifie sa prescription.
Chez les personnes souffrant d'un ulcère gastrique, l'aspirine peut occasionner une hémorragie digestive, par inhibition de la synthèse des prostaglandines, substances protectrices pour la muqueuse de l'estomac.
Lors d'une grossesse, elle peut être prise à titre ponctuel pendant les deux premiers trimestres (notamment associée à l'héparine pour prévenir le risque de fausse-couche lors du syndrome des antiphospholipides). Puis, l'utilisation d'aspirine est contre-indiquée au troisième trimestre : sur le fœtus à partir du sixième mois, ce type de médicament exerce des effets vasoconstricteurs au niveau des reins et peut conduire à une insuffisance rénale ou encore à des troubles de l'appareil cardiopulmonaire.
Ce médicament passe dans le lait, mais compte tenu de la demi-vie d'élimination très courte, l'usage de ce médicament est généralement autorisé pendant l'allaitement en utilisation de courte durée (quelques jours).
En cas de risque de dengue, l'utilisation de médicaments à base d'aspirine est fortement désapprouvée, vu le risque d'apparition de la forme hémorragique de la maladie. Cet avis doit accompagner, au Brésil, toute publicité du produit[64].
Chez les personnes présentant un syndrome de Widal (association d'asthme, polypose nasale et allergie à l'aspirine), la prise d'aspirine peut entraîner des difficultés respiratoires allant jusqu'à la crise d'asthme[65].
Par ailleurs, la prise d'aspirine (comme celle d'anti-inflammatoires ou d'antibiotiques, médicaments ototoxiques) a été signalée comme pouvant occasionner une perte d'audition ou l'apparition d'acouphènes [66]. De manière anecdotique, lors de la pandémie de grippe espagnole (vers 1919), de très fortes doses d'aspirine telles qu'elles ont été préconisées à l'époque (plus de 8 g en 24 h) ont pu contribuer à accroître la mortalité et la sévérité des symptômes [67] - [64].
Propriétés chimiques

L'acide acétylsalicylique est la dénomination commune internationale de l'acide 2-(acétyloxy) benzoïque (selon les normes IUPAC).
Au cours des années, il fut aussi appelé acide 2-acétyloxybenzoïque, acide 2-acétoxybenzoïque, acétylsalicylate, acide ortho-acétylsalicylique, acide ortho-acétyloxybenzoïque ou encore acétosal.
Les pharmacopées européenne (Ph. Eur.), américaine (USP) et japonaise (en) décrivent des méthodes d'identification et d'analyses de l'acide acétylsalicylique destiné aux médicaments.
Synthèse
La synthèse initiale de Gerhardt décrite en 1853[22] fut améliorée en 1975[68]. Elle est assez simple et consiste en l'estérification de la fonction hydroxyle de l'acide salicylique avec l'anhydride acétique, en milieu acide. On obtient l'acide acétylsalicylique et de l'acide acétique comme sous-produit (la synthèse de l'acide salicylique se fait par réaction de Kolbe).

La purification peut se faire de deux manières : par recristallisation dans l'acétone (selon un brevet de Monsanto de 1959), par recristallisation dans un solvant mixte éthanol/eau 1:2,5 ou par un procédé mettant en œuvre une distillation (brevet de Norwich Pharma de 1966). Le produit purifié se présente sous la forme de cristaux blancs en forme d'aiguille.
Un test au chlorure de fer(III) FeCl3 peut servir à déterminer l'éventuelle présence d'acide salicylique n'ayant pas réagi. Le chlorure de fer(III) réagit avec le groupe OH phénol et donne lieu à une coloration rouge du produit.
Marché
C'est un des médicaments les plus consommés au monde, avec une consommation annuelle estimée à 40 000 t, soit l'équivalent de 120 milliards de comprimés de 300 mg[69]. En 2008, 85 % de la production d'acide acétylsalicylique est réalisée à Langreo en Espagne, dans une usine chimique de la multinationale Bayer[69]. De là, il est envoyé dans le monde entier où il est intégré à de nombreuses autres préparations.
En France, 237 médicaments commercialisés contiennent de l'aspirine. Annuellement, 1 500 t d'aspirine sont consommées[70]. Sachant qu'un comprimé contient 500 mg, chaque Français consomme en moyenne soixante comprimés d'aspirine par an.
Il est concurrencé par le paracétamol, autre antalgique et antipyrétique mais dépourvu d'effets au plan gastrique (l'aspirine favorise l'ulcère comme les autres anti-inflammatoires non stéroïdiens). En revanche, le paracétamol a des effets néfastes irréversibles sur le foie à très fortes doses. L'acide acétylsalicylique reste un antiagrégant plaquettaire de référence.
Divers
L'aspirine fait partie de la liste modèle des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en novembre 2015)[71].
Dans les années 1980, il était concevable dans certains milieux sportifs d’utiliser un cachet d’aspirine lors de la reprise des entraînements après long arrêt afin de diminuer les effets de courbature des muscles.
Aspirine est une nouvelle d'Amélie Nothomb (2001) comprenant des histoires autour de l'aspirine.
Notes et références
- ACIDE 2 - ACETYLOXYBENZOIQUE, Fiches internationales de sécurité chimique .
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Acetylsalicylic Acid », sur Hazardous Substances Data Bank (consulté le ).
- (en) R. E. Kirk (dir.), D. F. Othmer (dir.) et al., Encyclopedia of Chemical Technology, vol. 22 : Silicon Compounds to Succinic Acid and Succinic Anhydride, Wiley-Interscience, , 4e éd., 1136 p. (ISBN 9780471526919, présentation en ligne).
- « Acetyl salicylic acid », sur www.reciprocalnet.org (consulté le ).
- « Acide acétylsalicylique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009.
- « RCP aspirine comprimé »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ), AFSSAPS.
- (en) History, « Bayer patents aspirin », sur history.com (consulté le ).
- (de) Bayer Austria, « Geschichte : Histoire », sur aspirin.at (consulté le ).
- Dominique Frémy, Quid, Éditions Robert Laffont, , p. 183
- Le terme d'aspirine a été forgé pour distinguer de l'acide acétylsalicylique naturel, extrait des fleurs de la reine-des-prés ou spirée ulmaire (à l'époque, le nom latin binomial de cette plante était Spiraea ulmaria), d'où le nom d'acide spirique dont la structure est équivalente à l'acide salicylique extraite de l'écorce du saule (Salix alba).
- (en) Farbenfabriken of Elberfeld Co, « Patent US 644077A : Acetyl salicylic acid. », sur patents.google.com (consulté le ).
- Olivier Bruzek, Pour l'Aspirine, 10001 Mots, , 40 p. (ISBN 9782371980037, lire en ligne), Début chapitre II
- (en) Mary Bellis, « History of Aspirin », sur http://inventors.about.com.
- H. Lévesque et O. Lafont, « L'aspirine à travers les siècles: Rappel historique », La Revue de Médecine Interne, vol. 21, , S8–S17 (ISSN 0248-8663, DOI 10.1016/S0248-8663(00)88720-2, lire en ligne, consulté le )
- Olivier Lafont, « Revue d'Histoire de la Pharmacie : Du saule à l'aspirine », sur persee.fr, (consulté le ).
- (en) E. Stone, « An account of the success of the bark of the willow in the cure of agues », Philos. Trans., vol. 53, no titre, , p. 195-200 (ISSN 0261-0523, DOI 10.1098/rstl.1763.0033).
- (en) Marson Piero, Giampiero Pasero, « The Italian contributions to the history of salicylates », sur researchgate.net, (consulté le ).
- L. J. Gay-Lussac et F. Magendie, « Rapport fait à l'Académie royale des sciences le 10 mai 1830, sur le mémoire de M. Leroux, relatif à l'analyse de l'écorce de saule et à la découverte d'un principe immédiat propre à remplacer le sulfate de quinine », J. Chim. Med. Pharm. Toxicol., vol. 6, no titre, , p. 340-342 (lire en ligne).
- (de) C. Gerhardt, « Untersuchungen über die wasserfreien organischen Säuren », Liebigs Annalen, vol. 87, no 2, , p. 149–179 (ISSN 0075-4617, DOI 10.1002/jlac.18530870206).
- Philippe Albou, « Histoire du traitement de la fièvre avant l'aspirine » [vidéo], Société française d'histoire de la médecine, .
- (en) Tabea Tietz, « Felix Hoffmann and the Synthesis of Aspirin », sur scihi.org, (consulté le ).
- Pierre Bachoffner, « Les deux "pharmaciens" à l'aube de l'aspirine : Charles Gerhardt et Felix Hoffmann », sur persee.fr, (consulté le ).
- (en) Diarmuid Jeffreys, Aspirin: The Remarkable Story of a Wonder Drug, Bloomsbury Publishing, , p. 69-75
- (en) V. Fuster et J. M. Sweeny, « Aspirin - A Historical and Contemporary Therapeutic Overview », Circulation, vol. 123, no titre, , p. 768-778 (ISSN 0009-7322, DOI 10.1161/CIRCULATIONAHA.110.963843).
- (de) A. Eichengrün, « 50 Jahre Aspirin », Pharmazie, vol. 4, no titre, , p. 582-584.
- (en) W. Sneader, « The discovery of aspirin: a reappraisal », BMJ, vol. 321, no 7276, , p. 1591–1594 (ISSN 0959-8138, PMCID PMC1119266, DOI 10.1136/bmj.321.7276.1591, lire en ligne).
- (en) J. R. Vane, « Inhibition of prostaglandin synthesis as a mechanism of action for aspirin-like drugs », Nat. New. Biol., vol. 231, no 25, , p. 232-235 (PMID 5284360, DOI 10.1038/newbio231232a0).
- (en) M. Hemler, W. E. Lands et al., « Purification of the cyclooxygenase that forms prostaglandins. Demonstration of two forms of iron in the holoenzyme », J. Biol. Chem., vol. 251, no titre, , p. 5575-5579 (ISSN 0021-9258, lire en ligne).
- (en) H. J. Weiss et L. M. Aledort, « Impaired platelet-connective-tissue reaction in man after aspirin ingestion », Lancet, vol. 290, no 7514, , p. 495-497 (ISSN 0140-6736, DOI 10.1016/S0140-6736(67)91658-3).
- (en) The Canadian Cooperative Study Group, « A Randomized Trial of Aspirin and Sulfinpyrazone in Threatened Stroke », N. Engl. J. Med., vol. 299, no titre, , p. 53-59 (ISSN 0028-4793, DOI 10.1056/NEJM197807132990201).
- (en) United States District Court for the Southern District of New York (en), « Bayer Co. v. United Drug Co., 272 F. 505 (S.D.N.Y. 1921) : Bayer Co contre United Drug Co », sur cyber.harvard.edu, (consulté le ).
- (en) National Museum of American History, « Bayer-Tablets of Aspirin : Bayer-comprimés d'aspirine », sur americanhistory.si.edu (consulté le ).
- H. Lévesque et O. Lafont, L'aspirine à travers les siècles : rappel historique, La Revue de médecine interne, 2000 ; 21 Suppl. 1 : 8-17, Éditions scientifiques et médicales Elsevier, 2000, lire en ligne [PDF], p. 7.
- (en) Société Radio-Canada, « Aspirin: the versatile drug : Aspirine : le médicament polyvalent », sur cbc.ca, (consulté le ).
- (en) Volker Knappertz, « The dose of aspirin for the prevention of cardiovascular and cerebrovascular events - PubMed », Current medical research and opinion, vol. 22, no 7, , p. 1239–1248 (ISSN 0300-7995, PMID 16892516, DOI 10.1185/030079906x112624, lire en ligne, consulté le ).
- (en) M. Jäpel, H. Lötzerich et al., « Role of Acetylsalicylic Acid in Cytokine Stimulation of Macrophages in Antibody-Dependent Cellular Cytotoxicity (ADCC) », Mediators Inflamm., vol. 3, no 6, , p. 419-424 (ISSN 0962-9351, PMCID PMC2365582, DOI 10.1155/S0962935194000591, lire en ligne).
- (en) C. Härtel, J. Von Puttkamer et al., « Dose-dependent Immunomodulatory Effects of Acetylsalicylic Acid and Indomethacin in Human Whole Blood: Potential Role of Cyclooxygenase-2 Inhibition », Scand. J. Immunol., vol. 60, no 4, , p. 412–420 (ISSN 1365-3083, DOI 10.1111/j.0300-9475.2004.01481.x, lire en ligne).
- (en) L. Cruz, G. Castañeda-Hernández et al., « Ingestion of chilli pepper (Capsicum annuum) reduces salicylate bioavailability after oral aspirin administration in the rat », Canadian Journal of Physiology and Pharmacology, vol. 77, no 6, , p. 441-446 (ISSN 0008-4212, DOI 10.1139/y99-032).
- Bhatt DL, Grosser T, Dong JF et al., Enteric coating and aspirin nonresponsiveness in patients with type 2 diabetes mellitus, J. Am. Coll. Cardiol., 2017, 69:603–612.
- (en) Antithrombotic Trialists' Collaboration, « Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients », BMJ, vol. 324, no titre, , p. 71-86 (ISSN 0959-8138, DOI 10.1136/bmj.324.7329.71, lire en ligne).
- « Bon usage des agents antiplaquettaires » [PDF], sur has-sante.fr,
- (en) Steering Committee of the Physicians' Health Study Research Group, « Final Report on the Aspirin Component of the Ongoing Physicians' Health Study », N. Engl. J. Med., vol. 321, no 3, , p. 129-135 (ISSN 0028-4793, DOI 10.1056/NEJM198907203210301, lire en ligne).
- (en) P. M. Ridker, N. R. Cook et al., « A Randomized Trial of Low-Dose Aspirin in the Primary Prevention of Cardiovascular Disease in Women », N. Engl. J. Med., vol. 352, no 13, , p. 1293-1304 (ISSN 0028-4793, DOI 10.1056/NEJMoa050613, lire en ligne).
- (en) « Malignant melanoma associated with chronic once-daily aspirin exposure in males: A large, single-center, urban, US patient population cohort study from the “Research on Adverse Drug events And Report” (RADAR) project », sur www.jaad.org, (consulté le )
- (en) « Low-Dose Aspirin for Primary Prevention of Atherosclerotic Events in Patients With Type 2 Diabetes », JAMA, vol. 300, no 18, , p. 2134-2141 (ISSN 0098-7484, PMID 18997198, DOI 10.1001/jama.2008.623, lire en ligne).
- (en) G. R. Fowkes, J. F. Price et al., « Aspirin for Prevention of Cardiovascular Events in a General Population Screened for a Low Ankle Brachial Index », JAMA, vol. 303, no 9, , p. 841-848 (ISSN 0098-7484, PMID 20197530, DOI 10.1001/jama.2010.221, lire en ligne).
- Mahmoud AN, Gad MM, Elgendy AY, Elgendy IY, Bavry AA, Efficacy and safety of aspirin for primary prevention of cardiovascular events: a meta-analysis and trial sequential analysis of randomized controlled trials, Eur Heart J, 2019;40:607–617
- Hennekens CH, Schror K, Weisman S, FitzGerald GA, Terms and conditions: semantic complexity and aspirin resistance, Circulation, 2004, 110:1706–1708.
- Gum PA, Kottke-Marchant K, Poggio ED et al., Profile and prevalence of aspirin resistance in patients with cardiovascular disease, Am. J. Cardiol., 2001, 88:230–235.
- Grosser T, Fries S, Lawson JA et al., Drug resistance and pseudoresistance: An unintended consequence of enteric coating aspirin, Circulation, 2013, 127:377-385.
- Simon TG, Duberg AS, Aleman S et al. Association of aspirin with hepatocellular carcinoma and liver-related mortality, N Engl J Med, 2020;382:1018-1028
- (en) D. M. Schreinemachers et R. B. Everson, « Aspirin use and lung, colon, and breast cancer incidence in a prospective study », Epidemiology, vol. 5, no 2, , p. 138-146 (ISSN 1044-3983, lire en ligne).
- chimioprévention, INRA.
- (en) A. T. Chan, « Aspirin, non-steroidal anti-inflammatory drugs and colorectal neoplasia: future challenges in chemoprevention », Cancer Cause. Control, vol. 14, no 5, , p. 413-418 (ISSN 0957-5243, DOI 10.1023/A:1024986220526, lire en ligne).
- (en) A. T. Chan, S. Ogino et al., « Aspirin and the risk of colorectal cancer in relation to the expression of COX-2 », N. Engl. J. Med., vol. 356, no 21, , p. 129-135 (ISSN 0028-4793, DOI 10.1056/NEJMoa067208, lire en ligne).
- (en) U.S. Preventive Services Task Force, « Routine aspirin or nonsteroidal anti-inflammatory drugs for the primary prevention of colorectal cancer: U.S. Preventive Services Task Force recommendation statement », Ann. Intern. Med., vol. 146, no 5, , p. 361-364 (ISSN 0003-4819, PMID 17339621, lire en ligne).
- Hoffman MK, Goudar SS, Kodkany BS et al. Low-dose aspirin for the prevention of preterm delivery in nulliparous women with a singleton pregnancy (ASPIRIN): a randomised, double-blind, placebo-controlled trial, Lancet, 2020;395:285-293
- « Low-dose aspirin in a short regimen as standard treatment in in vitro fertilization: a randomized, prospective study ».
- (en) Emmanuel Bujold, « Low-dose aspirin reduces morbidity and mortality in pregnant women at high-risk for preeclampsia », Evid Based Nurs, vol. 18, no 3, , p. 71. (PMID 25743941, DOI 10.1136/ebnurs-2014-101915).
- Kelly JP, Kaufman DW, Jurgelon JM et al., Risk of aspirin-associated major upper-gastrointestinal bleeding with enteric-coated or buffered product, Lancet, 1996, 348:1413–1416.
- (pt) Sare Drogarias, « Efeitos Colaterais de Somalgin - Ácido Acetilsalicílico: : Effets secondaires de Somalgin - Acide acétylsalicylique : », sur saredrogarias.com.br (consulté le ).
- G Bochenek, K Bánska, Z Szabó, E Nizankowska et A Szczeklik, « Diagnosis, prevention and treatment of aspirin-induced asthma and rhinitis », Current drug targets. Inflammation and allergy, vol. 1, no 1, , p. 1–11 (PMID 14561202, DOI 10.2174/1568010023345011, lire en ligne).
- Biorl Acouphènes, « Attention aux médicaments qui provoquent des acouphènes! », sur biorl.fr, (consulté le ).
- (en) K. M. Starko, « Salicylates and Pandemic Influenza Mortality, 1918–1919 Pharmacology, Pathology, and Historic Evidence », Clin. Infect. Dis., vol. 49, no 9, , p. 1405-1410 (ISSN 1058-4838, DOI 10.1086/606060, lire en ligne).
- (en) F. A. Lowenheim (dir.) et M. K. Moran (dir.), Faith, Keyes & Clark's industrial chemicals, New York, Wiley-Interscience, , 4e éd.
- (en) T. D. Warner et J. A. Mitchell, « Cyclooxygenase-3 (COX-3): Filling in the gaps toward a COX continuum? », Proc. Natl. Acad. Sci. USA, vol. 99, no 21, , p. 13371-13373 (ISSN 0027-8424, PMID 12374850, DOI 10.1073/pnas.222543099).
- dossier de ac-nancy-metz.fr, introduction.
- WHO Model List of Essential Medicines, 19th list, novembre 2015.
Voir aussi
Bibliographie
- Marie Germaine Bousser, L'aspirine, pour ou contre ?, Éd. Le pommier, 2006.
Articles connexes
Sites internet
- Compendium suisse des médicaments : spécialités contenant Acide acétylsalicylique
- Site canadien, sur aspirin.ca.
Bases de données
- Ressources relatives à la santé :
- ChEMBL
- DrugBank
- (en) Australian Register of Therapeutic Goods
- (en) International Union of Pharmacology
- (en) Medical Subject Headings
- (en + es) MedlinePlus
- (en) National Drug File
- (en) PatientLikeMe
- (no + nn + nb) Store medisinske leksikon
- (cs + sk) WikiSkripta
- Notices dans des dictionnaires ou encyclopédies généralistes :