Toluène
Le toluène, également appelé méthylbenzène ou phénylméthane est un hydrocarbure aromatique. Il est couramment utilisé en tant que réactif ou solvant, notamment dans le milieu industriel. Il dissout un grand nombre d'huiles, graisses, ou résines (naturelles ou de synthèse). Dans les conditions normales, c'est un liquide transparent à l'odeur caractéristique, rappelant celle du dissolvant pour peinture ou celle du benzène apparenté.
| Toluène | |
| |
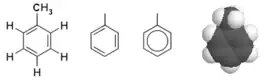
| Structure et représentations du toluène. | |
| Identification | |
|---|---|
| Nom UICPA | toluène |
| Synonymes |
méthylbenzène |
| No CAS | |
| No ECHA | 100.003.297 |
| No CE | 203-625-9 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | liquide incolore, d'odeur caractéristique[1] |
| Propriétés chimiques | |
| Formule | C7H8 [Isomères] |
| Masse molaire[2] | 92,138 4 ± 0,006 2 g/mol C 91,25 %, H 8,75 %, |
| Moment dipolaire | 0,375 ± 0,010 D[3] |
| Susceptibilité magnétique | 66,1 × 10−6 cm3 mol−1[4] |
| Diamètre moléculaire | 0,568 nm[5] |
| Propriétés physiques | |
| T° fusion | −95 °C[1] |
| T° ébullition | 110,58 °C[6] |
| Solubilité | 0,53 g l−1 dans l'eau infinie dans l'éthanol, l'acétone, l'hexane, le dichlorométhane |
| Paramètre de solubilité δ | 18,2 MPa1/2 (25 °C)[7] |
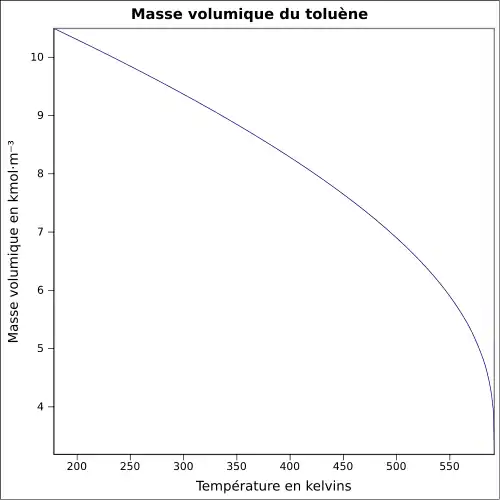
| Masse volumique | 0,867 0 g cm−3[8]
|
| T° d'auto-inflammation | 480 °C[1] |
| Point d’éclair | 4 °C (coupelle fermée)[1] |
| Limites d’explosivité dans l’air | 1,1–7,1 %vol[1] |
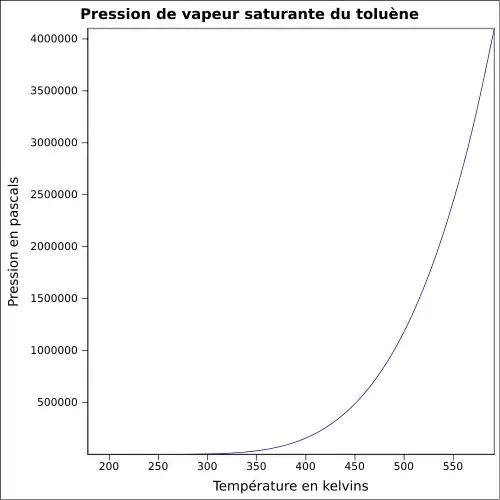
| Pression de vapeur saturante | 29 hPa (20 °C)
|
| Viscosité dynamique | 0,59 × 10−3 Pa s à 20 °C[10] |
| Viscosité cinématique | 0,681 × 10−6 m2 s−1 |
| Point critique | 318,65 °C[6], 41,1 bar[11] |
| Thermochimie | |
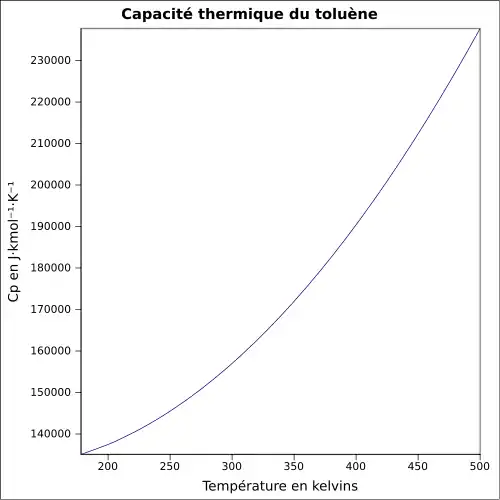
| Cp | |
| PCS | 3 910,3 kJ mol−1 (25 °C, liquide)[13] |
| Propriétés optiques | |
| Indice de réfraction | 1,4941[5] |
| Précautions | |
| SGH[14] | |
   Danger |
|
| SIMDUT[15] | |
  B2, D2A, D2B, |
|
| NFPA 704 | |
| Transport | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[16] | |
| Inhalation | Nausée, vomissements |
| Écotoxicologie | |
| LogP | 2,69[1] |
| DJA | 0,22 mg/kg p.c./jour[17] |
| Seuil de l’odorat | bas : 0,16 ppm haut : 37 ppm[18] |
| Unités du SI et CNTP, sauf indication contraire. | |
Historique
Le composé est isolé la première fois en 1837 par distillation de l'huile de pin par le chimiste polonais Philippe Walter (en) qui le baptise « rétinnaphte »[19] - [20]. En 1841, le chimiste français Henri Sainte-Claire Deville l'isole du baume de Tolu – un extrait aromatique de l'arbre tropical colombien Myroxylon balsamum – que Deville identifie à la rétinnaphte de Walter et au benzène ; il appelle alors ce nouvel hydrocarbure « benzoène »[21] - [22] - [23]. En 1843, Jöns Jacob Berzelius recommande le nom « toluin »[24]. En 1850, le chimiste français Auguste Cahours isole un hydrocarbure d'un distillat de bois qu'il reconnaît identique au « benzoène » de Deville qu'il baptise « toluène »[25] - [26].
Propriétés chimiques
Le toluène réagit comme un hydrocarbure aromatique normal par substitution électrophile aromatique. Le groupe méthyle le rend approximativement 25 fois plus réactif que le benzène dans ce genre de réactions. Par sulfonation, il donne l'acide paratoluènesulfonique, tandis que sa chloration par le chlore en présence de chlorure ferrique donne un mélange d'isomères ortho et para de chlorotoluène. La nitration par l'acide nitrique donne un mélange d'ortho- et de para-nitrotoluène. En chauffant, la réaction se poursuit pour donner le dinitrotoluène et finalement le trinitrotoluène (TNT) qui est explosif.
Le groupe méthyle peut également réagir dans d'autres réactions d'oxydation. Le permanganate de potassium donne l'acide benzoïque, tandis que le chlorure de chromyle donne le benzaldéhyde (réaction d'Étard). Une halogénation en conditions radicalaires donne les halogénures de benzyle. Par exemple, avec la N-Bromosuccinimide en présence d'AIBN, on obtient le bromure de benzyle.
L'hydrogénation catalytique du toluène donne le méthylcyclohexane. À cause de la stabilité particulière du système aromatique, cette réaction requiert une pression élevée d'hydrogène.
Propriétés physiques
Le toluène est un liquide aux conditions normales de température et de pression. Il est quasi-insoluble dans l'eau (0,535 g l−1 à 25 °C), mais miscible à beaucoup de solvants organiques (acétone, oxyde de diéthyle, chloroforme, éthanol, etc.), et soluble dans l'acide acétique glacial.
Le toluène a une constante molale cryoscopique de 3,55 °C kg mol−1 et une constante molale ébullioscopique de 3,40 °C kg mol−1. Sa vapeur est plus lourde que l'air, et forme avec ce dernier un mélange explosif.
En RMN du proton, le toluène se présente sous la forme de plusieurs pics entre 7,28 ppm et 7 ppm pour les hydrogènes du cycle benzénique et d'un singulet à 2,38 ppm pour les hydrogènes du groupe méthyle. En RMN du carbone, le toluène se présentent sous plusieurs pics, à 137,8 ppm pour le carbone en α du méthyle, à 129,09 ppm pour les carbones β, à 128,28 ppm pour les carbones γ et à 125,38 ppm pour le carbone opposé au méthyle. Le carbone du groupe méthyle présente un pic à 25 ppm.
La conductivité thermique (en W·m−1·K−1) vaut 0,1425 – 0,00025T, avec T exprimé en °C.
Fabrication et synthèse
Le toluène est présent en faible proportion dans le pétrole brut. Il est habituellement produit par reformage catalytique dans le procédé de fabrication de l'essence. On l'obtient également par craquage dans le procédé de fabrication de l'éthylène ou alors, à partir du charbon. Sa purification finale se fait par distillation ou par extraction.
Production
En France, entre les deux guerres, la fabrication se faisait à la poudrerie annexe située à Salin-de-Giraud (Bouches-du-Rhône). Cet établissement était chargé du traitement de toutes les essences venant de Bornéo (camphre), achetées par le service des poudres, afin d'en extraire le toluène nécessaire à la fabrication de la tolite. C'était la seule usine de ce type en France, et on imagine la catastrophe qu'aurait constituée sa destruction, ou simplement sa mise hors-service. Durant la Seconde Guerre mondiale, sa production est essentielle à la fabrication d'explosifs puissants comme le TNT.
L'industrie chimique de l'URSS a produit 245 500 t de ce produit entre 1940 et 1945, auxquelles s'ajoutent 103 000 t produites par les Alliés[27].
L'Allemagne nazie avait planifié une production de 9 600 t en décembre 1939, et, en septembre 1944, comptait sur une production de 15 500 t mais n'a finalement produit que 12 200 t[28].
Selon l’ECB, en 2003, l’Union européenne produit chaque année près de 16,75 millions de tonnes de toluène dont 14 millions sous forme de mélanges incorporés à l’essence et 2,75 millions sous forme de toluène commercial[29].
Deux des principaux fabricants de ce produit sont, en 2006, Total Petrochemicals et EniChem. En France, à la même date, 163 854 t de toluène ont été produites, 57 512 t importées et 11 237 t exportées[30].
| États-Unis | 10 900 |
| Japon | 6 100 |
| Corée du Sud | 3 080 |
| Chine | 2 830 |
| Union européenne | 2 040 |
| Canada | 1 630 |
Utilisation
Le toluène sert :
- à élever l'indice d'octane dans les carburants, mélangé avec du benzène et des xylènes. Il est donc présent dans divers carburants pétroliers ;
- de solvant d’extraction dans l’industrie cosmétique (parfum) et dans l’industrie pharmacochimique ;
- comme solvant ou élément de fabrication de peintures, vernis, laques, cires et encres (imprimerie…) ;
- de produit de départ pour divers procédés industriels : synthèse du caoutchouc, du phénol, du TNT, du diisocyanate de toluène (TDI), nécessaire pour obtenir la mousse de polyuréthane, benzène et xylènes, nitrotoluène, chlorure de benzyle, benzaldéhyde, acide p-toluènesulfonique, vinyltoluène, etc. ;
- à la fabrication d'adhésifs et de colles ;
- au tannage du cuir ;
- comme booster pour les revêtements de certains pongistes (malgré son interdiction).
Toxicologie, écotoxicologie, précautions et métabolisme
C'est un produit nocif et écotoxique (souvent présent dans certains sols industriels pollués). Sa toxicité aiguë est faible, mais il a comme premiers organes-cibles le système nerveux central (cerveau, moelle). C'est aussi un irritant pour la peau, l'œil et le système respiratoire.
Chez l'animal de laboratoire, l'exposition à des taux significatifs de toluène induit des symptômes généraux : hyperactivité, irritation de la peau et surtout des muqueuses (écoulement nasal, larmes), irritation des voies respiratoires, avec essoufflement. À des taux d'exposition supérieurs à 2 000 ppm dans l'air, le stade suivant est celui d'une narcose (ataxie, dégradation des fonctions cognitives, troubles de l’équilibre et altérations neurochimiques. La mort est due à un arrêt respiratoire induit par une déplétion du système nerveux central).
L'irritation augmente selon la durée d'exposition et la dose : chez le lapin, un érythème modéré puis un œdème léger apparaissent après 72 heures, irréversibles à 7 jours, et — toujours chez le lapin — un rinçage de l'œil exposé après 4 et 30 secondes ne diminuent pas l’intensité de l’irritation.
Sa toxicité chronique a été étudiée chez l'animal de laboratoire (souris, rat) chez lequel on observe :
- une augmentation de poids de divers organes impliqués dans la détoxication (foie, rein par exemple après exposition à 1 250 ppm durant 15 jours chez le rat ; à 2 500 ppm, le rat grossit, avec augmentation du poids du cerveau, du cœur, des poumons et des testicules, avec des symptômes de dyspnée et d'ataxie) ;
- une modification du taux de neurotransmetteurs ;
- une neurotoxicité affectant notamment l’hippocampe et le cervelet ;
- une ototoxicité[31] chez le rat avec une interaction synergique avec le bruit[32] - [33];
- une exposition longue (2 ans à 1 500 ppm) chez le rat a induit une inflammation des muqueuses nasales avec érosion de l’épithélium olfactif, métaplasie et dégénérescence de l’épithélium respiratoire, mais en dessous de 300 ppm, aucun symptôme n'a été observé (la NOAEL ou concentration sans effet toxique observé était de 625 ppm pour une exposition de 6,5 heures par jour, 5 jours par semaine durant 15 semaines ; ou de 300 ppm sur une durée d'exposition de 2 ans. Par voie orale, la NOAEL était pour le rat et la souris de 625 mg kg−1 j−1 pendant 13 semaines)[34] - [35].
Le toluène ne semble pas avoir d'effets sur l'ADN in vivo, alors qu'il en a in vitro.
Via la peau ou par inhalation, il ne semble pas cancérogène[36] - [37] - [38] - [39], mais en tant que solvant pourrait contribuer à l'entrée dans l'organisme de produits cancérigènes.
Le toluène est reprotoxique[40] (altération de la fécondité à des taux où il n'est pas toxique pour la mère, chez le rat). Il altère aussi la fertilité des mâles via une altération de la spermatogenèse et/ou peut-être du fonctionnement de l'épididyme : réduction de 20 % du nombre de spermatozoïdes sans réduction de leur mobilité sous 6 000 ppm. Au-delà, le nombre de spermatozoïdes diminue, ainsi que leur mobilité, mais sans modification de poids des testicules ou de la spermatogenèse testiculaire, et sans altération du taux d'hormones après un mois d’exposition. La fertilité n'est pas affectée en deçà de 600 ppm.
Il passe facilement dans l'embryon, induisant au-delà de 600 ppm chez l'animal (pas de donnée pour l'homme) un retard de croissance et de poids à la naissance et des troubles psychomoteurs postnataux qui traduisent la neurotoxicité du toluène pour le cerveau embryonnaire, bien que sans malformations externes[41] - [42], y compris par inhalation[43]. Il n’est pas réputé tératogène in vivo ni in vitro. L'UE l'a classé toxique pour la reproduction, catégorie 3, R 63.
Cinétique dans l'organisme
Même sous forme liquide, il franchit mal la barrière de la peau (14 à 23 mg/cm2 par heure) et sous forme vapeur encore moins (4,6 μg/cm2 par heure pour la souris nude exposée à 1 000 ppm, alors que de la peau de rat, in vitro, en absorbe 0,78 μg/cm2 par minute[44]).
Il traverse cependant aisément la muqueuse pulmonaire, dans les deux sens (10-20 % du toluène ingéré et/ou inhalé est ensuite excrété sous forme de vapeur via l'expiration). Le taux de benzène exhalé augmente après ingestion d'alcool éthylique, ce dernier inhibant le métabolisme du toluène, ce qui diminue son excrétion urinaire.
L'inhalation de vapeurs de toluène est nocive. À hautes doses, elle induit des nausées. L'inhalation chronique de toluène cause des dommages irréversibles au cerveau. Il passe facilement des poumons dans le sang, pour moitié fixé à l'hémoglobine et pour moitié dans le sérum (chez l'homme ; chez le rat, il est majoritairement véhiculé par le sérum). Il est détectable dans le sang 10 à 15 min après le début de l’exposition (à un taux d'autant plus élevé que le taux de benzène était élevé dans l'air respiré ; le degré d’absorption (50 % environ de la concentration) dépendant aussi du taux de ventilation pulmonaire. On peut donc supposer que les joggers courant près d'un grand axe de circulation y sont plus exposés. Il passe rapidement dans le cerveau : des rats expérimentalement exposés montrent un pic dans le sang 53 min après l'exposition et 5 min plus tard (58 min) dans le cerveau (riche en tissus gras). On le trouve aussi dans les moelles osseuse et épinière, les tissus adipeux, le foie et les reins.
Le toluène est aussi très bien absorbé via le tractus gastro-intestinal ; avec (chez l'homme et le rat) un pic détectable dans le sang environ deux heures après ingestion.
Il est à peine filtré par la barrière placentaire ; chez le rat, la concentration dans le fœtus est environ 75 % de celle du sang maternel. Le lait maternel, s'il en contient en permet aussi le transfert de la mère à l'enfant(chez l’homme et l’animal).
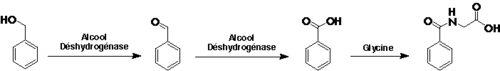
Sa toxicité s'explique par son métabolisme : le toluène étant très peu soluble dans l'eau, il ne peut pas quitter l'organisme par les voies traditionnelles (urine, fèces, transpiration). Il doit être métabolisé pour être excrété. Le groupe méthyle du toluène s'oxyde plus facilement que le noyau aromatique. Cette réaction est réalisée dans le foie par les monooxygénases à cytochromes P450. 95 % du toluène est alors transformé en alcool benzylique. Ce sont les 5 % restant qui créent les métabolites toxiques, les époxydes du noyau aromatique. La grande majorité de ces époxydes est conjuguée à la glutathione, cependant le peu qui parvient à s'échapper endommage gravement la machinerie cellulaire en allant alkyler certaines protéines, voire l'ADN.
Le toluène est excrété principalement via l'urine sous forme d'acide benzoïque - obtenu par oxydation enzymatique de l'alcool benzylique - et sous forme d'acide hippurique obtenu par conjugaison de l'acide benzoïque avec la glycine.
Synergies
De nombreuses synergies sont probables, car le toluène est un puissant solvant. On sait par exemple que l'association toluène-xylène induit, par compétition métabolique, une augmentation du taux (sanguin et cérébral) de toluène[44].
Valeurs limites d'exposition professionnelle contraignantes
En France, elles sont de 20 ppm soit 77 mg m−3 (pour 8 h) et de 100 ppm soit 384 mg m−3 (pour une exposition de court terme, ou 15 min) établies par le décret no 2012-746 du . Ces valeurs servent notamment pour réaliser les dosimétries réglementaires déterminées par le décret no 2009-1570 du .
Notes et références
- TOLUENE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, Handbook of Chemistry and Physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 9-50
- (en) Hyp J. Dauben Jr., James D. Wilson et John L. Laity, « Diamagnetic Susceptibility Exaltation in Hydrocarbons », Journal of the American Chemical Society, vol. 91, no 8, , p. 1991-1998
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1), p. 85
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Temperatures. Part II. Aromatic and Cyclic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 33, no 2, , p. 541 (DOI 10.1063/1.1647147)
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- (en) J.G. Speight et Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.289
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- Éditions techniques de l'ingénieur, Article B 1201
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub., , 396 p. (ISBN 0-88415-858-6)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Toluène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme », sur monographs.iarc.fr, CIRC, (consulté le )
- Concentrations/doses journalières admissibles et concentrations/doses tumorigènes des substances d'intérêt prioritaire calculées en fonction de critères sanitaires, publié par Santé Canada
- « Toluene », sur hazmap.nlm.nih.gov (consulté le )
- Pelletier et Walter (1837) Examen des produits provenant du traitement de la résine dans la fabrication du gaz pour l'éclairage, Comptes rendus, 4 : 898–899.
- Pelletier et Philippe Walter (1838) Examen des produits provenant du traitement de la résine dans la fabrication du gaz pour l'éclairage Annales de Chimie et de Physique, 2nd series, 67 : 269-303. Le toluène est nommé pp. 278-279: « Nous désignerons la substance qui nous occupe par le nom de rétinnaphte, qui rappelle son origine et ses propriétés physiques (ρητίνη-νάφτα). »
- Deville (1841) "Recherches sur les résines. Étude du baume de Tolu" (Investigations of resins. Study of Tolu balsam), Comptes rendus, 13 : 476–478.
- H. Deville (1841) "Recherches chimiques sur les résines; Premier mémoire" (Chemical investigations of resins; first memoir), Annales de Chimie et de Physique, 3rd series, 3 : 151-195. Deville names toluene on p. 170: « J'ai adopté, pour le corps qui m'occupe dans ce moment, le nom de benzoène, qui rappelle, dans les baumes dont il provient, ce caractère presque générique qui est de contenir de l'acide benzoïque. »
- Jaime Wisniak, « Henri Étienne Sainte-Claire Deville: A physician turned metallurgist », Journal of Materials Engineering and Performance, vol. 13, no 2, , p. 117–118 (DOI 10.1361/10599490418271, Bibcode 2004JMEP...13..117W)
- Jacob Berzelius (1843) Jahres Berichte, 22 : 353-354..
- Cahours, Auguste (1850) "Recherches sur les huiles légères obtenues dans la distillation du bois" (Investigations of light oils obtained by the distillation of wood), Compte rendus, 30 : page 320
- Jaime Wisniak (October 2013) "Auguste André Thomas Cahours," Educación Química, 24 (4) : 451–460.
- The USSR's economy in 1941-1945
- (en) Appendix D. Strategic Air Attack on the Powder and Explosives Industries: Table D6 Plants for Production of Raw Materials for Powders and Explosives
- INERIS - Données technico-économiques sur les substances chimiques en France : Toluène [PDF]
- Hydrocarbures aromatiques, Société française de chimie
- Campo P. et al., Toluene-induced hearing loss: A mid-frequency location of the cochlear lesions, Neurotoxicology and Teratology, 1997, 19: 129-40.
- Søren Lund et Gitte Kristiansen, « Hazards to Hearing from Combined Exposure to Toluene and Noise in Rats », International Journal of Occupational Medicine and Environmental Health, vol. 21, no 1, (ISSN 1896-494X et 1232-1087, DOI 10.2478/v10001-008-0008-x, lire en ligne, consulté le )
- R. Lataye et P. Campo, « Combined effects of a simultaneous exposure to noise and toluene on hearing function », Neurotoxicology and Teratology, vol. 19, no 5, , p. 373–382 (ISSN 0892-0362, PMID 9380004, lire en ligne, consulté le )
- Guillot J.-P. et al., Evaluation of the cutaneous-irritation potential of 56 compounds, Food and Chemical Toxicology, 1982, 20: 563-572.
- Guillot J.-P. et al., Evaluation of the ocular-irritation potential of 56 compounds, Food and Chemical Toxicology, 1982, 20: 573-582.
- Toxicity summary for toluene. Toxicity profiles, Risk Assessment Information System, 1994. Consultable sur le site http://risk.lsd.ornl.gov/tox/rap_toxp.shtml
- Toxicology and carcinogenesis studies of toluene (CAS n° 108-88-3) in F344/N Rats and B6C3F1 Mice (Inhalation Studies), Toxicity Review TR- 371, NTP, 1990. Lien NIEHS
- Toluene. In : IARC monographs on the evaluation of carcinogenic risks to humans, Lyon : IARC, 1999, 71 (2) ; 829-864.
- Toxicology and carcinogenesis studies of toluene (CAS n° 108-88-3) in F344/N Rats and B6C3F1 Mice (Inhalation Studies), Toxicity Review TR-371, NTP ; 1990. Site NIEHS
- Toluène, fiche toluène de DEMETER. Documents pour l’évaluation médicale des produits toxiques vis-à-vis de la reproduction, INRS, 2006
- Dalgaard M. et al., Developmental toxicity of toluene in male rats: effects on semen quality, testis morphology, and apoptotic neurodegeneration, Archives of Toxicology, 2001, 75 (2) : 103-109.
- Wilkins-Haug L., Teratogen update: toluene, Teratology, 1997, 55: 145-151.
- Ono A. et al., Toluene inhalation induced epididymal sperm dysfunction in rats, Toxicology, 1999, 139 (3) : 193-205.
- Fiche toxicologique INRS, accessible via les liens externes de cette page
Voir aussi
Articles connexes
- Xylène, benzène avec deux groupes méthyle
- Nitrotoluène, toluène substitué par un groupe nitro
- Dinitrotoluène, toluène substitué par deux groupes nitro
- Trinitrotoluène toluène substitué par trois groupes nitro
- Toluidine, toluène substitué par un groupe amine
Liens externes
- Fiche toxicologique, INRS.
- Base de données Biotox, INRS.
- Fiche internationale de sécurité, sur www.cdc.gov.