Altérations du vin
Les altérations du vin sont variées, modifient son équilibre et ses propriétés visuelles, olfactives et gustatives.

Définition
Les altérations diffèrent suivant leurs origines (microbiologiques, physico-chimiques, etc), et les composants du vin avec lesquels elles réagissent.
Le vin est un produit ayant en dégustation des propriétés organoleptiques, qui peuvent devenir des défauts principalement lorsqu'ils dépendent de l'état de ses équilibres :
- physique : dépendant de la température, de l'oxydo-réduction ;
- chimique : dépendant de la stabilité et de la concentration des différentes molécules présentes (ions métalliques, acides, protéines, polyphénols) ;
- microbiologique : dépendant des populations de micro-organismes présentes (levures et bactéries), et leur capacité à se développer. Cette dernière est en fonction de la température, du pH, du degré d'alcool, du taux de sulfites, et des substrats que les micro-organismes vont consommer.
D'autres altérations peuvent provenir d'éléments extérieurs, ou de transfert de composants par les équipements viti-vinicoles. Certaines origines sont quant à elles encore mal connues du fait de la complexité de la matrice.
Des solutions existent pour la plupart des altérations, notamment en respectant l'hygiène en préventif, et/ou en utilisant des moyens de stabilisation du vin en curatif.
Altérations microbiologiques
Maladie de la fleur

Candida vini, Pichia membranaefaciens, et Hansenula sont des levures responsables de la maladie de la fleur[1], qui forme un voile à la surface du vin et lui donne des odeurs d'évent. Elles se développent en présence d'air et oxydent l'éthanol en éthanal, cette réaction peut se poursuivre jusqu'à la transformation en gaz carbonique et en eau[2].
Dégradation d'acides phénols

Les levures Brettanomyces bruxellensis et parfois Saccharomyces cerevisiae sont responsables de la dégradation des acides phénols en d'autres composés phénoliques. Ils confèrent des arômes désagréables rappelant l'écurie ou la sueur de cheval.
Il existe également des cas de dégradation de ces composés par des bactéries lactiques[2].
L'apparition de ce défaut se fait en plusieurs étapes :
- Les esters d’acides cinnamiques (acide p-coumaryl-tartrique, acide férulyl-tartrique) naturellement présents dans le vin sont transformés en acides cinnamiques (acide p-coumarique, acide férulique, acide caféique) sous l'action d'une enzyme, la cinamyl-estérase. Pour prévenir l'apparition de goûts de Brettanomyces il est donc utile d'utiliser des enzymes œnologiques purifiée FCE (Free Cinamyl-Estérase) ;
- Les acides cinnamiques ainsi produits peuvent être transformés en vinyl-phénols (vinyl- 4-phénol, vinyl-4-gaïacol, vinyl-4-catéchol) sous l'action d'une autre enzyme, la cinnamate décarboxylase produite par des levures qui peuvent être du genre Saccharomyces ou Brettanomyces ;
- Enfin, les vinyl-phénols peuvent être transformés en phénols volatils (éthyl-4- phénol (4EP), éthyl-4-gaïacol (4EG), éthyl-4-catéchol (4EC)) sous l'action de la vinyl-phénol réductase essentiellement produite par les levures du genre Brettanomyces. Ces composés sont responsables de l'odeur animale caractéristique de « sueur de cheval ».
Refermentation de sucres résiduels
Les sucres résiduels d'un vin peuvent subir, au cours de l'élevage ou en bouteille, un nouveau départ de fermentation alcoolique par les levures encore présentes dans le milieu (Saccharomyces cerevisiae, Zygosaccharomyces bailii ou Saccharomycodes ludwigii).
Piqûre acétique

La piqûre acétique est une dégradation de l'éthanol en acide acétique et acétate d'éthyle par des bactéries acétiques[3]. Elle a notamment pour effet d'augmenter l'acidité volatile et de provoquer une fermentation acétique à l'origine du vinaigre.
Acescence
L'acescence est un défaut olfactif qui découle de l'altération de la piqûre acétique par les bactéries. La molécule responsable de l'acescence est l'acétate d'éthyle, un composé chimique issu de la réaction chimique entre une molécule d'éthanol et une molécule d'acide acétique.
La perception sensorielle de cette molécule rappelle l'odeur du vernis à ongles ou des solvants utilisés dans certaines colles.
Piqûre citro-acétique
C'est une dégradation de l'acide citrique par des bactéries lactiques, Œnococcus œni[4] - [5]. Elle produit de l'acide acétique, du diacétyle[6] et des substances acétoïniques. Le diacétyle peut conférer des arômes beurrés au vin[7].
Piqûre lactique
La piqûre lactique est une dégradation des sucres (fructose, glucose, mais aussi xylose...) par des bactéries lactiques, en lieu et place des levures saccharomyces de la fermentation alcoolique classique. Elle aboutit a une forte production d'acide acétique[2]. Un pH haut est un facteur de risque, qui favorise ce métabolisme[8].
Piqûre mannitique
Dérivée de la piqûre lactique, elle se fait par les bactéries lactiques qui dégradent le fructose en mannitol[2] - [9]. Elle survient possiblement lors des arrêts de fermentation dû à un dépassement des températures de fermentation (35 °C)[10].
La teneur en mannitol maximale acceptable est considérée à 100 mg/L, le vin prend alors un goût aigre.
Dégradation d'acide sorbique
La dégradation de l'acide sorbique par les bactéries lactiques peut produire des arômes et des saveurs proches des arômes des feuilles de Geranium[11].
Les bactéries lactiques peuvent métaboliser le sorbitol issu de l'acide sorbique, cela se produit lorsqu'un déclenchement de la fermentation malolactique se fait, en présence de quantités importantes d'acide sorbique, et en absence de sulfitage.
Le composé responsable des odeurs de Geranium engendrées est le 2-éthoxyhexa-3,5-diène, dont le seuil de détection est faible (0,1 ng/L à 10 ng/L selon les sources)[12] - [13] - [14].
Maladie de la tourne
La maladie de la tourne est une dégradation de l’acide tartrique par les bactéries lactiques Œnococcus œni. Elle engendre une production d’acides acétique, lactique et succinique, ainsi que du CO2[2].
L'acidité totale du vin s'en trouve diminuée[15].
Maladie de l'amertume
Étudiée par Louis Pasteur en 1873[16], elle est due a des bactéries lactiques hétérofermentaires (Lactobacillus hilgardii et Lactobacillus diolivorans) qui dégradent le glycérol en acroléine[2] - [15]. Elle provoque une amertume par association de l'acroléine à des composés phénoliques, une altération de la matière colorante, et une production de CO2.
Maladie de la graisse
Les bactéries (Pediococcus parvulus et Pediococcus damnosus) peuvent dans certains cas former des polymères de glucane à partir de glucose (liés entre eux par les sites β 1,2 et β 1,3) issu de sucres résiduels. Cela intervient lorsqu'elles possèdent un gène spécifique (gtf) présent sur un plasmide et que leur population dépasse 105 UFC/mL[15]. Le vin prend un caractère huileux et filant, avec une forte viscosité. Une action mécanique (pompage, brassage...) peut suffire à casser ces molécules colloïdales polysaccharidiques. Les glucanases naturellement présentent dans le vin n'y parviennent pas à cause de la structure particulière des polymères. La maladie de la graisse apparaît généralement sur les vins manquant d'acidité (pH élevé) et du fait d'un sulfitage tardif après la fermentation malolactique.
Carbamate d’éthyle
Le carbamate d’éthyle (ou uréthane) est parfois retrouvé dans le vin. Des acides aminés ayant une fonction carbamate comme l’arginine, la citrulline et l’ornithine[17] que l'on retrouve dans les vins sont des précurseurs des mécanismes de sa formation.
L'arginine est dégradée par l'arginase des levures, entraînant la formation d’urée, lors de la fermentation alcoolique. Des fortes teneurs en azote dans les moûts favorisent cette voie métabolique[18]. L’urée est alors capable de réagir avec l’éthanol pour former du carbamate d’éthyle[19].
Œnococcus œni peut également utiliser l'arginine par une déiminase, qui forme ensuite la citrulline[20]. Les acides aminés (la citrulline et l’ornithine) sont, alors utilisés dans le métabolisme bactérien, avec le même résultat de formation de carbamate d'éthyle[21].
La majorité des souches d’Œnococcus œni sont capables de dégrader l’arginine, un des acides aminés majoritaires dans le vin, par la voie de l’arginine déiminase (voie ADI). Ce catabolisme conduit notamment à la libération de citrulline, qui réagit avec l’éthanol pour former du carbamate d’éthyle.
Lors du vieillissement, le processus peut également être déclenché sous l’effet du temps et de la température[21].
Cette molécule présente un risque pour la santé humaine car elle est classée parmi les cancérigènes[19]. Dans la plupart des vins, les teneurs restent très limitées. Elles ne sont réglementées ni en France, ni au niveau de la Communauté européenne[19]. Néanmoins, l’OIV « recommande aux États membres de […] suivre toutes les pratiques appropriées pour minimiser la formation de carbamate d’éthyle ». D'autre part, les États-Unis et le Canada ont défini pour les vins des teneurs maximales en carbamate d’éthyle, respectivement de 30 et 15 µg/L[19].
Production d'amines biogènes
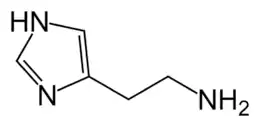
La production d'amines biogènes peut comporter un risque allergique pour la santé, notamment dû à la présence d'alcool dans le vin qui inhibe les enzymes permettant de le dégrader naturellement chez l'Homme. Elles sont dérivées d'acides aminés, et présentes à l'ordre de quelques mg/L dans le vin[22].
La plus importante en quantité est l'histamine (on trouve également la tyramine, la putrescine, et la cadavérine), des normes existent pour la teneur maximale suivant la législation de plusieurs pays (à environ 10 mg/L).
Leur présence est due à la décarboxylation d'acides aminés présents naturellement dans le raisin, par des bactéries lactiques notamment, mais potentiellement aussi par des levures saccharomyces ou brettanomyces. Une présence trop importante d'azote dans les moûts peut favoriser leur production dans le métabolisme des micro-organismes cités. La faible production d'amines biogènes est un des critères de sélection des bactéries lactiques utilisées en œnologie.
Production d'ochratoxine A
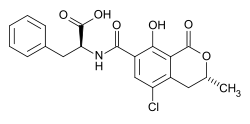
Le micro-organisme responsable est Aspergillus niger, il produit de l'ochratoxine A (OTA), composé toxique à doses trop importantes.
Développement de « goût de souris »
Les origines supposées sont diverses, elles mettent souvent en cause des vins avec une activité microbiologique indésirable, notamment due à un sulfitage insuffisant.
Les causes potentielles sont :
- Dégradation de l'acide tartrique, et production d'acide propionique[23] ;
- Dégradation de lysine et d'ornithine, et production de tétrahydropyridine, par des bactéries (Lactobacillus brevis, Lactobacillus hilgardii) ;
- Dégradation d'acides coumarique et férulique, et production respectivement de 4-vinylphénol et 4-vinylgaïacol par des levures (non-Saccharomyces, Saccharomyces cerevisiae, Brettanomyces bruxellensis), ou des bactéries (lactobacillus plantarum et Pediococcus parvulus).
Contrairement à d'autres défauts, l'intensité du goût de souris d'un vin peut varier en fonction du temps. Des mécanismes d'oxydo-réduction sont suspectés dans l'expression de ce défaut. L'ajout d'acide citrique dans des vins non sulfités favorise l'apparition de ce défaut.
Altérations physico-chimiques
Précipitations
Dans le vin, les composés sont en solution, et sont dissous dans la phase liquide. Il peut arriver que suivant les conditions (de température, d'oxydo-réduction...), ces composés s'agglomèrent entre eux, ou via d'autres molécules, et précipitent. Cela forme des sédiments divers, ou un trouble du vin.
Casse ferrique
La casse ferrique est la précipitation d'ions de fer dans le vin. On trouve le fer naturellement à faible dose dans le raisin, voire la terre et la poussière des vignobles riches en fer. Le vin peut ensuite s'enrichir en fer par le matériel vinicole utilisé (pompes, cuves usagées avec structures métalliques, matériel, etc.). Le risque est important lorsque la dose de fer dépasse 8 à 15 mg/L[24].
Le fer est présent en solution sous ses formes d'ions ferreux (Fe++, Fe+++).
Vins blancs
Le fer peut précipiter à basse température, avec un pic de risque à un pH de 3,3[25].
Il précipite avec l'acide phosphorique, formant des complexes colloïdaux. C'est alors une casse ferrique blanche, ces complexes chargés négativement peuvent floculer avec des protéines. Il y a un trouble et un dépôt blanc qui se forment.
Vins rouges
Le fer peut précipiter à basse température, avec un risque à pH plus élevé, et avec un état oxydatif du vin[25].
Il s'associe avec des composés phénoliques (tanins), formant des complexes solubles, qui peuvent précipiter en dépôts de couleur bleue-noire.
Traitements
Des traitements sont possibles, suivant les conditions et les vins, par le ferrocyanure de potassium (vins blancs et rosés), le phytate de calcium (vins rouges), l'acide ascorbique, l'acide citrique (complexant du fer), ou la gomme arabique (utilisé pour réduire le risque de casse cuivrique)[26].
Casse protéique
Les protéines peuvent être à l'origine de la formation d'un trouble, favorisé par l'élévation de la température, dans les vins blancs et rosés. Elles s'agglomèrent et forment un précipité floconneux blanchâtre.
De plus les protéines réagissent avec l'acide métatartrique ou les gommes de cellulose (carboxyméthylcellulose) ajoutées pour éviter les précipitations tartriques de sorte qu'il est nécessaire de s'assurer de la stabilité protéique avant de les utiliser.
Un collage à la bentonite, un chauffage à +55 °C, ou un ajout de tanins incolores peuvent être réalisés préventivement pour éliminer les protéines responsables de la casse[27].
Précipitations tartriques
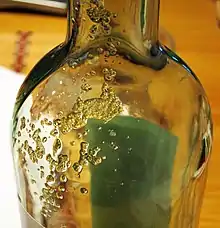
Communément appelées le « tartre » du vin, ces précipitations sont des cristaux solides ayant diverses origines.
Bitartrate de potassium
L'acide tartrique peut former des sels insolubles, comme le bitartrate de potassium et le tartrate de potassium, sous l'action du froid.
Tartrate neutre de calcium
Lorsque la teneur en calcium du vin est particulièrement élevée (plus de 70 mg/L), l'acide tartrique peut former un autre sel insoluble, le tartrate neutre de calcium responsable d'un dépôt en bouteilles. Ce trouble est plus rare et peut se produire dans les vins issus de terroirs riches en calcaire actif comme la Champagne.
Traitement
Le traitement par stabilisation tartrique est préventif, il se fait par deux méthodes[25] :
- l'ajout de colloïdes protecteurs comme l'acide métatartrique, la gomme de cellulose ou le polyaspartate de potassium[note 1] ;
- l'élimination du potassium par électrodialyse ou résines échangeuses d'ions.
Précipitation polyphénolique
Les précipitations de matière colorante se font lors d'un déséquilibre du vin en anthocyanes-tanins, et souvent en présence de polysaccharides, d'une oxygénation, et à basse température[25]. L'utilisation de gomme arabique issue de l'acacia verek (Senegalia senegal), réduit le risque de précipitation de matière colorante des vins en bouteilles.
Oxydation

Différents phénomènes sont liés à l'oxydation du vin, dans tous les cas, l'oxygène est responsable de modifications d'équilibre entre les composés du vin.
Casse oxydasique
La casse oxydasique est aussi appelée casse brune.
C'est une oxydation généralement enzymatique par le biais de la laccase ou de la tyrosinase. Ces enzymes responsables sont souvent issues de vendanges abîmées par Botrytis cinerea. Ils altèrent des composés phénoliques (matière colorante) qui se transforment en quinones, puis en précipitent en composés mélaniques, dont la couleur est brune/marron[25].
Rosissement des vins blancs

Le rosissement des vins blancs se manifeste par la légère coloration rosée de vins normalement blancs qui prennent l'apparence de vins « tachés » c'est-à-dire comme ceux qui seraient contaminés par la présence d'anthocyanes des vins rouges.
Le phénomène est dû à la présence d'un polyphénol dissous normalement incolore, mais qui devient rose sous l'effet de l'oxydation. Sa structure moléculaire est affectée par ce changement, ce qui modifie également la façon dont il renvoie la lumière. Un traitement préventif des cépages sensibles (sauvignon blanc, viognier...) et des vins fragiles (après test de rosissement à l'eau oxygénée) peut-être réalisé par collage à la PVPP (polyvinylpolypyrrolidone ou Crospovidone).
Réduction
Un vin dans un état réducteur peut voir sa matrice modifiée. La réduction impacte le métabolisme des levures sur les molécules soufrées[28] - [note 2], la principale cause est une mauvaise clarification du vin (débourbage ou soutirage insuffisants)[29], qui laisse des composés réducteurs sédimentés dans les cuves ou les fûts. La réduction modifie également la réaction de molécules entre elles dans l'équilibre du vin.
L'expression des arômes s'en trouve affectée, elle peut souvent s'améliorer et retrouver sa qualité originelle par une simple aération, ou un traitement au cuivre.
Sulfure d'hydrogène
La production de sulfure d'hydrogène (H2S) est généralement considérée comme un sous-produit métabolique de la fermentation des levures dans des environnements limités en azote. Il se forme lorsque la levure fermente via la voie de la réduction des sulfates[30]. Certaines levures sélectionnées (LSA) ne produisent pas ces composés.
Le seuil de perception pour le sulfure d'hydrogène est de 8 à 10 µg/L, des niveaux supérieurs à celui-ci confèrent au vin un arôme d'œuf pourri.
Il peut également être la base d'une réaction avec d'autres composés pour former des mercaptans et des disulfures.
Mercaptan
Le mercaptan est un composé thiolé (éthanethiol), produit dans le vin par la réaction du sulfure d'hydrogène avec des alcools, tel que l'éthanol. La réaction se fait en phase réductrice[28].
Les mercaptans ont un seuil de perception bas, environ 1,5 µg/L. Des niveaux supérieurs provoquent des odeurs d'oignon, de caoutchouc, de putois, de gaz ou d'eau croupie.
Sulfure de diméthyle
Le sulfure de diméthyle est naturellement présent dans la plupart des vins, du fait de la dégradation des acides aminés soufrés. Des niveaux supérieurs au seuil sensoriel de 30 µg/L dans les vins blancs, et de 50 µg/L dans les vins rouges donnent des arômes de chou cuit, d'asperge, d'aliments en conserve, de coing ou de truffe.
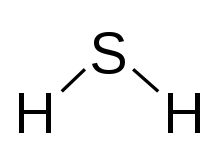 Sulfure d'hydrogène.
Sulfure d'hydrogène.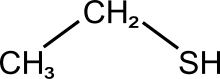 Molécule d'éthanethiol.
Molécule d'éthanethiol.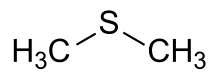 Molécule de sulfure de diméthyle.
Molécule de sulfure de diméthyle.
Casse cuivreuse
La casse cuivreuse est la précipitation d'ions de cuivre dans le vin. On trouve le cuivre naturellement à faible dose dans le raisin, puis le vin, mais il est éliminé pendant la fermentation alcoolique, dans les lies. Un vin nouveau contient donc 0,3 à 0,4 mg/L de cuivre (Cu), ce qui ne provoque pas de trouble[31]. Le vin peut ensuite s'enrichir en cuivre par le matériel contenant du cuivre (en bronze, en laiton) utilisé pendant la viniculture (pompes, raccords, vannes, etc.).
Le cuivre est présent en solution sous la forme d'ion cuivrique (Cu++), mais peut précipiter à un état réducteur, à température élevée, et en présence de SO2[25]. Les ions cuivriques passent sous leur forme réduite, les ions cuivreux (Cu+). Le SO2 passe lui sous sa forme réduite H2S. Les deux molécules forment alors des flocons en suspension de couleur blanche (sulfure de cuivre : CuS). S'il y a présence de protéines, elles précipitent ensuite avec le sulfure de cuivre en un dépôt brun, en formant des supports colloïdaux.
Les tanins des vins rouges protègent de la casse cuivreuse, par leur action sur les protéines, empêchant qu'elles réagissent avec le sulfure de cuivre. Cette casse est donc à risque sur les vins blancs et rosés, surtout s'ils sont pauvres en protéines. Plusieurs traitements curatifs sont possibles.
Autres origines
Goût de lumière
Le « goût de lumière » est dû à un ensemble de molécules, qui apparaissent dans le temps. Le défaut apparaît sur des vins ayant une présence de riboflavine (Vitamine B2) supérieure à 100 µg/L (teneur dans le vin 30 à 170 μg/L[32]), et qui ont subi une exposition à la lumière, favorisée par des températures supérieures à 20 °C[33].
Le processus se déclenche par une exposition aux rayons ultraviolets, à la longueur d'onde de 375 nm, et à la lumière visible, à la longueur d'onde de 446 nm. Cette énergie lumineuse rend rapidement la riboflavine instable. Pour retrouver son état stable, elle retransfère l'énergie captée à d'autres molécules du vin, plus lentement. Le ratio est important, une molécule de riboflavine peut transmettre de l'énergie à 100 voire 1000 autres molécules, ce qui explique son rôle prépondérant comme intermédiaire dans le processus[33].
Les molécules ainsi impactées sont diverses, surtout des acides aminés, comme la méthionine, qui évolue en méthanethiol et en diméthyldisulfure (odeurs désagréables)[34], ou encore le tryptophane et le lysozyme qui donnent de la 2-aminoacétophénone (odeur de naphtaline, savon, vieux linge humide, acacia)[33].
L’irradiation de la riboflavine modifie les esters aromatiques, et provoque une baisse de la couleur et de l’astringence des vins, par la polymérisation de polyphénols[33].
Les vins clairs, tels que les effervescents, les blancs ou les rosés, sont les plus touchés, plus globalement on retrouve le goût et les arômes de carton mouillé ou de laine humide.
Les vins rouges développent rarement de « goût de lumière » grâce aux composés phénoliques présents, responsables de sa couleur rouge, qui l'en protègent.
Les bouteilles fabriquées avec un verre coloré ou traité contre les ultraviolets, présentent une meilleure protection en bloquant les longueurs d'onde. Plus la teinte du verre bloque la lumière bleue, plus les vins sont protégés. Avec une efficacité croissante, on a donc les verres transparents, puis verts, puis marrons. L'épaisseur du verre augmente également la protection.
Les problèmes surviennent avec la lumière naturelle, et la plupart des éclairages artificiels, les meilleures solutions seraient les lampes à sodium, et depuis peu, les lumières LED. Le vin conservé dans des environnements sombres n'aura pas de déviations.
Des collages à la bentonite ou au charbon actif peuvent fixer la riboflavine. En prévention, des essais sur des levures produisant moins de riboflavines ont été effectués[32]. Des études ont été menées pour étudier le potentiel d'oxydoréduction des vins face à une exposition à la lumière[35].
Altérations par des composés chlorés
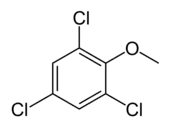
Il existe des composés chlorés responsables de déviances odorantes. On retrouve :
- le goût de bouchon (liège moisi, poussiéreux, etc.), dont les responsables sont des halophénols et des haloanisoles (notamment le 2,4,6-trichloro-anisole, ou TCA) ;
- les odeurs de moisi causées par des composés tels que les chloroanisoles ou les chlorophénols qui sont issues de contamination directe du vin, par dissolution, à cause de leur caractère volatile. Les composés sont souvent transformés par des moisissures, telles que Penicillium.
Géosmine
La présence de géosmine n'est pas due à une contamination simple, mais à un ensemble de contaminations microbiennes[36] - [37] - [38] :
- Botrytis cinerea (pourriture grise)[39] : lors d'essais de microvinification par l'IFV du Beaujolais, Botrytis cinerea a toujours été présent sur des vins géosminés et le raisin sans Botrytis cinerea ne donne jamais d'arômes terreux. Mais il n'y a pas de corrélation entre l'intensité de l'attaque de Botrytis cinerea et le taux de géosmine du vin. La pourriture est donc nécessaire mais pas suffisante pour donner des arômes de géosmine à un vin ;
- Penicillium expansum : facteur de la pourriture des fruits, il est associé à la pourriture grise au niveau microscopique par leurs filaments ;
- autres Penicillium : P. thomii, P. purpurogenum, P. glabrum, P. brevicompactum et P. carneum.
Certains facteurs sont favorables à la recrudescence de ce phénomène, les conditions de température et d'humidité doivent être réunies pour la prolifération des micro-organismes responsables[40] - [41].
La géosmine confère des goûts moisis, terreux, perceptibles a de très faibles concentrations dans le vin.
Coccinelle asiatique

La coccinelle asiatique est considérée comme un nuisible en œnologie, elle peut se regrouper dans les grappes de raisin à l'automne, et être présente dans les moûts. Elle confère alors au vin lors de sa dégustation des défauts organoleptiques comme de l'amertume, ou des flaveurs herbacées et de verdeur. La cause des déviances semble être la contamination par l'hémolymphe des coccinelles, contenant de l'isopropyl-methoxypyrazine, relargué avec le stress induit par l'opération de vendange. La methoxypyrazine se retrouve habituellement responsable de goûts herbacés, de poivrons, dans les vins[42] - [43].
« Goût d’huître »
La molécule de 2-bromo-4-méthylphénol, un bromophénol, est responsable de goûts iodés (d’huitre parfois) pouvant apparaître à la suite de traitements d’acidification des vins sur résines échangeuses d’ions[44].
Odeurs végétales
Certains défauts herbacés sont attribués à des contaminations par des végétaux qui poussent dans les vignes et qui peuvent être récoltés en même temps que le raisin, en particulier en cas de récolte mécanique : Erigeron[45], Datura stramoine (goût de patate crue et présence d'alcaloïdes), fenouil (odeur anisée)...
Aldéhydes benzoïques
L'aldéhyde benzoïque est un composé responsable de goûts d'amande amère, produits à faibles doses naturellement lors de la fermentation alcoolique.
Lorsqu'il altère le vin, il est souvent originaire d'une migration depuis un revêtement de cuve en résine époxydique, mal réalisé. Dans ces conditions l’alcool benzylique issu du plastifiant passe dans le vin, où il est oxydé en benzaldéhyde. Il peut également être décrit comme une odeur de punaise[46].
Styrènes

La contamination de styrènes provient d’un défaut de fabrication des cuves en résine de polyester stratifié, renforcées de fibre de verre. La contamination peut se faire si ces cuves n'ont pas subi d'étuvage lors de leur fabrication[46].
Les odeur et goût spécifiques du styrène peuvent être caractérisés par celui plus générique de « plastique ». Le seuil de perception est de 0,15 mg/L, et descend à 0,10 mg/L pour des dégustateurs entraînés[47].
Ces contaminations sont apparues dans les années 1970, et ont fini par être contrôlées dans les années 1980-1990, après que des travaux de recherche aient été réalisés[48].
Notes et références
Notes
Références
- LONVAUD-FUNEL, RENAUF et STREHAIANO, Microbiologie du vin : bases fondamentales et applications, Lavoisier, , 380 p. (ISBN 978-2-7430-1915-0, lire en ligne).
- Colette NAVARRE, L'œnologie, Paris, Tec & Doc, dl 2010, 433 p. (ISBN 978-2-7430-1297-7 et 2743012978, OCLC 758742402, lire en ligne), p. 262-293.
- « La piqûre acétique », sur IFV Occitanie (consulté le ).
- (en) Davis, C. R. Wibowo, D. J. Lee, T. H. Fleet, G. H., Growth and Metabolism of Lactic Acid Bacteria during and after Malolactic Fermentation of Wines at Different pH (OCLC 679537208, lire en ligne).
- El Khoury, Mariette (1987-...)., Etude de la diversité des souches d'Oenococcus oeni responsables de la fermentation malolactique des vins dans différentes régions vitivinicoles (OCLC 911260608, lire en ligne).
- (en) Brigitte Martineau, Terry E. Acree et Thomas Henick-Kling, « Effect of wine type on the detection threshold for diacetyl », Food Research International, vol. 28, no 2, , p. 139–143 (ISSN 0963-9969, DOI 10.1016/0963-9969(95)90797-e, lire en ligne, consulté le ).
- (en) Eveline J. Bartowsky et Paul A. Henschke, « The ‘buttery’ attribute of wine—diacetyl—desirability, spoilage and beyond », International Journal of Food Microbiology, vol. 96, no 3, , p. 235–252 (ISSN 0168-1605, DOI 10.1016/j.ijfoodmicro.2004.05.013, lire en ligne, consulté le ).
- « Oenologie | Le pH, premier facteur de piqûre lactique pour les vins de Bourgogne », sur Vigne (consulté le ).
- Jacques Blouin et Émile Peynaud, Connaissance et travail du vin - 5e édition, Dunod, , 416 p. (ISBN 978-2-10-058330-0, lire en ligne).
- « Mannitique (fermentation) - Dico du vin, le dictionnaire du vin », sur https://dico-du-vin.com/ (consulté le ).
- E. Klein, H. A. Schlotter et G. Würdig, « Etude de l'origine de l'arôme de géranium dans les vins traités par l'acide sorbique », OENO One, vol. 9, no 1, , p. 43–55 (ISSN 2494-1271, DOI 10.20870/oeno-one.1975.9.1.1676, lire en ligne, consulté le ).
- (en) Jancis Robinson et Julia Harding, The Oxford Companion to Wine, Oxford University Press, , 912 p. (ISBN 978-0-19-870538-3, lire en ligne).
- (en) Alice Vilela, Generation of Aromas and Flavours, BoD – Books on Demand, , 82 p. (ISBN 978-1-78984-452-8, lire en ligne).
- (en) M. Victoria Moreno-Arribas et Carmen Polo, Wine Chemistry and Biochemistry, New York, Springer Science & Business Media, (ISBN 978-0-387-74118-5, lire en ligne).
- RENOUF Vincent, La fermentation malolactique dans les vins : Mécanismes et applications pratiques, Lavoisier, , 232 p. (ISBN 978-2-7430-6534-8, lire en ligne), p. 54-60.
- Louis Pasteur, Études sur le vin : ses maladies, causes qui les provoquent, procédés nouveaux pour le conserver et pour le vieillir., Simon Raçou et Comp., (lire en ligne), p. 62-77.
- Marie-Lise Bonnet & Carole Puech, « Guide de la vinification rhodanienne - Maîtriser les composants indésirables du vin » [PDF], sur Institut rhodanien (consulté le ).
- (en) Gérald Ferrari, « Influence of must nitrogen composition on wine and spirit quality and relation with aromatic composition and defects - A review », OENO One, vol. 36, no 1, , p. 1 (ISSN 2494-1271, DOI 10.20870/oeno-one.2002.36.1.979, lire en ligne, consulté le ).
- (en) Zhihua Jiao, Yachen Dong, & Qihe Chen, « Ethyl Carbamate in Fermented Beverages: Presence, Analytical Chemistry, Formation Mechanism, and Mitigation Proposals », Comprehensive Reviews in Food Science and Food Safety, Institute of Food Technologists, vol. 13, , p. 611-626 (lire en ligne [PDF], consulté le ).
- TONON Thierry, BOURDINEAUD Jean-Paul et LONVAUD-FUNEL Aline, Catabolisme de l'arginine par Œnococcus œni : aspects énergétiques et génétiques (OCLC 870191195, lire en ligne).
- Julia Capitanio, « Compréhension des mécanismes de formation du carbamate d'éthyle dans les vins de champagne », sur Université de technologie de Compiègne, (OCLC 494482665, consulté le ).
- RENOUF Vincent, La fermentation malolactique dans les vins : Mécanismes et applications pratiques, Lavoisier, , 232 p. (ISBN 978-2-7430-6534-8, lire en ligne), p. 60.
- « Tourne (maladie de la tourne) - Dico du vin, le dictionnaire du vin », sur https://dico-du-vin.com/ (consulté le ).
- Michel Veron, « Cours Œnologie - Michel VERON: Casse ferrique », sur Cours Œnologie - Michel VERON, (consulté le ).
- Navarre, Colette,, L'œnologie, Paris, Tec & Doc, dl 2010, 433 p. (ISBN 978-2-7430-1297-7 et 2743012978, OCLC 758742402, lire en ligne), p. 273-288.
- (en) M. A. Joslyn et Aaron Lukton, « Prevention of copper and iron turbidities in wine », Hilgardia, vol. 22, no 14, , p. 451–533 (ISSN 0073-2230, DOI 10.3733/hilg.v22n14p451, lire en ligne, consulté le ).
- Michel Veron, « Cours Œnologie - Michel VERON: Casse protéique », sur Cours Œnologie - Michel VERON, (consulté le ).
- Jacques Blouin, Le SO2 en oenologie, Dunod, , 304 p. (ISBN 978-2-10-071956-3, lire en ligne), p. 12-14.
- Valérie Lavigne-Cruège, Jean-Noël Boidron et Denis Dubourdieu, « Formation des composés soufrés lourds au cours de la vinification des vins blancs secs », OENO One, vol. 26, no 2, , p. 75 (ISSN 2494-1271, DOI 10.20870/oeno-one.1992.26.2.1200, lire en ligne, consulté le ).
- Lavigne-Cruège, Valérie, Auteur., Recherches sur les composés soufrés volatils formés par la levure au cours de la vinification et de l'élevage des vins blancs secs, s.n., (OCLC 489643585, lire en ligne).
- « Synthèse bibliographique sur la filtration des vins », DAVAUX François, IFV Sud-Ouest, (lire en ligne) [PDF].
- (en) D. Fracassetti, M. Gabrielli, J. Encinas et M. Manara, « Approaches to prevent the light-struck taste in white wine », Australian Journal of Grape and Wine Research, vol. 23, no 3, , p. 329–333 (ISSN 1322-7130, DOI 10.1111/ajgw.12295, lire en ligne, consulté le ).
- BAZIREAU Marion et Yann Vasserot, « Goûts de lumière, les bons réflexes », La Vigne, no 291, (lire en ligne [PDF]).
- (en) Paris Grant-Preece, Celia Barril, Leigh M. Schmidtke et Geoffrey R. Scollary, « Light-induced changes in bottled white wine and underlying photochemical mechanisms », Critical Reviews in Food Science and Nutrition, vol. 57, no 4, , p. 743–754 (ISSN 1040-8398 et 1549-7852, DOI 10.1080/10408398.2014.919246, lire en ligne, consulté le ).
- Alain Maujean, M. Haye, Michel Feuillat et J. C. Thomas, « Contribution à l'étude des « goûts de lumière » dans le vin de champagne. II. Influence de la lumière sur le potentiel d'oxydoreduction. Corrélation avec la teneur en thiols du vin », OENO One, vol. 12, no 4, , p. 277 (ISSN 2494-1271, DOI 10.20870/oeno-one.1978.12.4.1427, lire en ligne, consulté le ).
- « Viticulture / oenologie -Viticulture- : Protéger ses vins des goûts moisis terreux », sur Vitisphere.com (consulté le ).
- LA GUERCHE, Stéphane. "Les défauts moisis terreux des vins: la géosmine identifiée comme principale responsable.", Université Bordaux-Ségalen, 2005 (lire en ligne, [PDF]).
- Daniela Correia, « Le goût moisi-terreux du vin : contribution à la caractérisation cinétique et métabolique des moisissures associées à ce défaut organoleptique », Université de Dijon, (lire en ligne, consulté le ).
- Claude Gros et Stéphane Yerle, Guide pratique de la vinification en rouge, Dunod, , p. 25.
- IFV : D. Lafond, V. Lempereur, B. Vincent, L. Guérin, Corrections et relecture : R. Cailleau, A-M. Denizot et J. Langella, Chambre d’Agriculture d’Indre-etLoire : P. Mallier, Chambre d’Agriculture du Rhône : C. Le Roux, « Goûts Moisis Terreux : Origine et moyens de lutte » (Lire en ligne, [PDF]).
- Camelia Filofteia Diguta, « Ecologie des moisissures présentes sur les baies de raisin », Université de Technologie de Compiègne, (lire en ligne, consulté le ).
- « Viticulture / oenologie -Viticulture- : Une menace potentielle pour la viticulture », Vitisphere.com, (lire en ligne, consulté le ).
- « La coccinelle asiatique, une alliée devenue envahissante », Le Monde.fr, (lire en ligne, consulté le ).
- Michèle Trévoux, « Le goût d'huître, un nouveau défaut du vin », sur Vitisphere, (consulté le ).
- « Viticulture / oenologie -Oenologie- : Attention à la contamination des vins par l'érigéron », sur Vitisphere.com (consulté le )
- A. DESENNE, J.M. MARON, J.M. JACOB, « Choix des récipients vinaires - Incidences œnologiques et environnementales », Matévi - Chambre Agriculture Gironde - Vigne et vin, (lire en ligne [PDF]).
- J.-C. CABANIS, Alain BLAISE, Centre de Formation et de Recherche en Œnologie Université de Montpellier I, « Odeurs et goûts anormaux des vins liés aux matériaux de stockage », La revue des œnologues, (lire en ligne).
- Giffone, Michel, pharmacien., Dosage du styrène et du chlorure de vinyle dans les aliments et boissons en contact avec les matières plastiques. Étude de la migration du styrène dans le vin., s.n., n.d. (OCLC 464794900, lire en ligne).
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Wine faults » (voir la liste des auteurs).
Annexes
Bibliographie
- Colette Navarre, L'œnologie, Lavoisier, , 7e éd., 468 p. (ISBN 978-2-7430-1806-1 et 2-7430-1806-2, lire en ligne).
- Girard Guillaume, Bases scientifiques et technologiques de l'oenologie, Lavoisier, , 2e éd., 272 p. (ISBN 978-2-7430-6346-7 et 2-7430-6346-7, lire en ligne).
- Jacques Blouin et Émile Peynaud, Connaissance et travail du vin, Dunod, , 5e éd., 416 p. (ISBN 978-2-10-058330-0, lire en ligne).
- Aline Lonvaud-Funel, Vincent Renouf et Pierre Strehaino, Microbiologie du vin : Bases fondamentales et applications, Lavoisier, , 380 p. (ISBN 978-2-7430-1915-0, lire en ligne).
Articles connexes
Liens externes
- INAO, « Définitions des mots exprimant un avis négatif sur la qualité d'un vin » [PDF], sur Planète Bordeaux, (consulté le ).
- Maladies du vin, Brettanomyces et Les casses sur le site Wine happened?.