Resvératrol
Le resvératrol est un polyphénol de la classe des stilbènes présent dans certains fruits comme les raisins, les mûres ou les cacahuètes. On le retrouve en quantité notable dans le raisin, et donc dans le jus de raisin et le vin qui en est issu.
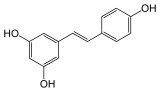
| trans-resvératrol | ||
| ||
 | ||
| Structure du trans-resvératrol | ||
| Identification | ||
|---|---|---|
| Nom UICPA | 5-[(E)-2-(4-hydroxyphényl)-éthényl] benzène-1,3-diol | |
| No CAS | ||
| No ECHA | 100.121.386 | |
| No RTECS | CZ8987000 | |
| DrugBank | DB02709 | |
| PubChem | 5056(Z/E), 445154 | |
| SMILES | ||
| InChI | ||
| Apparence | solide | |
| Propriétés chimiques | ||
| Formule | C14H12O3 [Isomères] |
|
| Masse molaire[1] | 228,243 3 ± 0,012 9 g/mol C 73,67 %, H 5,3 %, O 21,03 %, |
|
| Propriétés physiques | ||
| T° fusion | 254 °C[2] | |
| Solubilité | eau ~0,03 mg·ml-1 éthanol 50 mg·ml-1 DMSO ~16 mg·ml-1 |
|
| Précautions | ||
| SGH[3] | ||
 |
||
| Unités du SI et CNTP, sauf indication contraire. | ||
Bien que couramment utilisé comme complément alimentaire et étudié en laboratoire via des modèles de maladies humaines[4], il n'existe aucune preuve de haute qualité que le resvératrol prolonge la vie ou a un effet substantiel sur une quelconque maladie humaine[5] - [6] - [7] - [8].
Historique
Son nom viendrait[9] de Veratrum album L. var grandiflorum, le vératre blanc, d’où il a été extrait pour la première fois en 1939 par un Japonais, Takaoka. Il est aussi identifié en 1959 dans un eucalyptus puis en 1963 dans la racine de la renouée du Japon, Fallopia japonica (ou Polygonum cuspidatum), une polygonacée d’Asie orientale très invasive en Europe, mais utilisée depuis des siècles en médecine traditionnelle chinoise et japonaise. La découverte du resvératrol dans la pellicule du raisin date de 1976 mais il a fallu attendre 16 ans pour qu’en 1992 Siemann et Creasy l’identifient finalement dans le vin.
À la même époque paraissent deux articles qui vont avoir un grand retentissement sur les études du resvératrol. Le premier en 1992, de Renaud et de Lorgeril[10] montre qu’une consommation modérée de vin peut protéger de la maladie coronarienne et le second en 1993, de Frankel et al.[11] démontre que c'est le resvératrol du vin qui, en inhibant l’oxydation du LDL, doit être responsable de son effet cardioprotecteur. Le resvératrol est donc un bon candidat pour résoudre l’énigme du paradoxe français, expression qui renvoie à la situation surprenante de la région du sud-ouest, où malgré une consommation élevée de graisses animales, est observé un taux relativement bas de maladies cardio-vasculaires (comparativement aux pays du nord de l’Europe).
Ces travaux ont déclenché une pléthore d’études sur le rôle chimiopréventif des polyphénols du vin et en particulier du resvératrol. En dehors de la prévention de la maladie coronarienne, la liste des effets bénéfiques bien documentés de ce composé n'a cessé de croître : elle concerne l’inflammation, l’activation plaquettaire, l’angiogenèse, le maintien de la masse osseuse, la réduction de la masse adipeuse, la neuroprotection, la photoprotection, le vieillissement. Pendant une décennie, les observations étayant les bénéfices pour la santé du resvératol n’ont cessé de s’accumuler mais en s’appuyant majoritairement sur des preuves indirectes comme les études épidémiologiques ou sur les effets biologiques établis sur des systèmes in vitro ou d’animaux de laboratoire. Pour l'instant, en raison du manque de preuves directes, beaucoup de ces résultats ne peuvent être étendus à l'homme qu'avec la plus grande prudence, notamment depuis que le , une équipe italienne a montré que sur une cohorte de 783 personnes de plus de 65 ans, les taux urinaires de resvératrol n'étaient liés à aucun déterminant de santé ou de mortalité[12].
En 2017, une étude publiée par la revue Science rappelle que cette molécule a fait l'objet de nombreux travaux de recherche mais « qui ont produit des preuves contradictoires des effets du resvératrol dans différents contextes ». Certains auteurs ont conclu que seules de faibles doses étaient efficacement utiles pour la santé[13], puis Craveiro et al. ont conclu que de fortes doses de resvératrol inhibent les réponses des cellules humaines T CD4 + face aux antigènes et à faible dose le resvératrol modifie le métabolisme cellulaire en rendant la cellule plus sensible aux antigènes avec une production accrue d'interféron-γ (une cytokine inflammatoire). Ces deux données plaident selon les auteurs en faveur d'une évaluation poussée des risques d'utilisation de resvératrol pour traiter diverses pathologies notamment en contexte auto-immun[14].
Propriétés physiques
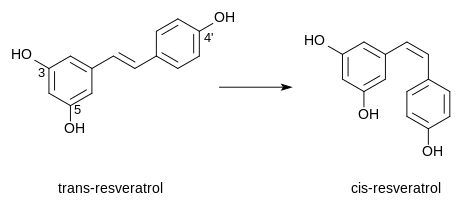
Le resvératrol se présente sous deux formes isomères, trans- et cis-, avec un passage de la forme trans- (E) à la forme cis- (Z) par irradiation UV (photoisomérisation). Le trans-resvératrol est donc une molécule photosensible qu’une simple exposition à la lumière suffit à transformer de manière irréversible dans son isomère cis. C'est un composé instable supportant aussi assez mal la chaleur et les milieux oxydants.
L'isomère trans est la forme bioactive. Contrairement à ce dernier, l'isomère cis ne présente que peu d'effets bénéfiques avérés sur la santé à ce jour[15].
 |
Plantes riches en resvératrol
Le resvératrol est une phytoalexine, c’est-à-dire une substance induite par un stress environnemental ou pathogène (tel qu’une attaque fongique comme le Mildiou ou le Botrytis chez la vigne) et destinée à contenir localement les dégâts du pathogène. La forme isomérique trans- est plus abondante dans les plantes que la forme cis-. On la trouve dans au moins 72 espèces de plantes réparties dans 12 familles[16]. Ce sont les familles de plantes supérieures suivantes : Vitaceae, Myrtaceae, Dipterocarpaceae, Cyperaceae, Gnetaceae, Fabaceae, Pinaceae, Polygonaceae, Moraceae, Fagaceae, Liliaceae.
Parmi les plantes alimentaires, on trouve le resvératrol dans[17] - [18] - [19] :
- le raisin et ses dérivés. Le resvératrol est surtout concentré dans la pellicule du grain de raisin et on le trouve en quantité variable suivant le cépage, l’origine géographique et l’exposition aux maladies fongiques[20]. Il est majoritairement présent sous forme de glucoside (trans-resvératrol-3-O-glucoside).
- Les raisins secs ont une teneur variable et pouvant être élevée en resvératrol (de 1,9 mg·kg-1 pour un raisin de Corinthe[21], à 486 mg·kg-1 pour un Thompson Seedless de Californie, avec une méthode d'analyse élaborée[22]).
- Pour le vin, l’importance du resvératrol dépend en outre de la durée de macération des peaux dans le jus. Cela explique pourquoi les vins blancs, peu ou pas macérés, ont moins de resvératrol (0,13 mg·l-1 de trans- et 0,06 mg·l-1 de cis-resvératrol) que les rosés et ceux-ci moins que les vins rouges. Les plus riches sont les vins de Pinot noir (Bourgogne), de Merlot, de Grenache ou de Mourvèdre. Le cépage Pinot noir contient le plus de resvératrol avec une concentration pouvant aller jusqu’à 11,9 mg·l-1 (en Suisse) ; en France, sa teneur moyenne est de 5,4 ± 1,2 mg·l-1[23]. Le resvératrol y est majoritairement présent sous forme aglycone, sous les formes isomériques trans- et cis-[24]. La teneur en trans-resvératrol du vin rouge varie beaucoup suivant la région de production. Si on classe les cinq plus grands producteurs mondiaux de vin par la teneur moyenne en resvératrol de leur vin rouge[19], on obtient dans l'ordre la France, l'Australie, l'Italie, l'Espagne et les États-Unis.
- les fèves de cacao constituent une source importante de flavonoïdes et de resvératrol. Le chocolat noir contient 0,4 mg·kg-1 de resvératrol[17], soit la deuxième source alimentaire de ce polyphénol après le vin ou le raisin;
- les baies rouges du genre Vaccinium : jus de canneberge avec un taux de 0,278 mg·kg-1 ;
- l’arachide (Arachis hypogaea) : les cacahuètes grillées sont relativement pauvres en resvératrol (0,03 à 0,147 mg·kg-1) ;
- Gnetum gnemon, un petit arbre d'Asie[25] important dans la cuisine indonésienne ;
- la rhubarbe (Rheum tataricum), la mûre (Morus spp.), la grenade (Punica granatum), le sorgho, etc.
Plantes médicinales riches en resvératrol :
- la renouée du Japon (Reynoutria japonica ou Fallopia japonica ou Polygonum cuspidatum), est une Polygonacée originaire d’Asie orientale, appelée 虎杖 huzhang en chinois et itadori en japonais. C’est une plante très vigoureuse, pouvant atteindre 3 m de haut, qui a tendance à devenir invasive en Europe et aux États-Unis. La plante entière est utilisée comme matière médicale en Chine (sous le nom de 石莽草 shimangcao) et au Japon (sous le nom d'itadori ou de kojôkon pour la racine). La racine de cette renouée est une des sources les plus riches en resvératrol connue (2,96–3,77 g·kg-1). Une fois séchée, la racine fournit une infusion, le « thé d’itadori », traditionnellement utilisé depuis des siècles en Chine et au Japon dans le traitement des maladies cardio-vasculaires et comme anti-inflammatoire. Il a été trouvé dans cette infusion 9,74 mg·l-1 de resvératrol, principalement sous forme de glucoside, ce qui place cette boisson dans la moyenne supérieure des vins rouges[24].
- les deux vératres, Veratrum album L. var grandiflorum et Veratrum formosanum ont aussi leurs racines et rhizomes utilisés comme matière médicale dans la médecine traditionnelle chinoise (sous le nom de 藜芦 li lu) et japonaise.
- le Yucca schidigera, le Dracaena loureiri
Absorption et métabolisme
Pendant longtemps, des études sur les activités pharmacologiques du resvératrol ont été menées sans connaître les mécanismes d’absorption et de biodisponibilité de ce composé. Quand l’obtention de trans-resvératrol radiomarqué comme traceur a permis de faire les premières observations, la surprise a été grande de découvrir qu’après une prise orale, on le retrouvait en majorité dans les urines sous des formes conjuguées et qu’il n’était pratiquement pas décelable dans le plasma sanguin. Le resvératrol ingéré oralement est absorbé à hauteur de 70 % dans l’intestin, ce qui est un taux remarquablement élevé pour un polyphénol[26]. Il apparaît chez certains sujets très rapidement (30 min environ) après ingestion à l’état de trace dans le plasma sanguin mais très rapidement il est métabolisé dans le foie en resvératrol-3-sulfate (ou -4’-sulfate) ou en resvératrol-3-4’-disulfate (ou 3,5-disulfate) et en resvératrol-3-O-glucuronide (ou 4’-O-glucuronide). La glucuronidation en 4’ semble préférentielle[27]. En 2003, Goldberg[28] en déduisait qu’il « semblait que le rôle bénéfique pour la santé de ces composés sous leur forme non conjuguée, fondé sur des études de leur activité in vitro, était irréaliste et avait été très exagéré ».
L’étude de la distribution du 14C-trans-resvératrol dans tous les tissus de la souris peut se faire de manière très précise par autoradiographie. Vitrac et ses collaborateurs (2003)[29] ont observé que la concentration de la radioactivité dans le sang était relativement basse et constante durant les 6 h de l’expérience. Au bout de 3 h, on trouve la concentration la plus élevée dans le duodénum, puis par ordre décroissant, les reins, le foie et les poumons, la rate et le côlon, le cœur, le cerveau et les testicules. En utilisant la microautoradiographie, les auteurs montrèrent que le trans-resvératrol peut pénétrer les tissus, en particulier le foie où les hépatocytes sont capables d’incorporer la radioactivité. En tenant compte de la présence de glucosides du resvératrol (picéide, astringine) dans le vin rouge et de leur possible hydrolyse dans l’intestin, les auteurs concluent ainsi: « il peut être suggéré qu’une consommation régulière et modérée de vin rouge devrait pouvoir garantir au corps humain la quantité de resvératrol suffisante pour assurer une action chimiopréventive du cancer ».
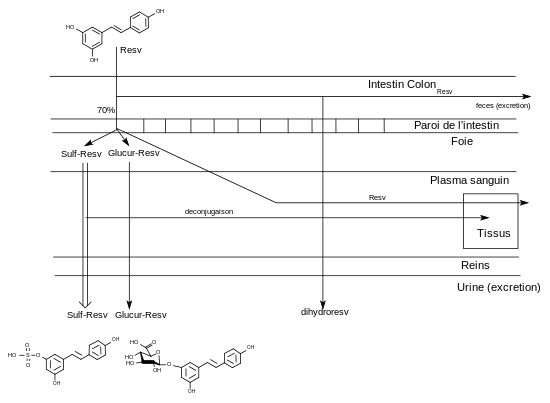
Il existe de plus des synergies entre les divers polyphénols contenus dans une boisson qui peuvent changer leur biodisponibilité. Il a été montré que le quercétol (contenu aussi dans le vin) interférait avec la sulfatation et la glucuronidation du resvératrol dans le foie et pouvait ainsi accroître sa biodisponibilité[30].
Activités biologiques
Activités anti-oxydantes
Une production excessive de radicaux libres dans l’organisme peut provoquer des dégâts importants sur les macromolécules et les cellules de cet organisme. La dégradation des lipides par le stress oxydant provoquera des dépôts de lipides oxydés dans les vaisseaux à l’origine des plaques d’athérome, perturbera le fonctionnement des membranes cellulaires et produira des dérivés carcinogènes. Les attaques radicalaires de l’ADN seront source de mutations carcinogènes et celles des protéines inhiberont les enzymes et dérégleront les signaux cellulaires de prolifération ou de défense.
Mode d’action
Les antioxydants peuvent agir à deux niveaux de la réaction d’oxydation :
- dès la phase d’initiation, ils peuvent empêcher la formation de radicaux en bloquant, dans des complexes, les métaux de transition (fer, cuivre) qui agissent autrement comme de puissants catalyseurs. Ce sont des chélateurs de métaux de transition ;
- lors de la phase de propagation, ils peuvent intercepter les radicaux et briser la chaîne de réaction. Ce sont des piégeurs de radicaux.
Le resvératrol, comme tous les polyphénols, possède des groupes hydroxyles phénoliques, Ar-OH, pouvant fournir des hydrogènes H aux radicaux peroxyles L-OO• et par là, les neutraliser sous la forme d’hydroxydes L-OOH :
Ar-OH + L-OO• → Ar-O• + L-OOH
Le radical Ar-O• étant assez stable et moins réactif, va briser la chaîne.
Comme il n’existe pas de mesure absolue d’évaluation du potentiel antioxydant d’un composé, il faut recourir à des évaluations comparatives avec d’autres composés. De plus ces comparaisons vont dépendre de la méthode d’évaluation et en particulier du radical libre péroxyle utilisé.
- En comparant la capacité in vitro à piéger les radicaux libres du DPPH• (2,2-diphényl 1-picrylhydrazyl)[31] par le resvératrol ou certains flavonoïdes du vin, Iacopini et ses collaborateurs[32] ont obtenu la hiérarchie suivante :
- Mais si on utilise un générateur de radicaux impliqué dans les processus physiopathologiques comme le peroxynititre ONOO−, on obtient l’ordre suivant :
- Quercétol > Catéchol > Resvératrol > Rutoside > Trolox
- Le resvératrol se retrouve alors dans la moyenne des potentiels antioxydants des flavonoïdes.
- Un test encore plus intéressant sur le plan physiopathologique consiste à évaluer la capacité à réduire la peroxydation des lipoprotéines de basse densité LDL (transporteur du cholestérol)[33]. Il est maintenant largement admis que la formation de radicaux libres à partir des lipides du LDL est un facteur essentiel de la genèse de l’athérosclérose.
En incubant le LDL avec l’ion cuivrique Cu2+ pour catalyseur, l’effet d’inhibition de la peroxydation des lipides, obtenu en ajoutant des polyphénols, se fait dans l’ordre suivant :- Resvératrol > Quercétol > Trolox > Catéchol
- Le resvératrol est un puissant antioxydant, plus efficace même que les flavonoïdes à empêcher la peroxydation du LDL. Il agit principalement « en amont » de la réaction en rendant inopérant le catalyseur cuivrique. C’est un chélateur de l’ion cuivrique Cu2+. Le grand pouvoir de chélation du resvératrol est utile in vivo car on sait que le LDL a une forte propension à se lier au cuivre. La capacité de chélation du cis-resvératrol n’est par contre que de la moitié de celle du trans-resvératrol.
- Lorsque le LDL est incubé avec comme générateur de radicaux libres, l’AAPH[34], le resvératrol agit « en aval » de la réaction en piégeant les radicaux libres de lipide péroxyle formés et en empêchant la propagation de la réaction en chaîne d’oxydation. Le resvératrol est toutefois un piégeur de radicaux libres moins puissant que les flavonoïdes et à peu près similaire à la vitamine E :
- Quercétol > Catéchol > Resvératrol > Trolox
- Avec une autre technique conçue pour mettre en évidence le mécanisme de piégeur de radicaux libres (et non pas de chélateur), Sojanovic et collaborateurs (2001)[35] ont montré que le resvératrol et les flavonoïdes, quercétol et épicatéchol, étaient tous également puissants. Tous les trois étaient capables de réduire d’environ 95 % la peroxydation lipidique de liposomes[36].
- L’effet antioxydant du vin devrait donc être imputé aux flavonoïdes et aux acides-phénols plutôt qu’au resvératrol, puisque ce dernier y est présent à des doses plusieurs centaines de fois inférieures (0,1 – 10 mg·l-1 de trans-resvératrol contre 1000 – 3 000 mg·l-1 de flavonoïdes).
Ils ont également montré que c’était principalement le groupe hydroxyle OH en position 4’ qui donnait son H pour piéger les radicaux libres.
Propriétés anti-oxydantes du resveratrol et protection de la peau
L’exposition aux rayonnements ultra-violets provoque un stress oxydatif au niveau cutané, qui constitue l’un des principaux facteurs du vieillissement de la peau et du risque de mélanome. Plusieurs polyphénols connus pour leurs propriétés antioxydantes, dont le resvératrol, ont fait l’objet d’études portant sur leurs effets photoprotecteurs potentiels dans le cadre d’applications topiques[37] - [38].
Sur des cultures cellulaires de kératinocytes, le traitement avec du resvératrol avant exposition aux UVB induit une inhibition de l’activation de la voie NF-κB et une meilleure survie de cellules, avec une réduction de la production de dérivés réactifs de l’oxygène[39] - [40].
Plusieurs expérimentations sur des souris sans poils montrent par ailleurs que l’application de resvératrol entraîne une réduction significative d’effets d’une exposition aux UVB tels que la prolifération cellulaire, la production de peroxyde d’hydrogène, l’infiltration leucocytaire et la phosphorylation de la survivine[41] - [42] - [43].
Une étude récente[44] réalisée sur des kératinocytes humains a également montré l’effet photoprotecteur du resvératrol contre les UVA, vraisemblablement en agissant sur la voie Keap1-Nrf2 qui constitue le principal régulateur de l’activité protectrice des cellules contre le stress oxydatif. Le resvératrol peut dégrader la protéine Keap1, augmenter la quantité de protéine Nrf2 et faciliter son accumulation dans le noyau, protégeant ainsi les kératinocytes contre le stress oxydatif induit par les UVA.
En 2013, une étude sur l’homme portant sur l’effet combiné des UVA et des UVB a mis en évidence plusieurs actions photoprotectrices d’un dérivé stable du resvératrol, le resvératrate. Des effets significatifs ont été observés concernant la coloration de la peau, le développement d’un érythème et l’apparition de cellules entrant en apoptose sous l’effet du coup de soleil. L’action inhibitrice du resvératrol sur la production de mélanine s’est montrée comparable à celle de préparations antioxydantes utilisées dans les protections solaires, mais avec peut-être un mode d’action plus diversifié sur les différentes composantes du bronzage[45].
Les rayons ultra-violets provoquent un vieillissement prématuré de la peau qui se traduit par une altération des tissus conjonctifs du derme, riches en collagène, occasionnant l’apparition de rides. Une étude récente[46] a montré que le resvératrol et la metformine inhibent l’expression du gène de la métalloprotéinase matricielle 9 et protègent le collagène de la dégradation sous l’effet des UV, par le biais de l’activation de la sirtuine 1.
Des récepteurs spécifiques du 3H-resvératrol ont été découverts dans l’épiderme humain. L’activation de ces récepteurs chez des kératinocytes humains en culture réduit le nombre de cas d’apoptoses artificiellement provoquées par l’exposition au SNP et le relargage de monoxyde d’azote[47]. Selon les auteurs de cette étude, l’action protectrice du resvératrol pour la peau serait probablement due à un effet anti-apoptose de ce composé, dans la mesure où à une même concentration il réduit le nombre de cellules en apoptose tout comme les évènements conduisant à la mort cellulaire déclenchés par le SNP.
Les études cliniques, quand elles sont accessibles, semblent confirmer l’effet anti-vieillissement du resvératrol sur la peau. Par exemple, une étude de l’entreprise Caudalie a montré qu’après 28 jours d’utilisation topique d’une formule à base de resvératrol, les rides profondes étaient réduites de 24 %[48].
Activités anti-inflammatoires
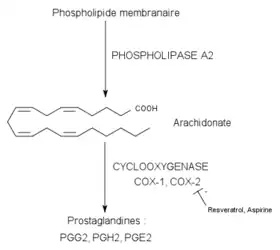
Le resvératrol est capable d’inhiber l’agrégation des plaquettes sanguines. À la suite d'une lésion d’une paroi artérielle, les plaquettes viennent s’accrocher aux parties endommagées du vaisseau et produisent de l’ADP et du thromboxane A2. Ces composés déclenchent l’agrégation des plaquettes entre elles et le thromboxane A2 provoque de surcroît une vasoconstriction. L’accumulation d’un grand nombre de plaquettes forme une masse compacte pouvant obstruer le vaisseau.
En 1995, Pace-Asciak et ses collaborateurs[49] montrent que deux polyphénols du vin rouge, le quercétol et le resvératrol, peuvent inhiber in vitro l'agrégation plaquettaire induite par l’ADP (ou par la thrombine). Ils établissent également que le resvératrol est capable de bloquer la synthèse du thromboxane A2 à partir de l’arachidonate. La même équipe poursuit l’année suivante ses travaux[50] sur 24 sujets humains auxquels ils font boire par période de 4 semaines, du vin rouge, du vin blanc, du jus de raisin et du jus de raisin additionné de 4 mg·l-1 de resvératrol. L’analyse de leurs plaquettes montre que les groupes qui ont consommé du vin ou du jus additionné de resvératrol accroissent leur résistance à l’agrégation plaquettaire et diminuent leur thromboxane. Les propriétés proprement anti-inflammatoires du resvératrol sont mises en évidence en 1997 sur la souris. On s’aperçoit que le resvératrol peut réduire un œdème de la patte de la souris induit par le carraghénane, en agissant au niveau des prostaglandines[51]. Les prostaglandines et les thromboxanes sont des médiateurs lipidiques de l’inflammation dérivés de l’acide arachidonique. L’arachidonate provient lui, en général, des phospholipides de la membrane plasmique (par action de la phospholipase A2). De ce composé dérivent ensuite par la voie de la cyclooxygénase (COX-1 et COX-2) les prostaglandines et les thromboxanes (voir schéma).
Plusieurs travaux ont montré que le resvératrol est en mesure d’inhiber l’enzyme cible COX-2. Les études in vitro sur les cellules épithéliales[52] et sur les macrophages[53] ont montré qu'il peut réduire la synthèse de prostaglandines en inhibant l’expression du gène de la COX-2 et en diminuant directement l’activité de la COX-2.
L’aspirine est un médicament antithrombotique très souvent prescrit bien qu’une proportion importante des patients y soit résistante. En traitant des prélèvements sanguins avec le collagène (pour provoquer l’agrégation plaquettaire), Stef et ses collaborateurs[54] ont montré que le resvératrol peut réduire l’agrégation des plaquettes des patients cardiaques résistants à l’aspirine, là où l’aspirine échoue. Toutefois le mécanisme précis d’action du resvératrol n’est pas parfaitement compris.
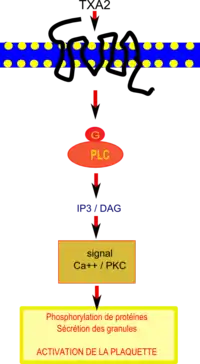
Des travaux récents[55]suggèrent que l’effet cardioprotecteur du resvératrol, obtenu grâce à sa puissante inhibition de l’agrégation plaquettaire et son atténuation de l’expression d’une protéine de surface, la sélectine P[56], serait lié en amont à la diminution de l’activité de la phospholipase C β (PLC β). Le thromboxane A2 active les plaquettes en se fixant sur un récepteur spécifique de celles-ci couplé à une protéine G et à la phospholipase C (PLC) qui catalyse des réactions produisant IP3 (inositol triphosphate) et DAG (diacylglycérol).
Des travaux réalisés en 2010 montrent que le resvératrol augmente l'expression d'un microARN (nommé miR-663) dans les cellules immunitaires humaines, ce qui diminue l'expression d'un autre microARN (le miR-155), ce dernier favorisant la réaction inflammatoire[57].
Activité antitumorale
Le resvératrol est un agent prometteur dans la chimio-prévention. Il assure la médiation de nombreuses cibles cellulaires impliqués dans les voies de signalisation du cancer. On a étudié la cytotoxicité induite par le resvératrol dans les cellules H1299, des cellules du cancer du poumon non à petites cellules ayant une délétion partielle du gène qui code la protéine p53[58]. Le resvératrol a réduit la viabilité de quatre lignées de cellules avec une relation dose et temps-dépendante. La cytotoxicité induite par le resvératrol dans ces cellules a été en partie médiée par la protéine p53 et a participé à l'activation des caspases 9 et 7 et au clivage de la Poly (ADP-ribose) polymérase. Ces résultats suggèrent une possible stratégie thérapeutique basée sur l'utilisation de resvératrol pour le traitement des tumeurs qui sont généralement insensibles aux thérapies conventionnelles en raison de leur perte de fonction p53 normale[58].
La transition épithéliale-mésenchymateuse joue un rôle dans la progression tumorale. Pour comprendre le rôle du resvératrol dans l'invasion tumorale et les métastases du cancer du poumon, les auteurs ont cherché à étudier son activité à inhiber le TGF-β1, qui induit in vitro le développement de cette transition épithéliale-mésenchymateuse dans les cellules du cancer du poumon. Il est apparu que le resvératrol inhibe l'initiation du TGF-β1 induit par la transition épithéliale-mésenchymateuse. Ainsi, in vitro il inhibe le processus invasif et les métastases dans le cancer du poumon[59].
L'efficacité du traitement combiné de composés phytochimiques avec la clofarabine, un médicament anticancéreux employé dans le mésothéliome malin, a été étudiée[60]. Le traitement associant le resvératrol à la clofarabine a produit un effet synergique anti-prolifératif dans certaines cellules. Dans l'ensemble, les données publiées indiquent que l'effet synergique anti-prolifératif du resvératrol et de la clofarabine est lié à l'inhibition de l'oncogène Akt1 et du facteur de transcription Sp1. Ces données suggèrent que cette association pourrait avoir une valeur thérapeutique dans le traitement du mésothéliome malin[60].
Le traitement par resvératrol a réduit le volume et le poids des tumeurs dans des modèles animaux de cancer du col de l'utérus mais des études animales utilisant des modèles de cancer du col de l'utérus orthotopiques et des modèles cliniquement pertinents sont essentiels pour mieux comprendre le potentiel anticancéreux de cette molécule[61].
Allongement de la durée de vie
Les études montrent que le resvératrol allonge la durée de vie chez les levures, les nématodes et les killis, mais nous n'avons pas d'explication quant à la raison pour laquelle cet effet n'est pas présent chez les mouches et les souris[62].
Levure de bière
L’intérêt pour le resvératrol est relancé en 2003 lorsqu’Howitz et ses collaborateurs[63] après avoir testé de nombreux polyphénols sur la longévité de la levure de bière (Saccharomyces cerevisiae) s’aperçoivent que le resvératrol est le plus efficace de tous. Lorsqu’une cellule de levure se divise, on peut distinguer la cellule mère de la cellule fille qui est plus petite et compter ainsi le nombre de divisions de la cellule mère jusqu’à sa mort. Alors que la longévité moyenne de la levure sauvage est de 21 générations, celle de la levure avec du resvératrol dans son milieu de culture est 35,7 générations, soit une augmentation de durée de vie de 70 %.
Les auteurs ont ensuite essayé de voir si cet effet pouvait être rapproché d’un autre mécanisme très étudié d’allongement de vie par restriction alimentaire (restriction calorique). On sait depuis les années 1930 que le moyen le plus simple et le plus efficace de rallonger la durée de vie d’un animal est de restreindre sa prise alimentaire. En diminuant sa ration alimentaire normale de 30 à 40 %, on permet à l’animal de vivre en meilleure santé et plus longtemps. Cet effet de restriction calorique (RC) sans malnutrition a été observé chez des espèces aussi diverses que les mouches, les vers ou les rongeurs. Lin et ses collaborateurs[64] - [65] (2000, 2002) ont montré qu’en réduisant la concentration en glucose dans le milieu de culture de 2 % à 0,5 %, on peut allonger la durée de vie réplicative de la levure, accroître sa respiration et activer le gène Sir2. Et inversement, en invalidant le gène Sir2, la restriction calorique (RC) ne produit plus d’extension de durée de vie. Le mécanisme d’action de la restriction calorique modérée (confirmé et précisé depuis) peut donc être résumé ainsi :
RC ⇒ activation des mitochondries ⇒ activation de SIR2 ⇒ allongement de vie
Peu de temps après ces travaux, Howitz et ses collaborateurs[63] s’aperçoivent que, parmi les polyphénols testés, le resvératrol non seulement allonge le plus la durée de vie de la levure mais aussi produit la meilleure activation de SIR2. Ils postulent donc que le resvératrol mime l’effet de la restriction calorique sur l’allongement de vie. La protéine SIR2 qui appartient à la famille des protéines antivieillissement, les sirtuines, possède chez les mammifères, un orthologue, SIRT1. Les sirtuines sont des enzymes dépendantes du NAD, capables de désacétyler des protéines et d’accroître la durée de vie de la levure, du ver Caenorhabditis elegans et de la mouche Drosophile[66].
D’autres analyses génétiques ont montré que dans la restriction calorique sévère, avec moins de 0,05 % de glucose (soit 1/10 de la RC modérée), l’allongement de vie se produit aussi mais sans activer les mitochondries et Sir2[67]. Il semble donc que le degré de restriction calorique et son déroulement temporel puissent influencer la relation entre mitochondries, sirtuines et longévité. Plusieurs voies métaboliques d’allongement de la vie par RC sont possibles[68].
Les vertébrés
Une des premières études de l’effet du resvératrol sur la durée de vie des vertébrés a porté sur un petit poisson à durée de vie courte, le Nothobranchius furzeri. Grâce à une supplémentation en resvératrol, ce poisson voit sa durée de vie médiane et maximum s’allonger et les effets du vieillissement sur l’activité motrice se faire moins sentir[69].
Deux études récentes indiquent qu’un traitement au resvératrol étend la durée de vie de la souris obèse et permet de contrecarrer les effets délétères d’un régime riche en graisse. Le groupe d’Auwerx près de Strasbourg (Lagouge et al. 2006)[70] et le groupe de Sinclair de Boston (Baur et al., 2006)[71] ont montré que les effets bénéfiques du resvératrol sur le niveau de glucose et d’insuline des souris obèses ouvrent des perspectives intéressantes pour le traitement du diabète de type 2. Lagouge et ses collaborateurs ont administré pendant 9 semaines un régime riche en graisse, représentatif de l’alimentation des pays occidentaux, à deux groupes de souris. Le groupe dont l’alimentation était très fortement enrichie en resvératrol[72] a montré une prise de poids inférieure de 40 %. En analysant les tissus musculaires, ils se sont aperçus qu’ils contenaient beaucoup plus de mitochondries et que celles-ci étaient très actives. En accroissant la consommation d’oxygène dans les mitochondries, le resvératrol permet d’éviter une prise de poids indue et fournit une meilleure résistance à la fatigue. Lors d'un test d’endurance, les souris ayant reçu du resvératrol pouvaient courir deux fois plus loin que les autres. L’équipe a établi que l’action du resvératrol passe par l’activation de la sirtuine SIRT1 et d’un coactivateur de transcription PGC-1α qui joue un rôle fondamental dans la biogenèse mitochondriale et l’adipogenèse[73].
Le groupe de Sinclair eut recours à un protocole expérimental différent de celui d’Auwerx : il utilisa des doses beaucoup plus faibles de resvératrol (1/18e de la dose d’Auwerx), durant une période plus longue (deux ans) sur les souris plus âgées. Mais même avec ce traitement à faible dose au long cours, les souris recevant une alimentation grasse additionnée de resvératrol améliorent leur sensibilité à l’insuline et accroissent leur durée de vie de manière sensible par rapport aux souris recevant seulement une nourriture grasse. Par contre, elles connaissent à peu près la même prise de poids. Les études des deux groupes montrent un accroissement de la biogenèse mitochondriale, de l’activité PGC-1α, de la protéine kinase activée par AMP et des fonctions motrices.
Des travaux montrent néanmoins que le resvératrol n'améliore pas le fonctionnement des mitochondries chez le rat et la souris et que des doses élevés ont un effet toxique[74].
Pour les souris nourries normalement, ad libitum, on constate qu’elles ne vivent pas plus longtemps lorsqu’elles reçoivent du resvératrol[75] - [76]. Mais elles manifestent une plus grande résistance aux affections liées à l’âge telle une moindre albuminurie, une diminution de l’inflammation, moins de cataractes, une plus grande coordination motrice, une perte de la densité osseuse moins importante[77].
Chez des lémuriens microcèbe, le resvératrol diminue la prise de poids et augmente le métabolisme dans une période d'engraissement naturel. Cet effet, non observé chez les rongeurs, serait propre des primates. Une étude continue sur le retardement des déficits liés à l'âge et l'augmentation de la longévité[78] - [79].
On ne dispose pas encore de publications portant sur les effets du resvératrol sur l’activation des sirtuines chez l’homme, mais l’étude de Civitarese et de ses collaborateurs (2007)[80] portant sur l’effet de la restriction calorique sur l’expression de SIRT1 est assez instructive. Grâce à un petit groupe de personnes qui ont accepté de réduire de 25 % la valeur calorique de leur alimentation pendant 6 mois, ces auteurs ont pu observer une plus grande expression de SIRT1, un plus grand nombre de mitochondries dans les muscles, de moindre dégâts de l’ADN et une amélioration de la fonction mitochondriale.

En raison d’une forte exposition aux espèces réactives oxygénées, l’ADN mitochondrial accumule au cours du temps des mutations qui provoquent le déclin des enzymes mitochondriales. Les dysfonctionnements des mitochondries pourraient être le facteur majeur des maladies neurodégénératives[81] - [82]. Le resvératrol qui peut passer la barrière hémato-encéphalique pourrait avoir un rôle protecteur vis-à-vis des processus neurodégénératifs dans la maladie de Huntington, de Parkinson et d'Alzheimer.
L’effet du resvératrol a été étudié sur deux modèles animaux de la maladie d’Huntington : le ver Caenorhabditis elegans surexprimant la huntingtine mutée responsable de la maladie, sur lequel des tests in vivo ont été effectués et une souris transgénique portant le gène muté (codant la huntingtine) dont les neurones ont été analysés in vitro. Dans les deux modèles, le resvératrol supprime les effets toxiques de la huntingtine mutée. Les neurones du ver retrouvent leur réactions normales et la mort neuronale est diminuée chez la souris. L’activation de SIRT1 par le resvératrol conduit à une moindre toxicité dans les cellules neurales qui expriment une forme mutée de la huntingtine[83].
La destruction par un neurotoxique des neurones dopaminergiques de la substantia nigra permet de simuler chez le rat la maladie de Parkinson. Après avoir fait ingérer du resvératrol (10, 20, 40 mg·kg-1) à ces rats, Jin et ses collaborateurs[84] ont montré qu’au bout de 2 semaines les animaux peuvent récupérer une partie de leur fonction. Ils ont testé les réponses des rats en leur injectant de l’amphétamine : les animaux n’étant lésés que d’un côté, vont se mettre à tourner rapidement sur eux-mêmes, mais ceux qui ont ingéré du resvératrol tournent beaucoup moins.
L’effet du resvératrol a été testé sur deux modèles murins de la maladie d’Alzheimer (MA) : soit des souris transgéniques portant le gène muté de l’APP, lié à la forme familiale de la MA et développant d’importantes plaques β-amyloïdes sans perte neurale[85], soit des souris transgéniques surexprimant la protéine p25 qui provoque une dérégulation de la protéine tau et une dégénérescence neuronale massive[86]. On constate que les souris p25 ont un niveau de SIRT1 qui croît au fur et à mesure de la perte neurale alors que les souris du premier type ne montrent aucune augmentation de la SIRT1. En additionnant durant 45 jours à la nourriture des souris APP du resvératrol (à raison de 300 mg·kg-1·j-1), Karuppagounder et ses collaborateurs[85] ont pu observer une diminution importante de la surface des plaques amyloïdes dans le cortex médial, le striatum et l’hypothalamus. Par contre, aucun changement significatif n’a été trouvé dans l’hippocampe, foyer principal de la maladie d’Alzheimer. Kim et ses collaborateurs[86] ont observé in vitro que le resvératrol via l’activation de SIRT1, diminue de moitié la mort neurale de cellules transfectées par p25-GFP. Pour réduire in vivo la neurodégénération au niveau de l’hippocampe, ils ont dû injecter directement le resvératrol dans les ventricules du cerveau des souris p25. Ils ont alors pu observer une réduction du déficit d’apprentissage et du déclin cognitif. Le resvératrol active SIRT1 qui désacétyle la protéine p53 et l'inhibition de l'apoptose a un effet neuroprotecteur.
Chez l'être humain
Malgré tous ces résultats très favorables sur des modèles animaux ou au niveau cellulaire, l’efficacité et la sécurité du resvératrol en tant que complément alimentaire n’a toujours pas été démontrée chez l’homme. Certaines contre-indications sont déjà connues : un effet sur les plaquettes sanguines qui pourraient augmenter le risque de saignement. L'augmentation de durée de vie de certains animaux traités au resvératrol a été remise en question par plusieurs laboratoires travaillant sur la levure, la drosophile et le nématode. Il n'est encore pas possible de tirer des conclusions définitives quant aux effets du resvératrol sur l'être humain[87].
Chez l'être humain, il a été testé dans différentes maladies mais sur peu de personnes. Il pourrait ainsi avoir une action favorable sur les différents paramètres d'un syndrome métabolique[88]. Dans la stéatose hépatique non alcoolique, il s'avère, par contre, décevant[89]. Son effet hypolipémiant suspecté chez la souris n'est pas retrouvé chez l'homme[90]. Des revues de la littérature publié en 2022 montre quelques effets sur des marqueurs biologiques sans pour autant conclure à un effet clinique significatif[91] - [92].
Une revue systématique et une méta-analyse ont conclu que de fortes doses de resvératrol (≥1000 mg) ont réduit les niveaux de glucose à jeun (WMD: -18,76 mg/dL, IC 95%: -23,43, -14,09; P < 0,00001)[93]. De plus, le resvératrol a réduit la pression artérielle systolique (WMD: -7,97 mmHg, IC 95%: -10,63, -5,31; P < 0,00001) et la pression artérielle diastolique (WMD: -3,55 mmHg, IC 95%: -5,18, -1,93; P < 0,00001) chez les patients atteints de diabète de type 2[93].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Resvératrol », sur ChemIDplus, consulté le 20 août 2009
- (en) « Resveratrol: MedlinePlus Supplements », sur medlineplus.gov (consulté le )
- Vang O, Ahmad N, Baile CA, Baur JA, Brown K, Csiszar A, Das DK, Delmas D, Gottfried C, Lin HY, Ma QY, Mukhopadhyay P, Nalini N, Pezzuto JM, Richard T, Shukla Y, Surh YJ, Szekeres T, Szkudelski T, Walle T, Wu JM, « What is new for an old molecule? Systematic review and recommendations on the use of resveratrol », PLOS ONE, vol. 6, no 6, , e19881 (PMID 21698226, PMCID 3116821, DOI 10.1371/journal.pone.0019881, Bibcode 2011PLoSO...619881V)
- Sahebkar A, Serban C, Ursoniu S, Wong ND, Muntner P, Graham IM, Mikhailidis DP, Rizzo M, Rysz J, Sperling LS, Lip GY, Banach M, « Lack of efficacy of resveratrol on C-reactive protein and selected cardiovascular risk factors--Results from a systematic review and meta-analysis of randomized controlled trials », Int. J. Cardiol., vol. 189, , p. 47–55 (PMID 25885871, DOI 10.1016/j.ijcard.2015.04.008)
- HR Warner, « NIA's Intervention Testing Program at 10 years of age. », Age (Dordrecht, Netherlands), vol. 37, no 2, , p. 22 (PMID 25726185, PMCID 4344944, DOI 10.1007/s11357-015-9761-5)
- (en) Sheida Zeraattalab-Motlagh, Ahmad Jayedi et Sakineh Shab-Bidar, « The effects of resveratrol supplementation in patients with type 2 diabetes, metabolic syndrome, and nonalcoholic fatty liver disease: an umbrella review of meta-analyses of randomized controlled trials », The American Journal of Clinical Nutrition, vol. 114, no 5, , p. 1675–1685 (ISSN 0002-9165 et 1938-3207, DOI 10.1093/ajcn/nqab250, lire en ligne, consulté le )
- Uni. Freibourg
- (en) S. Renaud, Michel de Lorgeril, « Wine, alcohol, platelets, and the French paradox for coronary heart disease », Lancet, vol. 339, no 8808, , p. 1523-6
- (en) E. N. Frankel, A. L. Waterhouse and J. E. Kinsella, « Inhibition of human LDL oxidation by resveratrol », The Lancet, vol. 341, no 8852, , p. 1103-4
- (en) R.D. Semba et al., « Resveratrol Levels and All-Cause Mortality in Older Community-Dwelling Adults. », JAMA Intern Med., (DOI 10.1001, résumé, lire en ligne [PDF]).
- H. Cai, E. Scott, A. Kholghi, C. Andreadi, A. Rufini, A. Karmokar, R. G. Britton, E. Horner-Glister, P. Greaves, D. Jawad, M. James, L. Howells, T. Ognibene, M. Malfatti, C. Goldring, N. Kitteringham, J. Walsh, M. Viskaduraki, K. West, A. Miller, D. Hemingway, W. P. Steward, A. J. Gescher, K. Brown, Cancer chemoprevention: Evidence of a nonlinear dose response for the protective effects of resveratrol in humans and mice | Sci. Transl. Med. 7, 298ra117 (2015)
- Craveiro M, Gaspard Cretenet, Cédric Mongellaz, Maria I. Matias, Olivier Caron, Maria C. Pedroso de Lima, Valérie S. Zimmermann, Eric Solary, Valérie Dardalhon, Vjekoslav Dulić et Naomi Taylor (2017) Resveratrol stimulates the metabolic reprogramming of human CD4+ T cells to enhance effector function | Sci. Signal. | 17 octobre 2017: Vol. 10, Issue 501, eaal3024 DOI: 10.1126/scisignal.aal302|résumé
- Natalia YU Anisimova, Mikhail V Kiselevsky, Andrey V Sosnov et Sergey V Sadovnikov, « Trans-, cis-, and dihydro-resveratrol: a comparative study », Chemistry Central Journal, vol. 5, , p. 88 (ISSN 1752-153X, PMID 22185600, PMCID PMCPMC3313904, DOI 10.1186/1752-153X-5-88, lire en ligne, consulté le )
- (en) Jang, M., Cai, L., Udeani, G. O., Slowing, K. V., Thomas, C. F., Beecher, C. W., « Cancer chemopreventive activity of resveratrol, a natural product derived from grapes », Science, vol. 275, , p. 218-220 (DOI 10.1126/science.275.5297.218)
- (en) Christine Counet, Delphine Callemien, Sonia Collin, « Chocolate and cocoa: New sources of trans-resveratrol and trans-piceid », Food Chemistry, vol. 98, , p. 649-657
- (en) Lucie Frémont, « BIOLOGICAL EFFECTS OF RESVERATROL », Life Sciences, vol. 66, no 8, , p. 663-673
- (en) Ulrik Stervbo, Ole Vang, Christine Bonnesen, « A review of the content of the putative chemopreventive phytoalexin resveratrol in red wine », Food Chemistry, vol. 101, , p. 449-457 (DOI 10.1016/j.foodchem.2006.01.047)
- de 5 ppm à 7 ppm dans la pellicule et 1 ppm dans les pépins, d'après Counet et al.(2006) (réf. ci-dessus)
- Antonia Chiou, Vaios T. Karathanos, Anastasia Mylona, Fotini N. Salta, Fani Preventi and Nikolaos K. Andrikopoulos, « Currants (Vitis vinifera L.) content of simple phenolics and antioxidant activity », Food Chemistry, vol. 102, no 2, (lire en ligne)
- Bin Zhao, Clifford A. Hall, « Composition and antioxidant activity of raisin extracts obtained from various solvents », Foof Chemistry, vol. 108, , p. 511-518
- en moyenne dans le monde, les Pinot noir ont 3,6 ± 2,9 mg·l-1, les Merlot 2,8 ± 2,6 mg·l-1, d'après Stervbo et al. (2006), réf. ci-dessus
- (en) JENNIFER BURNS, TAKAO YOKOTA HIROSHI ASHIHARA,MICHAEL E. J. LEAN, ALAN CROZIER, « Plant Foods and Herbal Sources of Resveratrol », J. Agric. Food Chem., vol. 50,
- Hisada, H., et al.. (2005). Antibacterial and Antioxidative Constituents of Melinjo Seeds and Their Application to Foods. Japan. Science Links Japan.
- (en) Thomas Walle, Faye Hsieh, Mark H. DeLegge, John E. Oatis, Jr., and U. Kristina Walle, « HIGH ABSORPTION BUT VERY LOW BIOAVAILABILITY OF ORAL RESVERATROL IN HUMANS », Drug Metabolism and Disposition, vol. 32, no 12,
- (en) VITAGLIONE Paola, SFORZA Stefano, GALAVERNA Gianni, GHIDINI Cristiana, CAPORASO Nicola, VESCOVI Pier Paolo, FOGLIANO Vincenzo, MARCHELLI Rosangela, « Bioavailability of trans-resveratrol from red wine in humans », Molecular nutrition & food research, vol. 49, no 5, , p. 495-504
- (en) David M. Goldberga, Joseph Yanb, George J. Soleas, « Absorption of three wine-related polyphenols in three different matrices by healthy subjects », Clinical Biochemistry, vol. 36, , p. 79-87
- (en) Xavier Vitrac, Alexis Desmoulière, Brigitte Brouillaud, Stéphanie Krisa, Gérard Deffieux, Nicole Barthe, Jean Rosenbaum, Jean-Michel Mérillon, « Distribution of [14C]-trans-resveratrol, a cancer chemopreventive polyphenol, in mouse tissues after oral administration », Life Sciences, vol. 72, , p. 2219-2233
- (en) De Santi C, Pietrabissa A, Mosca F, Pacifici, « Glucuronidation of resveratrol, a natural product present in grape and wine, in the human liver. », Xenobiotica, vol. 30, , p. 1047-54
- quand un agent antiradicalaire est ajouté au DPPH•, l’électron libre est apparié et la couleur pourpre change en jaune
- (en) P. Iacopini, M. Baldi, P. Storchi, L. Sebastiani, « Catechin, epicatechin, quercetin, rutin and resveratrol in red grape: Content,in vitro antioxidant activity and interactions », Journal of Food Composition and Analysis, vol. 21, , p. 589-598 (doi:10.1016/j.jfca.2008.03.011)
- (en) Leila Belguendouz, Lucie Fremont, Alain Linard, « Resveratrol Inhibits Metal Ion-Dependent and Independent Peroxidation of Porcine Low-Density Lipoproteins », Biochemical Pharmacology, vol. 53, , p. 13-47-1355
- 2,2'-azobis(2-amidinopropane) dihydrochloride
- (en) Sandra Stojanovic, Helmut Sprinz, and Ortwin Brede, « Efficiency and Mechanism of the Antioxidant Action of trans-Resveratrol and Its Analogues in the Radical Liposome Oxidation », Archives of Biochemistry and Biophysics, vol. 391, no 1, (doi:10.1006/abbi.2001.2388)
- vésicules formés par deux couches de lipide, à l'intérieur desquels est enfermé l'antioxydant étudié. La peroxydation est déclenchée par une irradiation gamma γ
- Afaq F, Mukhtar H, « Botanical antioxidants in the prevention of photocarcinogenesis and photoaging ». Exp Dermatol 2006; 15: 678–84
- Baliga MS, Katiyar SK, « Chemoprevention of photocarcinogenesis by selected dietary botanicals ». Photochem Photobiol Sci 2006; 5: 243–53
- Afaq F, Adhami VM, Ahmad N, « Prevention of short-term ultraviolet B radiation-mediated damages by resveratrol in SKH-1 hairless mice ». Toxicol Appl Pharmacol 2003; 186: 28–37.
- Aziz MH, Afaq F, Ahmad N, « Prevention of ultraviolet-B radiation damage by resveratrol in mouse skin is mediated via modulation in survivin ». Photochem Photobiol 2005; 81: 25–31.
- Afaq F, Adhami VM, Ahmad N, « Prevention of short-term ultraviolet B radiation-mediated damages by resveratrol in SKH-1 hairless mice ». Toxicol Appl Pharmacol 2003; 186: 28–37
- [Reagan-Shaw S, Afaq F, Aziz MH et al, « Modulations of critical cell cycle regulatory events during chemoprevention of ultraviolet B-mediated responses by resveratrol in SKH-1 hairless mouse skin ». Oncogene 2004; 23: 5151–5160.]
- Aziz MH, Afaq F, Ahmad N, « Prevention of ultraviolet-B radiation damage by resveratrol in mouse skin is mediated via modulation in survivin ». Photochem Photobiol 2005; 81: 25–31
- Liu Y, Chan F, Sun H, Ya J, Fa D, Zhao D, An J, Zhou D, « Resveratrol protects human keratinocytes HaCaT cells from UVA-induced oxidative stress damage by downregulating Keap1 expression ». Eur J Pharmacol. 2011;650:130–7
- Wu Y, Jia LL, Zheng YN, Xu XG, Luo YJ, Wang B, et al, « Resveratrate protects human skin from damage due to repetitive ultraviolet irradiation ». Journal of the European Academy of Dermatology and Venereology JEADV 2012 ; Jan 5
- Lee JS, Park KY, Min HG, Lee SJ, Kim JJ, Choi JS, Kim WS, Cha HJ, « Negative regulation of sress-induced matrix metalloproteinase-9 by SirT1 in skin tissue ». Exp Dermatol. 2010;19:1060–6
- Bastianetto S, Dumont Y, Duranton A, Vercauteren F, Breton L, Quirion R, « Protective action of resveratrol in human skin: possible involvement of specific receptor binding sites ». PLoS One. 5(9): e12935. . DOI 10.1371/journal.pone.0012935
- Watson, Ronald Ross; Zibadi, Sherma (Eds.), « Bioactive Dietary Factors and Plant Extracts in Dermatology » (2013) pp 177-187
- (en) Cecil R. Pace-Asciak, Susan Hahn, Eleftherios P. Diamandis, George Soleas, David M. Goldberg, « The red wine phenolics trans-resveratrol and quercetin block human platelet aggregation and eicosanoid synthesis: Implications for protection against coronary heart disease », Clinica Chimica Acta, vol. 235, , p. 207-219
- (en) Cecil R. Pace-Asciak, Olga Rounova, Susan E. Hahn, Eleftherios P. Diamandis, David M. Goldberg, « Wines and grape juices as modulators of platelet aggregation in healthy human subjects », Clinica Chimica Acta, vol. 246, nos 1-2,
- (en) Jang M, Cai L, Udeani GO, Slowing KV, Thomas CF, Beecher CW, et al., « Cancer chemopreventive activity of resveratrol, a natural product derived from grapes », Science, vol. 275, , p. 218-220
- (en) Kotha Subbaramaiah, Wen Jing Chung, Pedro Michaluarti, Nitin Telang, Tadashi Tanabe, Hiroyasu Inoue, Meishiang Jang, John M. Pezzuto, and Andrew J. Dannenberg, « Resveratrol Inhibits Cyclooxygenase-2 Transcription and Activity in Phorbol Ester-treated Human Mammary Epithelial Cells », The Journal of Biological Chemistry, vol. 273, no 34,
- (en) Javier Martinez and Juan J. Moreno, « Effect of Resveratrol, a Natural Polyphenolic Compound, on Reactive Oxygen Species and Prostaglandin Production », Biochemical Pharmacology, vol. 59, , p. 865-870
- (en) Stef G, Csiszar A, Lerea K, Ungvari Z, Veress G., « Resveratrol inhibits aggregation of platelets from high-risk cardiac patients with aspirin resistance. », J Cardiovasc Pharmacol., vol. 48, no 2, , p. 1-5
- (en) Yu-Min Yang, Jun-Zhu Chen, Xing-Xiang Wang,Shi-Jun Wang, Hu Hu, Hong-Qiang Wang, « Resveratrol attenuates thromboxane A2 receptor agonist-induced platelet activation by reducing phospholipase C activity », European Journal of Pharmacology, vol. 583, , p. 148-155
- La P-sélectine est exprimée à la surface des plaquettes lors de leur activation. Elle intervient de façon précoce dans les interactions des leucocytes avec les plaquettes lors du processus inflammatoire.
- (en) Esmerina Tili, « Resveratrol decreases the levels of miR-155 by upregulating miR-663, a microRNA targeting JunB and JunD », Carcinogenesis, vol. 31, , p. 1561-1566 (lire en ligne)
- (en) Ferraz da Costa DC, Casanova FA et al. « Transient Transfection of a Wild-Type p53 Gene Triggers Resveratrol-Induced Apoptosis in Cancer Cells » PLOS One 2012;7(11):e48746. Epub 2012 novembre 2012
- (en) Wang H, Zhang H, Tang L et al. « Resveratrol inhibits TGF-β1-induced epithelial-to-mesenchymal transition and suppresses lung cancer invasion and metastasis »] Toxicology 9 novembre 2012 pii: S0300-483X(12)00373-3. DOI 10.1016/j.tox.2012.09.017
- Lee YJ, Lee YJ, Im JH et al. « Synergistic anti-cancer effects of resveratrol and chemotherapeutic agent clofarabine against human malignant mesothelioma MSTO-211H cells » Food Chem Toxicol. 9 novembre 2012 pii: S0278-6915(12)00805-8. DOI 10.1016/j.fct.2012.10.060
- Matteo Nadile, Maria Ilektra Retsidou, Katerina Gioti et Apostolos Beloukas, « Resveratrol against Cervical Cancer: Evidence from In Vitro and In Vivo Studies », Nutrients, vol. 14, no 24, , p. 5273 (ISSN 2072-6643, PMID 36558430, PMCID 9787601, DOI 10.3390/nu14245273, lire en ligne, consulté le )
- Katie L. Hector, Malgorzata Lagisz et Shinichi Nakagawa, « The effect of resveratrol on longevity across species: a meta-analysis », Biology Letters, vol. 8, no 5, , p. 790–793 (ISSN 1744-957X, PMID 22718956, PMCID 3440975, DOI 10.1098/rsbl.2012.0316, lire en ligne, consulté le )
- (en) Konrad T. Howitz, Kevin J. Bitterman, Haim Y. Cohen, Dudley W. Lamming, Siva Lavu, Jason G. Wood, Robert E. Zipkin, Phuong Chung, Anne Kisielewski, Li-Li Zhang, Brandy Scherer & David A. Sinclair, « Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan », Nature, vol. 425, , p. 191-6
- (en) Su-Ju Lin, Pierre-Antoine Defossez, Leonard Guarente, « Requirement of NAD and SIR2 for Life-Span Extension by Calorie Restriction in Saccharomyces cerevisiae », Science, vol. 289,
- (en) Lin SJ, Kaeberlein M, Andalis AA, Sturtz LA, Defossez PA, Culotta VC, Fink GR, Guarente L., « Calorie restriction extends Saccharomyces cerevisiae lifespan by increasing respiration », Nature, vol. 418, , p. 344-8
- (en) Guarente L, Picard F., « Calorie restriction--the SIR2 connection. », Cell, vol. 120, no 4, , p. 473-82
- (en) Kaeberlein, M., Powers, R.W., 3rd, Steffen, K.K., Westman, E.A., Hu, D., Dang,N., Kerr, E.O., Kirkland, K.T., Fields, S., and Kennedy, B.K., « Regulation of yeast replicative life span by TOR and Sch9 in response to nutrients », Science, , p. 1193-1196
- (en) Guarente Leonard, « Mitochondria – A Nexus for Aging, Calorie Restriction, and Sirtuins? », Cell, vol. 132,
- (en) Valenzano, D.R., Cellerino, A.,, « Resveratrol and the pharmacology of aging: a new vertebrate model to validate an old molecule », Cell Cycle, vol. 5, , p. 1027-1032
- (en) Marie Lagouge, Carmen Argmann, Zachary Gerhart-Hines, Hamid Meziane, Carles Lerin, Frederic Daussin, Nadia Messadeq, Jill Milne, Philip Lambert, Peter Elliott, Bernard Geny, Markku Laakso, Pere Puigserver, and Johan Auwerx, « Resveratrol Improves Mitochondrial Function and Protects against Metabolic Disease by Activating SIRT1 and PGC-1a », Cell, vol. 127, , p. 1109-1122
- (en) Joseph A. Baur, Kevin J. Pearson, Nathan L. Price, Hamish A. Jamieson, Carles Lerin, Avash Kalra, Vinayakumar V. Prabhu, Joanne S. Allard, Guillermo Lopez-Lluch, Kaitlyn Lewis, Paul J. Pistell, Suresh Poosala, Kevin G. Becker, Olivier Boss, Dana Gwinn, Mingyi Wang, Sharan Ramaswamy, Kenneth W. Fishbein, Richard G. Spencer, Edward G. Lakatta, David Le Couteur, Reuben J. Shaw, Placido Navas, Pere Puigserver, Donald K. Ingram, Rafael de Cabo & David A. Sinclair, « Resveratrol improves health and survival of mice on a high-calorie diet », Nature, vol. 444,
- à la dose de 400 mg·kg-1·j-1
- ainsi que dans la différenciation cellulaire du muscle et le métabolisme énergétique
- Dong-Ho Han, « Effects of Resveratrol and SIRT1 on PGC-1α Activity and Mitochondrial Biogenesis: A Reevaluation », PLOS Biology, vol. 11, no 7, , e1001603 (ISSN 1545-7885, DOI 10.1371/journal.pbio.1001603, lire en ligne, consulté le ).
- Richard A. Miller, David E. Harrison, C. M. Astle et Joseph A. Baur, « Rapamycin, but not resveratrol or simvastatin, extends life span of genetically heterogeneous mice », The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences, vol. 66, no 2, , p. 191–201 (ISSN 1758-535X, PMID 20974732, PMCID 3021372, DOI 10.1093/gerona/glq178, lire en ligne, consulté le )
- Randy Strong, Richard A. Miller, Clinton M. Astle et Joseph A. Baur, « Evaluation of resveratrol, green tea extract, curcumin, oxaloacetic acid, and medium-chain triglyceride oil on life span of genetically heterogeneous mice », The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences, vol. 68, no 1, , p. 6–16 (ISSN 1758-535X, PMID 22451473, PMCID 3598361, DOI 10.1093/gerona/gls070, lire en ligne, consulté le )
- (en) Kevin J. Pearson, Joseph A. Baur, Kaitlyn N. Lewis, Leonid Peshkin, Nathan L. Price, Nazar Labinskyy, William R. Swindell, Davida Kamara, Robin K. Minor, Evelyn Perez, Hamish A. Jamieson, Yongqing Zhang, Stephen R. Dunn, Kumar Sharma, Nancy Pleshko, Laura A. Woollett, Anna Csiszar, Yuji Ikeno, David Le Couteur, Peter J. Elliott, Kevin G. Becker, Placido Navas, Donald K. Ingram, Norman S. Wolf, Zoltan Ungvari, David A. Sinclair, and Rafael de Cabo, « Resveratrol Delays Age-Related Deterioration and Mimics Transcriptional Aspects of Dietary Restriction without Extending Life Span », Cell Metabolism, vol. 8, , p. 157-168
- (fr) Fabienne Aujard du laboratoire "Mécanismes adaptatifs: des organismes aux communautés" (CNRS/Museum national d'Histoire naturelle), journal BMC Physiology, 22 juin 2010, techno-science
- (en) Fabienne Aujard, Resveratrol suppresses body mass gain in a seasonal non-human primate model of obesity, BMC Physiology, 22 juin 2010
- Anthony E. Civitarese, Stacy Carling, Leonie K. Heilbronn et Mathew H. Hulver, « Calorie Restriction Increases Muscle Mitochondrial Biogenesis in Healthy Humans », PLOS Med, vol. 4, , e76 (ISSN 1549-1676, PMID 17341128, PMCID 1808482, DOI 10.1371/journal.pmed.0040076, lire en ligne, consulté le )
- (en) Douglas C. Wallace, « The mitochondrial genome in human adaptive radiation and disease:On the road to therapeutics and performance enhancement », Gene, vol. 354, , p. 169-180
- S. Rasouri, M. Lagouge, J. Auwerx, « SIRT1/PGC-1 Un axe neuroprotecteur ? », m/s médecine/sciences, vol. 23, , p. 840-4
- (en) Parker JA, Arango M, Abderrahmane S, Lambert E, Tourette C, Catoire H, Néri C., « Resveratrol rescues mutant polyglutamine cytotoxicity in nematode and mammalian neurons », Nat. Genet., vol. 37, no 4,
- (en) Feng Jin, Qin Wu, Yuan-Fu Lu, Qi-Hai Gong, Jing-Shan Shi, « Neuroprotective effect of resveratrol on 6-OHDA-induced Parkinson's disease in rats », European Journal of Pharmacology, vol. 600, , p. 78-82
- (en) Saravanan S. Karuppagounder, John T. Pinto, Hui Xu, Huan-Lian Chen, M. Flint Beal, Gary E. Gibson, « Dietary supplementation with resveratrol reduces plaque pathology in a transgenic model of Alzheimer’s disease », Neurochemistry International,
- (en) Dohoon Kim, Minh Dang Nguyen, Matthew M Dobbin, Andre Fischer, Farahnaz Sananbenesi, Joseph T Rodgers, Ivana Delalle, Joseph A Baur, Guangchao Sui, Sean M Armour, Pere Puigserver, David A Sinclair, and Li-Huei Tsai, « SIRT1 deacetylase protects against neurodegeneration in models for Alzheimer’s disease and amyotrophic lateral sclerosis », EMBO Journal, vol. 26, no 13,
- (en) CH Cottart, « Resveratrol bioavailability and toxicity in humans. », Mol Nutr Food Res, vol. 54, no 1, , p. 7-16 (lire en ligne)
- Méndez-del Villar M, González-Ortiz M, Martínez-Abundis E, Pérez-Rubio KG, Lizárraga-Valdez R, Effect of resveratrol administration on metabolic syndrome, insulin sensitivity, and insulin secretion, Metab Syndr Relat Disord, 2014;12:497–501
- Chachay VS, Macdonald GA, Martin JH et al. Resveratrol does not benefit patients with nonalcoholic fatty liver disease, Clin Gastroenterol Hepatol, 2014;12:2092–2103.e1–6
- Sahebkar A, Effects of resveratrol supplementation on plasma lipids: a systematic review and meta-analysis of randomized controlled trials, Nutr Rev, 2013;71:822–835
- Xinyi Cao, Wang Liao, Hui Xia et Shaokang Wang, « The Effect of Resveratrol on Blood Lipid Profile: A Dose-Response Meta-Analysis of Randomized Controlled Trials », Nutrients, vol. 14, no 18, , p. 3755 (ISSN 2072-6643, PMID 36145131, PMCID 9506025, DOI 10.3390/nu14183755, lire en ligne, consulté le )
- Nazanin Mohammadipoor, Fatemeh Shafiee, Amirabbas Rostami et Mohammad Saeed Kahrizi, « Resveratrol supplementation efficiently improves endothelial health: A systematic review and meta-analysis of randomized controlled trials », Phytotherapy research: PTR, vol. 36, no 9, , p. 3529–3539 (ISSN 1099-1573, PMID 35833325, DOI 10.1002/ptr.7562, lire en ligne, consulté le )
- Wei Gu, Jianlin Geng, Hang Zhao et Xiaolong Li, « Effects of Resveratrol on Metabolic Indicators in Patients with Type 2 Diabetes: A Systematic Review and Meta-Analysis », International Journal of Clinical Practice, vol. 2022, , p. 9734738 (ISSN 1742-1241, PMID 35685602, PMCID 9158797, DOI 10.1155/2022/9734738, lire en ligne, consulté le )
