Mescaline
La mescaline (ou 3,4,5-triméthoxyphénéthylamine) est un alcaloïde psychotrope aux propriétés psychédéliques et enthéogènes qui possède une structure de phényléthylamine substituée. Elle est souvent rattachée à la catégorie mal définie des « drogues hallucinogènes ».
| Mescaline | ||
| ||
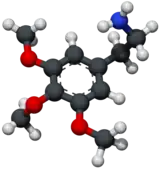 | ||
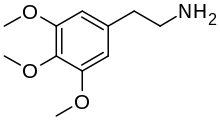
| Structure de la mescaline | ||
| Identification | ||
|---|---|---|
| Nom UICPA | 2-(3,4,5-triméthoxyphényl)éthanamine | |
| Synonymes |
3,4,5-triméthoxyphénéthylamine |
|
| No CAS | ||
| No ECHA | 100.000.174 | |
| SMILES | ||
| InChI | ||
| Apparence | poudre blanche | |
| Propriétés chimiques | ||
| Formule | C11H17NO3 [Isomères] |
|
| Masse molaire[1] | 211,257 6 ± 0,011 1 g/mol C 62,54 %, H 8,11 %, N 6,63 %, O 22,72 %, |
|
| Propriétés physiques | ||
| T° fusion | 35 à 36 °C[2] - [3] - [4] | |
| T° ébullition | 180 °C (à 12 mmHg)[2] - [3] - [4] | |
| Miscibilité | soluble dans l'eau, l'alcool et le chloroforme. Peu soluble dans l'éther[2]. | |
| Écotoxicologie | ||
| DL50 | souris (par ingestion) 880 mg·kg-1[5] souris (intraveineuse) |
|
| Données pharmacocinétiques | ||
| Excrétion |
urine |
|
| Caractère psychotrope | ||
| Catégorie | Hallucinogène psychédélique | |
| Mode de consommation |
Ingestion |
|
| Autres dénominations |
Mescalito, mess, wizz |
|
| Risque de dépendance | Nul | |
| Unités du SI et CNTP, sauf indication contraire. | ||
On la trouve à l'état naturel dans les tissus végétaux de plusieurs espèces de cactus, en particulier le peyotl (L. williamsii), d'où elle est extraite depuis des millénaires pour être consommée lors de rituels religieux. La détermination de sa structure à la toute fin du XIXème siècle a ouvert la voie à sa synthèse totale.
Historique
Les premiers travaux sur la mescaline datent de 1888, mais la molécule n'a été isolée et identifiée qu'en 1894[6] par l'Allemand Arthur Heffter, puis synthétisée en 1919 par Ernst Späth (en). Le pharmacologiste allemand Louis Lewin s'y était déjà intéressé en 1886. On décèle la mescaline dans plusieurs cactus comme certaines espèces des genres Echinopsis ou Lophophora, plus connu sous le nom de peyotl dont le principe actif le plus présent est la mescaline. L'usage du peyotl à des fins rituelles par les Amérindiens est ancien et son utilisation cérémoniale remonte à au moins trois mille ans comme l'ont démontré des fouilles archéologiques dans des grottes du Texas[7]. Il faut souligner que durant les cérémonies chamaniques, le chaman utilise le cactus entier, qui contient parfois d'autres principes actifs, et non de la mescaline purifiée ou synthétisée.
En Occident, la mescaline est commercialisée par deux grands laboratoires pharmaceutiques, Merck, en Allemagne, et Roche en Suisse. La substance fait l'objet de plusieurs thèses et articles de médecine[8] - [9] et de pharmacie et est notamment particulièrement étudiée par le psychiatre Henri Ey[10]. Des intellectuels comme Jean-Paul Sartre[11], Antonin Artaud[12], Allen Ginsberg[13], ou Henri Michaux[14] se prêtent à l'expérience de la substance dans un cadre expérimental.
Aldous Huxley la découvre en 1953 grâce au psychiatre Humphry Osmond, et à la suite de ses propos élogieux dans son ouvrage Les Portes de la perception, de nombreux psychiatres l'utiliseront comme moyen d'investigation du psychisme mais également dans un but thérapeutique. À partir des années 1950 et en lien avec l'intérêt porté à cette époque sur un autre psychédélique, le LSD, la mescaline devient de plus en plus étudiée en médecine jusqu'à son classement dans la liste des stupéfiants en 1971 qui sonne l'arrêt des recherches sur cette classe de substances[15] - [16].
Chimie

Sa structure est proche de celle de l'adrénaline (les deux molécules partagent la même base phényléthylamine, qui est un dérivé de la phénylalanine, un acide aminé). Elle est également proche de celle de l'amphétamine.
Extraction

La molécule est présente à l'état naturel dans plusieurs variétés de cactus (famille des cactacées) dont le Lophophora williamsii ou Anhalonium lewinii[17] (voir aussi peyotl), le Trichocereus pachanoi (San Pedro) et le Trichocereus peruvianus (en) (torche péruvienne) ainsi que dans le Trichocereus bridgesii (torche bolivienne)
Il est possible d'extraire la mescaline en faisant sécher les boutons puis en les faisant tremper dans du méthanol pendant une journée. Le résultat est ensuite filtré, en laissant le méthanol s'évaporer. La poudre obtenue est ensuite traitée avec du chloroforme et de l'acide chlorhydrique pour extraire les alcaloïdes[18]. Il existe une méthode alternative qui utilise la faible solubilité du sulfate de mescaline, où l'acide chlorhydrique est remplacé par de l'acide sulfurique.
Un procédé moins élaboré consisterait à cuire les boutons dans un autocuiseur.
Synthèse
De nombreuses voies de synthèse de la mescaline sont décrites dans la littérature scientifique. Une publication de 2018 en recense neuf, dont sept qualifiées de classiques et deux de plus modernes[19].
Une synthèse classique (décrite dès 1919 par Ernst Späth[20] et reprise en 1991 par Alexander Shulgin dans PiHKAL) démarre par une réaction de Henry au cours de laquelle le 3,4,5-triméthoxybenzaldéhyde se condense avec le nitrométhane en présence d'acide acétique (solvant) et de cyclohexylamine (catalyseur). Pour obtenir la mescaline, le nitrostyrène formé doit ensuite subir une double réduction, à la fois de la double liaison éthylénique de la chaîne latérale et du groupe nitro qu'il faut convertir en amine. Pour cela le plus simple est d'employer un hydrure capable de réduire les deux fonctions, typiquement LiAlH4. À défaut il est possible de faire agir successivement deux agents réducteurs, l'un pour la double liaison et l'autre pour le groupe nitro.
Une alternative consiste à traiter successivement le 3,4,5-triméthoxybenzaldéhyde par le tétrahydruroborate de sodium, le tribromure de phosphore, et le cyanure, puis à hydrogéner le produit obtenu[21].
Pharmacologie
La demi-vie de la mescaline est de l'ordre de six heures. La plus grande partie est éliminée par les urines.
Elle agit comme un agoniste sur les récepteurs sérotoninergiques[6], en particulier sur les récepteurs 5-HT2A et 5-HT2C[22]. La raison pour laquelle l'activation de ces récepteurs induit des effets psychédéliques reste méconnue, mais il semblerait que ce soit lié à l'activation de neurones dans le cortex préfrontal[23].
Le dosage effectif est de 200–500 mg pour un adulte (ou 3,75 mg kg−1) avec des effets qui durent au moins 12 heures[6] - [24]. Ce dosage en fait une drogue à faible activité comparée au LSD puisqu'il faut une dose 5 000 fois plus faible de LSD pour obtenir des effets similaires ; autrement dit, 100 µg de LSD équivalent à environ 500 mg de mescaline (entre 250 mg et 1 000 mg)[25]. Comme pour les autres phényléthylamines psychédéliques, le rapport entre dose létale et dose active est assez élevé par rapport à d'autres classes d'hallucinogènes (anticholinergiques par exemple).
Usage détourné et récréatif
Elle se vend (illégalement dans la plupart des pays) sous forme de poudre de différentes couleurs, de liquide, de capsules de gélatine ou de comprimés. Les échantillons vendus comme de la mescaline contiennent très souvent de la PCP ou du LSD.
Effets et conséquences
Les effets physiques peuvent inclure :
- mydriase (dilatation des pupilles) ;
- nausée, vomissement (surtout lors de l'ingestion) ;
- hypertension artérielle (augmentation de la pression artérielle), tachycardie (augmentation du rythme cardiaque) ;
- hyperthermie, sudation (transpiration) voire fièvre.
Les effets psychiques et d'altération de la perception peuvent inclure :
- euphorie ;
- phosphènes et autres hallucinations visuelles de type psychédélique ;
- hallucinations auditives ;
- synesthésie ;
- perception déformée du corps ;
- troubles de la concentration ;
- désorientation ;
- altération de la mémoire à court terme.
À forte dose, la mescaline peut provoquer :
- céphalées (maux de tête) ;
- hypotension artérielle (diminution de la pression artérielle), bradycardie (baisse du rythme cardiaque) ;
- assèchement de la peau ;
- dépression respiratoire ;
- confusion onirique et perte des repères spatio-temporels.
Dans le cas d'un bad trip, les effets sont plutôt négatifs, l'euphorie et l'extase pouvant laisser place à l'angoisse et la peur.
La mescaline ne semble pas provoquer de dépendance physique ni psychique. Aucun cas de décès directement lié à la mescaline n'a jamais été recensé en France. Utilisée dans un contexte traditionnel (chamanique) ou dans le cadre d'un groupe religieux comme l'église des Indiens Natifs aux États-Unis (NAC), elle possède des propriétés anti-addictives, permettant de lutter contre l'alcoolisation de ces populations[26].
En revanche, comme toute substance hallucinogène, elle peut causer des accidents psychiatriques graves et durables, parfois dès la première prise. On parle alors de « syndrome post-hallucinatoire persistant », à savoir angoisses, phobies, état confusionnel, dépression voire pseudo-hallucinations, critiquées et reconnues comme telles, pouvant persister plusieurs années[27]. Ces incidents ne semblent pas survenir chez les Navajos qui l'utilisent dans leurs rituels[28].
Législation
La mescaline est répertoriée par la convention sur les substances psychotropes de 1971 ce qui rend son usage réglementé et surveillé.
La mescaline est classée comme stupéfiant en France par l'arrêté du fixant la liste des substances classées comme stupéfiants (JO du )[29].
La mescaline a été rendue illégale aux États-Unis par le Comprehensive Drug Abuse Prevention and Control Act en 1970. Une dérogation autorise cependant les membres de la Native American Church (environ 250 000 membres[30]) à l'utiliser pour leurs sacrements.
Consommateurs célèbres
- Antonin Artaud
- Syd Barrett
- William S. Burroughs
- Carlos Castaneda
- Pierre Dunn : L'Ange de Longueuil
- Domino Harvey
- Aldous Huxley qui l'expérimenta avant de la théoriser dans un livre célèbre paru en français sous le titre : Les Portes de la perception
- Ernst Jünger dans Approches, drogues et ivresse, 1970
- Henri Michaux (cf. Misérable Miracle, récit de son expérience de la mescaline, et L'Infini turbulent)
- Jim Morrison (le nom du groupe de rock qu'il co-fonda, les Doors, s'inspire du titre du livre d'Aldous Huxley, The Doors of perception, lui-même issu d'une œuvre de William Blake).
- Jean Paulhan
- Keith Richards
- Bernard Saby (cf. Misérable Miracle, « L'image privilégiée »)
- Jean-Paul Sartre (en , au centre hospitalier Sainte-Anne, dans le cadre de recherches phénoménologiques sur l'imagination ; il est suivi par son ancien condisciple, le docteur Daniel Lagache ; l'expérience entraîne six mois de dépression et d'hallucinations)
- James Taylor (cf. One Man Dog (1972), « Mescalito »)
- Hunter S. Thompson
- Carlos Santana qui a notamment pris de la mescaline avant de monter sur scène lors de sa célèbre performance de Woodstock.
Dans la culture
Certains écrivains comme Jean-Paul Sartre et Henri Michaux ont été de grands consommateurs de mescaline[31]. Michaux lui a consacré un livre, Misérable Miracle, dans lequel il parle de son expérience personnelle avec cette drogue.
Dans le roman Las Vegas Parano (1972) et son adaptation cinématographique (1998), les deux personnages principaux (interprétés dans le film par Johnny Depp et Benicio del Toro) en utilisent à très forte dose (« la bonne mescaline ça met du temps à faire effet »). En effet, dans Las Vegas Parano les personnages enchaînent expériences, délires, et par conséquent, déformations de la perception en tous genres. Le film traduit bien l'aspect hallucinogène qui se manifeste notamment par la peur constante d'autrui dans leurs délires prolongés.
Dans le film Matrix (1999), le personnage de Choi, qui achète un programme pirate à Neo au début du film, y fait allusion comme étant pour lui « la seule façon de planer ».
Dans le film A Single Man (2009), réalisé par le couturier Tom Ford, le personnage principal (incarné par Colin Firth) est un professeur d'université dans les années 1960 qui, lors d'une discussion avec l'un de ses étudiants, déclare s'être rasé un sourcil après avoir pris de la mescaline. Dans le film Les Amants passagers (2013) de Pedro Almodóvar, plusieurs personnages prennent de la mescaline, volontairement ou à leur insu, durant leur vol.
Molécules voisines
Plusieurs dérivés de la mescaline ont été synthétisés, comme l'escaline, la proscaline, la thiomescaline, la triméthoxyamphétamine (TMA), etc. Ces dérivés sont pour la plupart bien plus puissants que la mescaline.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) L. Reti, « The Chemistry of the Plant Phenethylamines Part 3.11 - Mescaline »,
- (en) Erowid, « Mescaline Chemistry »
- Les constantes physiques données concernent la mescaline pures, pour le chlorhydrate et le sulfhydrate, ces constantes diffèrent (se reporter aux sources pour plus de précision)
- (en) « Health hazard data »
- Denis Richard, Jean-Louis Senon et Marc Valleur, Dictionnaire des drogues et des dépendances, Paris, Larousse, , 626 p. (ISBN 2-03-505431-1)
- (en) Peter Stafford, Psychedelics Encyclopedia, New York, Ronin Publishing, , 1004 p. (OCLC 897069457, lire en ligne), p. 388
- M. Ropert, La Mescaline en psychiatrie clinique et expérimentale (Thèse de médecine), (lire en ligne)
- ROUHIER A et ROUHIER A., La plante qui fait les yeux émerveillés : le Peyotl, (ISBN 978-2-85707-332-1, lire en ligne)
- Henri Ey (1900-1977), Traité des hallucinations, (lire en ligne)
- « Études psychédéliques - Gautier Dassonneville : "Sartre et la mescaline" 03/21 » (consulté le )
- (en-US) Patrick Doyle, « Patti Smith Channels French Poet Antonin Artaud on Peyote », sur Rolling Stone, (consulté le )
- (en-US) Condé Nast, « The Father of Flower Power », sur The New Yorker, (consulté le )
- Henri Michaux, « Misérable miracle », sur www.gallimard.fr, (consulté le )
- Aymon de Lestrange, « Histoire de la découverte de quelques hallucinogènes », sur societepsychedelique.fr, Société psychédélique française, (consulté le )
- (en) Eric Bender, « Finding medical value in mescaline », Nature, vol. 609, no 7929, , S90–S91 (DOI 10.1038/d41586-022-02873-8, lire en ligne, consulté le )
- Aldous Huxley, Les Portes de la perception, 10/18, (ISBN 978-2-264-00125-2).
- (en) « Acid-Base Extraction of Mescaline from San Pedro », sur www.erowid.org, (consulté le ).
- Cassels BK & Sáez-Briones P « Dark classics in chemical neuroscience : mescaline » ACS Chem Neurosci. 2018;9(10):2448-2458. https://doi.org/10.1021/acschemneuro.8b00215
- Späth E « Über die Anhalonium-Alkaloide. I. Anhalin und Mezcalin » Monatsh Chem. 1919;40, 129–154. Accès libre
- (en) « Synthesis of Mescaline », sur www.erowid.org
- (en) BilZ0r, « Neuropharmacology of Hallucinogens: a brief introduction », Erowid.org, (lire en ligne).
- (en) Béïque JC, Imad M, Mladenovic L, Gingrich JA, Andrade R, « Mechanism of the 5-hydroxytryptamine 2A receptor-mediated facilitation of synaptic activity in prefrontal cortex », Proc Natl Acad Sci. USA, vol. 104, no 23, , p. 9870–5 (PMID 17535909, PMCID PMC1887564, DOI 10.1073/pnas.0700436104, lire en ligne).
- Malin Vedøy Uthaug, Alan K. Davis, Trevor Forrest Haas et Dawn Davis, « The epidemiology of mescaline use: Pattern of use, motivations for consumption, and perceived consequences, benefits, and acute and enduring subjective effects », Journal of Psychopharmacology (Oxford, England), vol. 36, no 3, , p. 309–320 (ISSN 1461-7285, PMID 33949246, PMCID 8902264, DOI 10.1177/02698811211013583, lire en ligne, consulté le )
- Chiffres obtenus à partir de LSD, mon enfant terrible écrit par Albert Hofmann.
- Olivier Chambon, La médecine psychédélique : le pouvoir thérapeutique des hallucinogènes, Paris, Éditions des Arènes, 2009, 396 p. (OCLC 318664421).
- (en) Hermle L, Simon M, Ruchsow M, Geppert M, « Hallucinogen-persisting perception disorder », Ther Adv Psychopharmacol (en), vol. 2, no 5, , p. 199-205 (PMID 23983976, PMCID PMC3736944, DOI 10.1177/2045125312451270, lire en ligne).
- (en) JH Halpern, « Hallucinogens: an update », Curr Psychiatry Rep (en), vol. 5, no 5, , p. 347-354 (PMID 13678554).
- arrêté du fixant la liste des substances classées comme stupéfiants (JO du ).
- Anne Garrait-Bourrier, « Spiritualité et fois amérindiennes : Résurgence d’une identité perdue », Cercles, vol. 15, , p. 80 (lire en ligne [PDF]).
- Alexis Broca, « Mescaline, la fleur et les épines du cactus », Le Magazine Littéraire, no 542, , p. 60 (lire en ligne
 )
)
Voir aussi
Articles connexes
Liens externes
- Mescaline sur PsychonautWiki
- Photographie d'un Lophophora williamsii
- Images du monde visionnaire, film réalisé en 1964 par Henri Michaux et Éric Duvivier pour le compte de la firme pharmaceutique Sandoz, et décrivant les images provoquées par l'absorption de mescaline.