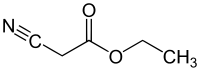
Cyanoacétate d'éthyle
Le cyanoacétate d'éthyle est un composé organique, de formule brute C5H7NO2, contenant à la fois une fonction ester et un groupe nitrile. Il se présente sous la forme liquide incolore avec une odeur plaisante[5]. C'est un composé utile comme réactif de départ en synthèse organique du fait de la variété de ses groupes fonctionnels et de sa réactivité chimique.
| Cyanoacétate d'éthyle | |
| |
| Identification | |
|---|---|
| Nom systématique | cyanoéthanoétate d'éthyle |
| No CAS | |
| No ECHA | 100.003.009 |
| PubChem | 7764 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore, faible odeur aromatique[1] |
| Propriétés chimiques | |
| Formule | C5H7NO2 [Isomères] |
| Masse molaire[2] | 113,114 6 ± 0,005 3 g/mol C 53,09 %, H 6,24 %, N 12,38 %, O 28,29 %, |
| Propriétés physiques | |
| T° fusion | −22 °C[1] |
| T° ébullition | 209 °C[1] |
| Solubilité | 20 g·L-1 (25 °C, eau)[1] |
| Masse volumique | 1,06 g·cm-3 (20 °C)[1] |
| Densité de vapeur | 3,91[1] |
| Densité du mélange air-vapeur | 1,00[1] |
| T° d'auto-inflammation | 460 °C[1] |
| Point d’éclair | 110 °C[1] |
| Pression de vapeur saturante | 0,03 hPa (20 °C) 0,052 hPa (25 °C) 1,33 hPa (67,8 °C)[1] |
| Conductivité électrique | 6,5×10-5 S·m-1[1] |
| Thermochimie | |
| Cp | 220,22 J·K-1·mol-1 (25 °C)[3]. |
| Précautions | |
| SGH[1] | |
| Pas dangereux selon le SGH | |
| Écotoxicologie | |
| DL50 | 2 820 mg·kg-1 (rat, oral)[4] |
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés
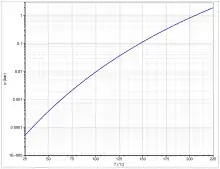
Le cyanoacétate d'éthyle se présente sous la forme liquide incolore qui bout vers 209 °C[1] à pression atmosphérique. Sa pression de vapeur suit l'équation d'Antoine log10(P) = A−(B/(T+C)) (P en bar, T en K) avec A = 7,46724, B = 3693,663 et C = 16,138, dans la gamme de température allant de 67,9 à 205,9 °C[6]. En phase solide, deux formes polymorphes existent[3]. En dessous de −111 °C, la forme cristalline II est dominante[3], au-dessus, c'est la forme I, qui fond vers −22 °C[1]. Sa capacité thermique à 25 °C est de 220,22 J·K−1·mol−1[3].
Le cyanoacétate d'éthyle est combustible mais peu inflammable[1]. Il est peu soluble dans l'eau et est peu à très peu volatil. Il réagit dangereusement avec les acides forts, les bases fortes, les oxydants forts et les réducteurs forts[1].
Réactivité
Le cyanoacétate d'éthyle possède trois centres réactifs différents – nitrile, ester, méthylène acide –, ce qui en fait un matériau de base polyvalent en synthèse pour la préparation d'un grand nombre de substances fonctionnelles et pharmacologiquement actives.
Le pont méthylène, entre la fonction nitrile et le groupe ester, est acide et possède une réactivité similaire à celle des esters de l'acide malonique. Il peut ainsi être utilisé dans des réactions de condensation comme la condensation de Knoevenagel ou l'addition de Michael.
Le groupe nitrile peut lui réagir :
- par hydrogénation, formant la β-alanine, un acide β-aminé ;
- comme cible d'attaque nucléophile sur son carbone, une étape dans la synthèse de nombreux hétérocycles et d'autres produits ;
- comme donneur de cyanure ne présentant pas de danger[7].
Le groupe ester peut lui être la cible d'attaques nucléophiles, dans le cadre d'une substitution d'acyle ; la réaction avec l'ammoniac produit le cyanoacétamide (en) qui peut ensuite être converti par déshydratation avec PCl5 ou POCl3 en malononitrile[8].
Chauffé en présence d'éthanolate de sodium, le cyanoacétate d'éthyle forme un dimère, le 3-amino-2-cyano-2-penténoate de diéthyle[9].
Synthèse
Le cyanoacétate d'éthyle peut être préparé de diverses façons :
- par estérification de l'acide cyanoacétique (en) avec l'éthanol en présence d'un acide minéral fort (par exemple, de l'acide sulfurique concentré). L'acide cyanoacétique peut lui-même être préparé par synthèse de nitrile de Kolbe (en) entre le chloroacétate de sodium (de) et le cyanure de sodium ;
- par synthèse de nitrile de Kolbe entre le chloroacétate d'éthyle (de) et le cyanure de sodium ;
- par réaction entre le cyanoacétate de sodium et le bromoéthane dans un système diphasé aqueux-organique, avec l'aide d'un catalyseur de transfert de phase[10] ;
- par oxydation du 3-éthoxypropionitrile, un éther, par de l'oxygène sous pression, en présence d'acétate de cobalt(II) (en) tétrahydraté comme catalyseur, et de N-hydroxyphtalimide (en) comme générateur de radical[11].
Applications
Le cyanoacétate d'éthyle est un élément de base pour la synthèse d'hétérocycles qui sont utilisés, par exemple, comme médicaments :
- l'allopurinol, utilisé dans le traitement de la goutte chronique, peut être synthétisé en commençant par une condensation de Knoevenagel avec l'orthoformiate de triéthyle ; le produit de condensation est ensuite cyclisé avec l'hydrazine pour donner une pyrazole substituée qui réagit enfin avec le formamide pour donner l'allopurinol[12] ;
- des dérivés de purine comme la théophylline, la caféine ou l'acide urique peuvent être obtenus synthétiquement à partir de cyanoacétate d'éthyle et de N,N'-diméthylurée[13] ;
- l'acide folique, une ptéridine appartenant aux Vitamines B, peut être le produit final d'une synthèse convergente dont le réactifs initiaux sont le cyanoacétate d'éthyle et la guanidine ;
- l'éthosuximide, un pyrrole utilisée pour traiter l'épilepsie, peut être obtenu dans un synthèse multi-étapes à partir du cyanoacétate d'éthyle et de la butanone ;
- le triméthoprime, un dérivé de la pyrimidine, utilisé comme co-trimoxazole en combinaison fixe avec le sulfaméthoxazole comme bactériostatique, peut être synthétisé à partir du cyanoacétate d'éthyle et du 3,4,5-triméthoxybenzaldéhyde (en) ou du chlorure de benzyle.
D'autres hétérocycles peuvent être obtenus avec de bons rendements ä partir du cyanoacétate d'éthyle, par exemple les dérivés 3-substitués de coumarine[14].
Parmi les produits non-cycliques synthétisables à partir du cyanoacétate d'éthyle, on peut citer :
- l'acide valproïque, un antiépileptique ;
- le cyanoacrylate d'éthyle (en), un composant utilisé pour former de la superglue, en réaction avec le formaldéhyde.
Le cyanoacétate d'éthyle est enfin aussi utilisé pour préparer la 3,3-diphénylpropan-1-amine, un précurseur dans la synthèse de la prénylamine (en) et de la droprénilamine.
Notes et références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Cyanessigsäureethylester » (voir la liste des auteurs).
- Entrée « Ethyl cyanoacetate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais) (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Askhakov, B.G., Ismailov, T.S., Khodzhaeva, M.G. et al., « Specific heat of ethyl cyanoacetate », Journal of Engineering Physics, vol. 61, , p. 1117–1119 (DOI 10.1007/BF00872889).
- Harald Strittmatter, Stefan Hildbrand and Peter Pollak "Malonic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2007, Wiley-VCH, Weinheim. DOI 10.1002/14356007.a16_063.pub2
- (de) « Cyanessigsäureester », sur Römpp Online, Georg Thieme Verlag (consulté en )
- D.R. Stull, « Vapor Pressure of Pure Substances Organic Compounds », Ind. Eng. Chem., vol. 39, no 4, , p. 517–540 (DOI 10.1021/ie50448a022)
- Shuyan Zheng, Chunhui Yu et Zhengwu Shen, « Ethyl Cyanoacetate: A New Cyanating Agent for the Palladium-Catalyzed Cyanation of Aryl Halides », Org. Lett., vol. 14, no 14, , p. 3644–3647 (DOI 10.1021/ol3014914)
- Mary Eagleson: Concise encyclopedia chemistry, Walter de Gruyter, Berlin - New York 1994, (ISBN 3-11-011451-8).
- V. A. Dorokhov, S. V. Baranin, A. Dib et V. S. Bogdanov, « 'Codimers' of N-(pyrid-2-yl) amides and ethyl cyanoacetate », Russ. Chem. Bulletin, vol. 41, no 2, , p. 287–291 (DOI 10.1007/bf00869516)
- EP application 1028105, Hanselmann, Paul & Hildebrand, Stefan, "Process for the preparation of cyanoacetic esters", published 2000-08-16, assigned to Lonza AG
- EP patent 1208081, Hanselmann, Paul & Hildebrand, Stefan, "Method for producing cyanoacetic acid esters", issued 2004-04-14, assigned to Lonza AG
- (de) Axel Kleemann, Jürgen Engel, Pharmazeutische Wirkstoffe, Stuttgart - New York, Georg Thieme, , 2e, éd. (ISBN 3-13-558402-X).
- Beyer-Walter: "Lehrbuch der Organischen Chemie", 24. Aufl., S. Hirzel, Stuttgart - Leipzig 2004.
- A. A. Avetisyan, É. V. Vanyan et M. T. Dangyan, « Synthesis of functionally substituted coumarins », Chem. Heterocycl. Compounds, vol. 15, no 9, , p. 959–960 (DOI 10.1007/BF00473834)