Allopurinol
L'allopurinol est un médicament hypo-uricémiant, faisant baisser l'uricémie (concentration sérique en acide urique) et soignant la goutte mis au point par Gertrude Elion et son équipe en 1960 et administré la première fois en 1963 .
| Allopurinol | |
| |
| Identification | |
|---|---|
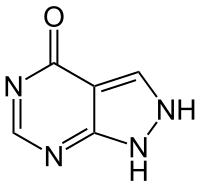
| Nom UICPA | 1,2-dihydro-4H-pyrazolo[3,4-d]pyrimidin-4-one |
| No CAS | |
| No ECHA | 100.005.684 |
| No CE | 206-250-9 |
| Code ATC | M04 |
| DrugBank | APRD00435 |
| PubChem | 2094 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H4N4O [Isomères] |
| Masse molaire[1] | 136,111 5 ± 0,005 4 g/mol C 44,12 %, H 2,96 %, N 41,16 %, O 11,75 %, |
| Propriétés physiques | |
| T° ébullition | 350 °C |
| Solubilité | 569 mg·L-1 (eau, 25 °C) |
| Précautions | |
| Directive 67/548/EEC | |
| Données pharmacocinétiques | |
| Biodisponibilité | 78±20 % |
| Liaison protéique | négligeable |
| Métabolisme | hépatique (80 % oxypurinol , 10 % allopurinol ribosides) |
| Demi-vie d’élim. | 2h (18-30h pour l'oxypurinol) |
| Unités du SI et CNTP, sauf indication contraire. | |
Mode d'action
Il diminue le taux d'acide urique et le volume des tophus. En effet, ce médicament est un inhibiteur de l'action d'une enzyme, la xanthine oxydase, qui intervient dans le métabolisme de l'acide urique. Il baisse le taux de récidive de crise articulaire de la goutte. Son administration se fait conjointement avec la colchicine pendant plusieurs mois à des doses progressivement croissantes de 100 jusqu'à 300 mg. Il n'a aucune action sur la crise goutteuse, une fois celle-ci déclenchée.
Il diminue également la consommation d'oxygène du muscle cardiaque[2], et par ce biais, retarde ou diminue les symptômes de l'angine de poitrine[3]. À fortes doses (600 mg/j), il permet une régression modérée de la masse du ventricule gauche en cas de cardiomyopathie hypertrophique et ischémique[4]. La raison en reste inconnue mais peut faire intervenir une diminution du stress oxydatif du tissu vasculaire[5] ainsi qu'une amélioration de la fonction endothéliale des vaisseaux[6].
Effets indésirables
- Les effets indésirables les plus graves sont le syndrome de Lyell et le syndrome de Stevens-Johnson (deux types de toxidermies à risque létal). L'allopurinol est connu en Europe pour être un des plus gros pourvoyeurs de victimes de ces syndromes[7]. Il peut également provoquer un syndrome d'hypersensibilité médicamenteuse (ou « DRESS syndrome »)[8]. Son association avec l'amoxicilline augmenterait la fréquence des éruptions cutanées. Le risque est également plus élevé en cas d'utilisation concomitante de diurétiques, la présence d'une insuffisance rénale[9] ou d'une maladie cardiaque[10]. Une association de ces réactions d'hypersensibilité avec la présence de l'allèle HLA-B*5801 a été retrouvé[11], mais il n'est pas recommandé en pratique de le rechercher à l'introduction du médicament[12]. Cet allèle est plus fréquent chez les asiatiques[9].
- Autres allergies et réactions de sensibilité
- Cytolyse hépatique
- Lésions tubulaires rénales, par précipitation intra-tubulaire avec formation de cristaux
- L'allopurinol peut aussi précipiter une crise de goutte s'il est utilisé trop tôt après la fin d'une crise, ou s'il n'est pas combiné à la colchicine en début de traitement. Toutefois, à long terme et en monothérapie, il diminue le nombre de crises de gouttes[13].
Métabolisme
L'allopurinol est transformé dans l'organisme en oxypurinol qui est un métabolite actif[14].
La voie d'excrétion est essentiellement rénale : la posologie doit donc être particulièrement adaptée à la clairance de la créatinine afin de limiter son accumulation et celle de l’oxypurinol, et ainsi prévenir la survenue d’un effet indésirable rare mais très grave, le syndrome d’hypersensibilité à l’allopurinol[15]. Le côté risque dépendant du dosage reste cependant discuté[9].
Divers
L'allopurinol fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[16].
Selon une étude chinoise publiée en 2015, chez le rat de laboratoire, il semble pouvoir réduire ses séquelles neurologiques d'une intoxication au monoxyde de carbone[17].
Lien externe
- Compendium suisse des médicaments : spécialités contenant Allopurinol
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en)Ekelund UE, Harrison RW, Shokek O et al. « Intravenous allopurinol decreases myocardial oxygen consumption and increases mechanical efficiency in dogs with pacing-induced heart failure » Circ Res. 1999;85:437-445
- (en)Noman A, Ang DS, Ogston S, Lang CC, Struthers AD, « Effect of high-dose allopurinol on exercise in patients with chronic stable angina: a randomised, placebo controlled crossover trial » Lancet 2010;375:2161-2167
- Rekhraj S, Gandy TJ, Szwejkowski BR et al. High-dose allopurinol reduces left ventricular mass in patients with ischemic heart disease, J Am Coll Cardiol, 2013;61:926-932
- Rajendra NS, Ireland S, George J, Belch JJ, Lang CC, Struthers AD, Mechanistic insights into the therapeutic use of high-dose allopurinol in angina pectoris, J Am Coll Cardiol, 2011;58:820-828
- George J, Carr E, Davies J, Belch JJ, Struthers A, High-dose allopurinol improves endothelial function by profoundly reducing vascular oxidative stress and not by lowering uric acid, Circulation, 2006;114:2508-2516
- Halevy S, Ghislain PD, Mockenhaupt M et al. Allopurinol is the most common cause of Stevens-Johnson syndrome and toxic epidermal necrolysis in Europe and Israel, J Am Acad Dermatol, 2008;58:25-32
- Yaylacı S, Demir MV, Temiz T, Tamer A, Uslan MI, Allopurinol-induced DRESS syndrome, Indian J Pharmacol. 2012;44:412-414
- Ramasamy SN, Korb-Wells CS, Kannangara DR et al. Allopurinol hypersensitivity: a systematic review of all published cases, 1950-2012, Drug Saf, 2013;36:953-980
- Yang CY, Chen CH, Deng ST, Allopurinol use and risk of fatal hypersensitivity reactions, a nationwide population-based study in Taiwan, JAMA Intern Med, 2015;175:1550-1557
- (en)Somkrua R, Eickman EE, Saokaew S, Lohitnavy M, Chaiyakunapruk N. « Association of HLA-B*5801 allele and allopurinol-induced Stevens Johnson syndrome and toxic epidermal necrolysis: a systematic review and meta-analysis » BMC Med Genet. 2011 Sep 9;12:118
- D'après l'Agence Européenne du Médicament, « PhVWP monthly report on safety concerns, guidelines and general matters » juillet 2012 - Issue number 1207
- Association des pharmaciens du Canada. Allopurinol. E-CPS [En ligne] Consulté le 6 décembre 2010.
- Pacher P, Nivorozhkin A, Szabó C, Therapeutic effects of xanthine oxidase inhibitors: renaissance half a century after the discovery of allopurinol, Pharmacol Rev, 2006;58:87-114
- [PDF]Fiche Adenuric-CT-6315, HAS (France), juin 2009 (consultée le 6 février 2013)
- WHO Model List of Essential Medicines, 18th list, avril 2013
- Dong, G., Ren, M., Wang, X., Jiang, H., Yin, X., Wang, S., ... & Feng, H. (2015). Allopurinol reduces severity of delayed neurologic sequelae in experimental carbon monoxide toxicity in rats. Neurotoxicology, 48, 171-179.
| Allopurinol | |
| Informations générales | |
|---|---|
| Princeps | 1- Formes mono Allopur (Suisse),
Alpuric (Belgique), |
| Classe | Hypouricémiant |
| Identification | |
| No CAS | |
| No ECHA | 100.005.684 |
| Code ATC | M04AA01 |
| DrugBank | 00437 |