Développement des mycètes
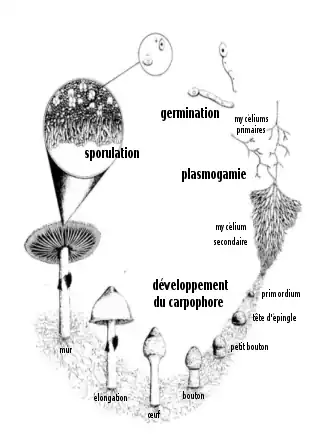
Le développement des mycètes est caractérisé chez les fonges (plus communément appelés champignons), par divers processus : la sporulation, la germination des spores, la croissance de l'appareil végétatif (mycélium composé d'hyphes), les associations symbiotiques (lichens, mycorhizes) et la reproduction par voie asexuée ou sexuée en différenciant un appareil reproducteur, le sporophore.
Appareil végétatif

Hyphes
L’appareil végétatif des mycètes constitue d’un assemblage extensif d’hyphes. Ce sont des microfilaments cylindriques ramifiés et organisés en réseau appelé mycélium. Il existe deux types de microfilaments : filaments non-cloisonnés ou cœnocytiques, et les filaments cloisonnés ou septés. Les hyphes coenocytiques sont plurinucléés et sont retrouvés chez les champignons primitifs. Dans les hyphes septés, les cellules sont séparées par des cloisons appelés septum. Durant la croissance, les septa sont pourvus de pores permettant la continuité du cytoplasme à travers le mycélium ; ce sont des septa primaires. Grâce à ces pores, le passage des petites organites d’un compartiment à l’autre est possible[2]. Dans les hyphes âgés, les cloisons sont dépourvues de pores et servent de délimitation entre les parties vivantes (extrémités) et les parties mortes (centre) du mycélium. Les hyphes septés sont généralement retrouvés chez les champignons évolués.
Le mycélium fongique constitue un réseau invasif qui explore et colonise le milieu souterrain à l'aide de ses hyphes[3]. Les hyphes sont délimités par une paroi cellulaire comme chez une cellule végétale. La paroi est plus mince à l’apex de l'hyphe convenant au site d’élongation des filaments. Cette partie terminale est caractérisée par une concentration importante de vésicules et de filaments d’actine. Ces derniers sont les composants essentiels dans la croissance du mycélium. La fonction principale des filaments d'actine est le transport des vésicules à l'intérieur de la cellule. Les vésicules sont dirigées vers la partie apicale de l'hyphe et libèrent par l'exocytose, les matériaux utilisés dans la synthèse de la nouvelle paroi[3]. Les microtubules du cytosquelette et les filaments d'actine contribuent très peu au renforcement structural de la cellule. Griffin et al. (1974) a démontré que chez les champignons à thalle filamenteux, la ramification du mycélium est équivalent à la division cellulaire chez les animaux, plantes et protistes[2]. Ainsi, l’élongation des hyphes peut être interprétée comme cycle de développement d’une cellule.
Chez le champignon mycorhyzien (symbiose entre champignon et la racine d'une plante) Gigaspora margarita, la croissance du mycélium est sous influence directe des métabolites phénoliques relâchés par la plante. Les flavonoïdes tels que le quercétine, le myricétine et le kaempférol stimulent l’élongation des hyphes. Parmi ces flavonoïdes, l'effet stimulant de la quercétine est suffisant pour augmenter le taux de croissance des hyphes et prolonger la période de croissance. De plus, si ce facteur est combiné avec le dioxyde de carbone (CO2), cette croissance sera amplifiée davantage (effet synergique)[4]. Le CO2 constitue, par ailleurs, une source essentielle de carbone dans l’élongation des hyphes lorsque le catabolisme de lipides est impliqué.

Les cellules des hyphes possèdent dans leurs vacuoles des tanins qui sont libérés lors d'une lésion des champignons. Certains se spécialisent en laticifères qui accumulent du latex sous pression et qui peut être libéré à la cassure de la chair ou des lames (latex immuable ou non qui contient des sesquiterpènes). Les tanins en s'oxydant forment une couche de protection freinant le stress oxydant et la contamination par la constitution de complexes tanins-protéines faisant office de barrière. Les sesquiterpènes ont également un rôle protecteur en s'oxydant et constituent des molécules toxiques de défense[5] - [6].
Paroi cellulaire
Contrairement à la paroi cellulaire des plantes qui est composée principalement de cellulose, la paroi fongique est constituée plutôt par la chitine (sauf celle des zygomycètes qui est composée de cellulose).
La paroi cellulaire constitue non seulement la limite des hyphes, mais elle a un rôle important dans l’interaction entre les mycètes et son environnement. « La paroi est une structure dynamique adaptée aux changements constants, par exemple, durant l’expansion cellulaire et la division en levures, la germination de la spore, la croissance des hyphes et la formation de septum dans les champignons filamenteux »[7]. Divers enzymes hydrolytiques comme les chitinases et les glucanases sont étroitement liés à la paroi cellulaire des mycètes. Leurs activités enzymatiques contribuent aux remodelages de la paroi durant la croissance et la morphogénèse[7]. D’autres enzymes hydrolytiques sont impliquées dans la nutrition du champignon. Les matières organiques environnantes qui constituent principale source alimentaire des mycètes, sont dégradées par les enzymes de la champignon puis sont absorbées par celle-ci à travers sa paroi. Plus les hyphes sont allongés, plus le mycélium est étendu, plus l’organisme absorbe le plus de nutriments.
La paroi est une structure à plusieurs couches et sa composition varie en fonction des différentes espèces de champignons et des conditions environnementales. La chitine et les β-glucanes sont des polysaccharides qui forment la structure de base de la paroi fongique[2]. La chitine (polymère de β1-4 N-acétylglucosamine) est synthétisée par une chitine synthase ou synthétase. Cette molécule est retrouvée en abondance dans l'exosquelette des insectes qui n'est pas présent chez les mycètes. « La forme et l’intégrité des champignons dépendent des propriétés mécaniques de la paroi cellulaire »[7]. D’autres composants de la paroi fongique sont les mannoprotéines, les glycoprotéines, la mélanine et les sporopollénines.
La mélanine est un pigment brun foncé, formée par la polymérisation oxydative des composants phénoliques. Sa production peut être induite par la limitation de glucose dans l’environnement puis elles sont synthétisées durant la sporulation. Déposée dans la paroi fongique[8], elle assume un rôle de résistance contre les enzymes et forces mécaniques provenant des autres organismes (ex : animaux). Un autre rôle est la protection contre les radiations solaires et la déshydratation. Pour les mycètes pathogènes, la mélanine a un effect important sur la virulence. Sa biosynthèse est associée à la formation des appressoria, qui sont indispensables dans la pénétration des cellules d’hôte durant une infection[8].
La paroi cellulaire est organisée de manière suivante :
- un réseau de microfibrilles de chitine est localisé dans la partie la plus interne de la paroi, directement en contact avec la membrane plasmique ;
- des fillaments de β-glucanes s’installent par-dessus la couche de chitine ;
- des polysaccharides amorphes (sous forme de gel) font la liaison entre les microfibrilles renforçant la structure ;
- la couche la plus externe est composée de mannoprotéines constituant une matrice autour de la paroi. Des glycoprotéines ancrées dans cette couche, jouent un rôle dans l'interaction entre les cellules.
Organites
Les organites de la cellule fongique (ex: appareil de Golgi, reticulum endoplasmique, mitochondries, etc.) exercent les mêmes fonctions que les organites de n'importe quelle cellule des eucaryotes. Par contre, le noyau des mycètes est considérablement plus petit que celui des plantes et des animaux puisque leur génome est très petit[2].
Stades de développement
Sporulation
Le mycète est un organisme sessile dans la nature. Comme tout autre organisme, la continuité de son existence dépend de la reproduction. Chez les champignons, la reproduction se fait par la sporulation qui consiste une production de spores rigide et résistante[9].
La sporulation facilite la dispersion des champignons dans l’environnement, soit par le vent, par l’eau ou par les animaux[10]. En d’autres termes, la sporulation contribue à la colonisation de nouvelles niches écologiques. Les spores matures sont caractérisées par une paroi épaisse et par une réserve abondante en lipide, car elle représente la source d’énergie exclusive durant la germination d'une spore » [4]. Les spores servent aussi dans la préservation de la croissance lorsque les conditions environnementales sont défavorables: température élevée, dessiccation, radiation, pH extrême et produits toxiques. Dans ce cas, les spores sont métaboliquement dormantes[10] et attendent à ce que les conditions environnementales et nutritives redeviennent favorables pour procéder à la germination et à la croissance cellulaire par élongation des hyphes.
La sporulation fongique est un processus complexe qui correspond à une différenciation des cellules reproductives et de leurs structures de support provenant des cellules somatiques. Cette différenciation peut être impliquée au niveau morphologique, physiologie et biochimique. En d'autres termes, la sporulation comprend des changements de l’apparence, de la fonction et de la composition chimique des cellules[2]. Le développement de spores est sous l'influence de divers facteurs comme la lumière, l’humidité, l’aération, le pH, les dommages à la culture, le type et la composition des nutriments environnants. Le mécanisme qui induit la sporulation est encore mal connu. En général, elle est déclenchée quand le taux de croissance des hyphes diminue[11].
Germination
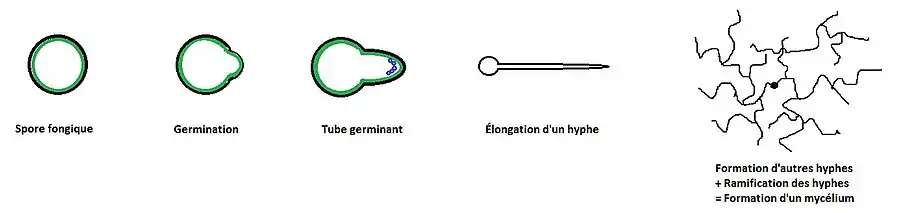
La germination est caractérisée par l'émergence d'un tube germinant à partir de la spore fongique. Une spore qui est métaboliquement dormante, est protégée par une paroi épaisse et rigide due à la réduction du contenu d'eau. La germination des spores dépend largement aux conditions environnementales car la présence d'eau ou l'augmentation de l'humidité est suffisante pour déclencher l'hydratation de ces spores. L'hydratation requiert un changement dans la perméabilité de la paroi pour hydrater davantage les spores afin de ré-initier les activités métaboliques de ses cellules. Le développement du tube germinant dépend aussi de la disponibilité des nutriments dans l'environnement, autrement dit une réserve exogène qui est constituée principalement d'acides aminés, de sucres et de nucléosides. Similaire à la croissance des hyphes, de nombreuses vésicules sont concentrées près de la membrane plasmique pour livrer les matériaux essentiels à la paroi en formation. Ces vésicules s'organisent de manière à former une zone en forme de croissant (Complexe Apical des vésicules) dans la partie terminale du tube germinant au fur et à mesure de son développement. Le point d'émergence du tube peut être prédéterminé à une région où la paroi est amincie, ou il peut être situé n'importe où sur la spore.
La germination des spores est un événement critique dans le développement des champignons phytopathogènes. « Une germination dans le bon temps et lieu est primordiale pour la réussite d’une infection »[12].
De ce tube germinatif se développe un réseau constitué d'hyphes qui se ramifient et s'agglomèrent, formant un mycélium dit « primaire » (car directement issu de la germination)[13].
Plasmogamie
La reproduction sexuée est initiée par le contact de deux hyphes compatibles de polarités complémentaires (issus de deux mycéliums primaires, généralement de polarités + et –)[14] dont la rencontre donne lieu à une plasmogamie (processus de fusion de la membrane plasmique, du cytoplasme et de son contenu — sauf les noyaux — de deux cellules compatibles), ce qui mène à la formation d'une cellule à deux noyaux haploïdes (n+n) appelée dicaryon et d'hyphes dicaryotiques[15].
Une plasmogamie à partir de deux hyphes issus de la même spore donne un mycélium homothallique. Une plasmogamie de deux hyphes issus de deux spores de sexe compatible donne un mycélium hétérothallique. Lorsque les hyphes de deux individus non compatibles se fusionnent, le mycélium est non-viable.
Chez les Basidiomycètes, la phase dycaryotique est bien plus prolongée que chez les Ascomycètes. Permettant le masquage de l'expression de mutations délétères (provenant d'une exposition aux UV) par complémentation génétique et la réparation des cassures doubles-brins de l'ADN, cette phase prolongée aurait pu favoriser l'accroissement de la taille du génome, et donc du contenu en information, associé à de meilleures adaptation à leur environnement[16] - [17].
Caryogamie
La caryogamie est la fusion des noyaux haploïdes du mycélium dicaryotique provenant de la plasmogamie. L'union des noyaux forme une cellule diploïde (2n) qui correspond à un zygote ou zygospore.
Développement du carpophore
.jpg.webp)
« Les champignons poussent dans les endroits humides. C'est pourquoi ils ont la forme d'un parapluie »
L'anastomose des deux mycéliums primaires issus de deux spores génétiquement différentes, conduit à la formation d'un mycélium secondaire fertile. Celui-ci se différencie en un primordium[19], futur carpophore qui n'est autre que cette partie émergée de l'iceberg biologique que nous nommons habituellement champignon. En effet, à l'instar du volume du système racinaire presqu'équivalent au volume du houppier d'un arbre, le volume moyen du réseau mycélien sous le carpophore (quelques dizaines de cm3, voire de dm3) se rapproche de celui du sporophore[20]. Sans compter les hyphes extra-radiculaires mycorhiziens dont la croissance peut atteindre plusieurs mètres par cm3 de sol[21]. Si la croissance des hyphes, de 2 à 6 mm par jour selon les espèces, n'est pas stoppée (stress environnementaux, sénescence), le développment mycélien peut atteindre des records : les corps fructifères d'une armillaire sombre qui appartiennent à un seul et même individu, envoient leurs filaments à travers toute la Forêt nationale de Malheur dans l'est de l'Oregon aux États-Unis, s'étendant sur 9,6 km2 de superficie[22] - [23].
Les mycologues distinguent conventionnellement six stades de développement du carpophore, nommés : tête d'épingle, petit bouton, bouton, œuf, élongation et mûr. Un dénombrement de sporocarpes permet d'apprécier l'importance des groupements que forment entre eux les carpophores d'un même mycélium : isolé, alignés formant des veines qui suivent les racines sous-jacentes, touffes, troupes, ronds de sorcières[24].
L'érection spectaculaire du carpophore pouvant prendre de un à quelques semaines, est dû à une cinétique de croissance exponentielle qui donne l'impression que les champignons surgissent apparemment de nulle part du jour au lendemain et disparaissent presque aussi vite. Cette croissance peut paraître étrange mais s'explique par leur stratégie de reproduction : l'organogenèse du sporophore met en évidence la croissance hypogée des hyphes mycéliens, de manière invisible, avant de s'agglomérer en un faux tissu, le plectenchyme et produire, en réponse à un géotropisme négatif et à un phototropisme positif[25], un sporophore éphémère (les hyphes du pied sont globalement parallèles, tandis que les hyphes de la trame du chapeau sont entrelacées) qui disparaît rapidement en se décomposant[26]. Cette croissance et l'irrégularité des poussées annuelles qui ne suivent exactement ni les variations de la pluviosité, ni les changements de l'état hygrométrique du milieu, est à l'origine de nombreuses expressions populaires (« pousser comme un champignon », « appuyer sur le champignon », ville champignon, « cèpe vu [par l'homme] ne pousse plus »)[27], de la fascination pour les champignons géants, et contribue à la diffusion de légendes fongiques associées dans les cultures mycophobes aux sorcières et démons à la réputation toute aussi sinistre[28] (les Phallus dont la croissance commence sous la forme d'un œuf hypogé et qui évoquent des sexes masculins étant considérés comme des cornes ou des œufs du Diable associés à la mort)[29], d'où les appellations populaires et noms vernaculaires (bolet Satan, trompette de la mort, satyre puant, cœur de sorcière, pieuvre des bois, rond de sorcières, balais de sorcière) qui révèlent à la fois la sûreté du regard et une imagination débridée qui se manifeste par la traduction de traits comparatifs, rapportés à des êtres maléfiques[30].
Méiose ou mitose
Le processus de la méiose et de la mitose se déroule de manière universelle chez les eucaryotes.
Dans la reproduction sexuée, la méiose a plus d'importance que la mitose car elle conduit la recombinaison génétique des cellules.
Dans la reproduction asexuée, les mycètes se reproduisent plutôt par la mitose.
Mode de reproduction

La reproduction est un moyen employé pour augmenter la variabilité génétique des espèces. Face aux changements environnementaux, les espèces avec la plus grande variabilité génétique possèdent la meilleure chance de survie.
Les mycètes ont la capacité de se reproduire soit d’une façon asexuée (mycète anamorphe) ou sexuée (mycète téléomorphe). Les champignons qui comprennent ces deux types de reproduction sont des mycètes holomorphes. Durant la phase asexuée, les spores sont appelées mitospores car elles sont produites par la mitose. Les spores formées via la reproduction sexuée sont nommées méiospores. Généralement, la reproduction asexuée est privilégiée car c’est plus rapide et énergétiquement moins coûteux.
Cycle de vie sexué
Au cours du développement, la ploïdie (le nombre de chromosomes) cellulaire est variable en fonction de différents processus et à différents moments du cycle de vie. La cellule passe d’un état diploïde à un état haploïde par la méiose. La transition de l’état haploïde à l’état diploïde se fait via la fécondation.
Haploïde (haplobiontique A)
Le terme haplobiontique signifie une génération. La phase haploïde est prédominante dans ce cycle de vie. La méiose se produit rapidement après la caryogamie (=fécondation qui donne un zygote diploïde). Le noyau suit la séquence : caryogamie → méiose → mitose. Ce cycle de vie est retrouvé chez les champignons inférieurs et certains ascomycètes[31].
Diploïde (haplobiontique B)
Dans ce cycle, le noyau suit la séquence : caryogamie → mitose → méiose. La phase mitotique diploïde est prolongée en comparaison avec la phase haploïde qui est limitée aux gamètes. La majorité des oomycètes possèdent ce type de cycle de vie[31].
Diploïde modifié (diploïde dicaryotique)
À la suite d'une plasmogamie, le mycélium est caractérisé par la présence de deux noyaux haploïdes (n+n) qui n'ont pas encore fusionné. Cette modification dans le cycle diploïde est retrouvée chez la majorité des basidiomycètes et les ascomycètes supérieurs[31].
Haploïde-diploïde (diplobiontique)
Le terme diplobiontique signifie deux générations. Il y a une alternance entre la génération haploïde et la génération diploïde. Le noyau suit la séquence : caryogamie → mitose → méiose → mitose. Ce cycle de vie n'est pas commun chez les mycètes. Uniquement, quelques espèces des chytridiomycètes et allomycètes suivent cette séquence de vie[31].
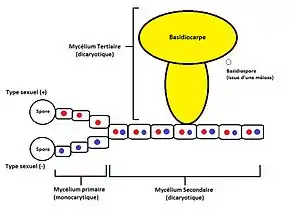
Exemple de reproduction sexuée des basidiomycètes
À la suite de la germination, les hyphes filamenteux passent brièvement à travers la phase haploïde (monocaryon). Cette période correspond au mycélium primaire. Lorsque deux mycéliums primaires et compatibles se rencontrent, leurs cellules se fusionnent (plasmogamie). Le mycélium secondaire est dit dycaryotique car chaque compartiment contient maintenant deux noyaux. Chez les basidiomycètes, le septum est caractérisé par un dolipore, pourvu de parenthèsomes, qui permet le déplacement et l'échange des éléments entre les compartiments (à l'exception des organites de grande taille)[2]. La division nucléaire se déroule simultanément dans les filaments qui s'allongent au fur et à mesure. Le mycélium secondaire est muni de boucles mycéliennes, une structure en forme de tube qui transporte les noyaux filles vers le compartiment adjacent[2]. Le mycélium tertiaire, toujours dicaryotique, se développe par-dessus le mycélium secondaire puis se spécialise en sporophore (pied et chapeau) via la fructification. Le sporophore appelé basidiocarpe contient des basides dicaryotiques. Après l’union des noyaux à l'intérieur des basides (caryogamie), l'organisme possède maintenant des noyaux diploïdes. Les cellules finiront par deux séquences méiotiques, résultant en quatre noyaux haploïdes qui vont migrer à l’extérieur des basides. Ces noyaux correspondent aux méiosores appelés basidiospores.
Transduction de signal dans le développement fongique
Le développement des mycètes est modulé par deux principales cascades de la transduction de signal, les MAP kinases et l’AMPc[32]. Ces cascades modulent l’interaction entre les signaux provenant de l’environnement et le fonctionnement cellulaire qui contrôle la croissance et la différenciation des cellules[32]. L'AMPc (adénosine 3’5’monophsphate cyclique) est un messager secondaire pour de nombreuses hormones et neurotransmetteurs, jouant des rôles fondamentaux dans la réponse cellulaire. Les MAP kinases (kinases activées par les mitogènes) sont impliquées dans plusieurs processus tels que la prolifération cellulaire, la réplication de l’ADN et la mitose des cellules[33]. Les cascades MAP kinases sont activées en réponse des phéromones et des nutriments disponibles dans le milieu. Chez les cellules haploïdes comme Saccharomyces cerevisiae, la voie MAP kinase régule la reproduction en réponse à des phéromones. Cette même voie de signalisation est utilisée chez les cellules diploïdes pour signaler la croissance des hyphes en réponse à des limitations d’azote et d’autres signaux environnementaux[8]. De ce fait, les composants impliqués dans la voie de signalisation de l'AMPc sont très conservé chez les mycètes, bien que les processus régulés par celle-ci sont autant diversifiés que les champignons[32].
Cryptococcus neoformans est un basidiomycète encapsulé de type levure. Le rôle de la voie de l’AMPc est la régulation de la reproduction et la virulence de ce pathogène. En absence de partenaire de reproduction, et dans les conditions de dessiccation et limitation d’azote, certaines souches peuvent former des hyphes puis procéder à la sporulation[32].
Schizosaccharomyces pombe (levure à fission) fait partie du phylum des ascomycètes de type levure. La germination de ses spores peut être induite par le glucose. Ainsi la voie de signalisaiton de l'AMPc et les cascades MAP kinases régulent de manière coordonnée, le développement sexuel, la gluconéogenèse et la tolérance de stress de l’organisme[32].
Références
- Dans les méristèmes des plantes à graines, elles sont aussi tangentielles. Ces divisions tangentielles et longitudinales sont à l'origine de tissus qui proviennent de la différenciation et de la spécialisation des cellules produites par les méristèmes, ce qui les distingue des autres plantes vasculaires et des thallophytes.
- (en) David H. Griffin, Fungal Physiology, New York, Wiley-Liss, , 337 p.
- (en) David Moore, Fungal Morphogenesis, Angleterre, Cambridge University Press, , 469 p.
- (en) G. Bécard, D. D. Douds et P. E. Pfeffer, « Extensive In Vitro Hyphal Growth of Vesicular-Arbuscular Mycorrhizal Fungi in the Presence of CO2 and Flavonols », Applied and Environmental Microbiology, vol. 58, , p. 821–825 (ISSN 0099-2240 et 1098-5336, PMID 16348673, PMCID 195340, lire en ligne, consulté le ).
- (en) Robert Nawrot, « Defense-related Proteins from Chelidonium majus L. as Important Components of its Latex », Current Protein & Peptide Science, vol. 18, no 8, , p. 864-880 (DOI 10.2174/1389203718666170406124013)
- (en) Henning Knudsen, Jan Vesterholt, Funga Nordica : agaricoid, boletoid and cyphelloid genera, Nordsvamp, , p. 8.
- David J. Adams, « Fungal cell wall chitinases and glucanases », Microbiology, vol. 150, , p. 2029–2035 (DOI 10.1099/mic.0.26980-0, lire en ligne, consulté le ).
- (en) Ana M. Calvo, Richard A. Wilson, Jin Woo Bok et Nancy P. Keller, « Relationship between Secondary Metabolism and Fungal Development », Microbiology and Molecular Biology Reviews, vol. 66, , p. 447–459 (ISSN 1092-2172 et 1098-5557, PMID 12208999, PMCID 120793, DOI 10.1128/MMBR.66.3.447-459.2002, lire en ligne, consulté le ).
- (en) [vidéo] New Atlantis WILD, Pluie de spores sur YouTube (consulté le )
- (en) Elizabeth Moore-Landecker, ELS, John Wiley & Sons, Ltd, , 14288 p. (ISBN 978-0-470-01590-2, DOI 10.1002/9780470015902.a0000378.pub2, lire en ligne).
- K R Dahlberg et and J. L. V. Etten, « Physiology and Biochemistry of Fungal Sporulation », Annual Review of Phytopathology, vol. 20, , p. 281–301 (DOI 10.1146/annurev.py.20.090182.001433, lire en ligne, consulté le ).
- Kye-Yong Seong, Xinhua Zhao, Jin-Rong Xu et Ulrich Güldener, « Conidial germination in the filamentous fungus Fusarium graminearum », Fungal Genetics and Biology, vol. 45, , p. 389–399 (DOI 10.1016/j.fgb.2007.09.002, lire en ligne, consulté le ).
- Guillaume Eyssartier, Les 50 règles d'or du cueilleur de champignons, Larousse, (lire en ligne), p. 11
- Schizophyllum commune a un record de 23 328 types de compatibilité sexuelle (en).
- Peter H Raven, Kenneth A Mason, Jonathan B Losos, Tod Duncan, Biologie, De Boeck Superieur, , p. 653
- (en) R M Wallen et Michael H Perlin, « An Overview of the Function and Maintenance of Sexual Reproduction in Dikaryotic Fungi », Front Microbiol, vol. 9, no 53, , p. 537–549 (DOI 10.3389/fmicb.2018.00503).
- (en) R.E. Michod et T.W. Gayley, « Masking of mutations and the evolution of sex », The American Naturalist, vol. 139, no 4, , p. 706–734 (DOI 10.1086/285354).
- Gérard Manachère, « Morphogenèse des carpophores de Basidiomycètes supérieurs, connaissances actuelles », Revue de Mycologie, no 42, , p. 191-252.
- Petit corpuscule sphérique se formant sur les cordons mycéliens. Il constitue l'« embryon » d'un futur carpophore. Cf Jacques Delmas, op. cit., p. 848
- (en) Stellan Sunhede, Geastraceae (Basidiomycotina): Morphology, Ecology and Systematics, with Special Emphasis on the North European Species, Fungiflora, , p. 43
- (en) Karl Ritz, The Architecture and Biology of Soils: Life in Inner Space, CABI, , p. 150
- (en) « Largest Living Organism: Fungus », sur extremescience.com.
- (en) Richard Webb, « Magic mushrooms: The hidden power of fungi », New Scientist, vol. 220, no 2946, , p. 39 (DOI 10.1016/S0262-4079(13)62855-9).
- Jacques Delmas, Les champignons et leur culture, Flammarion, , p. 146
- (en) R.E. Kendrick, G.H.M. Kronenberg, Photomorphogenesis in Plants, Springer Science & Business Media, , p. 763.
- Jean Béguino, « « Pousser comme un Champignon », ou comment s'élabore le carpophore chez les Basidiomycètes », Revue Scientifique Bourgogne-nature, no 15, , p. 85-95 (lire en ligne).
- Jean-Paul Maurice, François le Tacon, L'odyssée des champignons, Quæ, (lire en ligne), p. 9.
- (en) Frank M. Dugan, « Fungi, folkways and fairytales: Mushrooms and mildews in stories, remedies, and rituals, from Oberon to the Internet », North American Fungi, vol. 3, no 7, , p. 23-72 (DOI 10.2509/naf2008.003.0074)
- (en) Nicholas P. Money, Mushrooms: A Natural and Cultural History, Reaktion Books, (lire en ligne), p. 17
- (en) Walter Philip Kennedy Findlay, Fungi: Folklore, Fiction, & Fact, Mad River Press, , p. 6-25.
- (en) P.D. Sharma, Fungi and Allied Organisms, Oxford, Alpha Science International Ltd., , 545 p., p. 137-138.
- (en) Cletus A. D'Souza et Joseph Heitman, « Conserved cAMP signaling cascades regulate fungal development and virulence », FEMS Microbiology Reviews, vol. 25, , p. 349–364 (ISSN 1574-6976, PMID 11348689, DOI 10.1111/j.1574-6976.2001.tb00582.x, lire en ligne, consulté le ).
- Jacques Robert, Signalisation Cellulaire et Cancer : Un Manuel Pour Les Étudiants et Les Oncologues., Paris, Springer, , 335 p. (ISBN 978-2-8178-0027-1), p. 44.