Amitraze
L'amitraze est une substance active de produit phytosanitaire (ou produit phytopharmaceutique, ou pesticide), qui présente un effet antiparasitaire (insecticide et acaricide), et qui appartient à la famille chimique des formamidines.
| Amitraze | |
| |
| Identification | |
|---|---|
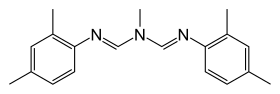
| Nom UICPA | N'-(2,4-diméthylphényl)-N-[(2,4-diméthylphényl)iminométhyl]-N-méthylméthanimidamide |
| No CAS | |
| No ECHA | 100.046.691 |
| No CE | 251-375-4 |
| No RTECS | ZF0480000 |
| Code ATC | « QP53AD01 » |
| PubChem | 36324 |
| ChEBI | 2665 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores[1] |
| Propriétés chimiques | |
| Formule | C19H23N3 [Isomères] |
| Masse molaire[2] | 293,406 ± 0,017 4 g/mol C 77,78 %, H 7,9 %, N 14,32 %, |
| Propriétés physiques | |
| T° fusion | 86 °C[1] |
| Solubilité | dans l'eau : nulle[1] |
| Masse volumique | 1,1 g·cm-3[1] |
| Pression de vapeur saturante | à 20 °C : très basse[1] |
| Précautions | |
| SGH[3] | |
   Attention |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Il est très utilisé dans le monde sur des animaux à sang chaud. Il est aussi parfois utilisé chez des animaux à sang froid comme chez l'abeille domestique dans les ruches par les apiculteurs pour protéger contre le varroa[4], ce qui explique qu'on puisse le détecter dans les ruches, dans le miel[5] et dans la cire des rayons[6].
Il a été testé chez le saumon d'élevage contre le pou du saumon, mais ne s'est pas montré efficace contre les larves de ce petit crustacé parasite (qui fait des ravages dans les élevages industriels de saumons)[7], et qui à leur tour contaminent les saumons sauvages en migration à leur proximité.
Réglementation
Sur le plan de la réglementation des produits phytopharmaceutiques :
- pour l’Union européenne : cette substance active est interdite à la suite de l'examen relatif à l'inscription à l’annexe I de la directive 91/414/CEE ;
- pour la France : cette substance active n'est pas autorisée dans la composition de préparations bénéficiant d’une autorisation de mise sur le marché.
Caractéristiques physico-chimiques
Les caractéristiques physico-chimiques dont l'ordre de grandeur est indiqué ci-après, influencent les risques de transfert de cette substance active vers les eaux, et le risque de pollution des eaux :
- hydrolyse à pH 7 : instable ;
- solubilité : 0,1 mg·l-1 ;
- coefficient de partage carbone organique-eau : 1 000 cm3·g-1. Ce paramètre, noté Koc, représente le potentiel de rétention de cette substance active sur la matière organique du sol. La mobilité de la matière active est réduite par son absorption sur les particules du sol ;
- demi-vie : 2 jours. Ce paramètre, noté DT50, représente le potentiel de dégradation de cette substance active, et sa vitesse de dégradation dans le sol ;
- coefficient de partage octanol-eau : 6,49. Ce paramètre, noté Log Kow ou logP, mesure l’hydrophilie (valeurs faibles) ou la lipophilie (valeurs fortes) de la substance active.
Écotoxicologie
Sur le plan de l’écotoxicologie, les concentrations létales 50 (CL50) dont l'ordre de grandeur est indiqué ci-après, sont observées [8] :
Des rats de laboratoire (souche Wistar albinos mâles) ont été exposés (par voie orale) à ce pesticide (seul ou en mélange avec de la cyperméthrine qui est un autre pesticide courant[9]. Pour cette étude, l'exposition d'un groupe de rats était de 170 mg d'amitraze par kg de poids corporel en dose unique, associés ou non à une dose unique de 80 mg de cyperméthrine par kg de poids corporel[9]. D'autres groupes de rats ont été soumis à des doses plus faibles (25 mg d'amitraze par kg de poids corporel et/ou 12 mg de cyperméthrine par kg de poids corporel) mais durant quarante jours[9]. Dans tous les cas, de nombreux paramètres physiologiques et métaboliques ont été modifiés, dont le stress oxydatif (évalué via la mesure du malondialdéhyde, de l'oxyde nitrique (NO), des enzymes superoxyde dismutase (SOD), catalase, glutathion peroxydase et glucose-6-phosphate déshydrogénase (G6PD))[9]. D'autres paramètres significativement modifiés ont été les sériques biochimiques (glucose, triglycérides, cholestérol, lipoprotéine de haute densité, lipoprotéine de basse densité, l'azote uréique sanguin, la créatinine, l'aminotransférase-asparate, l'alanine-aminotransférase, la phosphatase alcaline, la protéinémie, l'albumine, etc., dans le sang et dans certains tissus (foie, rein, cerveau, rate et/ou testicule)[9]. Le métabolisme hépatique (connu pour contribuer à la détoxication de l'organisme) a également été affecté et les autopsies de foies ont montré que les problèmes étaient aggravés quand l'amitraze était associé à la cyperméthrine[9].
On a récemment (2017) confirmé que ce produit peut affecter la fonction cardiaque et l'immunité de l'abeille face aux infections virales[10].
Toxicité pour l'Homme
Sur le plan de la toxicité pour l’Homme, la dose journalière admissible (DJA) est de l’ordre de 0,003 mg·kg-1·j-1 [11]. C'est un produit neurotoxique qui affecte le système nerveux central en se fixant sur les récepteurs α2-adrénergiques, induit une dépression respiratoire avec bradycardie, hypotension et hypothermie[12].
Des cas d'empoisonnements d'adultes par intoxication aiguë[13] - [14] - [15] ou d'enfants[16] - [17] - [18] - [19] sont depuis les années 1970 signalés, notamment dans les pays en développement. Certains chercheurs et médecins ont alerté en 2016 sur le fait qu'il s'agissait selon eux d'un poison sous-estimé (« underrecognized »[20]), bien qu'il ait déjà été considéré comme source d'un problème émergent en santé publique en 2003[21]. En 2017, Shashidhara et al. le considèrent notamment comme « une menace permanente et silencieuse » pour les enfants des zones rurales tropicales des pays en développement[22].
L'intoxication peut se faire par contact, inhalation et/ou ingestion ; il ne franchit la barrière intestinale qu'à partir de doses assez élevées (selon des données provenant de l'animal de laboratoire ou de compagnie adulte[23] - [24]). L'amitraze ingéré donne deux métabolites : le 2,4-diméthylformanilide (BTS 27 919) et un métabolite actif, le N-(2,4-diméthylphényl)-N'-méthylformamidine (BTS 27 271), qui, chez les invertébrés de type insectes et acariens, se fixe — mortellement — sur les récepteurs de l'octopamine.
Exposition percutanée : cette molécule a été utilisée chez de jeunes enfants (en traitement contre les poux ou contre la gale sarcoptique humaine, par exemple en Turquie[25] où l'amitraze s'est avéré pouvoir passer au travers de leur peau (qui est plus fine et perméable que celle de l'adulte) causant des dizaines de cas détectés d'empoisonnement systémique aïgu[26]. Les symptômes apparaissent plus rapidement en cas d'exposition percutanée qu'à la suite de l'ingestion du produit.
Il peut être analysé/dosé dans l'urine humaine[27] et dans le sang[28].
Divers traitements ont été testés. L'atropine semble par exemple pouvoir être considéré comme contre-poison dans ce cas[29]. Selon les cas documentés, l'intoxication n'est généralement pas mortelle si le patient est soigné.
Tératogénicité, cancérogénicité
Depuis 2014, l’EPA le considère aussi comme possiblement cancérogène[30] à la suite d'études faites sur la souris[30].
Il s'est montré tératogène pour la grenouille[31], mais il ne semble pas y avoir à ce jour d'études de tératogénicité pour l'Homme.
Scandale sanitaire
En 2017, de l'amitraze a été détecté dans des œufs d'élevage français.
Cette découverte fait suite au scandale des œufs contaminés au fipronil où du fipronil a été trouvé par les autorités néerlandaises dans des œufs issus d'élevage des Pays-Bas bien qu'interdit dans le traitement de tout animal destiné à l'alimentation, l'amitraze étant lui interdit pour le traitement des volailles[32] - [33].
Le ministère de l'Agriculture et de l'Alimentation a fait savoir que « Contrairement au fipronil […], l’amitraze est autorisée comme médicament vétérinaire pour le traitement antiparasitaire des ruminants, porcs et abeilles. Il n’a pas d’autorisation de mise sur le marché pour la filière volailles, que ce soit en traitement sur les animaux ou pour la désinfection des bâtiments d’élevage vides, car aucun dossier de demande n’a été déposé auprès de la Commission européenne. »[34]
Références
- AMITRAZE, Fiches internationales de sécurité chimique .
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008).
- Index des Médicaments vétérinaires autorisés en France, sur ircp.anmv.anses.fr.
- Lenoir A., Le miel et les pesticides [PDF], 3 janvier 2016 (consulté le 26 août 2017).
- Korta, E., Bakkali, A., Berrueta, L. A., Gallo, B., Vicente, F., Kilchenmann, V. et Bogdanov, S. (2001), Study of acaricide stability in honey ; Characterization of amitraz degradation products in honey and beeswax, Journal of Agricultural and Food Chemistry, 49(12), 5835-5842, lire en ligne.
- Aaen, S. M., Hamre, L. A. et Horsberg, T. E. (2016), A screening of medicinal compounds for their effect on egg strings and nauplii of the salmon louse Lepeophtheirus salmonis (Krøyer), Journal of Fish Diseases, 39(10), 1201-1212.
- Merck - MSD Santé Animale, « Fiche de données de sécurité Amitraz Solid Formulation », sur www.merck.com, (consulté le )
- Van Der Merwe JS, Smit FJ, Durand AM, Krüger LP, Michael LM (2005), Acaricide efficiency of amitraz/cypermethrin and abamectin pour-on preparations in game, Onderstepoort J. Vet. Res., 72:309–314 (résumé).
- O'Neal, S. T., Brewster, C. C., Bloomquist, J. R. et Anderson, T. D. (2017), Amitraz and its metabolite modulate honey bee cardiac function and tolerance to viral infection, Journal of Invertebrate Pathology, lire en ligne.
- ANSES, « Avis de l’Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail relatif à une demande d’avis sur le risque pour les consommateurs lié à la présence de résidus d’amitraze dans les oeufs et la viande de volaille », sur ANSES, (consulté le )
- Agin, H., Calkavur, S., Uzun, H. et Bak, M. (2004), Amitraz poisoning: clinical and laboratory findings, Indian Pediatrics, 41(5), 482-485, lire en ligne.
- Avsarogullari L, Ikizceli I, Sungur M, Sözüer E, Akdur O, Yücei M. (2006), Acute amitraz poisoning in adults: clinical features, laboratory findings, and management, Clin. Toxicol. (Phila), 44:19–23.
- Demirel, Y., Yilmaz, A., Gursoy, S., Kaygusuz, K. et Mimaroglu, C. (2006), Acute amitraz intoxication: retrospective analysis of 45 cases, Hum. Exp. Toxicol., 25(10), 613-617 (résumé).
- Jorens P.G, Zandijk E, Belmans L, Schepens P.J et Bossaert L.L (1997), An unusual poisoning with the unusual pesticide amitraz, Hum. Exp. Toxicol., 16(10), 600-601 (résumé).
- Ertekin, V., Alp, H., Selimoğlu, M. A. et Karacan, M. (2002), Amitraz poisoning in children: retrospective analysis of 21 cases, Journal of International Medical Research, 30(2), 203-205 (résumé).
- Aydin, K., Kurtoglu, S., Poyrazoglu, M. H., Üzüm, K., Üstünbas, H. B. et Hallaç, I. K. (1997), Amitraz poisoning in children: clinical and laboratory findings of eight cases, Hum. Exp. Toxicol., 16(11), 680-682 (résumé).
- Yaramis, A., Soker, M. et Bilici, M. (2000), Amitraz poisoning in children, Hum. Exp. Toxicol., 19(8), 431-433 (résumé).
- Atabek, M. E., Aydin, K. et Erkul, I. (2002), Different clinical features of amitraz poisoning in children, Hum. Exp. Toxicol., 21(1), 13-16 (résumé).
- Dhooria, S. et Agarwal, R., Amitraz, an underrecognized poison: A systematic review, Indian J. Med. Res., septembre 2016, 144(3), 348, DOI 10.4103/0971-5916.198723, PMC 5320840.
- Yilmaz H.L et Yildizdas D.R (2003), Amitraz poisoning, an emerging problem: epidemiology, clinical features, management, and preventive strategies, Archives of disease in childhood, 88(2), 130-134, lire en ligne.
- Shashidhara, S., Mundkur, S. C., Hebbar, S. A., Kumar, A. et Sambasivan, V. (2017), Amitraz: A Perpetual Silent Menace Among Children in Developing Countries-A Case Report, Pediatric Emergency Care (résumé).
- Folz SD, Kakuk TJ, Henke CL, Rector DL, Tesar FB, Clinical evaluation of amitraz as a treatment for canine demodicosis, Vet. Parasitol., 1984, 16:335–41.
- Grossman MR, Amitraz toxicosis associated with ingestion of an acaricide collar in a dog, J. Am. Vet. Med. Assoc., 1993, 203:55–7.
- Kalyoncu M, Dilber E, Okten A (2001) Amitraz intoxication in children in the rural Black Sea region: analysis of forty-three patients, Hum. Exp. Toxicol., mai 2002, 21(5):269-72.
- Cices A, Bayers S, Verzì A.E, Schachner L.A, West D. et Micali G (2017), Poisoning through pediatric skin: cases from the literature, American Journal of Clinical Dermatology, 1-13.
- Gao, X., Tan, Y. et Guo, H. (2017), Simultaneous determination of amitraz, chlordimeform, formetanate and their main metabolites in human urine by high performance liquid chromatography–tandem mass spectrometry, Journal of Chromatography B, 1052, 27-33 (résumé).
- Gao X, Guo H, Zhang W.W et Gu C (2016), Simultaneous determination of amitraz and its metabolites in blood by support liquid extraction using UPHLC-QTOF, Journal of Analytical Toxicology, 40(6), 437-444 (résumé).
- Jatav O.P, Tiwari D, Lahariya D, Varghese J, Kumar S et Jacob J (2016), Amitraz Poisoning Treated Successfully with Atropine, The Journal of the Association of Physicians of India, 64(7), 82-82, lire en ligne.
- Reregistration Eligibility Decision, Amitraz, Washington, États-Unis, 30 avril 2014, EPA, lire en ligne [PDF].
- Osano O, Oladimeji AA, Kraak MH, Admiraal W. (2002), Teratogenic effects of amitraz, 2,4-dimethylaniline, and paraquat on developing frog (Xenopus) embryos, Arch. Environ. Contam. Toxicol., 43:42–9.
- Avec AFP, « Œufs contaminés : l'enquête s'élargit à un second insecticide, l'amitraze », L'Express.fr, (lire en ligne).
- « Œufs contaminés : un deuxième insecticide interdit détecté dans des élevages de poules en France », Le Monde, (lire en ligne).
- Ministère de l'Agriculture et de l'Alimentation, « Fipronil dans les œufs : point de situation », .
Voir aussi
Articles connexes
Bibliographie
- (en) Kanbur, M., Siliğ, Y., Eraslan, G., Karabacak, M., Sarıca, Z. S. et Şahin, S., The toxic effect of cypermethrin, amitraz and combinations of cypermethrin-amitraz in rats, Environmental Science and Pollution Research, 2016, 23(6), 5232-5242.
- (en) Kita, T., Hayashi, T., Ohtani, T., Takao, H., Takasu, H., Liu, G., Ohta, H., Ozoe, F., Ozoe, Y., Amitraz and its metabolite differentially activate α‐and β‐adrenergic‐like octopamine receptors, Pest. Management Science, 2017, 73(5), 984-990 (résumé).
- (en) Prullage, J. B., Tran, H. V., Timmons, P., Harriman, J., Chester, S. T. et Powell, K., The combined mode of action of fipronil and amitraz on the motility of Rhipicephalus sanguineus, Veterinary Parasitology, 2011, 179(4), 302-310 (résumé).