Propane-1,3-diol
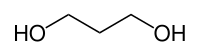
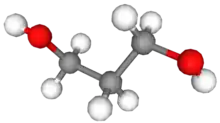
Le propane-1,3-diol ou PDO est un composé organique de la famille des diols, de formule CH2(CH2OH)2.
Sa structure est celle du propane auquel un groupe hydroxyle est attaché à chaque extrémité.
| Propane-1,3-diol | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | Propane-1,3-diol | |
| Synonymes |
Triméthylène glycol, 1,3-dihydroxypropane, 1,3-propanediol, PDO |
|
| No CAS | ||
| No ECHA | 100.007.271 | |
| No CE | 207-997-3 | |
| PubChem | 10442 | |
| SMILES | ||
| InChI | ||
| Apparence | liquide incolore, presque inodore[1]. | |
| Propriétés chimiques | ||
| Formule | C3H8O2 [Isomères] |
|
| Masse molaire[2] | 76,094 4 ± 0,003 6 g/mol C 47,35 %, H 10,6 %, O 42,05 %, |
|
| Propriétés physiques | ||
| T° fusion | −26 °C[1] | |
| T° ébullition | 213 °C[1] | |
| Solubilité | entièrement miscible (eau)[1] | |
| Paramètre de solubilité δ | 33,0 J1/2·cm-3/2 (25 °C)[3] | |
| Masse volumique | 1,05 g·cm-3[1] | |
| T° d'auto-inflammation | 400 °C[1] | |
| Point d’éclair | 131 °C[1] | |
| Limites d’explosivité dans l’air | 2,5 Vol.-%; 79 g·m-3 | |
| Pression de vapeur saturante | < 0,1 mbar à 20 °C 9 mbar à 100 °C[1] |
|
| Viscosité dynamique | 52,7 mPa·s (20 °C)[1] | |
| Précautions | ||
| Directive 67/548/EEC | ||
| Écotoxicologie | ||
| DL50 | 4 780 mg·kg-1 (souris, i.p.)[4] | |
| LogP | -1,04[1] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Synonymes[5]
Propriétés
Le propane-1,3-diol est un liquide incolore, visqueux, presque inodore et très peu inflammable (point d'éclair au-dessus de 100 °C)[1]. Il est très soluble dans l'eau, hygroscopique et légèrement volatil.
Synthèse
Le propane-1,3-diol peut être synthétisé chimiquement par l'hydration de l'acroléine, avec une solution diluée d'acide sulfurique en présence d'hydroquinone (qui empêche la polymérisation de l'acroléine), suivie par une hydrogénation catalysée par le nickel de Raney[6].
Il est également synthétisable par l'hydroformylation de l'oxyde d'éthylène qui mène au 3-hydroxypropanal. Ce dernier est ensuite hydrogéné pour donner le propane-1,3-diol.
Il existe aussi d'autre voies impliquant des bio-processus de certains micro-organismes :
- La conversion à partir du sirop de maïs effectué par une souche génétiquement modifiée d'E. coli par DuPont et Tate & Lyle Bioproducts. Environ 120 000 tonnes furent produites de cette façon en 2007[7]. Selon DuPont, ce type de production utilise 40 % moins d'énergie que le procédé conventionnel[8] - [9] et réduit l'émission de gaz à effet de serre de 20 %[8] - [9]. Pour avoir réussi à développer ce bio-processus de fabrication, renouvelable, du PDO, l'American Chemical Society a récompensé les équipes de recherche de DuPont et Tate & Lyle avec le prix « 2007 Heroes of Chemistry »[9].
- En France, le leader du secteur et le 2e au niveau mondial après DuPont Tate & Lyle Bioproducts[10], est l'entreprise Metabolic Explorer qui développe un procédé produisant du propane-1,3-diol (PDO) par voie totalement biologique à partir de glycérol, un sous-produit de la production de biodiesel. Il s'agit d'une matière première peu coûteuse et abondante. Metabolic Explorer propose par ce moyen un procédé performant du point de vue économique et environnemental[11].
- Le marché du PDO est > a 1,5 Milliard de $ / an[12]
- Depuis le , Metabolic Explorer fait partie du nouveau label d'enterNext "Tech 40" qui regroupe les 40 meilleures entreprises technologiques innovantes européennes[13]
- La conversion du glycérol (un sous-produit de la fabrication de biodiesel) en utilisant des bactéries Clostridium diolis et des Enterobacteriaceae[14] - [15].
Utilisations
Industrie
Le propane-1,3-diol est avant tout utilisé comme « bloc de construction » dans la production de polymères comme le polytriméthylène téréphtalate.
Il est aussi utilisé dans de nombreux produits industriels, comme des matériaux composites, des adhésifs, des films de pelliculage, des revêtements, des empreintes de moulage, des polyesters aliphatiques ou des copolyesters. Il est aussi utilisé comme solvant, antigel et peinture sur bois.
Chimie
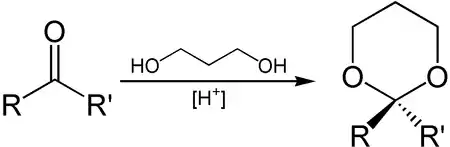
Le propane-1,3-diol peut servir à introduire un groupe protecteur sur un groupe carbonyle (aldéhydes et cétones)[16] : par une réaction d'acétalisation, il se forme un dérivé du 1,3-dioxane.
Ce groupe est stable en présence de base, et lorsque la protection n'est plus nécessaire, la réaction peut être inversée par action d'un acide dans l'eau.
Il est également possible de synthétiser le 1,3-dioxane en faisant réagir le propane-1,3-diol sur le méthanal en présence d'acide phosphorique[17]. Cette réaction peut aussi utiliser l'acide chlorhydrique et la méthénamine[18].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « 1,3-Propanediol » (voir la liste des auteurs).
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « 1,3-Propandiol » (voir la liste des auteurs).
- Entrée « 1,3-Propanediol » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 18/11/2010 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- Toxicology and Applied Pharmacology. Vol. 49, Pg. 385, 1979. PMID
- Fiche Chemicalland21.com
- C. H. Werkman, G. F. Gillen: Bacteria Producing Trimethylene Glycol, in: J. Bacteriol., 1932, 23, S. 167–182.
- Peter Werle, Marcus Morawietz, Stefan Lundmark, Kent Sörensen, Esko Karvinen, Juha Lehtonen "Alcohols, Polyhydric" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, 2006, Weinheim.
- http://www.chem.uu.nl/brew/BREWsymposiumWiesbaden11mei2005/WEBSITEBrewPresentations51105.PDF
- « Growing Demand for Products Manufactured from DuPont's Bio-Based Propanediol », sur AZoM.com, (consulté le ).
- « 1,3-Propanediol (PDO) Market by Applications & Geography - 2021 | MarketsandMarkets », sur www.marketsandmarkets.com (consulté le )
- « Butanol fermentation chimie biologique », sur www.metabolic-explorer.com (consulté le )
- « MPG 1.2 propanediol propylene », sur www.metabolic-explorer.com (consulté le )
- « Enternext lance « TECH 40 », un nouveau label pour promouvoir les sociétés européennes innovantes | Euronext », sur www.euronext.com (consulté le )
- http://biopol.free.fr/?p=342
- (en) H. Biebl, « Microbial production of 1,3-propanediol », Applied Microbiology and Biotechnology, vol. 52, no 3, , p. 289-297 (PMID 10531640, DOI 10.1007/s002530051523)
- E. J. Salmi: Untersuchungen über ätherartige Verbindungen, I. Mitteil.: Zur Darstellung der Acetale und Ketale, in: Chem. Ber., 1938, 71, S. 1803–1808; DOI 10.1002/cber.19380710905.
- R. Leutner: Zur Hydrolysegeschwindigkeit zyklischer Azetale, in: Monatsh. Chem., 1932, 60, S. 317–352; DOI 10.1007/BF01538573
- US-Patent ICI, US 2021680, 1930.
Voir aussi
Articles connexes
- Éthylène glycol
- Acide polylactique
- Propylène glycol
- Industrie pétrolière
- Fracturation hydraulique (composition du fluide)