Helicobacter pylori
Helicobacter pylori est une bactérie qui infecte la muqueuse gastrique. Sa structure externe est hélicoïdale (d'où son nom « Helicobacter »). Elle est munie de flagelles.
| Règne | Bacteria |
|---|---|
| Division | Pseudomonadota |
| Classe | Epsilonproteobacteria |
| Ordre | Campylobacterales |
| Famille | Helicobacteraceae |
| Genre | Helicobacter |
80 % des ulcères gastro-duodénaux sont causés par des infections de Helicobacter pylori[1], même si, chez beaucoup d'humains infectés, la maladie reste asymptomatique. Elle favorise de multiples maladies si elle reste dans l'estomac trop d'années.
Helicobacter pylori est une bactérie très commune (trouvée chez 50 % des humains)[2]. Elle vit exclusivement dans l'estomac humain et est la seule bactérie connue pouvant survivre dans un environnement aussi acide. Son enveloppe hélicoïdale pourrait l'aider à se visser dans le mucus de la paroi stomacale afin de la coloniser et d'y persister.
Cette bactérie est à l'origine notamment des ulcères gastro-duodénaux ou des gastrites chroniques atrophiques.
Histoire

En 1875, des scientifiques allemands découvrent une bactérie hélicoïdale dans des estomacs humains. Celle-ci ne pouvant être cultivée, les recherches la concernant furent finalement abandonnées.
Une découverte accidentelle
Cette bactérie est redécouverte accidentellement en 1982 par deux chercheurs australiens, J. Robin Warren (pathologiste) et Barry J. Marshall (gastroentérologue), qui isolaient et cultivaient des organismes à partir d'estomacs humains. Dans leur publication originelle, Warren et Marshall soutiennent que la plupart des ulcères stomacaux et gastriques sont causés par une infection de cette bactérie, et non par le stress ou la nourriture épicée, comme on le pensait auparavant. Cette découverte leur vaut le prix Nobel de physiologie ou médecine 2005.
La communauté médicale met du temps avant de reconnaître le rôle de cette bactérie dans les ulcères gastriques, pensant qu'aucune bactérie ne pouvait survivre bien longtemps dans l'environnement acide de l'estomac. Après que des études complémentaires ont été réalisées, dont celle durant laquelle Marshall ingurgita un tube à essai de H. pylori, contracta une gastrite (il n'eut pas la patience d'attendre le développement d'un ulcère) et se soigna avec des antibiotiques (satisfaisant de ce fait trois des quatre postulats de Robert Koch), la communauté médicale commence à changer d'avis. En 1994, les National Institutes of Health publient un texte soutenant que la plupart des ulcères gastriques récurrents étaient causés par H. pylori, et recommandaient que des antibiotiques soient inclus dans le traitement.
Avant que soit reconnu le rôle de cette bactérie, les ulcères stomacaux étaient habituellement soignés par des médicaments qui neutralisaient l'acidité stomacale, ou diminuaient sa production. Bien que cette technique donnât de bons résultats, les ulcères réapparaissaient très souvent. Un médicament classiquement utilisé était le subsalicylate de bismuth. Il fonctionnait assez bien, mais fut finalement abandonné, son mécanisme d'action étant inconnu et le bismuth étant un métal toxique. Il semble maintenant plausible que le sel de bismuth fonctionne comme un toxique tuant les bactéries (antibiotique). La plupart des ulcères sont maintenant efficacement traités par des antibiotiques ciblant H. pylori.
Cette bactérie fut initialement appelée Campylobacter pyloridis, puis C. pylori (après correction grammaticale latine). Finalement, après que le séquençage de son ADN eut montré que la bactérie n'appartenait pas au genre Campylobacter, elle fut placée dans un nouveau genre : Helicobacter. Le nom pylori tire son origine du latin « pylorus », qui signifie « gardien de l'ouverture », et qui fait référence à l'ouverture circulaire (pylore) menant de l'estomac au duodénum.
Alors que H. pylori reste la seule espèce connue capable de coloniser l'estomac humain, d'autres espèces de Helicobacter ont été identifiées chez d'autres mammifères, ainsi que chez certains oiseaux.
Une autre équipe de chercheurs a montré qu'Helicobacter pylori était déjà présente dans l'estomac d'environ la moitié des Homo sapiens il y a 58 000 ans dans la souche africaine, avant les grandes migrations des êtres humains vers l'Asie et l'Europe. Ces chercheurs ont en effet observé que la diversité génétique de H. pylori diminue lorsque l'on s'éloigne de l'Afrique de l'est, de la même façon que dans la lignée humaine, et que la bactérie semble avoir migré en dehors de l'Afrique vers -58 000[3].
Selon cette même étude, publiée dans le journal Nature en 2007, les chercheurs ont utilisé une technique appelée multilocus sequence typing afin d’amplifier puis de séquencer 7 gènes de ménage de la bactérie. Ils utilisèrent 769 souches isolées issues de 51 groupes géographiques, ethniques et linguistiques différents. Ils mirent en évidence que les populations génétiques de H.pylori sont assez spécifiques de continents. Ce phénomène permet de retracer l’histoire des migrations humaines. Par exemple, la souche amérindienne est proche des souches asiatiques, ce qui s’explique par une ascendance asiatique des premiers amérindiens, qui arrivèrent en Amérique il y a 12 000 ans en passant par le détroit de Béring, en Alaska. L’homme et H.pylori ont évolué ensemble depuis 150 000 ans[3].
Taxonomie
Étymologie
L'étymologie de cette espèce Helicobacter pylori est la suivante : N.L. masc. n.pylorus, orifice inférieur de l'estomac, le pylore; du grec masc./fem. n. pylôros, gardien de l'ouverture, du pylore[4].
Structure de la bactérie
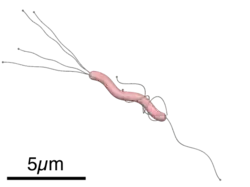
H. pylori est une bactérie Gram négatif de forme hélicoïdale, d'environ trois micromètres de long et d'environ 0,5 micromètre de diamètre. Elle porte quatre à six flagelles[5]. Elle est dite microaérophile, c'est-à-dire qu'elle nécessite un apport d'oxygène, mais dans des proportions inférieures à celles trouvées dans l'atmosphère. Enfin, elle peut produire son énergie par méthanogenèse à partir d'hydrogène.
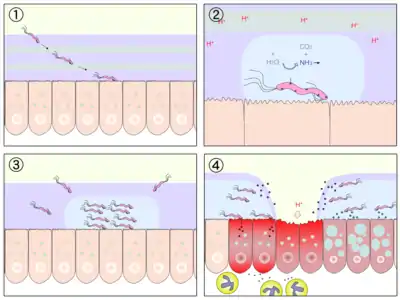
Grâce à sa forme hélicoïdale et à ses flagelles, la bactérie se glisse à travers le mucus et parfois les muqueuses de l'estomac en s'ancrant aux cellules épithéliales grâce à des adhésines (protéines fixatrices). Elle sécrète alors une enzyme appelée « uréase » qui transforme l'urée en ammoniaque et en dioxyde de carbone. Cette ammoniaque va partiellement neutraliser l'acidité gastrique (qui sert à prédigérer les aliments, tout en tuant la plupart des bactéries). L'ammoniac est toxique pour les cellules épithéliales, et va, de concert avec d'autres produits sécrétés par H. pylori (protéases, catalases, phospholipases, etc.) endommager la surface des cellules épithéliales, enclenchant de ce fait le processus de formation d'ulcères.
Des études récentes montrent que certaines souches de cette bactérie posséderaient un mécanisme particulier d'injection d'agents inflammatoires dans les cellules stomacales. Pour s'accrocher sur la paroi stomacale, elles perturbent aussi le cycle naturel du fer dans l'épithélium[6].
Génétique
Le génome de H. pylori est séquencé depuis 1997. La position et le nombre des gènes régulateurs, qui régulent la synthèse des produits d'autres gènes, restent mal connus. Une soixantaine de petites molécules d'ARN dites « small RNAs » (sRNAs) jouent également un rôle régulateur-inhibiteur, en se fixant à des séquences de gènes, ce qui a pour effet de bloquer la traduction des protéines codées par ces gènes. Elles ont été identifiées en 2009/2010[7], par séquençage à haut débit. Ceci a surpris les chercheurs car on pensait antérieurement que H pylori était dépourvue de sRNAs. Or, H pylori présente autant voire plus de sRNAs que des bactéries intestinales telles qu'Escherichia coli et les salmonelles. Cependant, une protéine réputée indispensable à la régulation des sRNAs est absente chez H pylori, ce qui laisse penser qu'elle dispose de systèmes de signaux internes aujourd'hui inconnus.
Des nouveaux vaccins contre H pylori pourraient éventuellement être développés sur ces bases.
Épidémiologie
Environ deux tiers de la population mondiale est infectée par cette bactérie. Le taux d'infection varie d'un pays à l'autre : environ 25 % dans les pays occidentaux avec d'importantes disparités. Aux États-Unis, les personnes atteintes sont essentiellement des personnes âgées (plus de 50 % de personnes contaminées au-delà de 60 ans, contre environ 20 % chez les moins de 40 ans), ainsi que les personnes les plus démunies. Le taux est plus élevé dans les pays du Tiers monde. Dans ces derniers, il est courant de rencontrer des enfants infectés, probablement à cause des mauvaises conditions sanitaires.
Une mutation sur le gène TLR1 codant un récepteur de type Toll pourrait être un facteur favorisant l'infection[8].
Le taux d'infection est essentiellement fonction des conditions d'hygiène, ainsi que du degré d'utilisation des antibiotiques. Néanmoins, des résistances contre certains antibiotiques sont apparues chez certaines souches de H. pylori. Par exemple, on peut trouver en Grande-Bretagne certaines souches résistantes au métronidazole.
Infection
Transmission
Cette bactérie a été isolée dans des selles, de la salive et sur des plaques dentaires, ce qui laisse supposer qu'une transmission est possible par ingestion d'aliments ou d'eau contaminés par les selles ou par voie gastro-orale.
Si elle n'est pas soignée par une prise d'antibiotiques, il semblerait qu'une infection par H. pylori puisse persister durant toute la vie d'un individu. Le système immunitaire humain ne serait donc pas capable d'éradiquer cette bactérie, en raison des mécanismes dont elle dispose pour déjouer les défenses immunitaires.
L'infection peut alors conduire à plusieurs maladies graves : reflux gastro-œsophagien, ulcère gastro-duodénal ou duodénal ou gastrique, ou encore cancer de l'œsophage et cancer de l'estomac.
Symptômes
L'infection peut être symptomatique ou asymptomatique (c'est-à-dire avec ou sans effets visibles).
Divers symptômes sont associés à H. pylori, mais plutôt vagues et pouvant varier dans le temps. Ils sont non spécifiques ou induits par une autre pathologie associée.
On estime que 70 % à 80 % des infections sont asymptomatiques[9].
L'inflammation ou des dommages plus profonds à la paroi stomacale (gastrite) dus à H. pylori peuvent causer des réactions légères ou graves, avec :
- douleurs stomacales ou abdominales ;
- reflux acide ;
- régurgitation ;
- vomissements ;
- éructations ;
- flatulences ;
- nausées.
- Pâleur.
- Dépression .
- Courbatures à répétitions.
- Somnolence.
- Constipation.
- Rosacé.
- Oppression thoracique.
Diagnostic
Il est possible de détecter la présence de H. pylori par différentes méthodes :
- Par ingestion d'urée marquée au carbone 13 (si le patient est infecté, cette urée est métabolisée par H. pylori, produisant ainsi du CO2 marqué, qui est ensuite expulsé hors du corps via les poumons, et peut donc être détecté par analyse du gaz expiré)[10]. Ce test est non invasif, a une très bonne fiabilité, est remboursé à 65 % par la Sécurité sociale en France[11] et est commercialisé sous l'appellation de Helikit en France[12].
- Détection dans les selles par dosage immunochromatograhique ou immunoassay. Cette méthode a été démontrée comme fiable pour le primo-diagnostic ainsi que pour vérifier le succès d'un traitement[13].
Les biopsies réalisées lors de la gastroscopie permettent aussi de constater d'éventuelles lésions atrophiques sur l'antre et le fundus. Un test à l'uréase peut être fait directement : cette dernière convertit l'urée en ammoniac, détectée par colorimétrie pH, permettant un dépistage quasi immédiat de l'hélicobacter[14].
- le dosage d'anticorps spécifiques, le test sérologique étant fiable pour détecter une infection, sans pouvoir la dater. Il ne l'est pas pour vérifier le succès d'un traitement anti-helicobacter car les anticorps subsistent plusieurs mois après une éventuelle éradication. Il existe des kits de dépistage sérologique permettant un dépistage quasi immédiat, de fiabilité moindre toutefois qu'une sérologie traditionnelle[15]. La sérologie n'est plus guère recommandée actuellement[16].
La plupart de ces tests (à part le test au carbone 13) perdent en sensibilité en cas d'hémorragie digestive d'origine gastrique ou duodénale[17]. De même, le test au carbone 13 peut être faussé en cas de prise d'inhibiteurs de la pompe à protons qui doivent être arrêtés idéalement deux semaines avant le test[18].
Maladies liées à cette infection
Helicobacter pylori cause plusieurs maladies plus ou moins graves suivant les individus. Ce germe cause :
- une dyspepsie non ulcéreuse ;
- des ulcères gastriques et/ou duodénaux ;
- des gastrites chroniques le plus souvent localisées sur l'antre mais qui s'étendent parfois sur le fundus. On parle alors dans ce cas de pangastrite ;
- une malabsorption de la vitamine B12 ;
- des gastrites atrophiques entraînant une hypochlorydrie voire une achlorhydrie ;
- des métaplasies intestinales qui traduisent un stade précancéreux ;
- des cancers (le cancer de l'estomac - adénocarcinome - et le lymphome du MALT gastrique) : l'helicobacter serait l'un des facteurs de risque principal du cancer gastrique[19]. L'éradication de ce germe permet de diminuer notablement la fréquence de ce type de cancer[20] - [21].
H. pylori pourrait contribuer à la survenue de la maladie de Parkinson[22] ; l'éradication d'Helicobacter pylori améliorerait les résultats du traitement par lévodopa[23].
Avantages
La présence de l'helicobacter serait protectrice contre le cancer de l'œsophage[24]. Ce type de cancer est cependant beaucoup plus rare que celui de l'estomac que la bactérie contribue à provoquer.
Des découvertes récentes ont montré que la bactérie n'est pas nécessairement pathogène, et qu'elle peut avoir des effets protecteurs contre l'obésité et le diabète de type 2[25]. Le caractère pathogène résulterait en réalité de l'interaction du patrimoine génétique de la bactérie avec le système immunitaire.
Traitement de l'infection
Il existe plusieurs recommandations internationales sur la prise en charge de l'helicobacter. Les recommandations européennes sont connues sous le nom de Conférence de consensus Maastricht V et ont été publiées en 2015[26]. Des recommandations américaines ont été publiées en 2007[27].
Le traitement diminue sensiblement le risque de récidive d'un ulcère gastrique et en améliore la cicatrisation[28].
En cas de dyspepsie non compliquée, il en améliore les symptômes[29].
Il pourrait par ailleurs diminuer le risque de survenue d'un cancer de l'estomac en cas de lésion précancéreuse[30].
L'efficacité du traitement est vérifiée le plus souvent par la négativation du test respiratoire à l'uréase.
Traitement antibiotique
Le traitement recommandé par la Haute Autorité de Santé (HAS) repose sur un algorithme intégrant deux grands types de traitement : la quadrithérapie bismuthée et la trithérapie concomitante[31].
La trithérapie dite « concomitante » constitue le « traitement guidé », c'est-à-dire guidée par le résultat d'analyse de l'antibiorésistance d'Helicobacter pylori. Elle consiste, pendant 10 jours, en :
- Amoxicilline 1g matin et soir
- IPP pleine dose (à dose curative) matin et soir, la quantité dépendant du médicament en question
- Clarithromycine 500mg matin et soir si la bactérie est sensible à la molécule, sinon Lévofloxacine 500mg matin et soir
La quadrithérapie dite « bismuthée » constitue le « traitement probabiliste », c'est-à-dire non guidée par les résistances de la bactérie. Cette thérapie est aussi utilisée si la bactérie s'avère résistante à la clarithromycine et à la lévofloxacine. Elle consiste, pendant 10 jours, en :
- 3 gélules de Pylera 4 fois par jour contenant comme substance active : Métronidazole 125mg, Tétracycline chlorhydrate 125mg, Sous-citrate de bismuth potassique 140mg[32]
- IPP pleine dose (à dose curative) matin et soir, la quantité dépendant du médicament en question
Il existe aussi comme alternative à la quadrithérapie bismuthée la quadrithérapie dite « concomitante » qui repose sur une association pendant 14 jours d'Amoxicilline, de Clarithromycine, de Métronidazole et d'IPP.
Ce traitement d'éradication de dix jours peut être suivi, selon les cas, d'un traitement par IPP simple dose pour quatre à six semaines.
Auparavant, il était recommandé une trithérapie associant deux antibiotiques (à choisir parmi amoxicilline, clarithromycine et métronidazole) à un IPP. La durée habituelle de traitement était alors entre une et deux semaines[33].
Le traitement antibiotique pour l'éradication de l'infection à H. pylori peut entraîner une augmentation significative de l'incidence de la dépression clinique dans un court laps de temps (moins de 30 jours), qui peut être négligée par les gastro-entérologues et les médecins généralistes[34].
Sels de bismuth
Des sels de bismuth (un métal lourd) peuvent aussi être utilisés en association avec une trithérapie. Cependant le bismuth est interdit en France depuis les années 1970 à la suite de cas d'intoxication et de troubles rénaux, ainsi que des encéphalopathies répertoriées, principalement dans des cas de surdose. Le bismuth continue d'être prescrit avec succès dans de nombreux autres pays. Celui-ci a même fait un retour en France en association avec de la tétracycline et du métronidazole sous le nom de PYLERA. À ce jour, aucun cas d'encéphalopathie n'a été rapporté avec l'utilisation de PYLERA[35]. Compte tenu d'une baisse d'efficacité de la trithérapie classique due essentiellement aux résistances à la clarithromycine (évaluée à 20 %), et à la suite des résultats d'une étude montrant l'intérêt du bismuth dans cette situation, une demande d'AMM européenne d'une association fixe de citrate de bismuth, métronidazole et tétracycline, avec prise concomitante d'oméprazole, est déposée en 2011[36].
Suivi de l'éradication
En raison du risque d’échec du traitement, il faut vérifier systématiquement que Helicobacter pylori a bien été éliminé de l’estomac.
Cette vérification est obligatoire effectuée par un test respiratoire, qui est l’examen de référence.
Ce test respiratoire n'a toutefois de valeur que s'il est pratiqué au moins 4 semaines après l'arrêt des antibiotiques et au moins deux semaines après l'arrêt d'un traitement par inhibiteur de la pompe à protons (IPP).
Autres traitements
D'après certains auteurs, le traitement par antibiotique a une efficacité limitée à 70 % des cas, moindre que dans d'autres études[37] à cause de la présence de biofilms[38]. Une vision plus récente de la microbiologie constate que la bactérie est hébergée par au moins la moitié de la population[39], ce qui en fait plutôt une bactérie du microbiote qui dans 80 % à 90 %[40] des cas ne donnera ni ulcère ni cancer. De plus la bactérie a une action contre l'obésité et le diabète[41]. L'action de la bactérie serait plutôt liée à sa capacité[42] à former un biofilm qui, en attaquant la muqueuse, crée un ulcère ou une tumeur[43] - [44] - [45] - [46]. L'acétylcystéine serait un inhibiteur de son biofilm[47] - [48] - [49].
Au lieu de vouloir éliminer la bactérie (qui finit souvent par réinfecter les sujets traités par des antibactériens), il serait plus judicieux de la contrôler en diminuant sa concentration gastrique. Les probiotiques contribuent à diminuer la puissance de la bactérie[50]. La souche Lactobacillus reuteri DSMZ 17648[51] fait preuve d'un effet inhibiteur encourageant, dont plusieurs études démontrant une réduction significative du taux de H. pylori. Les patients ayant recours à ce traitement voient leur symptômes régresser jusqu'à disparaître en quelques semaines.
En 2002, un essai vaccinal avait été tenté mais celui-ci a été abandonné parce que les effets secondaires étaient trop importants. Ces effets étaient liés à l'adjuvant utilisé (toxine cholérique). De plus, l'immunisation n'était pas suffisamment efficace. Seule une réduction de la concentration bactérienne a été observée. Les chercheurs tentent de mettre au point des adjuvants non toxiques permettant de stimuler efficacement la réponse immunitaire. L'immunisation des muqueuses est très complexe. Le vaccin est toujours en cours d'étude et pourrait voir le jour dans quelques années. Celui-ci devrait permettre de traiter l'infection ainsi que la prévenir. Au cours de l'année 2007 les chercheurs ont élucidé les mécanismes permettant à la bactérie d'échapper au système immunitaire[52].
Traitements alternatifs
Il existe des approches préventives ou des thérapeutiques dites naturelles[53]. Associés au traitement classique, certains polyphénols semblent améliorer très légèrement son efficacité[54].
Les huiles essentielles anti-infectieuses sont surtout les huiles essentielles à phénol comme Origanum compactum, Thymus vulgaris à thymol, Melaleuca alternifolia, Cinnamomum zeylanicum feuilles. La girofle (Eugenia caryophyllata) inhibe la croissance d'Helicobacter pylori in vitro[55]. Une publication italienne de 2017 fait l'inventaire des extraits d'agrumes reconnus pour leur activité anti-Helicobacter pylori in vitro seuls ou en association[56]. Plusieurs huiles essentielles comme Mentha piperita et Lemongrass ont montré in vitro une inhibition nette de la prolifération du HP[57] - [58]. Leurs efficacités en conditions réelles est inconnue.
L'efficacité de la mastication de résine de Pistacia lentiscus (lentisque pistachier), arbre méditerranéen exploité surtout dans l'île grecque de Chio, un temps alléguée[59] est débattue[60] - [61].
Il est aussi possible de réduire l'infection (dans les cas où les différents traitements ont échoué), sans pour autant l'éliminer, en buvant du jus de canneberge. Certaines molécules (proanthocyanidines à haut poids moléculaire) présentes dans la canneberge seraient efficaces pour empêcher l'adhésion de la bactérie aux cellules gastriques. Les bactéries sont alors éliminées naturellement lorsque l'estomac se vide[62].
La capsaïcine (extraite du piment) inhibe la croissance d'Helicobacter pylori[63]. Une faible consommation protège du cancer de l'estomac tandis qu'une consommation moyenne ou haute augmente le risque[64].
Les Indiens Kunas d'Amérique centrale sont habitués à traiter les maux d'estomac avec du Piper multiplinervium, herbe contenant des substances efficaces contre le germe[65] - [66].
Lors d'une expérience en 2004, l'ingestion (après mastication) de 14, 28, ou 56 g de pousses de brocoli, deux fois par jour pendant 7 jours a diminué ou supprimé la présence de la bactérie, et amélioré les symptômes chez un nombre significatif de patients[67]. En revanche, la bactérie réapparaît après quelques mois. Le brocoli et d'autres choux peuvent ainsi être utilisés de manière préventive (l'expérience a été menée au Japon sur environ 50 patients dont la moitié consommait des germes de luzerne et l'autre moitié du brocoli)[68]. Le sulforaphane a été testé en association mais l'essai était de trop petite taille pour conclure quoi que ce soit[69]. Utilisé seul, un extrait de graine de brocoli n'a pas prouvé son efficacité[70]. Cependant, 6 g/j de poudre de pousses de brocoli pendant 28 jours, éradique H.Pylori chez environ 45 % des personnes contre 85 % avec une trithérapie[71].
L'huile de nigelle est efficace contre la dyspepsie et H.Pylori[72]. 8 semaines de supplémentation avec 2 g/jour de poudre de N. sativa en association avec une quadruple thérapie pourraient augmenter de manière significative l'éradication de H. pylori (88 % contre 55 %)[73]
Lactobacillus acidophilus, L. casei, L. gasseri, and Bifidobacterium infantis sont efficaces en complément quand l'efficacité du traitement médicale est inférieur à 80 %[74].
La consommation au moins une fois par semaine de miel ou de thé semblerait efficace pour prévenir en partie l'infection[75].
La mélatonine (10 mg/d) ou le tryptophane (500 mg/d) ajoutés à l'oméprazole pourraient considérablement accélérer le taux de guérison des ulcères peptiques chroniques infectés par H. pylori par rapport à la seule administration d'oméprazole[76].
Un régime sans nickel améliore le taux d'éradication d'Helicobacter pylori[77].
Une revue systématique publié en 2021 conclue que « des études cliniques ont montré que les extraits végétaux et les micronutriments ne sont pas efficaces en tant qu'agents uniques dans l'éradication des infections à H. pylori, mais ils peuvent agir en synergie avec les thérapies pharmacologiques conventionnelles pour une efficacité améliorée lorsqu'ils sont utilisés en combinaison. Les germes de brocoli, la curcumine, le complexe de bardane et les vitamines (C et E) se sont avérés efficaces lorsqu'ils sont utilisés en association avec des trithérapies standard pour H. pylori. Nigella sativa L. en association avec l'oméprazole a montré des résultats similaires à la trithérapie standard composée d'antibiotiques et d'oméprazole. À l'inverse, GutGard s'est avéré significativement efficace en tant qu'agent unique par rapport au contrôle placebo dans deux essais cliniques. Polaprezinc a montré une bonne efficacité en association avec un traitement standard, mais le zinc n'a montré aucun avantage synergique »[78].
Notes et références
- (en) Chuan Zhang, Nobutaka Yamada, Yun-Lin Wu, Min Wen, Takeshi Matsuhisa, Norio Matsukura, « Helicobacter pylori infection, glandular atrophy and intestinal metaplasia in superficial gastritis, gastric erosion, erosive gastritis, gastric ulcer and early gastric cancer », World journal of gastroenterology: WJG, vol. 11, no 6, , p. 791-796 (ISSN 1007-9327, PMID 15682469, lire en ligne, consulté le )
- Hooi JKY, Lai WY, Ng WK, Suen MMY, Underwood FE, Tanyingoh D et al., « Global Prevalence of Helicobacter pylori Infection: Systematic Review and Meta-Analysis. », Gastroenterology, vol. 153, no 2, , p. 420-429 (PMID 28456631, DOI 10.1053/j.gastro.2017.04.022)
- (en) Linz B, Balloux F, Moodley Y et Als. An African origin for the intimate association between humans and Helicobacter pylori, Nature, 2007;445:915-918 doi:10.1038/nature05562
- (en) « Species Helicobacter pylori », sur LPSN,
- « Helicobacter pylori »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le )
- Tan S, J Noto, J Romero-Gallo, R Peek, Jr., and M Amieva (2011), Helicobacter pylori perturbs iron trafficking in the epithelium to grow on the cell surface. PLoS Pathog 7: e1002050
- (en) Sharma, Hoffmann, Darfeuille, Reignier, Findeiß, Sittka, Chabas, Reiche, Hackermüller, Reinhardt, Stadler & Vogel ; The primary transcriptome of the major human pathogen Helicobacter pylori, - Nature - 17/02/1984 Télécharger l'étude ; Travail piloté par Jörg Vogel du groupe « Biologie des ARN » de l'Institut Max Planck berlinois, en collaboration avec des scientifiques de Leipzig et de l'unité de recherche INSERM 869 de l'université de Bordeaux.
- Mayerle J, den Hoed CM, Schurmann C et al. Identification of genetic loci associated with Helicobacter pylori serologic status, JAMA. 2013;309:1912-1920
- Boyanova, L (editor) (2011). Helicobacter pylori. Caister Academic Press (en). (ISBN 978-1-904455-84-4).
- "haute autorité de santé, tests respiratoire à l'urée"
- "test respiratoire à l'urée"
- « Résumé des caractéristiques du produit - HELIKIT 75 mg, poudre pour solution buvable - Base de données publique des médicaments », sur base-donnees-publique.medicaments.gouv.fr (consulté le )
- Veijola L, Myllyluoma E, Korpela R, Rautelin H, Stool antigen tests in the diagnosis of Helicobacter pylori infection before and after eradication therapy, World J Gastroenterol, 2005;11:7340-7344
- (en) Vaira D, Vakil N, Gatta L et al. Accuracy of a new ultrafast rapid urease test to diagnose Helicobacter pylori infection in 1000 consecutive dyspeptic patients, Aliment Pharmacol Ther, 2010;31:331-8
- (en) Loy CT, Irwig LM, Katelaris PH, Talley NJ, Do commercial serological kits for Helicobacter pylori infection differ in accuracy? A meta-analysis, Am J Gastroenterol, 1996;91:1138-44
- Crowe SE, Helicobacter pylori infection, N Engl J Med, 2019;380:1158-1165
- (en) Gisbert JP, Abraira V, Accuracy of Helicobacter pylori diagnostic tests in patients with bleeding peptic ulcer: a systematic review and meta-analysis, Am J Gastroenterol, 2006;101:848-63
- (en) Laine L, Estrada R, Trujillo M, Knigge K, Fennerty MB, Effect of proton-pump inhibitor therapy on diagnostic testing for Helicobacter pylori, Ann Intern Med, 1998;129:547-50
- (en) Talley NJ, Fock KM, Moayyedi P, « Gastric Cancer Consensus conference recommends Helicobacter pylori screening and treatment in asymptomatic persons from high-risk populations to prevent gastric cancer » Am J Gastroenterol. 2008;103:510-514
- (en) Fukase K, Kato M, Kikuchi S et al. for the Japan Gast Study Group. « Effect of eradication of Helicobacter pylori on incidence of metachronous gastric carcinoma after endoscopic resection of early gastric cancer: an open-label, randomised controlled trial » Lancet. 2008;372:392-397
- (en) Fuccio L, Zagari RM, Eusebi LH et al. « Meta-analysis: Can Helicobacter pylori eradication treatment reduce the risk for gastric cancer? » Ann Intern Med. 2009;151:121-128
- (en) Dr Testerman Traci, Bacteria 'linked' to Parkinson's disease, BBC Online, consulté le 23 mai 2011.
- (en) Hashim H, Azmin S, Razlan H, Yahya NW, Tan HJ, Manaf MR, Ibrahim NM, « Eradication of Helicobacter pylori infection improves levodopa action, clinical symptoms and quality of life in patients with Parkinson's disease », PLoS One, vol. 9, no 11, , e112330. (PMID 25411976, PMCID PMC4239049, DOI 10.1371/journal.pone.0112330, lire en ligne [html])
- (en) Rokkas T, Pistiolas D, Sechopoulos P, Robotis I, Margantinis G, Relationship between Helicobacter pylori infection and esophageal neoplasia: a meta-analysis, Clin Gastroenterol Hepatol, 2007;5: 1413-1417
- Janlou Chaput Futura, « Une bactérie virulente nous protègerait contre l’obésité et le diabète », sur Futura (consulté le )
- (en) Malfertheiner P, Megraud F, O'Morain CA on behalf of the European Helicobacter and Microbiota Study Group and Consensus panel, et al. « Management of Helicobacter pylori infection—the Maastricht V/Florence Consensus Report », Gut 2017;66:6-30.
- (en) Chey WD, Wong BCY, American College of Gastroenterology, « Guideline on the management of Helicobacter pylori infection » Am J Gastroenterol, 2007;102:1808-25
- (en) Ford AC, Delaney BC, Forman D, Moayyedi P, « Eradication therapy in Helicobacter pylori positive peptic ulcer disease: systematic review and economic analysis » Am J Gastroenterol, 2004;99:1833-55
- (en) Zagari RM, Fuccio L, Bazzoli F, « Investigating dyspepsia » BMJ, 2008;337:a1400
- (en) Wong BC, Lam SK, Wong WM, Chen JS, Zheng TT, Feng RE, et al. China Gastric Cancer Study Group. Helicobacter pylori eradication to prevent gastric cancer in a high-risk region of China: a randomized controlled trial, JAMA, 2004;291:244-5
- HAS, « Fiche pertinence des soins - Traitement de l’infection par Helicobacter pylori chez l’adulte », sur has.sante.fr,
- « Pylera », sur eurekasante.vidal.fr (consulté le )
- (en) Malfertheiner P, Megraud F, O'Morain C, Bazzoli F, El-Omar E, Graham D et al. « Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report » Gut, 2007;56:772-81
- (en) Chia‐Fen Tsai, Mu‐Hong Chen, Yen‐Po Wang et Pei‐Yi Liu, « Increased risk of short‐term depressive disorder after Helicobacter pylori eradication: A population‐based nested cohort study », Helicobacter, vol. 26, no 4, (ISSN 1083-4389 et 1523-5378, DOI 10.1111/hel.12824, lire en ligne, consulté le )
- « PYLERA - Bismuth - Posologie, Effets secondaires, Grossesse », sur Doctissimo (consulté le )
- Résultats d'une étude phase III : citrate de bismuth, métronidazole et tétracycline versus une trithérapie comportant de la clarithromycine : (en) Peter Malfertheiner, Franco Bazzoli, Jean-Charles Delchier, Krysztof Celiñski, Monique Giguère, Marc Rivière, Francis Mégraud for the Pylera Study Group, « Helicobacter pylori eradication with a capsule containing bismuth subcitrate potassium, metronidazole, and tetracycline given with omeprazole versus clarithromycin-based triple therapy: a randomised, open-label, non-inferiority, phase 3 trial », The Lancet, vol. 377, no 9769, , p. 905-913 (ISSN 0140-6736, PMID 21345487, DOI 10.1016/S0140-6736(11)60020-2, lire en ligne, consulté le )
- "Helicobacter Pilori, efficacité traitement antibiotique"
- "2015:Biofilm Formation by Helicobacter pylori and Its Involvement for Antibiotic Resistance."
- "Groupe d'étude français des helicobacter"
- "British Society of Gastroenterology: Helicobacter pylori"
- "Mars, 2013: Hélicobacter pylori, la bactérie qui combat obésité et diabète"
- "Sciences daily, Juillet 2016: Genes found in H. pylori that influence biofilm formation"
- "Microbiology - Helicobacter Pylori (Ulcer)"
- "Pasteur contre Béchamp : le combat stérile des partisans"
- "Effect of curcumin on Helicobacter pylori biofilm formation"
- "Probiotic Lactobacillus fermentum UCO-979C biofilm formation on AGS and Caco-2 cells and Helicobacter pylori inhibition"
- "2010, Nbci:Biofilm demolition and antibiotic treatment to eradicate resistant Helicobacter pylori: a clinical trial."
- "Nbci,2015;Biofilm Formation by Helicobacter pylori and Its Involvement for Antibiotic Resistance"
- "2012:Review article: biofilm formation by Helicobacter pylori as a target for eradication of resistant infection"
- (en) Drahoslava Lesbros-Pantoflickova, Irène Corthésy-Theulaz, André L. Blum, « Helicobacter pylori and Probiotics », The Journal of Nutrition, vol. 137, no 3, , p. 812S-818S (ISSN 0022-3166 et 1541-6100, PMID 17311980, lire en ligne, consulté le )
- Heidrun Mehling et Andreas Busjahn, « Non-Viable Lactobacillus reuteri DSMZ 17648 (Pylopass™) as a New Approach to Helicobacter pylori Control in Humans », Nutrients, vol. 5, no 8, , p. 3062–3073 (ISSN 2072-6643, PMID 23917169, PMCID PMC3775242, DOI 10.3390/nu5083062, lire en ligne, consulté le )
- (en) Mario Milco D’Elios, Leif P. Andersen, « Helicobacter pylori Inflammation, Immunity, and Vaccines », Helicobacter, vol. 12, , p. 15–19 (ISSN 1523-5378, PMID 17727455, DOI 10.1111/j.1523-5378.2007.00530.x, lire en ligne, consulté le )
- Malliga Raman Murali, Sangeetha Vasudevaraj Naveen, Chang Gue Son et Hanumantha Rao Balaji Raghavendran, « Current knowledge on alleviating Helicobacter pylori infections through the use of some commonly known natural products: bench to bedside », Integrative Medicine Research, vol. 3, no 3, , p. 111–118 (ISSN 2213-4220, PMID 28664086, PMCID 5481734, DOI 10.1016/j.imr.2014.04.001, lire en ligne, consulté le )
- Qiuxiang Wang, Chengjiao Yao, Yilin Li et Lihong Luo, « Effect of polyphenol compounds on Helicobacter pylori eradication: a systematic review with meta-analysis », BMJ open, vol. 13, no 1, , e062932 (ISSN 2044-6055, PMID 36604137, PMCID 9827256, DOI 10.1136/bmjopen-2022-062932, lire en ligne, consulté le )
- Yang Li, Chen Xu, Qiang Zhang et Jun Yan Liu, « In vitro anti-Helicobacter pylori action of 30 Chinese herbal medicines used to treat ulcer diseases », Journal of Ethnopharmacology, vol. 98, no 3, , p. 329–333 (ISSN 0378-8741, PMID 15814268, DOI 10.1016/j.jep.2005.01.020, lire en ligne, consulté le )
- (en) Giuseppina Mandalari et al., « Effectiveness of Citrus Fruits on Helicobacter pylori », Hindawi - Evidence-Based Complementary and Alternative Medicine - Volume 2017, Article ID 8379262, , p. 8 pages (lire en ligne)
- Rabia Zahid, Hafiz Muhammad Asif, Faisal Rasheed et Faizan Rashid, « In vitro and in vivo anti-Helicobacter pylori activity of selected medicinal plants employed for the management of gastrointestinal disorders », Pakistan Journal of Pharmaceutical Sciences, vol. 33, no 6(Supplementary), , p. 2809–2814 (ISSN 1011-601X, PMID 33879441, lire en ligne, consulté le )
- Tomoyuki Ohno, Masakazu Kita, Yoshio Yamaoka et Shigeyoshi Imamura, « Antimicrobial activity of essential oils against Helicobacter pylori », Helicobacter, vol. 8, no 3, , p. 207–215 (ISSN 1083-4389, PMID 12752733, DOI 10.1046/j.1523-5378.2003.00146.x, lire en ligne, consulté le )
- (en) Huwez F.U., Thirlwell D., « Mastic Gum kills Helicobacter pylori » New-England Journal of Medicine, 339:1946, Dec. 24, 1998
- (en) James R. Bebb, Nathalie Bailey-Flitter, Dlawer Ala’Aldeen, John C. Atherton, « Mastic gum has no effect on Helicobacter pylori load in vivo », Journal of Antimicrobial Chemotherapy, vol. 52, no 3, , p. 522-523 (ISSN 0305-7453 et 1460-2091, PMID 12888582, DOI 10.1093/jac/dkg366, lire en ligne, consulté le )
- K. J. Dabos, E. Sfika, L. J. Vlatta et G. Giannikopoulos, « The effect of mastic gum on Helicobacter pylori: a randomized pilot study », Phytomedicine: International Journal of Phytotherapy and Phytopharmacology, vol. 17, nos 3-4, , p. 296–299 (ISSN 1618-095X, PMID 19879118, DOI 10.1016/j.phymed.2009.09.010, lire en ligne, consulté le )
- (en) Burger O, Ofek I, Tabak M, Weiss EI, Sharon N, Neeman I., « A high molecular mass constituent of cranberry juice inhibits helicobacter pylori adhesion to human gastric mucus », FEMS Immunol Med Microbiol, vol. 29, , p. 295-301 (PMID 11118911, DOI 10.1111/j.1574-695X.2000.tb01537.x, lire en ligne, consulté le )
- (en) Nicola L Jones, Souheil Shabib et Philip M Sherman, « Capsaicin as an inhibitor of the growth of the gastric pathogen Helicobacter pylori », FEMS Microbiology Letters, vol. 146, no 2, , p. 223–227 (DOI 10.1111/j.1574-6968.1997.tb10197.x, lire en ligne, consulté le )
- Noel Pabalan, Hamdi Jarjanazi et Hilmi Ozcelik, « The impact of capsaicin intake on risk of developing gastric cancers: a meta-analysis », Journal of Gastrointestinal Cancer, vol. 45, no 3, , p. 334–341 (ISSN 1941-6636, PMID 24756832, DOI 10.1007/s12029-014-9610-2, lire en ligne, consulté le )
- Armando A. Durant-Archibold, Ana I. Santana et Mahabir P. Gupta, « Ethnomedical uses and pharmacological activities of most prevalent species of genus Piper in Panama: A review », Journal of Ethnopharmacology, vol. 217, , p. 63–82 (ISSN 1872-7573, PMID 29428241, DOI 10.1016/j.jep.2018.02.008, lire en ligne, consulté le )
- (en) Rüegg T, Calderón AI, Queiroz EF, Solís PN, Marston A, Rivas F, Ortega-Barría E, Hostettmann K, Gupta MP, « 3-Farnesyl-2-hydroxybenzoic acid is a new anti-Helicobacter pylori compound from Piper multiplinervium » Jour. of Ethnopharmacology, 2006;103:461-7
- (en) Mark V. Galan, Arfana A. Kishan et Ann L. Silverman, « Oral Broccoli Sprouts for the Treatment of Helicobacter pylori Infection: A Preliminary Report » Digestive Diseases and Sciences Volume 49, Numbers 7-8, 1088-1090, DOI 10.1023/B:DDAS.0000037792.04787.8a (résumé, en anglais)
- Akinori Yanaka, Jed W. Fahey, Atsushi Fukumoto et Mari Nakayama, « Dietary sulforaphane-rich broccoli sprouts reduce colonization and attenuate gastritis in Helicobacter pylori-infected mice and humans », Cancer Prevention Research (Philadelphia, Pa.), vol. 2, no 4, , p. 353–360 (ISSN 1940-6215, PMID 19349290, DOI 10.1158/1940-6207.CAPR-08-0192, lire en ligne, consulté le )
- Young Woon Chang, Yoo Min Park, Chi Hyuk Oh et Shin Ju Oh, « Effects of probiotics or broccoli supplementation on Helicobacter pylori eradication with standard clarithromycin-based triple therapy », The Korean Journal of Internal Medicine, vol. 35, no 3, , p. 574–581 (ISSN 2005-6648, PMID 31830776, PMCID 7214376, DOI 10.3904/kjim.2019.139, lire en ligne, consulté le )
- Kai Guo, Lei Wang, Jinli Mahe et Liansheng Li, « Effect of aqueous extract of seed of broccoli on inflammatory cytokines and Helicobacter pylori infection: a randomized, double-blind, controlled trial in patients without atrophic gastritis », Inflammopharmacology, vol. 30, no 5, , p. 1659–1668 (ISSN 1568-5608, PMID 35831736, DOI 10.1007/s10787-022-01030-x, lire en ligne, consulté le )
- (en) Zahra Bahadoran, Parvin Mirmiran, Maryam Zarif Yeganeh et Farhad Hosseinpanah, « Complementary and alternative medicinal effects of broccoli sprouts powder on Helicobacter pylori eradication rate in type 2 diabetic patients: A randomized clinical trial », Journal of Functional Foods, vol. 7, , p. 390–397 (DOI 10.1016/j.jff.2014.01.020, lire en ligne, consulté le )
- Reza Mohtashami, Hasan Fallah Huseini, Mojtaba Heydari et Mohsen Amini, « Efficacy and safety of honey based formulation of Nigella sativa seed oil in functional dyspepsia: A double blind randomized controlled clinical trial », Journal of Ethnopharmacology, vol. 175, , p. 147–152 (ISSN 1872-7573, PMID 26386381, DOI 10.1016/j.jep.2015.09.022, lire en ligne, consulté le )
- Mahvash Alizadeh-Naini, Hedieh Yousefnejad et Najmeh Hejazi, « The beneficial health effects of Nigella sativa on Helicobacter pylori eradication, dyspepsia symptoms, and quality of life in infected patients: A pilot study », Phytotherapy research: PTR, vol. 34, no 6, , p. 1367–1376 (ISSN 1099-1573, PMID 31916648, DOI 10.1002/ptr.6610, lire en ligne, consulté le )
- Yini Dang, Jan D. Reinhardt, Xiaoying Zhou et Guoxin Zhang, « The effect of probiotics supplementation on Helicobacter pylori eradication rates and side effects during eradication therapy: a meta-analysis », PloS One, vol. 9, no 11, , e111030 (ISSN 1932-6203, PMID 25365320, PMCID 4217763, DOI 10.1371/journal.pone.0111030, lire en ligne, consulté le )
- Lyudmila Boyanova, Juliana Ilieva, Galina Gergova et Borislav Vladimirov, « Honey and green/black tea consumption may reduce the risk of Helicobacter pylori infection », Diagnostic Microbiology and Infectious Disease, vol. 82, no 1, , p. 85–86 (ISSN 1879-0070, PMID 25779680, DOI 10.1016/j.diagmicrobio.2015.03.001, lire en ligne, consulté le )
- K. Celinski, P. C. Konturek, S. J. Konturek et M. Slomka, « Effects of melatonin and tryptophan on healing of gastric and duodenal ulcers with Helicobacter pylori infection in humans », Journal of Physiology and Pharmacology: An Official Journal of the Polish Physiological Society, vol. 62, no 5, , p. 521–526 (ISSN 1899-1505, PMID 22204799, lire en ligne, consulté le )
- Saeed Abdi, Sara Ataei, Maede Abroon et Pantea Majma Sanaye, « A Comprehensive Review of the Role of Complementary and Dietary Medicines in Eradicating Helicobacter pylori », Iranian journal of pharmaceutical research: IJPR, vol. 21, no 1, , e127030 (ISSN 1726-6890, PMID 36060908, PMCID 9420233, DOI 10.5812/ijpr-127030, lire en ligne, consulté le )
- Hammad Ullah, Alessandro Di Minno, Cristina Santarcangelo et Haroon Khan, « Vegetable Extracts and Nutrients Useful in the Recovery from Helicobacter pylori Infection: A Systematic Review on Clinical Trials », Molecules (Basel, Switzerland), vol. 26, no 8, , p. 2272 (ISSN 1420-3049, PMID 33919894, PMCID 8070974, DOI 10.3390/molecules26082272, lire en ligne, consulté le )
Voir aussi
Articles connexes
Liens externes
- (en) Référence Catalogue of Life : Helicobacter pylori (Marshall et al., 1985) Goodwin et al., 1989 (consulté le )
- Le test respiratoire à l’urée marquée au 13C pour la détection de Helicobacter pylori : possibilités d’application au Québec. AETMIS, 2005
- Centre National de Référence des Campylobacters et Hélicobacters
Bibliographie
- (en) Hatakeyama M (2011), Anthropological and clinical implications for the structural diversity of the Helicobacter pylori CagA oncoprotein. Cancer Sci102:36-43