Anesthésique local
Un anesthésique local est un médicament qui inhibe de manière réversible la propagation des signaux le long des nerfs. Lorsqu'elle intéresse un nerf sensitif, cette inhibition se traduit cliniquement par une perte de sensibilité plus ou moins complète que l'on appelle analgésie ou « bloc sensitif » : c'est le but recherché lors de l'usage d'un tel médicament. Lorsqu'elle concerne un nerf moteur ou la composante motrice d'un nerf mixte, il en résulte une perte de motricité nommée paralysie ou encore « bloc moteur » généralement considérée comme un effet secondaire. Contrairement à ce qui a lieu lors d'une anesthésie générale, l'anesthésie locale ne supprime pas la perception douloureuse dans la totalité du corps et ne provoque pas de perte de conscience.
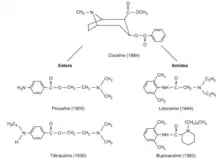
Dans la zone anatomique où ils sont administrés, les anesthésiques locaux (AL) agissent par un effet stabilisant de membrane (en) : ils inhibent l'ouverture de canaux ioniques – en particulier les canaux sodiques voltage-dépendants – impliqués dans la transmission des influx douloureux le long des nerfs périphériques. Bien que de nombreuses substances puissent produire différents degrés d'anesthésie locale, les médicaments de synthèse dédiés à cet usage se rangent en deux classes d'après leur structure chimique : les aminoamides et les aminoesters. Structurellement apparentés à la cocaïne, molécule naturelle anciennement utilisée comme AL, les AL actuels sont des substances de synthèse qui s'en distinguent par l'absence de potentiel addictif significatif et par des effets secondaires systémiques nettement moins marqués (en particulier sur le plan de la toxicité cardiovasculaire).
Les différents AL se distinguent les uns des autres par leurs propriétés pharmacologiques (puissance et posologie, délai et durée d'action, indications, effets indésirables). Ils sont utilisés dans différentes techniques telles que :
- l'anesthésie topique (dépôt d'AL sur la peau ou les muqueuses : anesthésie « de contact » ou « de surface ») ;
- l'anesthésie par infiltration (injection d'AL dans les tissus) ;
- l'administration périmédullaire: intrathécale et péridurale
- l'anesthésie périnerveuse (tronculaire et plexique)
- l'administration intraveineuse
Pharmacodynamique[1]
Les anesthésiques locaux bloquent la propagation des potentiels d'action en interagissant directement avec les canaux sodiques rapides. Le site d'action des anesthésiques locaux se trouve au niveau de la partie intracellulaire des canaux sodiques. Alors que la plupart des toxines animales (scorpion, poisson fugu produisant la tétrodotoxine [TTX]) agissent en se liant fortement à la partie externe du canal, la plupart des agents pharmacologiques (anesthésiques locaux, antiépileptiques, antiarythmiques) agissent par obstruction du pore central auquel ils accèdent par la face cytoplasmique.
En règle générale, les fibres de petit diamètre sont plus sensibles que les fibres larges. De même, les fibres non-myélinisées sont plus sensibles que les fibres myélinisées. Cette sensibilité accrue aux anesthésiques locaux explique le bloc différentiel lors que l'usage de solution faiblement concentrées : c'est à dire que le patient perd la perception thermo-algique mais conserve sa motricité et sensibilité au toucher[2] - [3].
Pharmacocinétique et métabolisme[4] - [2]
Les anesthésiques locaux se fixent aux composants du sang hématies et protéines sériques comme l'a-1-glycoprotéine acide (AGA) et l’albumine.
- Métabolisme des amino-esters:
Comme la succinylcholine, la cocaïne ou l’héroïne, les esters sont hydrolysés dans le sérum et les hématies par des estérases non spécifiques ou pseudocholinestérases. Seule la cocaïne a un métabolisme hépatique de relative importance. Les esters ont longtemps été considérés comme des agents très sûrs à cause de la dégradation plasmatique rapide.
- Métabolisme des amino-amides:
Après leur passage dans le courant sanguin, les AL amides sont éliminés par le foie. Cette élimination passe par le système du cytochrome P450. La lidocaïne et la bupivacaïne sont principalement métabolisées par l’isoenzyme CYP3A4, alors que la ropivacaïne est principalement métabolisée par le CYP1A2 et, dans une moindre mesure, par le CYP3A4.
Famille chimique et usages en médecine
Anesthésiques locaux à structure amino-ester[5]
Cette catégorie regroupe les AL dont la structure chimique comporte une fonction amine (tertiaire) et une fonction ester.
Leur chef de file est la cocaïne, substance naturelle extraite de l'espèce végétale Erythroxylon coca (spontanée et cultivée en Amérique du Sud). Sa structure est remarquable, caractérisée par une fonction amine tertiaire qui s'intègre à un système bicyclique de type tropane lui-même connecté par une liaison ester à une molécule d'acide benzoïque. Bien connue pour son usage récréatif de surcroît illicite dans la plupart des pays (substance classifiée comme stupéfiant), la cocaïne présente une importante toxicité cardiovasculaire et neurologique. Du point de vue de la médecine contemporaine, son usage anesthésique n'a plus qu'un intérêt historique.
Les substances suivantes sont des AL de synthèse à structure amino-ester (donc structurellement apparentés à la cocaïne) :
- chloroprocaïne (Clorotécal®) ; Elle s'utilise par voie intrathécale pour les interventions chirurgicales sous ombilicales de très courte durée.
- amylocaïne (Stovaïne®) ;
- benzocaïne ; anesthésie topique en proctologie.
- cyclométhycaïne ;
- diméthocaïne (Larocaïne®) ;
- hexylcaïne (Osmocaïne®) ;
- oxybuprocaïne (Novesine®) ; anesthésie locale en ophtalmologie
- pipérocaïne ;
- procaïne (Novocaïne®) ;
- propoxycaïne ;
- proxymétacaïne ou proparacaïne (Alcaïne®) ;
- tétracaïne (Améthocaïne®); anesthésie locale en ophtalmologie
Anesthésiques locaux à structure amino-amide[5]
On regroupe dans cette catégorie des AL de synthèse qui possèdent à la fois une fonction amine (tertiaire) et une fonction amide.
La lidocaïne (Xylocaine®, Versatis®) est le chef de file de cette catégorie. C'est une molécule de synthèse connue depuis les années 1940 et largement utilisée pour toutes sortes de gestes douloureux réalisés sous anesthésie locale :
- Par infiltration sous cutanée pour la« petite chirurgie » (sutures, exploration des plaies etc.) dans les services d'urgence, pour les ponctions d'organes et d'épanchements divers, abord veineux périphérique (notamment chez l'enfant), mise en place drains et cathéters...
- Par voie péridurale pour la réalisation d'interventions chirurgicales (e.g. Césarienne) ou à des fins d'analgésie post opératoire.
- Par voie périnerveuse pour la réalisation de blocs anesthésiques tronculaires (d'un tronc nerveux) ou plexiques (d'un plexus nerveux).
- Par voie topique, présente dans les patchs EMLA® et VERSATIS®(emplâtre)
- Par voie intraveineuse: elle est régulièrement administrée par voie intraveineuse continue pour les interventions de chirurgie abdominale majeure (gynécologique, digestive), parfois associée à la kétamine, avec un impact sur la douleur post oépratoire et la vitesse de reprise du transit[6].
Les substances suivantes sont des AL de synthèse à structure amino-amide (donc structurellement apparentés à la lidocaïne) :
- lévobupivacaïne (Chirocaïne®) ; utilisée par voie péridurale en obstétrique ou périnerveuse.
- bupivacaïne (Marcaïne®) ; utiliser par voie intrathécale pour les interventions sous ombilicales de longue durée.
- mépivacaïne (Carbocaïne®) ;utilisée par voie périnerveuse avec une cinétique proche de la lidocaïne.
- prilocaïne (Baritekal®, EMLA patch®) ; utilisée par voie topique (EMLA®) ou par voie intrathécale pour les chirurgies sous ombilicales de courte durée.
- ropivacaïne (Naropéine®); utilisée par voie sous cutanée, périnerveuse, péridurale et parfois intrathécale, elle a une place de choix pour une utilisation péridurale en raison de sa durée d'action prolongée.
- trimécaïne (Mésocaïne®).
- articaïne (Ultracaïne®) ; anesthésie locale en odontostomatologie
- cinchocaïne (Dibucaïne®) ;
- étidocaïne (Duranest®)
Autres anesthésiques locaux
On retrouve dans cette catégorie des substances d'origine naturelle qui ne partagent ni la structure de deux classes d'AL de synthèse, ni leur mode d'action :
- eugénol ;
- menthol ;
- plusieurs neurotoxines : néosaxitoxine (NSTX), saxitoxine (STX), tétrodotoxine (TTX).
Galénique[2]
Formes galéniques La plupart des AL sont commercialisés sous forme de sels (chlorhydrates en Europe) dont le pH est maintenu entre 4,0 et 5,5 pour assurer leur parfaite solubilité. Il n’existe plus de conservateur ni d’antioxydant dans les solutions non adrénalinées. En revanche, les formes adrénalinées contiennent des conservateurs du type oxybenzoate ou métabisulfite, incriminés dans des réactions allergiques. La crème Eutectic Mixture of Local Anesthetics (EMLA®), destinée à l’application topique, est composée d’un mélange équimolaire de prilocaïne et de lidocaïne.
Effets indésirables potentiels[6]
-Effets indésirables en cas de non respect des doses toxiques ou d'injection intravasculaire accidentelle:
- Toxicité cardiaque: bradycardie, extrasystoles ventriculaires et supraventriculaires, bloc intracardiaque (effet stabilisant de membrane) , état de choc cardiogénique, Tachycardie ventriculaire, Fibrillation ventriculaire.
- Toxicité neurologique centrale: Goût métallique, paresthésies péribuccales, acouphènes, baisse de l'acuité visuelle, vertiges, confusion, convulsions, coma.
-Effets indésirables sans lien avec un surdosage:
Les anesthésiques locaux ont une toxicité neurologique propre et peuvent dans d'extrrêmement rares cas être responsables de déficits sensitivomoteurs persistants.
-Effets indésirables en lien avec le déficit sensitif:
L'anesthésie locorégionale peut être responsable de blocs sensitifs étendus qui peuvent rendre le patient insensible aux positions vicieuses, et induire des complications liées à une compression cutanée prolongée (escarres) ou à une compression nerveuse non ressentie (e.g. compression du nerf sciatique poplitée externe dans les étriers lors de l'accouchement par voie basse)
-Certains anesthésiques locaux peuvent dans de rares cas induire une méthémoglobinémie, c'est particulier le cas pour la benzocaïne et prilocaïne, lidocaine et tétracaïne.
-Dans d'extrêmement rares cas les anesthésiques locaux peuvent être responsables de réactions allergiques, allant de l'urticaire à l'oedème de Quincke avec choc anaphylactique.
Conduite à tenir en cas d'intoxication[7]
Le traitement de l'intoxication aux anesthésiques locaux, qu'il se manifeste par des signes cardiovasculaires ou neurologiques, va consister à :
- Interrompre l'administration d'anesthésiques locaux : perfusion intraveineuse, administration périnerveuse, administration péridurale, administration cicatricielle...
- Administrer de du dioxygène afin de préparer une anesthésie générale ou d'éviter une désaturation importante en cas de crise convulsive.
- Administrer par voie intraveineuse de l'huile de soja purifiée (intralipide/médialipide) afin de tenter de séquestrer un maximum de molécules dans le compartiment plasmatique afin de limiter leur effets systémiques, le temps de leur élimination.
- Le reste de la prise en charge est essentiellement symptomatique et peut nécessiter selon la présentation clinique: des benzodiazepines en cas de convulsions, anesthésie générale et intubation endotrachéale, Circulation extracorporelle en cas d'arrêt cardiaque réfractaire ou choc cardiogénique réfractaire...
Historique[2]
Vingt-quatre ans après l’extraction de la cocaïne par Niemann en 1860, la première utilisation de ses propriétés anesthésiques eut lieu en 1884 par Köller. Depuis lors, de nombreuses molécules ont été synthétisées, d’abord les esters par les chimistes allemands avant la Seconde Guerre mondiale, puis plus récemment les amides par les chimistes suédois. Il semble que nous soyons arrivés au bout de cette classe pharmacologique dont les derniers-nés sont la ropivacaïne et la lévobupivacaïne.
Anesthésiques de surface par contact
Famille des amino-esters
- La cocaïne est un alcaloïde extrait de l’Erythroxylon Coca croissant à l’Amérique du Sud. cet Anesthésique Local (AL) trouble la capture neuronale inverse de la noradrénaline dans les synapses. Cela active la transmission d’irritation. Dans les synapses dopaminergiques la cocaïne trouble la capture de dopamine, ce qui provoque l’irritation du Système Nerveux Central (SNC). L’effet périphérique se manifeste par l’activation du Système Nerveux (SN) sympathique : la fréquence cardiaque, la tension artérielle augmentent, les vaisseaux sanguins se rétrécissent. De grandes doses de cocaïne provoque les convulsions, le tremblement, l’inhibition de SNC, la mort à cause de paralysie du centre respiratoire.
- La tetracaïne (nom commercial "dicaïne") – l’AL toxique actif. On l’applique essentiellement comme Anesthésique (A) de surface : les muqueuse d’œil (0,3 %), de nez et ge gorge (0,5-1 %). En cas d’A des voies respiratoires supérieurs la dose maximale à usage unique – 3 ml de solution 3 %. La durée d’effet – 2-3 heures. L’effet toxique se manifeste par l’irritation de SNC remplacée par la paralysie. La mort est à cause de paralysie du centre respiratoire. On ajoute de l’adrénaline pour la diminution d’absorption.
- La benzocaïne (nom commercial "anesthésine") – est peu hydrosoluble ; est liposoluble et soluble dans l’alcool. On l’applique seulement en cas d’A de surface dans les solutions huileuse (l’otite aigüe, les douleurs du méat acoustique externe), les pommades, les pâtes (5 %), les poudres (en cas de prurit), les suppositoire rectaux et les solutions huileuses en cas d’affection du rectum (l’hémorroïde, les fissures). On emploie cette A intérieurement en cas de douleurs à l’œsophage et l’estomac, en cas de vomissement.
- La proxymétacaïne, l’oxybuprocaïne (nom commercial "inocaïne"). On l’emploi à courte durée à l’ophtalmologie : l’anesthésie de conjonctive, de cornée pour déterminer la tension oculaire, enlever les corps étrangers.
- La bumécaïne (nom commercial "piromécaïne") est appliquée à l’ophtalmologie (0,5 %) pour l’A de surface de muqueuses buccales (1-2 %), nasales, de nasopharynx, de gorge, d’ œsophage, de rectum, de voies urinaires et respiratoires. On emploie la pommade de la bumécaïne 5 % à la stomatologie.
- La procaïne (nom commercial "novocaïne") – l’anesthétique actif, la durée de son effet – 30-60 min. Cet A est hydrolysé par la cholinestérase du plasma sanguin. La procaïne est bien hydrosoluble et peu toxique ; est appliquée pour l’A par infiltration (0,25%-0,5 %), de conduction et épidurale (1-2 %). Parfois on l’emploi pour l’A spinale (5 %) et de surface (10 %).
Famille des amino-amides
- La lidocaïne (nom commercial "xycaïne" ou "xylocaïne") - l’AL du type amidique. On l’emploi pour l’A de surface sous la forme de collyre 2-4 % ; de muqueuses orale, nasale, de nasopharynx, de gorge, d’ œsophage, de rectum, de voies urinaires et respiratoires – 1-2 % ; pour l’A épidurale – 2 %, pour l’A spinale – 5 %. On emploie à la stomatologie, au oto-rhino-laryngologie, à l’endoscopie la solution mesurée de lidocaïne 10 %. Pour la diminution d’effet résorptif on ajoute de l’adrénaline (l’épinéphrine). La lidocaïne, un anesthésique local, est également utilisée comme antiarythmique.
- La trimécaïne s'apparente à la lidocaïne. L’effet est plus durable. Le chlorure d'éthyle – le liquide volatil en ampoules. En cas d’application le chlorure d'éthyle s'exhale très vite, en cela les tissus refroidissent et perdent de la sensibilité. On l’emploie en cas de petites opérations de la peau, de contusion, d’entorse, de distortion du ligament, en cas de névrite, de radiculite.
- La bupivacaïne (nom commercial "marcaïne") – l’AL du type amidique. Sa période latente jusque 20 min. Cet anesthétique est employé en cas d’A par infiltration - 0,25 %, de conduction - 0,25-0,5 %, épidurale – 0,75 % et spinale – 0,5 %. La durée d’A épidurale et spinale – 3-4 heures. L’effet toxique, lié à la résorption, se manifeste comme le mal à la tête, le tournement de tête, les troubles de vision, la nausée, le vomissement, les troubles du rythme ventriculaire, le bloc auriculoventriculaire.
- L’articaïne (nom commercial "ultracaïne") - l’AL du type amidique. On l’emploi pour l’A par infiltrarion et de conduction. La durée d’effet – 1-2 heures.
- La ropivacaïne (nom commercial "naromine") – c’est l’amide. On l’emploi pour l’A épidurale (l’opération césarienne, l’abolition du syndrome douloureux aigu), pour L’A de conduction et sous-arachnoïdienne. La durée d’effet – 6-12 heures.
- La mepivacaïne est appliquée localement à la stomatologie pour l’A en cas d’ intubation de la trachée, de bronchoscopie, d’œsophagoscopie, de tonsillectomie.
Autres anesthésiques de surface
- Par réfrigération : cryoanesthésie
- Chlorure d'éthyle. Nocif et inflammable, n’est plus utilisé
- Fréon 114. Utilisé aussi pour les tests au froid
- Menthol. Utilisé pour soulager des maux et douleurs mineures telles que des crampes musculaires, entorses, migraines. Il peut être utilisé seul ou combiné à du piment ou du camphre. En Europe, il est plutôt utilisé en gel ou en crème
Adjuvants[2]
L’adrénaline et la clonidine sont souvent utilisées pour prolonger l’action des AL au site d’action. Cet effet a surtout été étudié pour les blocs centraux. L’adrénaline diminue la hauteur du pic de concentration sérique des AL (la concentration maximale de la lidocaïne peut être diminuée de 40 %), mais non le délai pour atteindre ce pic (Tmax). Elle prolonge le bloc en réduisant le débit sanguin local et en ralentissant la clairance des AL. Après une injection épidurale chez l’adulte, l’effet de l’adrénaline est d’autant plus net que les AL sont de courte durée d’action, comme la lidocaïne, alors qu’elle est moins efficace avec la bupivacaïne. Les effets de la clonidine sur la résorption des AL à partir de l’espace épidural restent mal connus. Aux doses utilisées (1 µg/kg), la clonidine ne diminue pas leur résorption.
Les opioïdes tels que le fentanyl et sufentanil sont également utilisés comme adjuvants en anesthésie loco-régionale périmédullaire pour prolonger la durée de l'anesthésie et en améliorer la qualité.
Les vasoconstricteurs
Ils augmentent la durée d’action et l’efficacité, diminuent la quantité d’anesthésique, donc la toxicité. Ils diminuent le saignement.
L’adrénaline
Agit sur les récepteurs α1 et 2 et β2 ( → vasodilatation). L'adrénaline augmente le rythme cardiaque et la contractibilité du myocarde. Un surdosage provoque : tachycardie, hypertension et augmentation du métabolisme basal
La [[noradrénaline|noradrénaline]]
Agit sur les récepteurs α1 et 2 mais pas sur les β2. Elle est moins efficace que l’adrénaline, et peut être plus nocive. Elle peut provoquer une augmentation de la tension artérielle, mais n’agit ni sur la contractibilité cardiaque ni sur le métabolisme basal.
La [[corbadrine|corbadrine]]
10 fois moins active que la noradrénalibne. Utilisée uniquement associée à l’aptocaïne en cas de porphyrie.
Les antiseptiques
Parabène = para-hydroxy-benzoïque : rôle anti-fongique et anti-microbien mais très allergisant, il est donc de moins en moins utilisé.
Les antioxydants
EDTA = acide-éthylène-diamide-tétra-acétique : diminue les réactions d’oxydations dans les capsules
Les conservateurs
- Sulfites : comme le métabisulfite de sodium ou potassium. Cette molécule est obligatoire s'il y a des vasoconstricteurs.
- L'eau
Notes et références
- Elsevier Masson, « Pharmacologie des anesthésiques locaux », sur EM-Consulte (consulté le )
- H. Beloeil, J.-X. Mazoit, Pharmacologie des anesthésiques locaux (lire en ligne)
- Edouard Simoneau, Yoann Elmaleh, Olivier Imauven, « Péridurale déambulatoire pour le travail obstétrical : pourquoi et comment ? », Le Praticien en Anesthésie-Réanimation, (lire en ligne)
- NYSORA, « Pharmacologie clinique des anesthésiques locaux », sur NYSORA, (consulté le )
- « *Anesthésiques locaux : Les points essentiels », sur pharmacomedicale.org (consulté le )
- Adrien Lemoine, « Pharmacologie des anesthésiques locaux : un rappel des fondamentaux », Le Praticien en Anesthésie Réanimation, vol. 25, no 6, , p. 272–276 (ISSN 1279-7960, DOI 10.1016/j.pratan.2021.10.005, lire en ligne, consulté le )
- « Intoxication aux anesthésiques locaux », sur Société Française d’Anesthésie et de Réanimation (consulté le )