Vaccin d'AstraZeneca-Oxford contre la Covid-19
Le vaccin d'AstraZeneca-Oxford contre la Covid-19, officiellement nommé COVID-19 Vaccine AstraZeneca[4] est un vaccin contre la Covid-19 mis au point par l'université d'Oxford et la société pharmaceutique AstraZeneca à partir de l'adénovirus ChAdOx1 (en) d'un chimpanzé[7] - [8] - [9] - [10]. Lors de son développement, il a précédemment été nommé ChAdOx1 nCoV-19[4] - [11], puis AZD1222[11]. Il est plus généralement connu par le nom de vaccin Oxford-AstraZeneca, ses noms commerciaux sont Covishield ou Vaxzevria. Il doit être injecté dans les muscles. Pour atteindre son efficacité maximale, deux doses doivent être injectées dans un intervalle maximal de 12 semaines[12].
| Vaccin d'AstraZeneca-Oxford contre la Covid-19 | |
| |
| Informations générales | |
|---|---|
| Princeps | vaccin Oxford-AstraZeneca, Covishield, Vaxzevria (Inde)[1] précédemment : AZD1222, ChAdOx1 nCoV-19 |
| Administration | injection intramusculaire |
| Laboratoire | Université d'Oxford et AstraZeneca |
| Statut légal | |
| Statut légal | Union européenne : CMA[2] - [3] - [4] Royaume-Uni : AUU temporaire[5] - [6] |
| Identification | |
| DCI | COVID-19 Vaccine (ChAdOx1-S [recombinant])[3] |
| No CAS | |
| DrugBank | 15656 |
À partir du 29 mars 2021, le vaccin AstraZeneca s'appelle désormais VaxZevria[13] - [3].
De rares cas de thromboses atypiques[14] - [15], liés à l'injection du vaccin, entravent le cours de la vaccination contre la Covid-19 dans certains pays. Pourtant, l'Agence européenne des médicaments (EMA) a depuis déclaré ne pas pouvoir confirmer de risques accrus de thromboses chez les femmes et adolescentes vaccinées[16],
Histoire
La recherche universitaire a été effectuée par le Jenner Institute (en) et par l'Oxford Vaccine Group (en), deux entités de l'université d'Oxford[17] - [18]. La société italienne Advent Srl de Pomezia a produit le 1er lot de vaccin pour les tests.
En mars 2020, le gouvernement britannique ainsi que les scientifiques concernés poussent l'Université d'Oxford à confier la production à AstraZeneca plutôt qu'à Merck & Co., par crainte que les vaccins fabriqués aux États-Unis ne soient pas exportés au Royaume-Uni et dans le reste du monde[19]. Leur méfiance était fondée, puisque le président américain Joe Biden a signé un décret en mars 2021 donnant aux Américains la priorité des vaccins produits aux États-Unis[20].
Principe
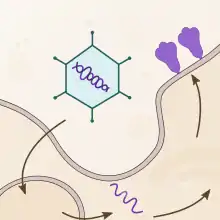
Le vaccin d'Oxford-AstraZeneca, à l'instar du vaccin Spoutnik V ou de l'Ad26.COV2.S de Johnson & Johnson, utilise comme vecteur viral un adénovirus (famille de virus très courants responsables notamment de rhumes). Le vecteur adénovirus est incapable de réplication car certains de ses gènes essentiels ont été supprimés et remplacés par un gène codant la protéine S des spicules S de SARS-CoV-2 (la protéine complète, codon optimisée, à laquelle a été ajoutée une séquence signal tPA)[21] - [22]. Lors de la vaccination, le virus modifié pénètre dans les cellules, libère ses gènes qui sont transportés vers le noyau, la machinerie cellulaire transcrit en acide ribonucléique messager (ARN messager) puis traduit en protéines, dont la protéine S, éduquant le système immunitaire à la reconnaître[23].
L'AZD1222 utilise un adénovirus de chimpanzé comme vecteur, alors que le Spoutnik V, développé par le Centre de recherches en épidémiologie Gamaleïa avec le ministère russe de la Défense, utilise deux adénovirus humains[24].
Excipients
- L-Histidine
- Chlorhydrate de L-histidine monohydraté
- Chlorure de magnésium hexahydraté
- Polysorbate 80
- Éthanol (2 mg dans une dose)
- Sucrose (synonyme : saccharose)
- Chlorure de sodium
- Édétate de disodium dihydraté
- Eau pour préparation injectable[25]
Réactions
En mars 2021, la conférence des évêques catholiques du Canada « [recommande] de ne pas recevoir les vaccins de Johnson & Johnson et d’AstraZeneca, parce que leur procédé de fabrication est lié à des cellules dérivées de l’avortement », ce qui est démenti par les deux sociétés pharmaceutiques et le gouvernement du Québec[26].
Essais cliniques et performances
Début , des essais de provocation immunitaire, tant sur le modèle animal (singes macaques) que pour certains essais humains à un stade précoce (visant à tester la sécurité de vaccins), suggèrent qu'un candidat-vaccin mis au point par l'université d'Oxford permettrait d'éviter l'infection pulmonaire (et donc la pneumonie induite), mais sans bloquer l'infection ailleurs dans le corps (y compris dans les fosses nasales où la charge virale reste aussi élevée que chez les individus non-vaccinés et exposés au virus)[27].
L'étude portant sur 1 077 personnes a permis d’obtenir une réponse immunitaire avec la production de lymphocytes T et d'anticorps ciblant la protéine Spike qui permet au virus d'infecter les cellules[28]. Quelques effets secondaires (fièvre et maux de tête) ont toutefois été relevés. AstraZeneca et l'université d'Oxford lancent l'étude phase III en .
Ce vaccin AZD1222 entre en production pour une livraison à partir de fin .
La survenue d'un cas sévère de réaction indésirable est signalée le . Les détails de l'incident restent inconnus. Les essais sont interrompus, mais reprennent peu après enquête d'un groupe indépendant. Selon le site Vaccination Info service, il convient de rester vigilant à cause du polysorbate 80, un excipient qui permet de fludifier le vaccin[29], et qui possède « une structure proche du PEG », dont le risque est un choc anaphylactique pour les personnes allergiques[30] - [29]. Selon BFM TV, seules les personnes ayant déjà fait une réaction sévère après un vaccin ou un traitement injectable doivent consulter un allergologue ou un médecin avant d'envisager de se faire vacciner[29].
Le , l'université d'Oxford et AstraZeneca annoncent des résultats intérimaires (en) tirés de la phase III des essais cliniques : ils affirment un taux de succès de 70 %[31]. Ils sont toutefois critiqués parce que la méthode de calcul s'appuie sur des taux de 62 % et 90 %, obtenus de deux groupes de sujets soumis à des doses différentes du vaccin candidat[32].
Le vaccin Oxford/AstraZeneca est, selon LCI, le premier vaccin dont les résultats d'efficacité ont été validés par une revue scientifique : The Lancet (8 décembre 2020[33]), le présente comme « sûr » mais efficace à seulement 70 %, et insuffisamment testé sur les personnes âgées[24]. Aussi Olivier Véran, ministre de la Santé de la France, estime qu'il faut le réserver aux « personnes plus jeunes »[34].
Études anglaises
Le , The Lancet publie une étude preprint analysant les détails des études de phase III menées au Royaume-Uni, au Brésil et en Afrique du Sud. La protection offerte en espaçant les deux injections de douze semaines est portée à 82 % et la réduction de transmission du virus est de 67 % dès la première dose[35] - [36].
L’université d’Oxford déclare, le , suspendre les essais sur les enfants du vaccin développé avec AstraZeneca, "dans l’attente de l’avis de l’Agence de réglementation des médicaments et des produits de santé (MHRA) britannique"[37].
Étude écossaise
Une étude est menée par des universités en Écosse sur l'efficacité de la première dose de vaccins Pfizer-BioNTech et Oxford-AstraZeneca COVID-19 contre les admissions à l'hôpital en Écosse, sur la base d'une étude de cohorte prospective nationale de 5,4 millions de personnes. Entre le et le , 1 137 775 patients ont été vaccinés dans le cadre de l'étude, dont 490 000 avec le vaccin Oxford-AstraZeneca. La première dose du vaccin Oxford-AstraZeneca a été associée à un effet vaccinal protecteur, réduisant de 94 %[38] l'hospitalisation liée à la Covid-19, 28 à 34 jours après la vaccination. Les résultats pour les deux vaccins combinés ont montré un effet vaccinal pour la prévention de l'hospitalisation liée à la Covid-19 qui était comparable en limitant l'analyse aux personnes âgées de ≥ 80 ans (81 %). La majorité des patients de plus de 65 ans ont reçu le vaccin Oxford-AstraZeneca. Au , l'étude est un preprint et n'a pas fait l'objet d'un examen par les pairs[39].
À la date du , alors que les incidents relatifs aux campagnes de vaccination à l'aide du vaccin AstraZeneca-Oxford, notamment au sein de l'Union Européenne, cette étude n'est toujours ni validée ni publiée par la prestigieuse revue The Lancet. Un débat scientifique est toujours en cours relativement à certaines études en preprint, qui pourraient notamment être en rapport avec les méthodologies des "méta-analyses" sur la base de "cohort datas" et les possibles suspicions de conflits d'intérêt entre producteurs pharmaceutiques -chercheurs - universités - administrations et autorités politiques[39] - [40].
Étude américaine
Le sont publiés les résultats d'une étude de phase III portant sur 32 449 participants aux États-Unis. On observe 79 % de prévention des infections symptomatiques et 100 % de prévention des cas sévères et des hospitalisations. L'efficacité est comparable chez les patients de plus de 65 ans qui représentaient 80 % des participants. Une attention particulière est portée sur l'effet secondaire thrombotique. Il n'est pas observé d’augmentation du risque de thrombose ou de thrombose veineuse cérébrale (CVST) parmi les 21 583 patients ayant reçu au moins une dose de vaccin[41] - [42]. La fiabilité de ces résultats est mise en doute par Anthony Fauci qui soupçonne AstraZeneca d'avoir utilisé des données partiellement obsolètes [43]. Le , AstraZeneca publie de nouveaux résultats actualisés. Avec 190 symptomatiques, l'efficacité ressort finalement à 76 % en population générale. Elle est supérieure pour les plus de 65 ans : 85 %. Avec 8 cas sévères dans le groupe placebo contre 0 dans le groupe traité, la prévention des cas sévères à 100% est confirmée dans cette étude[44].
Effets secondaires
Les effets secondaires du virus (ou du vaccin) seraient extrêmement rares selon les essais réalisées jusqu'en décembre 2020. Sur les 23 754 volontaires qui ont participé aux essais, seul un patient à qui ce vaccin a été administré a connu un « effet indésirable grave susceptible d'être lié » à cette injection (un cas de myélite transverse)[24].
En France, après quelques jours de vaccination des personnels médicaux, l'Agence nationale de sécurité du médicament (ANSM) décrit, le , des « syndromes grippaux souvent de forte intensité » constituant un « signal potentiel » (un « signal » étant défini comme une « relation entre un médicament et un effet inconnue ou non documentée »). Après 5 jours et 10 000 injections, le vaccin a fait l'objet de 149 déclarations de pharmacovigilance[45]. La forte fièvre, les maux de tête et les courbatures sont signalés comme étant intenses mais de courte durée. Pour limiter le nombre total d'arrêts de travail simultanés, la vaccination est alors prévue de façon échelonnée dans le personnel des hôpitaux[46]. Ces phénomènes d'effets secondaires sont observés principalement pour le personnel soignant. Le médecin Frédéric Adnet estime que cela est explicable par le fait que ces soignants ont probablement dus être déjà infectés par le virus : En France, le délai entre une infection et une vaccination a été fixé à trois mois. Une parade pour éviter les effets secondaires pourrait être de tester le personnel soignant pour repérer les personnes qui ont déjà été infectées[47].
« Comme [ces personnes] ont déjà des anticorps, donc une immunité, l'organisme pense de nouveau être infecté et réagit violemment. L'hypothèse que nous formulons est que nous observons ce type de réaction chez des personnes vaccinées trop tôt après la fin de la maladie. »
Au fur et à mesure de l'avancée des campagnes de vaccination dans le monde, de nouveaux effets secondaires se révèlent, comme la thrombocytopénie immunitaire prothrombotique induite par le vaccin. L’Agence européenne des médicaments ajoute, le 12 mars 2021, l’anaphylaxie et l’hypersensibilité, à la liste[48]. Ainsi, autour du 15 mars, les Pays-Bas et la République d'Irlande en suspendent-ils l'utilisation[49] - [50].
Au , des agences du médicament considèrent que les "thromboses veineuses cérébrales et viscérales abdominales, parfois associées à des diminutions des plaquettes sanguines", sont très rares[51].
Du au : 17 727 cas d'effets indésirables sont "analysés par les CRPV rapporteurs (Amiens et Rouen) sur plus de 5 318 000 injections", "la grande majorité de ces cas concerne des syndromes pseudo-grippaux, souvent de forte intensité (fièvre élevée, courbatures, céphalées)". Du au : 13 cas de colite ischémique sont observés, majoritairement chez des femmes (12 femmes pour 1 homme), d'un âge médian de 63 ans avec un délai de survenue moyen de 10 jours ; 56 cas de vascularite sont répertoriés "dont 25 considérés comme graves", 8 hommes pour 10 femmes d'un âge médian de 63,5 ans avec un délai de survenue de 7,5 jours environ[25].
En , un rapport du Comité de pharmacovigilance sur la gestion des risques (PRAC) de l’Agence européenne du médicament (EMA) relève un risque de développer le syndrome de Guillain-Barré, rare et grave atteinte neurologique, avec l’utilisation du vaccin AstraZeneca, à la suite de 156 cas rapportés dans l’Union européenne et la zone économique européenne, hors Royaume-Uni[52]. En France, dans un rapport publié le , collectant des données jusqu’au , l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) faisait état de 37 cas de syndromes de Guillain-Barré et de polyradiculonévrites chez des personnes récemment vaccinées avec AstraZeneca[53].
Performance réduite contre le variant sud-africain
Début , le Financial Times dévoile que le vaccin « a montré une efficacité significativement réduite contre la variante virale 501Y.V2. » AstraZeneca a confirmé le rapport, affirmant que son vaccin ne semble offrir qu'une protection limitée contre les maladies bénignes causées par la « variante sud-africaine » sur la base des premières données d'une étude menée par l'Université du Witwatersrand et l'Université d'Oxford[54].
L'essai mené depuis fin par le professeur Shabir Madhi, à l'université du Witwatersrand à Johannesburg, confirme que le vaccin développé par AstraZeneca « ne protège pas efficacement contre les infections du Covid-19 légères à modérées causées par le variant B.1.351 »[55]. et que le vaccin britannique offre une "protection limitée contre les formes modérées de la maladie dues au variant sud-africain, chez les jeunes adultes", à seulement 22 % [56].
Aussi, le ministre sud-africain annonce avoir commandé "20 millions de vaccins Pfizer/BioNTech pour pallier l’inefficacité du sérum AstraZeneca sur la souche locale du Covid-19"[57].
Performance confirmée contre le variant delta (anciennement dit indien)
Une étude du Public Health England publiée le montre que l'administration de deux doses du vaccin réduit de 92% le risque d'hospitalisation liée au variant delta (ex variant indien)[58].
Protection sur la durée
Selon des chercheurs britanniques dans une étude publiée en , la protection contre la Covid-19 offerte par deux doses des vaccins Pfizer/BioNTech et Oxford/AstraZeneca commence à s'estomper dans les six mois. Après cinq à six mois, l'efficacité du vaccin d'AstraZeneca-Oxford pour prévenir l'infection à la Covid-19 dans le mois qui suit la deuxième dose passe de 77 % à 67 %, montre une analyse des données recueillies dans l'étude britannique ZOE COVID. L'étude était basée sur les données de plus d'un million d'utilisateurs, comparant les infections auto-déclarées chez les participants vaccinés avec des cas dans un groupe témoin non vacciné[59] - [60].
Commandes publiques

En août 2020, le Serum Institute of India (SII) annonce que l'AZD1222 produit en Inde pourrait être commercialisé au prix de 3 dollars la dose dans les pays pauvres, en accord avec la Fondation Bill-et-Melinda-Gates[61].
En , AstraZeneca et l'université d'Oxford annoncent leur intention de produire un milliard de doses vaccinales, vendues à prix coûtant[62] - [63].
Après son autorisation en Europe, la Commission européenne a révélé les teneurs du contrat. Par erreur elle a révélé que le total des paiements est d'un minimum de 870 millions d'euros pour 300 millions de doses. La Commission s'est aussi engagée à verser environ 200 millions d'euros cinq jours après la signature du contrat, le [64].
Le vaccin commence à être livré en France le [65].
Certaines hésitations et controverses autour de ce vaccin amènent certains pays à tenter d'échanger leurs stocks contre d'autres médications[66] - [67] - [68] - [69].
Vaccination
La première dose du vaccin permet d'atteindre une bonne efficacité. « La deuxième dose permet d’assurer une protection à long terme ». Les deux doivent être injectées dans un intervalle maximal de 84 jours (12 semaines)[12].
Mises sur le marché dans le monde et campagnes de vaccination
| AMM pleine | Australie, Brésil, Canada, Corée du Sud, Malaisie, Norvège[71], Union européenne (y compris Andorre, Groenland, Îles Féroé et Islande) |
|---|---|
| AMM d'urgence | Organisation Mondiale de la Santé Afghanistan, Albanie, Arabie Saoudite, Argentine, Bahrain, Bangladesh, Colombie, Côte d'Ivoire, Equateur, Egypte, El Salvador, Ethiopie, Gambie, Grande Bretagne, Guyane, Inde, Indonésie, Irak, Kenya, Lesotho, Maldives, Maroc, Île Maurice, Mexique, Myanmar, Népal, Nigeria, Ouganda, Pakistan, Philippines, République dominicaine, Rwanda, Saint Vincent et Grenadines, Serbie, Sri Lanka, Soudan, Suriname, Taïwan, Thailande, Togo, Ukraine, Vietnam |
| Motif | Pays | |
|---|---|---|
| Non approbation | Etats-Unis, Suisse | |
| Refus d'approbation | Effets secondaires | Vénézuela |
| Renonciation définitive d'utilisation | Cas de thrombose | Danemark |
| Manque d'efficacité | Afrique du Sud |
Après quelques jours où l'injection du vaccin a été suspendue à la mi-mars 2021 dans une bonne moitié des pays européens pour cause de risque de thrombose, les vaccinations ont repris dans la plupart de ces pays, y compris en France, après que l'Agence européenne du médicament ait jugé le vaccin « sûr et efficace »[73].
| Age minimum requis pour l'injection | Pays ayant décidé cet âge minimum |
|---|---|
| 30 ans | Grèce, Royaume-Uni |
| 50 ans | Australie |
| 55 ans | Belgique, Canada, France |
| 60 ans | Allemagne, Espagne, Italie, Pays-Bas, Philippines, Portugal |
| 65 ans | Finlande, Suède |
| 70 ans | Islande |
Approbations nationales et hésitations concernant l'administration aux personnes âgées
Au , le vaccin est approuvé au Royaume-Uni[75] pour utilisation d'urgence pendant la campagne de vaccination contre la Covid-19 de ce pays. Le , l'Inde autorise l'usage de ce vaccin pour « usage restreint dans des situations d'urgence »[76]. Le , l'Agence européenne des médicaments approuve l'utilisation « conditionnelle » du vaccin « pour toutes les personnes âgées de 18 ans et plus »[77]. Le , le Canada approuve le vaccin, mais le déconseille aux personnes de 65 ans et plus[78].
_2021_C.jpg.webp)
Le , le directeur adjoint exécutif de l'Agence européenne des médicaments, Noel Wathion, annonce que les autorités européennes ne devraient pas approuver son usage avant février 2021, ajoutant que personne n'avait encore soumis une demande d'homologation à l'agence[79].
Fin , la commission de vaccination allemande déconseille le vaccin AstraZeneca pour les personnes âgées de plus de 65 ans[80], les données disponibles étant « insuffisantes pour évaluer l'efficacité du vaccin au-delà de 65 ans »[81]. En , l'Allemagne redevient favorable à l'injection aux plus âgés.
La Belgique, faute de données suffisantes sur l'efficacité pour les plus âgés, décide de ne pas administrer le vaccin aux plus de 55 ans[82]. Cependant, au cours de la première semaine de , la Belgique, comme la France, l'Allemagne et la Suède, recommande l'utilisation de l'AZD1222 aux plus de 65 ans, conformément aux préconisations de l'OMS[83]. À partir du , la France décide même de limiter provisoirement les injections aux personnes de plus de 55 ans compte-tenu de la pénurie provisoire du vaccin[73].
Aux États-Unis, quoique une usine américaine produise le vaccin, les essais cliniques et les évaluations ne permettront pas une acceptation avant [84]. Toutefois, le président Joe Biden interdit l'exportation du vaccin hors des Etats-Unis[20].
En Europe, le Vaxzevria reçoit l'autorisation de mise sur le marché complète de la part de l'Agence Européenne du médicament le . Auparavant, le vaccin ne bénéficiait que d'une autorisation conditionnelle[85].
Retards de livraison et interdiction d'exporter en dehors des États-Unis
A plusieurs reprises, et notamment au début de la campagne et à la mi-, la société AstraZeneca ne livre pas les quantités prévues contractuellement à l'Union européenne. Globalement, sur le 1er trimestre 2021, AstraZeneca livre à l'Union européenne 40 millions de doses sur une prévision initiale de 120 millions[86].
AstraZeneca impute ces retards notamment à l'interdiction faite successivement par les présidents américains Donald Trump, puis Joe Biden, d'exporter les vaccins américains, selon le principe que les citoyens américains doivent avoir la priorité sur le reste du monde[20].
Hésitations concernant l'efficacité contre des variants
De son côté, dimanche , l'Afrique du Sud annonce qu'elle suspend son programme de vaccination qui devait démarrer prochainement « avec un million de vaccins » d'AstraZeneca, à la suite d'une étude « révélant une efficacité «limitée» contre le variant sud-africain »[87].
Début , Swissmedic, l'agence suisse du médicament, « qui délivre les autorisations de mise sur le marché », estime que « des études supplémentaires sont nécessaires », les données actuellement disponibles ne permettant pas encore « de conclure à un rapport bénéfices-risques positif », avant d'autoriser le vaccin d'AstraZeneca[88].
De même aux États-Unis, le National Institute of Allergy and Infectious Diseases (NIAID) exprime ses doutes à propos de l'efficacité du vaccin, dans une déclaration parue le . Les données utilisées dans l'essai clinique leur semblent dépassées[89].
Suspensions à la suite de cas de thrombose
Les tergiversations des autorités sanitaires vis à vis du vaccin s’expliquent en grande partie par les taux d’occurrence de la « thrombocytopénie immunitaire prothrombotique induite par le vaccin (TIPIV) », variant d’un pays à l’autre[90].
Le , l'Autriche annonce cesser d'utiliser un lot (ABV5300) du vaccin, après le décès d'une infirmière de 49 ans à la suite de « graves troubles de la coagulation » quelques jours après avoir été vaccinée[91]. L'Estonie, la Lituanie, la Lettonie et le Luxembourg ont également suspendu les vaccinations avec les doses venant « de ce lot d'un million de vaccins, livré dans 17 pays ».
Le , suspectant des risques de caillots sanguins chez des personnes vaccinées, « le Danemark suspend par précaution, et jusqu'à nouvel ordre, l'utilisation du vaccin AstraZeneca »[92] - [93]. La Norvège et l'Islande suspendent le même jour l'usage du vaccin d'AstraZeneca[94] et l'Italie met au rebut tout un lot (ABV2856) du vaccin à la suite de deux accidents mortels[95]. Le 12 mars, c'est au tour du premier ministre de la Bulgarie d'arrêter la campagne, « jusqu'à ce que l'Agence européenne des médicaments (EMA) dissipe tout doute quant à son innocuité »[96], et de la Thaïlande de retarder le début de la sienne[97]. Le , l'Allemagne déclare arrêter sa campagne et l'Indonésie, prudente, retarde la sienne, « en attendant une décision de l’Organisation mondiale de la Santé »[98]. La France fait de même le soir du en attendant l'avis de l'EMA le [99].
Le , le communiqué de l'EMA déclare que les bénéfices de la vaccination surpassent les risques d'effet secondaire, et qu'aucun lien entre vaccination et augmentation de risque thrombose n'a pu être établi[100]. Or le même jour, un étudiant en médecine de 24 ans est retrouvé mort dans son appartement à Nantes, 10 jours après avoir été vacciné. L'autopsie révèle « une hémorragie interne causée par une thrombose »[101]. Et l'ANSM admet "neuf cas de thromboses des grosses veines", dont “deux décès”, rapportés en France entre le et le [102].
Le , deux cas suspects de thromboses cérébrales incitent la Finlande à cesser la vaccination avec ce vaccin[103]. En France, le , un homme de 63 ans meurt de multiples thromboses 10 jours après sa vaccination[104] et, le , une assistante sociale trentenaire meurt à Toulouse d’une thrombose survenue 14 jours après l’injection[105].
Le , la Finlande reprend la vaccination AstraZeneca pour les plus de 65 ans et l'Islande pour les plus de 70 ans[106]. Le vaccin AstraZeneca est également réservé aux plus de 65 ans en Suède[107].
Le groupe de chercheurs et de médecins « Du côté de la science » soutient, en , que les cas de thrombose peuvent être liés à des erreurs humaines. L'injection du vaccin en intraveineuse - au lieu d'être faite en intramusculaire - serait à l'origine des cas des thromboses[108] - [109].
Le , le Canada interrompt l'utilisation du vaccin pour les moins de 55 ans[110]. En Allemagne, le 30 mars 2021, l'autorité des vaccins fait état de « thrombose veineuse cérébrale (TVC) rare, dont neuf mortels, après l'administration du vaccin contre la Covid-19 d'AstraZeneca »[111], et les villes de Berlin et de Munich suspendent le vaccin pour les moins de 60 ans[112] - [113] avant que la mesure soit étendue à tout le pays le même jour[114]. En plus du Canada et de la France, la Belgique réserve le vaccin AstraZeneca aux plus de 55 ans. En plus de l'Allemagne, d'autres pays réservent le vaccin AstraZeneca aux plus de 60 ans comme l'Italie, l'Espagne, le Portugal et les Pays-Bas[115] - [116].
Le , l'EMA établit un lien entre le vaccin AstraZeneca et des cas de thrombose veineuse cérébrale (1 cas sur 100 000 vaccinations) tout en admettant ignorer ce qui provoque cette réaction[117]. Cette même agence déclarera plus tard ne pas pouvoir confirmer de lien direct entre le vaccin et le risque de thrombose, tout en ajoutant que retarder la seconde dose n'influence pas non plus les risques de thrombose[118].
Le , la Haute Autorité de santé annonce qu'en France, les moins de 55 ans vaccinés avec une première dose d’AstraZeneca auront leur deuxième dose avec un vaccin à ARN messager de Pfizer/BioNTech ou Moderna. Au Royaume-Uni, le vaccin d'AstraZeneca est réservé aux plus de 30 ans[119].
Mi-, les autorités du Danemark annoncent retirer ce vaccin de la campagne danoise[120].
Fin , « le régulateur britannique (Medicines and Healthcare products Regulatory Agency (en) – MHRA) » annonce avoir « recensé sur son sol 168 cas majeurs de caillots sanguins − dont 32 mortels − relatifs à des patients ayant reçu le vaccin d’AstraZeneca[121]. » Le , les chiffres passent à 412 cas majeurs dont 73 mortels pour environ 24 millions de vaccinations[122].
En France
En France, la vaccination avec le vaccin AstraZeneca commence le dans plusieurs établissements de santé en France ; l'Agence nationale de sécurité du médicament (ANSM) poursuit « son enquête de pharmacovigilance afin d'identifier les potentiels effets secondaires générés par la vaccination »[123].
Mi-, le président du conseil d'orientation de la stratégie vaccinale Alain Fischer, « suite à l'apparition d'effets secondaires chez de nombreux soignants après leur vaccination », notamment à Brest et à Morlaix, remet en cause l'efficacité du vaccin sur certains variants du Covid-19. L'ANSM annonce que 1,49 % des soignants vaccinés avec le vaccin AstraZeneca ont développé des « syndromes grippaux de forte intensité »[124] et recommande d'échelonner la vaccination du personnel d'un même service[125]. La vaccination pour le personnel de l'hôpital d'Arras est suspendue à la mi-février[126].
La secrétaire du Comité d'hygiène, de sécurité et des conditions de travail (CHSCT) du centre hospitalier de Périgueux fait part du pourcentage de soignants et agents ayant contracté des effets indésirables très élevé (entre 50 et 70 %) par rapport au seuil habituel de tolérance à 10 %, et demande de se tourner vers les autres vaccins[127].
Cependant, après que le vaccin a prouvé son efficacité sur le variant dit « anglais » et que les premières données en provenance d'Écosse ont montré que l'administration de la première dose permettait une baisse de plus de 80 % des hospitalisations des personnes âgées de plus de 80 ans, la Haute Autorité de santé recommande le l'administration de l'AZD1222 pour les plus de 65 ans en France également[128].
Le , à la suite d'effets secondaires aigus sur l'un des leurs, les pompiers des Bouches-du-Rhône suspendent leur vaccination[129]. Dans la foulée, le , le Président de la République Emmanuel Macron annonce qu'à la suite de l'Allemagne, la France suspend à son tour la vaccination par l'AZD1222 en attendant la recommandation officielle de l'EMA attendue pour le après-midi[130].
Le , l'EMA émet une recommandation officielle en faveur du vaccin, indiquant que le vaccin est sûr et efficace. Le Premier ministre Jean Castex annonce le soir-même la reprise de la campagne de vaccination pour le après-midi [131]. Le , la Haute autorité de santé (HAS) donne des nouvelles recommandations relatives à l'utilisation du vaccin AstraZeneca : à ce stade le vaccin ne doit être utilisé que pour les personnes âgées de 55 ans et plus ; dans l'attente de données supplémentaires les vaccins à ARN doivent être utilisés chez les personnes éligibles à la vaccination âgées de moins de 55 ans [132] . Le même jour, cette information est reprise sur le site internet grand public vaccination-info-services.fr géré par l’agence publique Santé publique France[133].
En , des médecins généralistes font part du fait qu'ils sont contraints de se débarrasser des doses, faute de candidats du fait de la réputation du vaccin[134].
À la fin d', le pôle santé publique du parquet de Paris se saisit « de trois enquêtes ouvertes à la suite de plaintes » pour « homicide involontaire », qu'ont déposées les familles des personnes décédées à la suite de la vaccination avec l'AstraZeneca[135]. Le , l'avocat de la famille de l'étudiant en médecine de Nantes, mort le après sa vaccination avec le vaccin, déclare que le rapport d'autopsie « renforce l'hypothèse d'un lien de causalité » entre l'injection et le décès[136].
En Belgique
Au , trois décès sont considérés comme « probablement liés au vaccin »[137].
Production
Au premier trimestre 2021, AstraZeneca a produit des vaccins dans l'union européenne, dont 30 millions à destination des 27 pays de l'Union européenne et 21 millions à destination du Royaume-Uni et quelques autres à destination de 32 autres pays[138].
Le Serum Institute of India (SII), « le plus gros producteur de vaccins au monde », affirme en fabriquer de 50 à 60 millions de doses de l'AZD1222[76] à Pune. Grâce à un investissement de 650 millions d'euros et au recrutement de 400 personnes, le SII crée 5 lignes de production de vaccins anti-Covid, avec comme objectif de vacciner les indiens et de fournir 600 millions de doses au GAVI[139].
Compte-tenu de capacités de production insuffisantes pour les livraisons promises en Europe, AstraZeneca décide en de s'associer avec le laboratoire allemand IDT Biologika (de) pour fabriquer des vaccins à Dessau (Allemagne) à partir de fin 2021[65].
Notes et références
(en) Cet article est partiellement ou en totalité issu de la page de Wikipédia en anglais intitulée « AZD1222 » (voir la liste des auteurs).
- (en) « Already produced 40-50 million dosages of Covishield vaccine, says Serum Institute », The Hindu, (lire en ligne)
- (en) « Conditional marketing authorisation », sur ema.europa.eu (consulté le )
- (en) « Vaxzevria (previously COVID-19 Vaccine AstraZeneca) », sur ema.europa.eu (consulté le ).
- (en) « COVID-19 Vaccine AstraZeneca authorised for use in the EU », sur astrazeneca.com, (consulté le )
- (en) « Information for Healthcare Professionals on COVID-19 Vaccine AstraZeneca », sur Medicines and Healthcare products Regulatory Agency (MHRA), (consulté le )
- (en) « Conditions of Authorisation for COVID-19 Vaccine AstraZeneca », sur Medicines and Healthcare products Regulatory Agency (MHRA), (consulté le )
- (en) Nick Walsh, Jo Shelley, Eduardo Duwe et William Bonnett, « The world's hopes for a coronavirus vaccine may run in these health care workers' veins », CNN, São Paulo, (lire en ligne [archive du ], consulté le ).
- (en) « Investigating a Vaccine Against COVID-19 » [archive du ], sur ClinicalTrials.gov, United States National Library of Medicine, (consulté le ).
- (en) « A Phase 2/3 study to determine the efficacy, safety and immunogenicity of the candidate Coronavirus Disease (COVID-19) vaccine ChAdOx1 nCoV-19 » [archive du ], sur EU Clinical Trials Register, European Union, (consulté le ).
- (en) p. O'Reilly, « A Phase III study to investigate a vaccine against COVID-19 », ISRCTN, (DOI 10.1186/ISRCTN89951424).
- (en) « AstraZeneca advances response to global COVID-19 challenge as it receives first commitments for Oxford’s potential new vaccine », sur astrazeneca.com, (consulté le ).
- Mélanie Meloche-Holubowski, « La stratégie de vaccination vouée à s’adapter à une réalité en mutation », Ici.Radio-Canada.ca, (lire en ligne).
- Le vaccin AstraZeneca va changer de nom et s'appellera désormais VaxZevria ; date=31 mars 2021 ; site=Midi libre
- « Vaccins AstraZeneca, Johnson et Johnson : 10 choses à savoir sur les thromboses », sur Santé Magazine,
- « Qu'est-ce qu'un effet indésirable ? », sur vaccin-info-service.fr,
- « Covid : pas de risque particulier de thromboses avec le vaccin d'AstraZeneca, estime l'EMA », Les Échos, (consulté le )
- (en) « COVID-19 Vaccine Trials », sur covid19vaccinetrial.co.uk (consulté le )
- (en) « Oxford team to begin novel coronavirus vaccine research », University of Oxford, (consulté le )
- Jenny Strasburg, « Oxford Developed Covid Vaccine, Then Scholars Clashed Over Money », The Wall Street Journal, (lire en ligne)
- « Joe Biden s’oppose à l’exportation de vaccins AstraZeneca vers l’Europe », La Croix, (lire en ligne)
- Arashkia A, Jalilvand S, Mohajel N, Afchangi A, Azadmanesh K, Salehi-Vaziri M, Fazlalipour M, Pouriayevali MH, Jalali T, Mousavi Nasab SD, Roohvand F, Shoja, « Severe acute respiratory syndrome-coronavirus-2 spike (S) protein based vaccine candidates: State of the art and future prospects », Reviews in Medical Virology, vol. n/a, no n/a, , e2183 (PMID 33594794, PMCID 7646037, DOI 10.1002/rmv.2183)
- Y. Watanabe, L. Mendonça, E. R. Allen, A. Howe, M. Lee, J. D. Allen, H. Chawla, D. Pulido, F. Donnellan, H. Davies, M. Ulaszewska, S. Belij-Rammerstorfer, S. Morris, A. S. Krebs, W. Dejnirattisai, J. Mongkolsapaya, P. Supasa, G. R. Screaton, C. M. Green, T. Lambe, P. Zhang, S. C. Gilbert et M. Crispin, « Native-like SARS-CoV-2 spike glycoprotein expressed by ChAdOx1 nCoV-19/AZD1222 vaccine », bioRxiv : The Preprint Server for Biology, , p. 2021.01.15.426463 (PMID 33501433, PMCID 7836103, DOI 10.1101/2021.01.15.426463)
- https://www.nytimes.com/interactive/2020/health/oxford-astrazeneca-covid-19-vaccine.html
- Audrey Le Guellec, « Vaccin AstraZeneca : quelles différences avec ceux de Pfizer et Moderna ? », sur lci.fr,
- « Vaccin AstraZeneca, composition efficacité, effets secondaires, délai », sur journaldesfemmes.fr/.
- « La position morale des évêques catholiques sur certains vaccins démentie et dénoncée », Ici.Radio-Canada.ca, (lire en ligne)
- (en) Neeltje van Doremalen, Teresa Lambe, Alexandra Spencer et Sandra Belij-Rammerstorfer, « ChAdOx1 nCoV-19 vaccination prevents SARS-CoV-2 pneumonia in rhesus macaques », bioRxiv, Microbiology, (PMID 32511340, PMCID PMC7241103, DOI 10.1101/2020.05.13.093195, lire en ligne, consulté le )
- James Gallagher, « Coronavirus : Un vaccin développé à Oxford déclenche une réponse immunitaire », BBC news, (lire en ligne)
- « Covid-19: souffrir d'allergie n'est pas une contre-indication à la vaccination », sur BFMTV, (consulté le )
- Vincent Richeux, « Choc anaphylactique après vaccin anti-COVID: le polyéthylène glycol suspecté », MedScape,
- (en) « AZD1222 vaccine met primary efficacy endpoint in preventing COVID-19 », sur astrazeneca.com (consulté le )
- (en) E. Callaway, « Why Oxford's positive COVID vaccine results are puzzling scientists », Nature, vol. 588, no 7836, , p. 16–18 (PMID 33230278, DOI 10.1038/d41586-020-03326-w, S2CID 227156970, lire en ligne)
- (en) Merryn Voysey, Sue Ann Costa Clemens, Shabir A Madhi, Lily Y Weckx, Pedro M Folegatti, Parvinder K Aley, Brian Angus, Vicky L Baillie, Shaun L Barnabas, Qasim E Bhorat, Sagida Bibi, Carmen Briner, Paola Cicconi, Andrea M Collins, Rachel Colin-Jones, Clare L Cutland, Thomas C Darton, Keertan Dheda, Christopher J A Duncan, Katherine R W Emary, Katie J Ewer, Lee Fairlie, Saul N Faust, Shuo Feng, Daniela M Ferreira, Adam Finn, Anna L Goodman, Catherine M Green, Christopher A Green, Paul T Heath, Catherine Hill, Helen Hill, Ian Hirsch, Susanne H C Hodgson, Alane Izu, Susan Jackson, Daniel Jenkin, Carina C D Joe, Simon Kerridge, Anthonet Koen, Gaurav Kwatra, Rajeka Lazarus, Alison M Lawrie, Alice Lelliott, Vincenzo Libri, Patrick J Lillie, Raburn Mallory, Ana V A Mendes, Eveline P Milan, Angela M Minassian, Alastair McGregor, Hazel Morrison, Yama F Mujadidi, Anusha Nana, Peter J O’Reilly, Sherman D Padayachee, Ana Pittella, Emma Plested, Katrina M Pollock, Maheshi N Ramasamy, Sarah Rhead, Alexandre V Schwarzbold, Nisha Singh, Andrew Smith, Rinn Song, Matthew D Snape, Eduardo Sprinz, Rebecca K Sutherland, Richard Tarrant, Emma C Thomson, M Estée Török, Mark Toshner, David P J Turner, Johan Vekemans, Tonya L Villafana, Marion E E Watson, Christopher J Williams, Alexander D Douglas, Adrian V S Hill, Teresa Lambe, Sarah C Gilbert et Andrew J Pollard, « Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK », The Lancet, (DOI 10.1016/S0140-6736(20)32661-1, lire en ligne)
- Marie Desbonnet, « Covid-19 : le vaccin AstraZeneca sera-t-il réservé aux moins de 65 ans ? », Passeport Santé,
- (en) « Single Dose Administration, And The Influence Of The Timing Of The Booster Dose On Immunogenicity and Efficacy Of ChAdOx1 nCoV-19 (AZD1222) Vaccine », sur The Lancet,
- « Covid-19: le vaccin d'AstraZeneca réduirait la transmission dès la première dose », sur huffingtonpost.fr,
- « Vaccin d'AstraZeneca et cas de thrombose, l'agence européenne des médicaments n'a pas encore abouti à une conclusion », Le Monde, (lire en ligne).
- (en) Ingrid Torjesen, « Covid-19: Les premières doses de vaccins en Écosse ont entraîné une baisse substantielle des admissions à l'hôpital », sur https://www.bmj.com, (consulté le )
- (en) Ivan F. N. Hung et Gregory A. Poland, « Single-dose Oxford–AstraZeneca COVID-19 vaccine followed by a 12-week booster », The Lancet, vol. 397, no 10277, , p. 854–855 (ISSN 0140-6736 et 1474-547X, PMID 33676614, DOI 10.1016/S0140-6736(21)00528-6, lire en ligne, consulté le )
- (en) Eleftheria Vasileiou, Colin R. Simpson, Chris Robertson et Ting Shi, « Effectiveness of First Dose of COVID-19 Vaccines Against Hospital Admissions in Scotland: National Prospective Cohort Study of 5.4 Million People », Preprint with the Lancet (prépublication), Social Science Research Network, no ID 3789264, (lire en ligne, consulté le )
- (en) « AZD1222 US Phase III trial met primary efficacy endpoint in preventing COVID-19 at interim analysis », sur pharmiweb.com,
- « ASTRAZENECA : 79% D'EFFICACITÉ DU VACCIN EN ESSAI DE PHASE 3 », sur tradingsat.com,
- « AstraZeneca devrait communiquer à nouveau sur son vaccin, dit Fauci », sur www.latribune.fr,
- « Coronavirus : Le vaccin d'AstraZeneca efficace à 76% selon les résultats actualisés d'un essai clinique mené aux US », sur www.latribune.fr,
- Corentin Lesueur avec Raphaêl Baldos, « Covid-19 : les effets secondaires du vaccin d’AstraZeneca inquiètent les hôpitaux », La Croix, (lire en ligne)
- « Santé. Covid-19 : vigilance sur les effets secondaires du vaccin AstraZeneca », sur ledauphine.com, (consulté le )
- « D'où viennent les nombreux effets secondaires du vaccin AstraZeneca ? », sur LCI.fr, (consulté le )
- https://www.huffingtonpost.fr/entry/vaccin-astrazeneca-des-allergies-severes-comme-possibles-effets-secondaires_fr_604b7a6fc5b65bed87da0ee6
- Coronavirus. Ces pays qui suspendent l’utilisation du vaccin AstraZeneca jusqu’à nouvel ordre
- La France suspend à son tour l'utilisation du vaccin AstraZeneca
- https://www.prescrire.org/fr/203/1845/60975/0/PositionDetails.aspx
- https://www.santemagazine.fr/traitement/medicaments/vaccins/vaccin-anti-covid-astrazeneca-10-choses-a-savoir-sur-les-thromboses-880450
- Soupçons de lien entre la vaccination à AstraZeneca et Janssen et des cas de syndrome de Guillain-Barré en Europe et aux Etats-Unis, usinenouvelle.com, 15 Juillet 2021
- (en) « AstraZeneca vaccine far less effective against South African Covid-19 variant », sur mybroadband.co.za,
- « « Il serait inconsidéré de jeter à la poubelle un million de doses disponibles » : en Afrique du Sud, les vaccins AstraZeneca en sursis », Le Monde, (lire en ligne).
- Coronavirus : le vaccin AstraZeneca est moins efficace face au variant sud-africain
- Inefficacité d’AstraZeneca : l’Afrique du Sud suspend son programme de vaccination
- « Variant Delta: deux doses de Pfizer ou d'AstraZeneca seraient efficaces à plus de 90% contre l'hospitalisation », sur BFM TV,
- (en) William Schomberg and Ludwig Burger, COVID vaccine protection wanes within six months - UK researchers, reuters.com, 19 août 2021
- (en) Michelle Roberts, Covid infection protection waning in double jabbed, bbc.com, 26 août 2021
- (en) « Coronavirus: India should have vaccine by December, says Serum Institute chief », Scroll.in,
- Aline Gérard, « Covid-19 : AstraZeneca fait une pause dans les essais cliniques de son vaccin », Le Parisien, no 23647, , p. 10 (rubrique Société) (lire en ligne, consulté le ). L'article est beaucoup plus complet dans la version papier du journal que dans la version à lire en ligne.
- Thuy-Diep Nguyen, « Pourquoi le retour d'AstraZeneca dans la course au vaccin anti-Covid est une bonne nouvelle », Challenges, (lire en ligne, consulté le ).
- Claudia Cohen, « Vaccins anti-Covid : le montant du contrat entre AstraZeneca et l'UE révélé à cause d'une grossière erreur », Le Figaro, (lire en ligne)
- Frédéric Bianchi, « AstraZeneca s'associe à l'allemand IDT Biologika pour produire plus de vaccins en Europe », BFMTV, (lire en ligne)
- Covid-19 : des États se débarrassent de leurs doses du vaccin AstraZeneca
- South Africa may swap or sell AstraZeneca's Covid-19 vaccine
- L'Afrique du Sud a revendu toutes ses doses du vaccin AstraZeneca
- Voir les références dans l'article de Wikipedia en anglais : COVID-19 vaccine
- Suspension provisoire, voir : « La Norvège prolonge la pause du vaccin AstraZeneca jusqu'au 15 avril », Le Figaro, (lire en ligne)
- « Vaccination : Le Danemark, premier pays d’Europe à renoncer définitivement au vaccin d’AstraZeneca »,
- Nicolas Berrod, « AstraZeneca : la vaccination va reprendre seulement pour les plus de 55 ans », Le Parisien, (lire en ligne)
- « Vaccin d'AstraZeneca : des recommandations tous azimuts en Europe », Les Échos, (lire en ligne)
- (en) « Covid-19: Oxford-AstraZeneca coronavirus vaccine approved for use in UK », sur BBC News, BBC, (consulté le )
- Agence France-Presse, « L'Inde autorise deux vaccins contre la COVID-19 », Ici.Radio-Canada.ca, (lire en ligne)
- Agence France-Presse, « Le régulateur européen approuve le vaccin AstraZeneca », Ici.Radio-Caanda.ca, (lire en ligne)
- François Messier, « Santé Canada autorise le vaccin d'AstraZeneca contre la COVID-19 », Ici.Radio-Canada.ca, (lire en ligne)
- (en) « AstraZeneca vaccine not ready for quick European approval, watchdog official says », sur reuters.com, Reuters, (consulté le )
- AFP et 20 Minutes, « Coronavirus : Face aux doutes allemands, AstraZeneca défend l’efficacité de son vaccin », sur msn.com,
- franceinfo et AFP, « Covid-19 : l'Allemagne déconseille le vaccin AstraZeneca pour les personnes âgées de plus de 65 ans », FranceInfo, (lire en ligne)
- Le Parisien avec AFP, « Suisse, Belgique… ces pays qui restent prudents avec le vaccin AstraZeneca », Le Parisien, (lire en ligne)
- « France, Allemagne, Belgique, Suède: ces États qui élargissent finalement l'accès au vaccin AstraZeneca », sur bfmtv.com,
- https://www.lapresse.ca/international/etats-unis/2020-12-30/vaccin-astrazeneca-oxford/les-etats-unis-misent-sur-une-autorisation-en-avril.php
- « AstraZeneca: AMM complète pour le vaccin Covid dans l'UE », sur boursorama,
- « Covid-19 : AstraZeneca annonce de nouveaux retards de livraison de son vaccin à l’Union européenne », Le Monde, (lire en ligne)
- Le Figaro et AFP, « L'Afrique du Sud suspend les vaccinations après une étude révélant l'efficacité limitée du vaccin AstraZeneca contre son variant », Le Figaro, (lire en ligne)
- La Provence (avec AFP), « Coronavirus : la Suisse demande de "nouvelles études" sur le vaccin AstraZeneca », La Provence, (lire en ligne)
- https://www.futura-sciences.com/sante/actualites/vaccin-anti-covid-astrazeneca-efficacite-vaccin-remise-question-agence-sante-americaine-86391/
- https://www.ledevoir.com/societe/science/597938/astrazeneca-les-risques-du-vaccin-remis-en-perspective
- « Accidents thrombo-emboliques : le vaccin d'AstraZeneca est-il en cause ? », sur Accidents thrombo-emboliques : le vaccin d'AstraZeneca est-il en cause ? (consulté le )
- « Coronavirus : le Danemark suspend jusqu'à nouvel ordre l'utilisation du vaccin AstraZeneca », sur France Bleu, (consulté le )
- « Le Danemark suspend le vaccin d’AstraZeneca », sur LeFigaro.fr (consulté le )
- « Le Danemark, la Norvège et l'Islande suspendent l’usage du vaccin d’AstraZeneca », Ici.Radio-Canada.ca, (lire en ligne)
- « Le vaccin Covid-19 d’AstraZeneca suspendu au Danemark, l'Italie écarte un lot ! », sur Capital.fr, (consulté le )
- « Le vaccin Covid-19 d’AstraZeneca suspendu par la Bulgarie ! », sur Capital.fr, (consulté le )
- https://www.ouest-france.fr/sante/vaccin/coagulation-les-x-polemiques-autour-du-vaccin-d-astrazeneca-7183417
- AFP, « L'Indonésie reporte le lancement de la vaccination avec AstraZeneca », sur Le Journal de Montréal (consulté le )
- « Le vaccin "COVID-19 Vaccine AstraZeneca" suspendu par précaution en France avant un nouvel avis de l'Agence européenne des médicaments », sur Le vaccin "COVID-19 Vaccine AstraZeneca" suspendu par précaution en France avant un nouvel avis de l'Agence européenne des médicaments (consulté le )
- (en) « Investigation of COVID-19 Vaccine AstraZeneca and thromboembolic events continues », sur Site web officiel de l'European Medecines Agency,
- https://www.ouest-france.fr/sante/virus/coronavirus/astrazeneca-enquete-ouverte-apres-le-deces-d-un-etudiant-en-medecine-a-nantes-0a3ad804-8b34-11eb-be07-a782e4049e5a
- https://www.huffingtonpost.fr/entry/vaccin-astrazeneca-lansm-confirme-un-risque-de-thrombose-rare_fr_605e422bc5b6531eed04d7b5
- https://www.francetvinfo.fr/sante/maladie/coronavirus/vaccin/astrazeneca-la-finlande-suspend-le-vaccin-malgre-le-feu-vert-europeen_4339785.html
- https://www.ledauphine.com/sante/2021/03/30/annecy-un-sexagenaire-decede-de-thromboses-10-jours-apres-son-injection-par-astrazeneca
- https://www.lavoixdunord.fr/972254/article/2021-03-31/astrazeneca-une-femme-de-38-ans-meurt-toulouse
- « AstraZeneca: la Finlande et l’Islande vont reprendre la vaccination pour certains aînés »
- « Covid-19 dans le monde : AstraZeneca annonce que son vaccin est efficace à 76 %, la Suède reprend la vaccination pour les plus de 65 ans »
- Lucas Person et Margot Brunet, « Vaccin AstraZeneca : une nouvelle théorie sur les cas de thromboses », sur www.marianne.net, 2021-04-06utc07:00:00+0000 (consulté le )
- "Nous ne savons pas trop sur quelle base cette décision a été prise", s'interroge le chercheur en immunologie, https://www.industrie-techno.com/article/astrazeneca-et-si-les-thromboses-etaient-causees-par-l-injection-accidentelle-du-vaccin-dans-le-sang.64404
- https://www.dailymail.co.uk/health/article-9415509/Canadian-panel-recommends-AstraZeneca-pause-55.html
- https://www.msn.com/fr-fr/actualite/monde/coronavirus-des-cas-de-thrombose-c%C3%A9r%C3%A9brale-signal%C3%A9s-en-allemagne-apr%C3%A8s-le-vaccin-astrazeneca/ar-BB1f7rtZ
- https://www.lindependant.fr/2021/03/30/astrazeneca-des-thromboses-cerebrales-signalees-en-allemagne-berlin-suspend-le-vaccin-chez-les-moins-de-60-ans-9458905.php
- https://www.swp.de/panorama/corona-impfung-astrazeneca-thrombose-nebenwirkungen-berlin-muenchen-impfen-impftermin-55997820.html
- « Vaccination : L'Allemagne suspend le vaccin AstraZeneca pour les moins de 60 ans »
- « Covid-19 : la Belgique réserve le vaccin AstraZeneca aux plus de 55 ans, l'Italie et l'Espagne aux plus de 60 ans »
- « Le Portugal limite à son tour le vaccin AstraZeneca aux plus de 60 ans »
- L'EMA établit un lien entre le vaccin AstraZeneca et des cas de thrombose-presse, boursorama.com, 6 avril 2021
- « Covid : pas de risque particulier de thromboses avec le vaccin d'AstraZeneca, estime l'EMA », sur Les Echos, (consulté le )
- « AstraZeneca : pour leur 2e dose, les moins de 55 ans auront le vaccin Pfizer ou Moderna »
- Magazine Marianne, « Covid : pourquoi le Danemark abandonne le vaccin AstraZeneca », sur www.marianne.net, 2021-04-14utc15:26:54+0000 (consulté le )
- « Covid19 dans le monde: le variant indien détecté en Belgique chez des étudiants passés par Roissy », Le Monde, (lire en ligne).
- « Coronavirus vaccine - weekly summary of Yellow Card reporting »,
- « Vaccin AstraZeneca : les effets secondaires observés en France », sur MediSite,
- « Alain Fischer recommande de ne pas administrer le vaccin d'AstraZeneca aux soignants du département de Moselle », La Dépêche, (lire en ligne)
- « Covid-19 : vigilance sur les effets secondaires du vaccin AstraZeneca », Le Bien public,
- Philippe Gaudin, « Covid-19 : vigilance sur les effets secondaires du vaccin AstraZeneca », sur bfmtv.com,
- Des agents de l’hôpital de Périgueux dénoncent les effets du vaccin AstraZeneca ; site:Journal régional français Sud Ouest ; date=16 février 2021 ; consulté le:6 mars 2021.
- « Le vaccin AstraZeneca contre le Covid-19 désormais recommandé pour les plus de 65 ans », sur lemonde.fr,
- https://www.lanouvellerepublique.fr/a-la-une/astrazeneca-les-pompiers-des-bouches-du-rhone-suspendent-leur-utilisation-du-vaccin
- « La France suspend pour 24 heures le vaccin AstraZeneca, annonce Emmanuel Macron », sur lci.fr,
- « La campagne de vaccination avec AstraZeneca relancée dès ce vendredi en France », sur lesechos.fr,
- « Avis n° 2021.0018/AC/SEESP du 19 mars 2021 du collège de la Haute Autorité de santé sur la place du vaccin AstraZeneca dans la stratégie vaccinale à la suite de l'avis de l’agence européenne des médicaments concernant des évènements indésirables survenus dans plusieurs pays européens chez des personnes vaccinées », sur Haute Autorité de Santé (consulté le )
- « COVID-19 », sur vaccination-info-service.fr (consulté le )
- « AstraZeneca : "Un crève-cœur" pour ces médecins contraints de jeter des doses inutilisées », sur Lci,
- https://www.francebleu.fr/infos/faits-divers-justice/vaccin-astrazeneca-apres-des-deces-le-parquet-de-paris-se-saisit-de-trois-plaintes-dont-une-a-1619609372
- https://www.francebleu.fr/infos/sante-sciences/etudiant-decede-a-nantes-l-hypothese-d-un-lien-avec-le-vaccin-astrazeneca-renforcee-selon-l-avocat-1619890658
- L'agence fédérale des médicaments et des produits de santé (AFMPS) a également enregistré 163 décès, « mais sans nécessairement pouvoir établir un lien causal »
- https://www.nicematin.com/faits-de-societe/pourquoi-leurope-va-t-elle-bloquer-les-exportations-de-vaccin-astrazeneca-662676
- Rajesh Lawale, « L'Inde précipite ses cadences », Challenges, (lire en ligne)
Voir aussi
Articles connexes
Liens externes
- Ressources relatives à la santé :