Calcination
La calcination, dans l'acception moderne du terme, est une opération consistant à chauffer intensément dans une enceinte fermée un corps inerte, afin de le décomposer ou de déclencher des réactions chimiques.
De manière plus précise, la calcination est un cas particulier de thermolyse, consistant en une décarbonatation. Étymologiquement, la calcination est en effet la transformation du calcaire en chaux par chauffage dans un four à chaux (réaction de décarbonatation).
Définition physique
À la fin du XVIIe siècle, on entendait par le mot « calcination », l'action de transformer le carbonate de calcium en chaux vive par chauffage du matériau, opération qui dégage du dioxyde de carbone, mais on l'étendait aussi en général à toute opération qui consistait à traiter par le feu une substance quelconque jusqu'à ce qu'elle ait perdu les matières décomposables ou volatiles qu'elle contenait. Les anciens chimistes croyaient en effet que les métaux chauffés au contact de l'air perdaient du phlogistique et revenaient à l'état de chaux et, pour cette raison, donnaient également à cette opération le nom de calcination. Il est reconnu maintenant qu'il s'agit de simples oxydations[1]. On donnait à la calcination deux objets[2] :
- la production de chaux et de plâtre ;
- la séparation des substances volatiles d'une substance qu'on veut isoler, comme dans la calcination des minerais.
Le résidu se nommait dans les deux cas « chaux ».
De nos jours, on étend souvent le sens de la calcination à la chauffe en présence d'air, c'est-à-dire d'oxygène, d'un corps afin de lui faire subir une action chimique : oxydation, réduction, etc.[3]. Cependant, lorsque les réactions chimiques avec l'air deviennent importantes, le terme « grillage » est plus précis.
Historique
Au début du XVIIIe siècle, le chimiste allemand Georg Ernst Stahl attribuait la perte au feu à un fluide qui sortait du corps lors de la combustion, le phlogistique. Cette théorie ne permettait pas d'interpréter une perte au feu négative, et a été balayée par la découverte de l'oxygène par Priestley : pour rendre compte du bilan de masse dans les combustions, Lavoisier lui substitua alors la théorie du calorique.
Réactions chimiques et physiques
Lors du chauffage, il se produit diverses réactions qui modifient l'échantillon :
- à 100 °C : l'eau libre se vaporise ;
- au-dessus, l'eau liée se libère (par exemple molécules d'eau liées dans le gypse, l'argile) (voir adsorption et désorption) ;
- vers 550 °C : sous air ou atmosphère oxydante, la matière organique brûle donnant du dioxyde de carbone (CO2) ou du graphite (C) ;
- le carbone s'oxyde lentement pour former du dioxyde de carbone ou du monoxyde de carbone ;
- les carbonates se décomposent, par exemple : CaCO3 → CaO + CO2
- sous air ou atmosphère oxydante, les métaux s'oxydent ;
- les sels volatils se vaporisent.
Les conditions de chauffage sont capitales :
- chauffage à la flamme : une flamme peut comporter des zones oxydantes et des zones réductrices, selon les conditions de combustion ;
- chauffage en four ou par induction : on peut travailler sous air (environnement oxydant) ou sous atmosphère neutre.
Perte au feu
Utilisation en analyse des roches
Lors de la chauffe d'un minéral, on peut avoir :
- une perte de masse du fait du départ des espèces volatiles : c'est la perte au feu ;
- un gain de masse dû à l'incorporation d'atomes d'oxygène (oxydation), on parle alors de « perte au feu négative » ou parfois de « gain au feu » (gain on ignition, GOI).
La « perte au feu » ou « LOI » (en anglais : loss on ignition) est simplement la différence de masse : perte au feu = masse avant calcination m0 - masse après calcination m1 on l'exprime parfois en pourcentage : perte au feu (%) = 100 × (m0 - m1) / m0.
Un cas typique est celui de l'analyse des roches. La perte au feu provoque une transformation du calcaire évoquée ci-dessus, mais si l'on n'est pas sous atmosphère neutre, cela provoque aussi l'oxydation de l'oxyde de fer : FeO → Fe3O4 → Fe2O3.
Dans ce cas-là, il faut titrer le fer(II) sur l'échantillon frais d'une autre manière, par exemple par voie humide, afin d'appliquer une correction exacte[4].
Utilisation en chimie analytique
La calcination est une technique de préparation d'échantillon utilisée en chimie analytique qui permet de prendre en compte ce phénomène. Elle consiste à chauffer l'échantillon à haute température (typiquement 500 à 1 000 °C) sous air ou sous atmosphère neutre pour provoquer des réactions physiques et chimiques et mettre ainsi l'échantillon dans un état de référence.
En effet, un certain nombre de propriétés des matériaux dépendent de la température et de l'historique de l'échantillon comme de l'humidité. La calcination permet de l'abstraire de ces effets et donc d'avoir des mesures reproductibles, de pouvoir comparer différents échantillons. En revanche, il faut être conscient que l'échantillon analysé n'est pas l'échantillon prélevé. La méthode est similaire à l'analyse des extraits secs mais utilise une température plus élevée.
Procédés

La méthode des calcaroni est une technique italienne d'extraction du soufre par calcination de pyrites sulfureuses, déployée surtout en Sicile vers 1850.
On dresse une enceinte circulaire en pierre au flanc d'un coteau : en bas de cette enceinte, on creuse une rigole dite morto d'une profondeur de 1,20 à 1,80 m, et large de 60 cm ; ce fossé est recouvert d'un abri en planches pour l'ouvrier. Les calcaroni peuvent contenir jusqu'à 6 l de soufre. On utilisait généralement cette installation une dizaine d'années. On sélectionnait les plus grosses pierres et on en faisait la couche de base, en ménageant des vides entre les pierres ; à mesure qu'on empilait des pierres plus petites, la taille des interstices diminuait naturellement. Deux petites ventelles dirigées vers le bas, d'environ 60 cm, était pratiquées de part et d'autre du tas pour évacuer l'air chaud. On recouvrait le tout d'une couche de rebut des opérations précédentes[5]. On donnait une inclinaison d'environ 10° à la base du tas[6]. Le soufre fondu descend lentement dans le Morto, où le soufre se fige en lingots appelés « balate »[6]. On pouvait traiter par ce procédé environ 2 000 m3 de minerais en 20-30 jours[6].
Quoiqu'ils diminuassent considérablement la quantité de vapeurs toxiques et les pertes, les Calcaroni n'avaient encore qu'un rendement de 50% à cause de la quantité de soufre relarguée en fumées[6], fumées d'ailleurs corrosives.
En 1870, on comptait 4 367 calcaroni en Sicile[5].
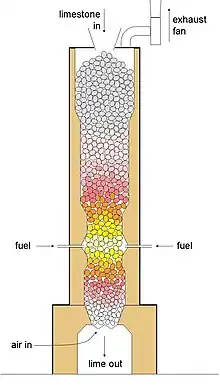
Le procédé industriel historique de calcination est le four à cuve vertical. Les fours rotatifs, très utilisés en cimenterie pour la production de clinker sont également bien adaptés. Ces deux types de fours travaillent à plus de 900 °C comme des réacteurs à contre-courant où les gaz échangent leur chaleur à des solides. Mais leur conception, très différente, se traduit par des intérêts distincts. Dans la production de chaux, on constate que :
- les fours rotatifs produisent au maximum 1 000 t/j avec des fines granulométries. Leur consommation énergétique est de 5 020 à 5 440 MJ/t car les pertes énergétiques sont importantes ;
- les fours à cuve verticaux, dont les plus récents ont une capacité de 600 t/j, traitent des granulométries plus élevées, de 15 à 150 mm, avec une consommation énergétique de l’ordre de 3 350 MJ/t[7].
Pour la calcination des minerais de phosphates, les productions sont plus importantes et peuvent atteindre 6 000 t/j. La calcination sert à éliminer la matière organique ou la gangue carbonatée. On rencontre les fours rotatifs, des fours à lit fluidisé, ou à calcination éclair ou flash (selon un principe proche de la fusion flash). Les fours rotatifs sont pénalisés par la formation d’anneaux, ceux à lit fluidisé sont sensibles à la prise en masse[7].
Notes et références
- William Duckett, Dictionnaire de la conversation et de la lecture : inventaire raisonné des notions générales les plus indispensables a tous, vol. 4, Firmin Didot, 1868, lire en ligne.
- Jean Élie Bertrand, Descriptions des arts et métiers, vol. 2, L'imprimerie de la Société Typographique, 1774, lire en ligne.
- CNRTL, Définition.
- P. J. Lechler et M. O. Desilets, « A review of the use of loss on ignition as a measurement of total volatiles in whole-rock analysis », Chemical Geology, vol. 63, , p. 341-344.
- Warnford Lock, « Sulphur and its Extraction », Popular Science Monthly, vol. 26, , p. 482–495.
- (en) Gerald Kutney, Sulfur. History, Technology, Applications & Industry, Toronto, ChemTec Publishing (réimpr. 2) (ISBN 978-1-895198-67-6).
- Pierre Blazy et El-Aid Jdid, « Métallurgie extractive - Pyrométallurgie », dans Techniques de l'ingénieur, Éditions techniques de l'ingénieur, (lire en ligne).