Fluorotoluène
Le fluorotoluène ou fluorométhylbenzène est un composé aromatique de formule C7H7F. Il est constitué d'un cycle benzénique substitué par un groupe méthyle et un atome de fluor. Comme tous les benzènes disubstitués, il existe sous la forme de trois isomères structuraux, les composés ortho, méta et para, selon la position relative des deux substituants sur le cycle.
Le fluorure de benzyle, parfois appelé α-fluorotoluène, est un isomère des fluorotoluènes où le fluor est substitué sur le groupe méthyle, mais il n'est pas considéré à proprement parler comme un fluorotoluène.
Propriétés
| Fluorotoluène | |||
| Nom | 2-Fluorotoluène | 3-Fluorotoluène | 4-Fluorotoluène |
| Autres noms | 1-Fluoro-2-méthylbenzène o-fluorotoluène orthofluorotoluène |
1-Fluoro-3-méthylbenzène m-fluorotoluène métafluorotoluène |
1-Fluoro-4-méthylbenzène p-fluorotoluène parafluorotoluène |
| Représentation | 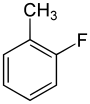 |
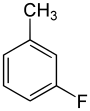 |
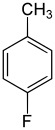 |
| Numéro CAS | |||
| ECHA | 100.002.208 | 100.005.932 | 100.005.928 |
| PubChem | 7241 | 9606 | 9603 |
| Formule brute | C7H7F (C6H4FCH3) | ||
| Masse molaire | 110,13 g mol−1 | ||
| État (CNTP) | liquide | ||
| Apparence | liquide incolore odeur caractéristique[1] |
liquide incolore odeur aromatique[2] |
liquide incolore odeur aromatique[3] |
| Point de fusion | −62 °C[1] | −88 °C[2] | −57 °C[3] |
| Point d'ébullition | 114 °C[1] | 116 °C[2] | 117 °C[3] |
| Masse volumique (20 °C) | 1,00 g·cm-3[1] | 1,00 g·cm-3[2] | 1,00 g·cm-3[3] |
| Pression de vapeur saturante | 25 hPa (20 °C)[1] | 21,5 hPa (20 °C)[2] | 23 hPa (20 °C)[3] |
| Point d'éclair (coupelle fermée) |
8 °C[1] | 9 °C[2] | 10 °C[3] |
| Solubilité (eau) |
pratiquement insoluble [1] - [2] | 0,2 g l−1 (20 °C)[3] | |
| Coefficient de partage octanol/eau (LogP) |
2,740[4] | 2,75[5] | 2,58[6] |
| SGH |
  [1] |
 [2] |
  [3] |
| Phrases H et P | H225 et H335 [1] |
H225 [2] |
H225, H315, H319 et H335 [3] |
| P210, P240 et P403+P233 |
P210, P370+P378 et P403+P235 |
P210, P304+P340 et P337+P313 P280, P312 et P332+P313 | |
Les fluorotoluènes se présentent sous la forme de liquide incolores, pratiquement insolubles dans l'eau. Les points de fusion des composés ortho et para sont relativement proches et bien plus élevés que celui composé méta. Cela peut s'expliquer par les fortes liaisons électrostatiques fluor-hydrogène des groupes méthyle, intramoléculaires pour le composé ortho et intermoléculaires pour le composé para. Les points de vaporisation de trois isomères sont par contre eux tous très proches, et également très proche de celui du toluène (111 °C). Les trois isomères sont hautement volatils, très inflammables (points d'éclair proche de 10 °C) et leur vapeurs forment des mélanges explosifs avec l'air.
Utilisations
Le 4-fluorotoluène a été utilisé en oxydation en phase vapeur catalysée par l'oxyde de vanadim/oxyde de titane pour former le 4-fluorobenzaldéhyde[7].
Le 3-fluorotoluène a été utilisé pour a génération de cations tolyle par ionisation chimique en spectrométrie de masse[8].
Notes et références
- Entrée « 2-Fluorotoluene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- Entrée « 3-Fluorotoluene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- Entrée « 4-Fluorotoluene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- Fiche (en) « Fluorotoluène », sur ChemIDplus, consulté le 6 septembre 2020.
- Fiche (en) « Fluorotoluène », sur ChemIDplus, consulté le 6 septembre 2020.
- Fiche (en) « Fluorotoluène », sur ChemIDplus, consulté le 6 septembre 2020.
- Sushil K. Maurya, Pratap Patil, Shubhangi B.Umbarkar, Mukund K. Gurjar, Mohan Dongare, Stephan Rudiger, Erhard Kemnitz, « Vapor phase oxidation of 4-fluorotoluene over vanadia–titania catalyst », Journal of Molecular Catalysis A: Chemical, vol. 234, nos 1-2, , p. 51-57 (DOI 10.1016/j.molcata.2005.02.020)
- T G Heath, J Allison, J T Watson, « Selective detection of the tolyl cation among other [C7H 7] (+) isomers by ion/molecule reaction with dimethyl ether », Journal of the American Society for Mass Spectrometry, vol. 2, no 4, , p. 270-7 (DOI 10.1016/1044-0305(91)80018-3)
Voir aussi
- Fluorure de benzyle ou α-fluorotoluène
- Difluorotoluène
- Trifluorotoluène
- Tétrafluorotoluène
- Pentafluorotoluène
| –F | –Cl | –Br | –I | |
|---|---|---|---|---|
| Benzène | Fluorobenzène | Chlorobenzène | Bromobenzène | Iodobenzène |
| Phénol (–OH) | Fluorophénol | Chlorophénol | Bromophénol | Iodophénol |
| Aniline (–NH2) | Fluoroaniline | Chloroaniline | Bromoaniline | Iodoaniline |
| Anisole (–OCH3) | Fluoroanisole | Chloroanisole | Bromoanisole | Iodoanisole |
| Toluène (–CH3) | Fluorotoluène | Chlorotoluène | Bromotoluène | Iodotoluène |
| Nitrobenzène (–NO2) | Fluoronitrobenzène | Chloronitrobenzène | Bromonitrobenzène | Iodonitrobenzène |
| Alcool benzylique (–CH2OH) | Alcool fluorobenzylique | Alcool chlorobenzylique | Alcool bromobenzylique | Alcool iodobenzylique |
| Benzaldéhyde (–CHO) | Fluorobenzaldéhyde | Chlorobenzaldéhyde | Bromobenzaldéhyde | Iodobenzaldéhyde |
| Acide benzoïque (–COOH) | Acide fluorobenzoïque | Acide chlorobenzoïque | Acide bromobenzoïque | Acide iodobenzoïque |