Dioxyde de thorium
Le dioxyde de thorium est un composé chimique de formule ThO2. Il se présente comme une poudre cristalline blanche, jadis connue sous le nom de thoria ou thorina. Il s'agit essentiellement d'un sous-produit de la production d'uranium et des lanthanides. La thorianite en est la forme minérale, relativement rare. Le nitrate de thorium Th(NO3)4 est un intermédiaire dans sa production.
| Dioxyde de thorium | |
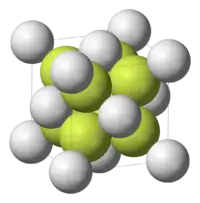
| |
| __ Th4+ __ O2− Maille cristalline du dioxyde de thorium. |
|
| Identification | |
|---|---|
| Nom UICPA | dioxothorium |
| Synonymes |
thoria, thorina, oxyde de thorium, thorianite, thorotrast, thortrast, umbrathor, oxyde de thorium(IV), thorium anhydre... |
| No CAS | |
| No ECHA | 100.013.842 |
| No CE | 215-225-1 |
| PubChem | 14808 |
| ChEBI | 37339 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | ThO2 |
| Masse molaire[1] | 264,036 9 ± 0,000 6 g/mol O 12,12 %, Th 87,88 %, |
| Propriétés physiques | |
| T° fusion | 3 390 °C |
| T° ébullition | 4 400 °C |
| Masse volumique | 9,86 g·cm-3 |
| Précautions | |
 Composé radioactif |
|
| SGH[2] | |
  Danger |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés générales
Ce composé, radioactif en raison du thorium, peut être utilisé comme combustible nucléaire. Il s'agit d'une céramique particulièrement réfractaire, ayant un point de fusion de l'ordre de 3 390 °C, le plus élevé de tous les oxydes — seuls quelques éléments, tels que le tungstène et le carbone, ainsi que quelques composés, tels que le carbure de tantale TaC ou le carbure d'hafnium HfC, ont un point de fusion supérieur (céramiques ultraréfractaires).
L'oxyde de thorium est très faiblement soluble dans l'eau, à pH inférieur à 4.
Sa structure cristalline est celle de la fluorine, partagée par quelques oxydes binaires tels que le dioxyde d'uranium UO2, le dioxyde d'hafnium HfO2 et le dioxyde de cérium CeO2, ainsi que le dioxyde de plutonium PuO2. La largeur de la bande interdite de ThO2 est d'environ 6 eV.
Utilisations
- L'une des principales utilisations passées du ThO2 était dans les manchons à incandescence, contenant parfois 99 % de dioxyde de thorium. On en trouve encore parfois aujourd'hui, mais c'est l'oxyde d'yttrium(III) Y2O3 qui est de plus en plus employé dans cet usage.
- Le ThO2 a été utilisé en radiologie comme contrastant (Thorotrast) dans la première moitié du XXe siècle, très efficace mais très cancérogène (développement de cholangiocarcinomes) ; il a été remplacé dans cet usage par le sulfate de baryum BaSO4.
- Le ThO2 était autrefois ajouté au verre pendant sa fabrication pour en augmenter l'indice de réfraction, conduisant à des verres au thorium contenant jusqu'à 40 % de ThO2 destinés à la fabrication de lentilles de qualité pour les appareils photo et des instruments scientifiques : le verre contenant de l'oxyde de thorium a un indice de réfraction élevé et une faible dispersion, ce qui diminue l'aberration optique ; l'oxyde de thorium est aujourd'hui remplacé par l'oxyde de lanthane La2O3, non radioactif et par conséquent qui ne dégrade pas le verre sous l'effet de son propre rayonnement (le verre au thorium tendait à jaunir ou à brunir avec le temps).
- Le ThO2 a été utilisé jusqu'au début du siècle comme stabilisant dans les électrodes au tungstène pour soudage TIG, les tubes électroniques et dans les moteurs d'avions. Les alliages métalliques de tungstène au thorium se déforment peu car la température de fusion élevée de l'oxyde de thorium améliore les propriétés mécaniques de ces alliages à haute température. Il tend néanmoins à être remplacé par des oxydes non radioactifs, tels que ceux de cérium, de lanthane et de zirconium.
- Le ThO2 est un catalyseur dans de nombreuses réactions chimiques : la cyclisation de Ruzicka, le craquage du pétrole et la conversion de l'ammoniac NH3 en acide nitrique HNO3 notamment.
- L'yttralox est une céramique transparente constituée d'une solution solide d'oxyde d'yttrium(III) Y2O3 contenant environ 10 % de dioxyde de thorium.
Risques sanitaires
Le dioxyde de thorium est irritant pour la peau et les yeux. Il peut pénétrer dans l'organisme par une lésion cutanée et présente dans ce cas une forte toxicité. Il se dépose dans les poumons par inhalation et peut y demeurer suffisamment longtemps pour produire des lésions par irradiation. Il s'accumule dans les tissus et peut y subsister plusieurs dizaines d'années, d'où son caractère cancérogène à long terme.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Thorium oxide » [PDF], sur https://www.sigmaaldrich.com/, Sigma-Aldrich, (consulté le ).