Triméthylphosphine
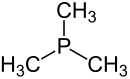
La triméthylphosphine est un composé organophosphoré de formule P(CH3)3, souvent abrégée PMe3. C'est un liquide incolore avec une forte odeur incommodante, caractéristique des alkylphosphines. C'est un composé couramment utilisé comme ligand en chimie des complexes.
| Triméthylphosphine | |||
  |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | triméthylphosphane | ||
| No CAS | |||
| No ECHA | 100.008.932 | ||
| No CE | 209-823-1 | ||
| PubChem | 68983 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide clair à incolore[1] | ||
| Propriétés chimiques | |||
| Formule | C3H9P [Isomères] |
||
| Masse molaire[2] | 76,077 3 ± 0,003 g/mol C 47,36 %, H 11,92 %, P 40,71 %, |
||
| pKa | 8,65 | ||
| Moment dipolaire | 1,19 D | ||
| Propriétés physiques | |||
| T° fusion | −86 °C[1] | ||
| T° ébullition | 38 à 40 °C[1] | ||
| Masse volumique | 0,738 g·cm-3 (20 °C)[1] | ||
| Point d’éclair | −19 °C (coupelle fermée)[1] | ||
| Pression de vapeur saturante | 499,0 hPa (20 °C) 1 643,3 hPa (55 °C)[1] |
||
| Cristallographie | |||
| Structure type | pyramide trigonale | ||
| Propriétés optiques | |||
| Indice de réfraction | 1,428[1] | ||
| Précautions | |||
| SGH[1] | |||
  Danger |
|||
| NFPA 704[1] | |||
| Transport[1] | |||
|
|||
| Écotoxicologie | |||
| LogP | 1,370[3] | ||
| Composés apparentés | |||
| Autres composés | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
Structure et liaisons
La triméthylphosphine possède une géométrie moléculaire de type pyramide trigonale avec une symétrie approximativement C3v — le même groupe de symétrie moléculaire que l'ammoniac (NH3) et la phosphine (PH3). Les angles de liaison C–P–C sont d'environ 98,6°[4] . Cette caractéristique est consistante avec le fait que le phosphore utilise principalement ses orbitales 3p pour former des liaisons, avec relativement peut d'hybridation sp, ce fait étant commun dans la chimie du phosphore, le gap entre les orbitales 3s et 3P étant plus important que celui entre les orbitales 2s et 2p où se trouvent les électrons de valence du carbone, de l'azote et de l'oxygène (qui eux présentent une forte hybridation sp). En conséquence, le double non-liant de la triméthylphosphine a un caractère s prédominant, comme dans le cas de la phosphine (PH3)[5].
Synthèse
PMe3 est habituellement préparé par réaction entre le phosphite de triphényle et le chlorure de méthylmagnésium[6] :
- 3 CH3MgCl + P(OC6H5)3 → P(CH3)3 + 3 C6H5OMgCl
La synthèse se fait dans l'éther dibutylique, à partir duquel le PMe3, plus volatil, peut être distillé.
Réactions
Réactions acide-base
Avec un pKA de 8,65, PMe3 réagit avec les acides forts pour former des sels [HPMe3]X[4]. Cette réaction est réversible. Avec des bases fortes, telles que les organolithiens, le groupe méthyle peut subir une déprotonation et former PMe2CH2Li.
PMe3 peut facilement être oxydé en oxyde de phosphine par le dioxygène. Elle peut aussi facilement être alkylée pour former des dérivés phosphonium, RPMe3+. Le composé est cependant stable dans l'eau.
Chimie de coordination
La triméthylphosphine est un ligand hautement basique qui forme des complexes avec la plupart des métaux. En tant que ligand, son angle conique de Tolman est de 118°[7]. Cet angle est une indication de la quantité de protection stérique que ce ligand fournit au métal auquel il est lié.
Étant un ligand relativement compact, plusieurs peuvent se lier au même métal de transition, comme illustré dans le cas du complexe de Fe(0):
- 2 PMe3 + Fe(CO)5 → Fe(CO)3(PMe3)2 + 2 CO
Son complexe avec l'iodure d'argent, AgI(PMe3), est stable dans l'air, qui relâche PMe3 lorsqu'il est chauffé.
Il est aussi utilisé comme ligand dans certains réaction organiques, comme dans la réaction de Mitsunobu[1].
Sécurité
PMe3 est potentiellement pyrophorique, ainsi que toxique. Il peut être converti en oxyde de phosphine, non pyrophorique, par traitement avec un oxydant.
Notes et références
- Fiche Sigma-Aldrich du composé Trimethylphosphine, consultée le 22 juin 2013.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Triméthylphosphine », sur ChemIDplus, consulté le 22 juin 2013.
- Annette Schier and Hubert Schmidbaur "P-Donor Ligands" in Encyclopedia of Inorganic Chemistry 2006, Wiley-VCH, Weinheim. DOI 10.1002/0470862106.ia177
- E. Fluck, The chemistry of phosphine, Topics in Current Chemistry Vol. 35, 64 pp, 1973.
- Leutkens, Jr., M. L.; Sattelberger, A. P.; Murray, H. H.;Basil, J. D.; Fackler, Jr. J. P., « Trimethylphosphine », Inorganic Syntheses, New York, J. Wiley & Sons, vol. 28, , p. 305–310 (ISBN 0-471-52619-3, DOI 10.1002/9780470132593.ch76)
- G. L. Miessler and D. A. Tarr Inorganic Chemistry, 3rd Ed, Pearson/Prentice Hall publisher, (ISBN 0-13-035471-6).
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Trimethylphosphine » (voir la liste des auteurs).


