Méthylglyoxal
Le méthylglyoxal, également appelé pyruvaldéhyde et 2-oxopropanal, est un composé chimique de formule CH3–CO–CHO. Il s'agit de l'aldéhyde de l'acide pyruvique. Il possède deux groupes carbonyle C=O, l'un formant une fonction cétone et l'autre une fonction aldéhyde.
| Méthylglyoxal | |
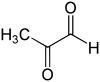 Structure du méthylglyoxal |
|
| Identification | |
|---|---|
| Nom UICPA | 2-oxopropanal |
| Synonymes |
pyruvaldéhyde, |
| No CAS | |
| No ECHA | 100.001.059 |
| No CE | 201-164-8 |
| PubChem | 880 |
| ChEBI | 17158 |
| SMILES | |
| InChI | |
| Apparence | liquide brun à l'odeur âcre |
| Propriétés chimiques | |
| Formule | C3H4O2 [Isomères] |
| Masse molaire[1] | 72,062 7 ± 0,003 3 g/mol C 50 %, H 5,59 %, O 44,4 %, |
| Propriétés physiques | |
| T° fusion | −20 °C[2] |
| T° ébullition | 72 °C[2] |
| T° d'auto-inflammation | 265 °C[2] |
| Pression de vapeur saturante | 2,4 kPa[2] à 20 °C |
| Précautions | |
| SGH[2] | |
 Attention |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Le méthylglyoxal apparaît comme sous-produit de diverses voies métaboliques[3]. Il peut dériver de l'aminoacétone H2N–CH2–CO–CH3, qui est un métabolite de la dégradation de la thréonine, ainsi que de la peroxydation des lipides. Mais la principale source de méthylglyoxal reste la glycolyse, où il se forme par clivage non enzymatique d'un groupe phosphate du glycéraldéhyde-3-phosphate et de la dihydroxyacétone phosphate. Il est présent dans de nombreux produits naturels[4], tels que le café[5].
Le méthylglyoxal étant fortement cytotoxique, l'organisme a développé plusieurs mécanismes de détoxication. L'un d'entre eux est le système glyoxalase. Le méthylglyoxal réagit avec le glutathion pour donner un hémithioacétal, converti en (R)-S-lactoylglutathion par la lactoylglutathion lyase (glyoxalase I)[6], à son tour converti en D-lactate par l'hydroxyacylglutathion hydrolase (glyoxalase II)[7].
L'un des effets du méthylglyoxal est d'accroître la sensation de douleur en se liant directement aux nerfs, ce qui provoque une hyperalgésie dans le cas d'une neuropathie diabétique (en)[8].
Sources notables
Le méthylglyoxal est un composant de certaines variétés de miel, y compris le miel de manuka ; il semble avoir un effet antibiotique contre E. coli et S. aureus et pourrait prévenir la formation de biofilms constitués par P. aeruginosa[9].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Pyruvaldehyde » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 9 décembre 2013 (JavaScript nécessaire)
- (en) Y. Inoue et A. Kimura, « Methylglyoxal and Regulation of its Metabolism in Microorganisms », Advances in Microbial Physiology, vol. 37, , p. 177-277 (lire en ligne) DOI 10.1016/S0065-2911(08)60146-0
- (en) Methylglyoxal, sur le site du CIRC.
- (en) J. Wang et T. Chang, « Methylglyoxal Content in Drinking Coffee as a Cytotoxic Factor », Journal of Food Science, vol. 75, no 6, , H167-H171 (lire en ligne) DOI 10.1111/j.1750-3841.2010.01658.x
- (en) P.J. Thornalley, « Glyoxalase I – structure, function and a critical role in the enzymatic defence against glycation », Biochemical Society Transactions, vol. 31, , p. 1343-1348 (lire en ligne) DOI 10.1042/BST0311343
- (en) D.L. Van der Jagt, « Glyoxalase II: molecular characteristics, kinetics and mechanism », Biochemical Society Transactions, vol. 21, no 2, , p. 522-527 (lire en ligne)
- (en) Angelika Bierhaus, Thomas Fleming, Stoyan Stoyanov, Andreas Leffler, Alexandru Babes, Cristian Neacsu, Susanne K Sauer, Mirjam Eberhardt, Martina Schnölzer, Felix Lasitschka, Winfried L Neuhuber, Tatjana I Kichko, Ilze Konrade, Ralf Elvert, Walter Mier, Valdis Pirags, Ivan K Lukic, Michael Morcos, Thomas Dehmer, Naila Rabbani, Paul J Thornalley, Diane Edelstein, Carla Nau, Josephine Forbes, Per M Humpert et al., « Methylglyoxal modification of Nav1.8 facilitates nociceptive neuron firing and causes hyperalgesia in diabetic neuropathy », nature medicine, vol. 18, , p. 926-933 (lire en ligne) DOI 10.1038/nm.2750
- ZH Israili, « Antimicrobial properties of honey. », American Journal of Therapeutics (en), vol. 21, no 4, , p. 304–23 (PMID 23782759, DOI 10.1097/MJT.0b013e318293b09b)