Ankylostomose
Les ankylostomoses sont des parasitoses intestinales provoquées par deux nématodes (petits vers ronds très voisins), des ankylostome présents dans le duodéno-jéjunum de mammifères :
| Médicament | Albendazole, mébendazole, pyrantel et mébendazole |
|---|---|
| Spécialité | Infectiologie et parasitologie |
![]() Mise en garde médicale
Mise en garde médicale
Parmi les 1,3 milliard de personnes infectées par ces vers, 150 millions seraient gravement atteintes de cette verminose cosmopolite occasionnant 65 000 décès annuels, selon l'OMS[1].
Parasite
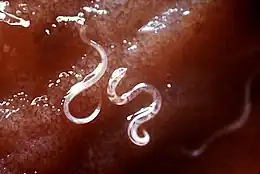
L'ankylostome est un ver parasite (de la classe des nématodes) qui vit dans le duodénum de son hôte, qui peut être un mammifère comme un chien, un chat, ou un humain. Deux espèces d'ankylostomes infectent habituellement les humains, Ankylostoma duodenale et Necator americanus. Necator americanus prédomine dans le continent américain, l'Afrique subsaharienne, le Sud-est asiatique, la Chine et l’Indonésie, alors que A. duodenale prédomine au Moyen-Orient, en Afrique du Nord, en Inde et (autrefois) en Europe méridionale. On pense que l’ankylostome infecte 800 millions de personnes dans le monde entier. Les espèces de Ancylostoma braziliense (en) et A. tubaeforme infectent les chats, alors que A. caninum infecte les chiens. Uncinaria stenocephala infecte les chiens et les chats.
Les ankylostomes sont beaucoup plus petits que le plus grand des vers ronds ascaris lumbricoïdes, et les complications de la migration dans les tissus et de l'obstruction mécanique si fréquemment observées avec l'infestation d'ascaris lumbricoïdes sont plus rares dans l'infestation par l'ankylostome. Le risque le plus caractéristique de l'infection par l'ankylostome est l’anémie, consécutive à la perte de fer (et de protéines) dans l'intestin. Les vers sucent le sang avec voracité et endommagent la muqueuse. Cependant, la perte de sang dans les selles est une perte occulte (qui n’est pas visiblement apparente). L'ankylostomiase, ou ankylostomose est également appelée helminthiase, anémie des mineurs, anémie des tunnels, anémie des briquetiers, chlorose égyptienne, en Allemagne Wurmkrankheit, et aux États-Unis Wakana disease.
L’ankylostome est une des causes prédominantes de morbidité maternelle et infantile dans les pays en voie de développement dans les régions tropicales et subtropicales. Chez les enfants les plus fragiles, l’ankylostome est responsable d’un retard mental, cognitif et d’un retard de croissance. Il entraîne un retard de croissance intra-utérin, un risque de prématurité, un bas poids de naissance chez les fœtus ou bébés nés de mères infectées. L'infection par l'ankylostome est rarement mortelle, mais l'anémie peut être significative chez l'individu fortement infesté.
Les larves peuvent survivre six mois dans le sol humide et les eaux boueuses à température tempérée. De ce fait, dans les régions tempérées, elles ne peuvent coloniser que les galeries souterraines comme les mines. En France, l'infestation atteignait essentiellement les mineurs, provoquant l’anémie des mineurs reconnue maladie professionnelle.
Historique
Les symptômes maintenant attribués à l'ankylostome apparaissent dans les papyrus de l’Égypte antique (1600 avant Jésus-Christ), décrits comme des troubles caractérisés par l'anémie. Avicenne, un médecin persan du XIe siècle, a découvert le ver chez plusieurs de ses patients et a établi la relation avec leur maladie. Dans les périodes plus récentes, cette affection était notoirement répandue dans l'industrie minière en Angleterre, en France, en Allemagne, en Belgique, sur la péninsule de cap York (au Queensland) et ailleurs.
Dans l’époque moderne, le médecin italien Angelo Dubini fut le découvreur du ver en 1838 après l’autopsie d'une paysanne. Dubini a publié les détails de sa découverte en 1843 et identifié l’espèce nommée A. duodenale. Travaillant dans le système de santé égyptien en 1852 le médecin allemand Theodor Bilharz, poursuivant le travail de son collègue Wilhelm Griesinger, a trouvé ces vers au cours de ses autopsies et a franchi une étape supplémentaire en les reliant aux cas endémiques survenant localement de chlorose, qu’on appellerait probablement aujourd'hui anémie par carence en fer.
Une percée est survenue 25 ans après en suivant une épidémie de diarrhée et d’anémie qui se propageait parmi les ouvriers italiens travaillant sur le tunnel ferroviaire du Saint-Gothard. Dans un article de 1880, les médecins Camillo Bozzolo, Edoardo Perroncito, et Luigi Pagliani ont démontré que la transmission de l'ankylostome était liée au fait que les ouvriers déféquaient à l'intérieur des 15 km de tunnel, et que beaucoup d’entre eux portaient des chaussures usagées. La publication du médecin Édouard Bugnion dans met fin à la controverse menée par ceux qui niaient l'existence du parasite[2] - [3]. En 1897, on a établi que la peau était la principale voie de pénétration du parasite et le cycle parasitaire de l'ankylostome a été éclairci. En 1899, le zoologiste américain Charles Wardell Stiles en a apporté la preuve dans les cas survenus dans le sud-est des États-Unis, identifiant « l'anémie pernicieuse progressive » connue dans le Sud des États-Unis comme une maladie provoquée par A. duodenale et il a également identifié l’autre espèce importante d'ankylostome : Necator americanus en examinant, dans les années 1900, les infestations massives découvertes chez les enfants d’âge scolaire.
Le , la Commission sanitaire Rockefeller pour l'éradication de l'ankylostomiase a été organisée à raison d'un don d'un million de dollars de John D. Rockefeller. Bien que des raisons humanitaires soient invoquées, certains soupçonnent que le motif était d’ouvrir de nouveaux marchés dans la région des Appalaches en augmentant le revenu net disponible. Néanmoins le programme d’une durée de cinq ans connut un succès remarquable et fut une contribution remarquable à la santé publique des États-Unis, associant l'éducation sanitaire, les traitements médicamenteux, les travaux sur le terrain et créant les départements modernes de santé publique dans onze États méridionaux. L’ankylostome constitua une part prédominante de la foire exposition du Mississippi en 1910. Le programme a presque totalement éradiqué l'ankylostome. Le programme atteindra son apogée avec la création de la division internationale de santé de la fondation Rockefeller. En 2017, la maladie connaît une résurgence en Alabama dans le comté de Lowndes[4] - [5].
Dans les années 1920, l'éradication de l'ankylostome s’est poursuivie aux Caraïbes et en Amérique latine, où une grande mortalité était constatée chez les Noirs des Indes occidentales vers la fin du XVIIIe siècle, dans les descriptions venues du Brésil et de diverses autres régions tropicales et subtropicales. Le premier traitement fut le thymol pour tuer les vers, suivi du sel d'Epsom pour dégager le corps des vers. Plus tard, l’utilisation du tétrachloroéthylène devint la principale méthode thérapeutique . Ce ne fut pas avant les dernières années de la deuxième moitié du XXe siècle que de « nouvelles drogues » furent développées à partir de composés organiques.
Pathologie
Du point de vue clinique, on distingue les manifestations aiguës dues à la pénétration et la migration des larves :
- dermatite d'invasion : érythème prurigineux de quelques jours aux extrémités des membres ;
- lésions cutanées (urticaires, plaques prurigineuses, pustules) plus ou moins surinfectées, dues à l'hypersensibilité créée par les infestations multiples : c'est la gourme des mineurs ;
- manifestations d'irritation des voies respiratoires supérieures : toux, dysphonie, pharyngite, sialorrhée… C'est le catarrhe des gourmes ;
- duodénite : douleurs épigastriques et diarrhées des manifestations chroniques représentées essentiellement par une anémie.
La plupart des individus infectés par l'ankylostome sont asymptomatiques (sans symptômes). Généralement, des charges très élevées en parasite associées à une nutrition carencée (apports insuffisants en protéines et en fer) provoquent par la suite une anémie. La maladie a été attribuée aux nématodes (Ankylostoma duodenalis) vers d'un tiers de pouce à un demi pouce de long dans l'intestin principalement par les travaux de Théodore Bilharz et Wilhelm Griesinger en Égypte (1854).
Les symptômes peuvent être liés à l'inflammation de l'intestin irrité par les lésions provoquées par les ankylostomes qui se nourrissent, tels que nausée, douleur abdominale et diarrhée intermittente, ainsi que l'anémie progressive dans la maladie prolongée : appétit capricieux, pica, constipation persistante entrecoupée de diarrhée, palpitations, pâleur de la peau et des muqueuses, fatigue et asthénie, essoufflement et dans certains cas évolution vers une issue mortelle, dysenterie, hémorragies et œdème. Les analyses de sang dans l'infection montrent souvent très tôt une augmentation du nombre de polynucléaires éosinophiles dans le sang, un type de globules blancs qui est préférentiellement stimulé par la présence de vers dans les tissus (un grand nombre d'éosinophiles sont également présents dans la réaction inflammatoire locale). Une baisse du taux d'hémoglobine dans le sang apparaîtra dans les cas d'infection prolongée en relation avec l'anémie.
Contrairement à la plupart des helminthiases intestinales où les charges parasitaires les plus élevées se retrouvent chez les enfants, la prévalence et l'intensité de l'ankylostome peuvent être plus élevées parmi les adultes de sexe masculin. La contraction de l'ankylostomose tendant à devenir essentiellement professionnelle, les ouvriers de plantation, les mineurs et d'autres groupes, en souillant leur environnement de travail maintiennent une forte prévalence de l'infection. Cependant, dans la plupart des secteurs endémiques, les femmes adultes sont les plus sévèrement affectées par l'anémie, principalement parce qu'elles ont des besoins physiologiques beaucoup plus élevés en fer (menstruations, grossesses répétées), mais également parce que leur nourriture est généralement beaucoup plus carencée que les hommes. Dans quelques communautés, par exemple dans les plantations d’hévéa où les femmes prélèvent le latex, travaillant nu-pieds, et sans latrines, ce sont elles également qui sont le plus fortement exposées professionnellement à l'ankylostome.
Une conséquence intéressante de ce fait dans le cas de l'infection par Ankylostoma duodenale est la transmission de l'infection par le lait maternel : les larves invasives par voie transcutanée de ces espèces ne passent pas toutes immédiatement par les poumons et vers l'intestin, mais se répandent dans tout l’organisme par transport sanguin, pour devenir des larves dormantes à l’intérieur des fibres musculaires. Chez la femme enceinte, après l'accouchement quelques-unes ou la totalité de ces larves sont stimulées pour être remises en circulation dans le sang (vraisemblablement par les changements hormonaux soudains), puis pour passer dans les glandes mammaires, de sorte que le bébé nouveau-né peut recevoir une dose élevée de larves contagieuses par le lait de sa mère. Ceci explique des cas autrement inexplicables d'infections par l'ankylostome très lourdes, voire mortelles, chez des enfants âgés de quelques mois, dans les endroits tels que la Chine, l'Inde et le nord de l'Australie.
Un phénomène identique est beaucoup plus souvent rencontré avec les infections par Ankylostoma caninum chez les chiens, où les chiots nouveau-nés peuvent même mourir d’hémorragies intestinales provoquées par un nombre massif d'ankylostomes dans leur alimentation. Ceci reflète également le lien évolutionnaire étroit entre les parasites humains et canins, lesquels avaient probablement un ancêtre commun remontant à l'époque où humains et chiens vivaient étroitement ensemble.
Cycle parasitaire
.GIF)
L’ankylostome prospère dans la terre chaude où la température dépasse 18 °C. Il vit principalement dans le sable ou les sols de terre grasse et ne peut pas vivre dans l’argile ou le fumier. Le niveau moyen des précipitations doit dépasser 1 000 mm par an. C’est seulement si ces conditions sont réunies que les œufs peuvent éclore. Les larves infestantes de Necator américanus peuvent survivre à des températures élevées, tandis que celles d’ Ankylostoma duodenale sont mieux adaptées à des climats plus frais. Généralement, elles ne survivent que durant quelques semaines, tout au plus dans des conditions normales, et meurent presque immédiatement au contact de la lumière directe du soleil ou sous l’effet de la dessiccation. Une fois dans l'intestin de l’hôte, Necator américanus tend à provoquer une infection prolongée, car on a observé quelques vers d'adulte capables de vivre pendant quinze années ou davantage encore. D'une part, les adultes d’Ankylostoma duodenale ont une durée de vie plus courte, puisqu’ils survivent en moyenne seulement pendant six mois environ. Cependant, l'infection peut être prolongée parce que des larves dormantes peuvent « être recrutées » séquentiellement à partir du tissu « de stockage » (voir la pathologie, ci-dessus) pendant de nombreuses années, pour remplacer les vers adultes morts. Ceci peut provoquer des fluctuations saisonnières dans la prévalence et l'intensité de l'infection (indépendamment des variations saisonnières de transmission habituelles).

Puisqu’il faut environ 5 à 7 semaines pour que les vers adultes deviennent matures, pour qu’ils s’accouplent et produisent des œufs, dans les premiers stades d’une infection massive, des symptômes aigus pourraient se manifester sans qu’aucun œuf ne soit détecté dans les selles du patient. Ceci peut rendre le diagnostic très difficile.
Prévention
Les larves infestantes se développent et survivent dans un environnement souillé et humide, un sol particulièrement sableux et gras. Ils ne peuvent pas survivre dans l’argile ou le fumier. Les axes principaux de la prévention sont ceux édictés par les règles sanitaires :
- empêcher le contact de la peau avec le sol : ne pas marcher nu-pieds ;
- ne pas déféquer à l'extérieur : installation de latrines, de toilettes… ;
- ne pas utiliser les excréments humains ou les eaux d'égout non traitées comme engrais dans l'agriculture ;
- les vers d'animaux de compagnie — ankylostomes canins et félins — se développent rarement jusqu’au stade adulte chez l'homme (Ancylostoma caninum, l'ankylostome le plus répandu chez le chien, se développe occasionnellement chez l’adulte pour provoquer l'eneritis éosinophile chez l’homme), mais leurs larves infestantes peuvent causer une éruption prurigineuse appelée larva migrans cutanée. Vers la fin du XIXe siècle et au début des années 1900, beaucoup d’habitants du Mississippi ont été infestés par des ankylostomes. Ils n'avaient pas d’installations sanitaires ou d’équipement d'hygiène approprié. La diffusion d'ankylostomes par contamination fécale de l'environnement était donc très fréquente (aussi bien que d'autres maladies provoquées par le manque d'hygiène).
Diagnostic

Il n'y a aucun symptôme ou signe spécifique de l'infection par l'ankylostome. Comme mentionné ci-dessus, ils résultent d'une combinaison de signes d'inflammation intestinale et d'anémie progressive par carence en fer. La pénétration de la larve à travers la peau peut provoquer des démangeaisons locales intenses, habituellement sur le pied ou le bas de la jambe, qui peut être suivie de lésions qui ressemblent aux piqûres d'insecte, avec des boursouflures (« gourme des mineurs »), et durent une semaine ou plus. La toux, la douleur thoracique, la dyspnée laryngée, et fièvre seront parfois présentes chez les personnes qui ont été infestées par un très grand nombre de larves. Les douleurs épigastriques, indigestion, nausées vomissements, constipation, et diarrhée peuvent survenir à l’étape initiale aussi bien que plus tardivement, bien que les symptômes gastro-intestinaux tendent à s'atténuer avec le temps. Les signes de l'infection grave évoluée sont ceux de l'anémie et de la déficience en protéines, y compris l'amaigrissement, la défaillance cardiaque et la distension abdominale avec de l'ascite.
Le diagnostic dépend de la découverte d’œufs d’ankylostomes caractéristiques à l'examen au microscope des selles, bien que ce ne soit pas possible au début de l'infection. Comme les œufs d’Ankylostome et de Necator (et de la plupart des autres espèces d'ankylostomes) sont impossibles à distinguer les uns des autres, pour identifier le genre, ils doivent être cultivés en laboratoire pour permettre à des larves d’éclore. Si l'échantillon de selles est laissé pendant un jour ou plus dans des conditions tropicales, les larves peuvent avoir éclos, aussi les œufs peuvent ne plus être détectables. En ce cas, il est essentiel de distinguer les ankylostomes des larves de Strongyloides, car l'infection avec ses dernières a des conséquences plus sérieuses et exige une gestion différente. Les larves des deux espèces d'ankylostomes peuvent également être distinguées au microscope, bien que ceci ne soit pas fait d’habitude, mais seulement pour des recherches. Les vers d'adulte sont rarement décelables (excepté par le biais de l'endoscopie, de la chirurgie ou l'autopsie), mais leur découverte permettrait l'identification définitive des espèces.
Traitement
L'ankylostome peut être traité localement par cryothérapie quand il est toujours dans la peau. L’albendazole est efficace à l'étape intestinale et pendant l'étape où le parasite migre toujours sous la peau. En cas d'anémie, la supplémentation en fer peut atténuer les symptômes de l’anémie ferriprive. Cependant, lorsque le taux de globules rouges revient à la normale, le manque d'autres substances comme l’acide folique ou la vitamine B12 peut apparaître qui peuvent également nécessiter une supplémentation.
Survol rapide
| Genre et espèce | Necator americanus | Ancylostoma duodenale |
|---|---|---|
| Nom commun | New world hookworm, American murderer | Old world hookworm |
| Agent étiologique de : | Necatoriasis, Uncinariasis | Ankylostomose, helminthiase, anémie des mineurs, ... |
| Stade infectieux | Filariform larva | Filariform larva |
| Hôte définitif | Humain | Humain |
| Mode de pénétration | Habituellement par pénétration de la peau plutôt que par ingestion | Habituellement par ingestion plutôt que par pénétration de la peau |
| Mode de transmission | Peau > Bouche | Bouche > Peau |
| Habitat | Petit intestin | Petit intestin |
| Stade pathogène | Larve adulte | Larve adulte |
| Mode d'attachement | Attachement oral par succion à la muqueuse | identique |
| Mode d'alimentation | Succion et ingestion de sang | identique |
| Pathogénèse | Larve : ground / dew itch, creeping eruption
Adulte : Anémie ferriprive microcytique (globules rouges de petite taille), Anémie hypochromique |
identique |
| Diagnostic en laboratoire | méthodes de concentration et frottis fécal direct | identique |
| Traitement | Albendazole, Mébendazole, ou Pyrantel Pamoate | identique |
| Caractéristique - Adulte | Semi-lunar cutting plate ; raie dorsale bipartite | Mâle : raie dorsale tripartite |
| Caractéristique - Œuf | Dans morula | Dans morula |
L’ankylostome comme piste thérapeutique
Des infections modérées par l’ankylostome pouvaient avoir des effets bénéfiques sur leur hôte. Des recherches ont démontré que les personnes atteintes d’infections par l'ankylostome ont deux fois moins de risque de souffrir de crises d’asthme[6]. L’explication théorique de ce phénomène est que notre système immunitaire a évolué sous la menace constante d'une grande variété de parasites, dont la plupart ont dû contourner nos défenses immunitaires pour survivre. C'est-à-dire qu’ils doivent réguler la réponse immunitaire qui devrait les attaquer. L'évolution avec un système immunitaire réglé à un bas niveau de réactivité signifie qu'en l'absence de ces parasites qui ont tendance à l’inhiber, notre système immunitaire attaque souvent nos propres tissus, ce qui conduit à l'asthme, au rhume des foins, à la colite, à la maladie de Crohn et peut-être à d'autres maladies autoimmunes.
Notes
- (en) Partnership for Parasite Control, Second Meeting Rome, avril 2002 [PDF]
- (en) R Peduzzi et J C Piffaretti, « Ancylostoma duodenale and the Saint Gothard anaemia. », BMJ, vol. 287, no 6409, , p. 1942–1945 (ISSN 0959-8138 et 1468-5833, PMID 6418279, PMCID PMC1550193, DOI 10.1136/bmj.287.6409.1942, lire en ligne [PDF], consulté le )
- (en) E. Bugnion, « On the Epidemic Caused by Ankylostomum among the Workmen in the St. Gothard Tunnel », BMJ, vol. 1, no 1054, , p. 382–382 (ISSN 0959-8138 et 1468-5833, PMID 20749811, PMCID PMC2263460, DOI 10.1136/bmj.1.1054.382, lire en ligne, consulté le )
- The Spark, « Une maladie du tiers-monde », Lutte ouvrière, no 2584, , p. 10 (lire en ligne, consulté le ).
- (en) « Hookworm, a disease of extreme poverty », The Guardian, (lire en ligne, consulté le ).
- David Pritchard, University of Nottingham, « Étude randomisée contrôlée par placebo sur les effets de l'infection thérapeutique par l'ankylostome dans l'asthme », (consulté le )
Références
- (en) « Ankylostomose », dans Encyclopædia Britannica, 1911 [
 (en) Lire en ligne sur Wikisource].
(en) Lire en ligne sur Wikisource]. - Albanese G.; Venturi C, ; Galbiati G (2001): Treatment of larva migrans cutanea (creeping eruption): a comparison between albendazole and traditional therapy. Int J Dermatol: 40(1): 67-71
- Hotez P.; Pritchard D. (1995): Hookworm infection. Sci Am June: 68-74
Voir aussi
- Larva migrans cutané (érythème migrant)
Liens externes
- (en) CDC Department of Parasitic Diseases images of the hookworm life cycle
- (en) Hookworm Infection ; Fact Sheet
- (en) What Is A Hookworm Infection? (Ancylostomiasis - Personal MD
- (en) How to cure your asthma or hayfever using hookworm - a practical guide
- Les vers tueurs du Saint-Gothard par Anne-Marie Moulin, (pour la revue L'Alpe)