Phtalate de benzyle et de butyle
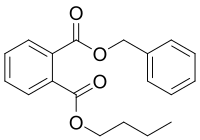
Le phtalate de benzyle et de n-butyle ou benzyle butyle phtalate (BBzP), n-butyl benzyl phtalate (BBP), calques de l'anglais benzyl butyl phthalate est un composé chimique qui est l'ester phtalate du butanol et de l'alcool benzylique, principalement utilisé comme plastifiant. Il est vendu sous plusieurs noms commerciaux dont Palatinol BB, Unimoll BB, Sicol 160 ou Santicizer 160.
| Phalate de benzyle et de n-butyle | |
| |
| Identification | |
|---|---|
| Nom UICPA | 2-O-benzyl 1-O-butyl benzène-1,2-dicarboxylate |
| Synonymes |
NCI-C54375 |
| No CAS | |
| No ECHA | 100.001.475 |
| No CE | 201-622-7 |
| No RTECS | TH9990000 |
| PubChem | 2347 |
| SMILES | |
| InChI | |
| Apparence | liquide |
| Propriétés chimiques | |
| Formule | C19H20O4 [Isomères] |
| Masse molaire[2] | 312,359 7 ± 0,017 8 g/mol C 73,06 %, H 6,45 %, O 20,49 %, 312,35 g/mol[3] |
| Propriétés physiques | |
| T° fusion | −35 °C[4] |
| T° ébullition | 370 °C à 10,10 hPa[5] - [3] |
| Solubilité | 8 mg·l-1[3] |
| Masse volumique | 0,97 g·cm-3[6] 0,985 g·cm-3[7] |
| T° d'auto-inflammation | 450 °F |
| Point d’éclair | 207 °C[7] |
| Pression de vapeur saturante | 0,16 mmHg (150 °C)[1] ou 1,12 mPa à 20 °C[8] |
| Précautions | |
| Directive 67/548/EEC[7] | |
 T  N |
|
| Données pharmacocinétiques | |
| Stockage | réfrigéré |
| Unités du SI et CNTP, sauf indication contraire. | |
Il est principalement utilisé dans les mousses de vinyle et dans les PVC (qui peuvent en contenir jusqu'à 60 % de leur masse, pour assouplir (RIVM, 1998).
En raison de sa toxicité mais surtout de son caractère de perturbateur hormonal d'abord démontré chez l'animal[10], il fait partie des substances jugées « substance extrêmement préoccupante » (Substance of very high concern) en France[11] et en Europe[12] et identifié comme CMR[13] au regard de la Directive REACH et classé comme reprotoxique en catégorie R 61, ce qui signifie qu'il peut altérer le développement de l'embryon[14] - [3]. Il a fait l'objet d'une première évaluation des risques par la Norvège, pour l'Europe[15] (rapport rendu en 2007[16]).
Toxique pour les plantes et les organismes aquatiques, c'est (comme d'autres phtalates et plastifiants[17] - [18]) un perturbateur endocrinien (anti-androgène, c'est-à-dire féminisant à haute dose (10 à 100 μM). Deux de ses métabolites semblent l'être également[19] - [20] - [21] - [22] - [23] - [3]).
Il est aussi source de réduction du poids des testicules[24] de réduction de la distance ano-génitale[25] - [26] et de mauvaise migration du testicule[27] - [28] (en cas d'exposition[29] entre le 6e et 20e jour de gestation), et de malformation génitale chez plus de 80 % de rats mâles exposés in utero[30] à des doses importantes (11 250 ppm[31]), avec des effets observables à partir de 3750 ppm[31]) et reprotoxique[31].
Il peut aussi être présent en tant qu'impureté d'autres produits chimiques.
En 2008, quatre vendeurs de BBP ont été sanctionnés en Belgique par le Belgian Competition Council pour avoir agi en cartel[32] - [33].
Fabrication et consommation
On le fabrique en faisant réagir le butanol et le chlorure de benzyle avec de l'anhydride phtalique. En 1997, l'Europe en aurait consommé de 20 000 à 50 000 t/an [RIVM, 1998], mais sa production aurait régressé depuis la fin des années 1990. Il ne reste que deux grands fabricants en Europe. En tant que produit commercialisé, il est considéré comme pur à plus de 98,5 % (w/w)[3]. Les impuretés sont selon l'ECHA :
- < 1,0 % phtalate de dibenzyle (no CAS )[3] ;
- < 0,5 % benzoate de benzyle (no CAS )[3] ;
- < 0,5 % phtalate de dibutyle (no CAS )[3] ;
- < 2 ppm α-chlorotoluène (no CAS )[3] ;
- < 2 ppm α,α-dichlorotoluène (no CAS )[3] ;
- additif < 0,5 ppm tétrakis (3-(3,5-di-tert-butyl-4-hydoxyphényl)propanoate de pentaérythritol (no CAS )[3].
Usages
- Le BBP est (aux États-Unis surtout) utilisé comme assouplissant du PVC. On le retrouve par exemple dans le PVC de bandes de convoyeur alimentaire, de revêtements de sol, dans certains Skaï (imitations de cuir) ou pour la fabrication de cônes de signalisation routière [CERHR, 2003].
- En Europe, plus de 90 % de la production est orientée vers la production de PVC ainsi que de divers polymères utilisés pour produire des revêtements de sol et certains emballages alimentaires, des peintures plastiques, joints ou colles.
Toxicologie
Elle fait encore l'objet d'une réévaluation, mais on sait que ce produit (comme les phtalates) peut migrer d'un contenant en plastique vers la nourriture ou l'environnement [EC, 2004]. Sa toxicité pour l'homme n'avait pas encore en 2004 été vraiment étudiée, mais une étude épidémiologique de type cas témoin, concluait à un risque accru de myélomes multiples chez les ouvriers fabricant du PVC depuis au moins cinq ans et exposés à un mélange de phtalate [Heineman, 1992], des indices (études sur quelques dizaines à centaines de sujets) laissaient penser que l'enfant pouvait conserver des séquelles d'une exposition in utero, et une étude (2006) ayant porté sur 463 hommes[34] a montré une mauvaise qualité de sperme fortement corrélée à des taux plus élevés de monoester de phtalate ou de ses métabolites urinaires. De plus, du MBeP (monobenzylphtalate) a été trouvé dans 94 % des échantillons de sperme, ce qui montre une large contamination par ce produit (au début des années 2000)[34]. Ce produit peut être trouvé dans le lait maternel humain[35].
Écotoxicologie
Des effets œstrogéniques et anti-androgéniques ont été recherchées chez le poisson, et constaté au moins chez Pimephales promelas[36], chez la truite[37] - [38], mais sans preuves de synergies avec l'estradiol[39] à forte concentration, mais pas chez la carpe à faible concentration[40].
Symptômes d'intoxication
Selon les données disponibles : à très haute dose, ce sont par ordre de gravité :
- perte d'appétit et inhibition de l'activité ;
- perte de poids ;
- apathie ;
- leucocytose ;
- collapsus, puis mort.
L'examen histologique post mortem montre des hémorragies pulmonaires, des inflammations gastrointestinales aiguës et une dégénérescence de certaines parties du système nerveux central [EC, 2004].
Doses toxiques
- DL50 orale : la dose létale dans 50 % des cas est de 2 330 mg/kg (dilué dans l'huile de maïs) chez le rat et de 20 400 mg/kg administré pur chez le rat également. Elle est de 4 170 – 6 160 mg/kg pour la souris.
- DL50 cutanée : la dose létale dans 50 % des cas est de plus de 10 000 mg/kg chez le lapin.
Chez le rat, à partir de 120 à 300 mg/kg par jour, une augmentation du poids relatif de certains organes (reins et foie surtout) est observée. Des lésions graves touchent d'abord le pancréas et les reins ; puis à plus forte dose, apparaît une dégénérescence testiculaire et des lésions dans le foie.
Classifications toxicologiques
Il est classé :
- reprotoxique chez l'homme, de catégorie 2, pour le développement de l'enfant par l'Union européenne ;
phrase de risque R61 : « risque pendant la grossesse d'effet néfaste pour l'enfant ») ; - reprotoxique chez l'homme, de catégorie 3, pour la reproduction ;
phrase de risque R62 : « risque possible d'altération de la fertilité » ; - écotoxique : il est classé R50-53 c'est-à-dire « Très toxique pour les organismes aquatiques, peut entraîner des effets néfastes à long terme pour l'environnement aquatique »).
Très toxique pour les espèces aquatiques [IPCS-CEC, 2005], Il est réputé peu toxique pour l'animal (DL50 > 2 g/kg).
Le CIRC a conclu en 1999, que faute de données chez l'homme ou l'animal, on ne pouvait pas le classer comme cancérogène pour l'homme (groupe 3 « not classifiable as to its carcinogenicity to human » [IARC, 1999].
L'US-EPA e, 2003, l'a classé cependant parmi les produits « possiblement cancérogène chez l'homme » (classe C) [US-EPA, 2003].
Métabolisation
Il est hydrolysé dans le foie et surtout dans l'intestin, puis conjugué (glucurono-conjugaison) et excrété via l'urine et/ou les excréments [EC, 2004].
- chez l'animal de laboratoire (rongeur) on a trouvé comme métabolites :
- le phtalate mono butyle (MBuP), dominant dans l'urine (3 fois plus de MBuP que de MBeP selon Agarwal 1985) ;
- le phtalate mono benzyle (MBeP), qui est soupçonné d'être aussi (faiblement) un perturbateur endocrinien dont l'activité endocrinienne a été étudiée in vitro et in vivo chez le rat de laboratoire[20] (il provoque une réduction du poids de l'utérus, mais qui pourrait également être due à sa toxicité systémique)[3] ;
- l'acide hippurique ;
- l'alcool benzylique ;
- le n-butanol.
Chez l'homme, la métabolisation semble utiliser les mêmes voies que chez le rat, mais chez l'homme le MBeP est le plus présent (>70 %), alors que le MBuP ne présent que +/-6 % des métabolites.**
Demi-vie du BBP
Cette demi-vie, chez l'Homme, semble est courte (elle l'est dans tous les tissus testés), de même que celle de ses deux mono-esters (environ 6 h).
L'excrétion est majoritairement urinaire (70 %) puis fécale (10 %) mais ce rapport s'inverse à forte dose (> 2 000 mg/kg par jour).
Évaluation de l'exposition
C'est un polluant principalement issu d'émissions industrielles et de déchets contenant du BBP. Il existe un modèle calé (par une expérience in vivo) en situation réelle pour évaluer l'exposition externe à partir de taux urinaires de MBeP [EC, 2004].
À partir de statistiques canadiennes, l'OMS a évalué (en 1985-1988) que l'exposition alimentaire moyenne au BBP était alors d'environ 2 µg/kg par jour chez l'adulte et 6 fois plus (12 µg/kg par jour) chez l'enfant [IPCS, 1999]. En 2003, le ministère anglais de l'Agriculture a estimé que l'exposition en population générale était comprise entre 0,11 et 0,29 µg/kg par jour [CERHR, 2003].
En Europe, la Commission européenne estimait en 2004, pour la population générale, que l'exposition par l'alimentation était de 0,3 µg/kg par jour pour les adultes et de 1,02 μg/kg par jour pour les enfants, ce à quoi il faut ajouter une exposition par inhalation (à partir des sols plastiques surtout) de 0,083 µg/kg par jour. Le plastique des jouets de jeunes enfants en contient environ 0,95 µg/kg par jour [EC, 2004].
Selon une étude des métabolites urinaires du BBP, l'exposition environnementale est généralement inférieure à 18,2 µg/kg par jour pour les enfants de 1 à 2 ans, et inférieure à 5,4 µg/kg par jour pour enfants de 6 à 11 ans, et de moins de 3,5 µg/kg par jour pour les adultes [EC, 2004].
Recherche, dosage
Elle peut être faite par chromatographie sur couche mince, chromatographie en phase gazeuse ou chromatographie en phase liquide couplée à un spectromètre de masse (GC/MS, LC/MS)[41].
Notes et références
- Chemical Book. Consulté le 11 novembre 2012.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ECHA, Benzyl butyl phthalate, MEMBER STATE COMMITTEE SUPPORT DOCUMENT FOR IDENTIFICATION OF Benzyl butyl phthalate (BBP) AS A SUBSTANCE OF VERY HIGH CONCERN, adopté 2008-10-01
- Monsanto Internal data (1988) Santicizer 160 bulletin. Monsanto Europe S.A., 8th edition.
- Bayer AG MSDS
- Entrée du numéro CAS « 117-81-7 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais) (JavaScript nécessaire)
- Bis(2-ethylhexyl) phthalate chez Sigma-Aldrich.
- Hoyer et Peperle (1957)
- R50/53 : Dangerous for the environment; very toxic to aquatic organisms, may cause long term effects in the aquatic environment
- Tyl R.W., Myers C.B., Marr M.C., Fail P.A., Seely J.C., Brine D.R., Barter R.A. et Butala J.H. (2004). Reproductive toxicity evaluation of dietary Butyl Benzyl Phthalate (BBP) in rats, Reprod. Toxicol. 18, 241-264
- Secrétariat de la Commission d'Évaluation de l'Écotoxicité des Substances Chimiques, Rapport d'activité de la commission d'évaluation de l'écotoxicité des substances chimiques pour l'année 2001 ; La Documentation française, 14 février 2002
- Commission européenne, DG ENV (2000) Towards the establishment of a priority list of substances for further evaluation of their role in endocrine disruption - preparation of a candidate list of substances as a basis for priority setting. Rapport final. BKH Consulting Engineers, Delft, The Netherlands in association with TNO Nutrition and Food Research, Zeist, The Netherlands. Project No M0355008/1786Q/10/11/00
- CMR according to Article 57 (c) of Regulation (EC) 1907/2006(REACH)
- Annex I to Directive 67/548/EEC, Benzyl butyl phthalate (BBP) is classified as asubstance toxic to reproduction Repr. Cat. 2; R 61 (may cause harm to the unborn child)
- Council Regulation (EEC) No 793/93 on the Control and Evaluation of the Risks of Existing Substances
- EU RAR, 2007: European Union Risk assessment report, Benzyl butyl phthalate (BBP), vol. 76 (ISSN 1018-5593)
- Jobling S., Reynolds T., White R., Parker M.G. et Sumpter J.P. (1995) A variety of environmentally persistent chemicals, including some phthalate plasticizers, are weakly estrogenic, Environ. Health Perspect. 103, 582-587
- Zacharewski T.R., Meek M.D., Clemons J.H., Wu Z.F., Fielden M.R. et Matthews J.B. (1998) Examination of the in vitro and in vivo estrogenic activities of eight commercial phthalate esters, Toxicol. Science 46, 282-293
- Piersma A.H., Verhoef A., te Biesebeek J.D., Pieters M.N. et Slob W. (2000) Developmental toxicity of butyl benzyl phthalate in the rat using a multiple dose study design, Reprod. Toxicol. 14, 417- 425. Issu du rapport : Piersma A.H., Verhoef A., Dormans JAMA, Elvers L.H., de Valk F., te Biesebeek J.D., Pieters M.N. et Slob W. (1999). Developmental and testicular toxicity of butyl benzyl phthalate in the rat and the impact of study design RIVM rapport no 650040 001.
- Gray Jr. LE, Ostby J., Furr J., Price M., Veermachaneni DNR and Parks L (2000) Perinatal exposure to the phthalates DEHP, BBP, and DINP, but not DEP, DMP, or DOTP, alters sexual differentiation of the male rat, Toxicol. Science 58, 350-365.
- Parks L.G., Ostby J.S., Lambright C.R., Abbott B.D. et Gray LE Jr. (1999), Perinatal butyl benzyl phthalate (BBP) and di-(2ethylhexyl) phthalate (DEHP) exposures induce antiandrogenic effects in Sprague-Dawley (SD) rats, Biol. Reprod. 60 (1), 153
- Nagao T., Ohta R, Marumo H., Shindo T., Yoshimura S. et Ono H. (2000) Effect of butyl benzyl phthalate in Sprague-Dawley rats after gavage administration: a two-generation reproductive study, Reproductive Toxicology 14, 513-532
- Imajima et al., 1997; Shono et al., 2000 ; Tyl et al., 2004; Ema et al., 2002; Ema et al., 2003, cités dans EU RAR
- Piersma et al. (2000) cités par l'ECHA (voir biblio)
- Ema M., Miyawaki E., Hirose A. et Kamata E. (2003) Decreased anogenital distance and increased incidence of undescended testes in fetuses of rats given monobenzyl phthalate, a major metabolite of butyl benzyl phthalate, Reprod. Toxicol. 17, 407-412.
- Swan S.H., Main K.M., Liu F., Stewart S.L., Kruse R.L., Calafat A.M., Mao C.S., Redmon J.B., Ternand C.L., Sullivan S., Teague J.L. et le Study for Future Families Research team (2005) Decrease in anogenital distance among male infants with prenatal phthalate exposure, Environ. Health Perspect. 113, 1056-1061
- Imajima T., Shono T., Zakaria O. et Sulta S. (1997) Prenatal phthalate exposure causes cryptorchidism postnatally by inducing transabdominal ascent of testis in fetal rats, J. Pediatric Surgery 32 (1), 18-21.
- Shono T., Kai H., Suita S. et Nawata H. (2000) Time-specific effects of mono-n-butyl phthalate on the transabdominal descent of the testis in rat fetuses, BJU International 86, 121-125
- 270 mg de BBP/kg bw/jour et 580 mg/kg bw/jour
- Dans 84 % des mâles de la progéniture (âgés approximativement de 90 jours) exposés à 750 mg/kg bw/jour de BBP du 14e jour de gestation au 2e jour postnatal
- Rochelle W. Tyl, Christina B. Myers, Melissa C. Marr, Patricia A. Fail, John C. Seely, Dolores R., Brine, Robert A. Barter, John H. Butala, Reproductive toxicity evaluation of dietary butyl benzyl phthalate (BBP) in rats, Reproductive Toxicology, vol. 18, Issue 2, mars–avril 2004, p. 241-264 (résum)
- Communiqué de presse Belgian Competition Council 2008-04-04 « Copie archivée » (version du 1 octobre 2011 sur Internet Archive)
- communiqué du ministère de l'Économie, 2008-04-04
- Hauser R., Meeker J.D., Duty S., Silva M.J., Calafat A.M. (2006) Altered semen quality in relation to urinary concentrations of phthalate monoester and oxidative metabolites. Epidemiolog, 17(6):682-91.
- Main K.M., Mortensen G.K., Kaleva M.M., Boisen K.A., Damgaard I.N., Chellakooty M., Schmidt I.M., Suomi A.M., Virtanen H.E., Petersen J.H., Andersson A.M., Toppari J. et Skakkebæk N.E. (2005) Human breast milk contamination with phthalates and alterations of endogenous reproductive hormones in three month old infants, Environ. Health Perspect., en ligne le 7 septembre 2005
- Harries C.E., Runnalls T., Hill E., Harris C.A., Maddix S., Sumpter J.P. et Tyler C.R. (2000) Development of a reproductive performance test for endocrine disrupting chemicals using pairbreeding fat-head minnows (Pimephales promelas), Environ. Sci. Technol. 34:3003–3011
- Christiansen L.B., Pedersen K.L., Pedersen S.N., Korsgaard B. et Bjerregaard P. (2000). In vivo comparison of xenoestrogens using rainbow trout vitellogenin induction as a screening system, Environ. Toxicol. Chem. 19, 1867-1874
- Knudsen F.R. et Pottinger T.G. (1998) Interaction of endocrine disrupting chemicals, singly and in combination, with estrogen-, androgen- and corticosteroid-binding sites in rainbow trout (Oncorhynchus mykiss), Aquat. Toxicol. 44, 159-170.
- butylbenzylphthalate and estradiol on liver estradiol receptor modulation and induction of zona radiata proteins in rainbow trout: no evidence of synergy, Env. Poll. 103, 75-80.
- ECHA, 2008, biblio, chap. 4, ENVIRONMENTAL HAZARD ASSESSMENT
- P.J Bloom, Application des chromatographies sur couche mince et gaz liquide à l'analyse qualitative et quantitative des esters de l'acide phtalique ; Journal of Chromatography A, vol. 72, Issue 1, 1972, p. 35-49
Voir aussi
Bibliographie
- ECHA, Benzyl butyl phthalate, MEMBER STATE COMMITTEE SUPPORT DOCUMENT FOR IDENTIFICATION OF Benzyl butyl phthalate (BBP) AS A SUBSTANCE OF VERY HIGH CONCERN, adopté 2008-10-01.
- Ema M. et Miyawaki E. (2002), « Effects on development of the reproductive system in male offspring of rats given butyl benzyl phthalate during late pregnancy ». Reprod. Toxicol. 16, 71-76.
- A.-M. Saillenfait, A. Laudet-Hesbert, EMC - Toxicologie-Pathologie, vol. 2, Issue 1, , p. 1-13.
- Chien-Sen Liao, Jui-Hung Yen, Yei-Shung Wang, « Effects of endocrine disruptor di-n-butyl phthalate on the growth of Bok choy », Chemosphere 65 (2006) 1715–1722.
- Nagao T., Ohta R., Marumo H., Shindo T., Yoshimura S. et Ono H. (2000) « Effect of butyl benzyl phthalate in Sprague-Dawley rats after gavage administration: a two-generation reproductive study », Reproductive Toxicology 14, 513-532.
- Jon N. Cammack, « Evaluation of Reproductive Development Following Intravenous and Oral Exposure to DEHP in Male Neonatal Rats », International Journal of Toxicology, 22:159–174, 2003.
- Hyun Jung Koo, Byung Mu Lee, « Estimated exposure to phthalates in cosmetics and risk assessment », Journal of Toxicology and Environmental Health, partie A, 67:1901–1914, 2004.
- J.-M. Brignon, L. Malherbe, S. Soleille, « Les substances dangereuses prioritaires de la directive cadre sur l'eau - Fiches de données technicoéconomiques », rapport du ministère de l'Écologie et du Développement durable, Unité MECO Direction des Risques Chroniques, .
Articles connexes
Liens externes
- (en) [PDF] Évaluations des risques du Bureau Européen des Substances Chimiques sur le DIDP, le DINP et le DBP
- Consensus Scientifique sur les Phtalates Résumés par GreenFacts des rapports du Bureau Européen des Substances Chimiques
- (en) Phthalates Information Centre Europe
- (en) Phthalates Information Centre
- (en) Health Care
- Société canadienne du cancer
- (en) Medicalplast.com
- Centre National d'Information Indépendant sur les Déchets
- Les cosmétiques bio et les phtalates