Chromatographie sur couche mince
La chromatographie sur couche mince (CCM, en anglais TLC pour Thin layer chromatography) est une technique de chromatographie planaire[1] dont la phase mobile est liquide. Elle est couramment utilisée pour séparer des composants dans un but d'analyse (CCM analytique) ou de purification (CCM préparative).
Elle comprend :
- une phase stationnaire : une couche mince de matériel adsorbant (usuellement du gel de silice, de l'oxyde d'aluminium ou de la cellulose) ;
- une phase liquide, dite phase mobile ou éluant : un solvant ou un mélange de solvants qui va entraîner les composés à se séparer le long de la phase stationnaire.
Le phénomène d’adsorption est prépondérant (mais il y a également partage si le solvant est un mélange) pour les phases stationnaires polaires. Dans le cas des phases inverses, c'est-à-dire hydrophobes, c'est le phénomène de chromatographie de partage qui prédomine.
Constitution d'une plaque de CCM
Une plaque de CCM est un support en verre, en aluminium ou en plastique sur lequel a été étalé une phase stationnaire en couche uniforme. L'épaisseur de cette couche est de l'ordre de 0,2 mm (200 μm) pour une plaque analytique et 1-3 mm pour une plaque préparative. Avant étalement, la phase stationnaire est une poudre fine et elle doit donc être mélangée à un liant qui assure la bonne cohésion de la couche et une bonne adhérence au support. On utilise le plus fréquemment un liant inorganique comme du gypse, du plâtre, du sulfate de calcium hémihydraté, ou un liant organique (par exemple l'alcool polyvinylique) notamment lorsque la phase stationnaire est hydrophobe.
On ajoute souvent un colorant fluorescent pour permettre une détection des produits à la lumière ultraviolette à 254 nm ou 366 nm ; à cette longueur d'onde, le colorant de la phase stationnaire émet une lumière, verte en général, sauf aux endroits où un produit absorbe le rayonnement UV ce qui provoque l'apparition de taches sombres.
À l'heure actuelle, il existe de nombreuses phases stationnaires de plus en plus efficaces et qui permettent des séparations très fines si bien que l'on parle, dans ce cas, de chromatographie sur couche mince à haute performance (HPTLC en anglais).
Migration des espèces chimiques
Rapport frontal
Le rapport frontal (Rf) ou facteur de rétention d'un composé est le rapport de la distance ligne de dépôt-composé sur la distance ligne de dépôt-front de solvant. Il est compris entre 0 et 1, et est caractéristique du composé, du matériau de la plaque et du système d'éluant.
Facteurs influençant la migration
Le Rf des produits dépend de leur affinité relative pour la phase stationnaire et la phase mobile. Dans la plupart des cas, la phase stationnaire est polaire (silice, alumine, cellulose). Plus un composé est lui-même polaire, plus il aura d'affinité pour la phase stationnaire et, par conséquent, plus il sera retenu sur la plaque. Plus on augmente la polarité de l'éluant, plus il entre en compétition avec la phase stationnaire et puisqu'il est en mouvement, plus il entraîne le composé avec lui.
L'éluant
Pour moduler la polarité de l'éluant, on utilise généralement un mélange de solvants et l'on indique le rapport en volumes des solvants utilisés en essayant de faire en sorte que la somme des volumes soit égal à 10 ou 100 ; par exemple, un mélange de chloroforme (8 ml) et d'acétate d'éthyle (2 ml) sera souvent désigné chloroforme/acétate d'éthyle 8/2 ou 80/20.
Ordre relatif de la polarité d'une sélection de solvants purs du plus polaire au moins polaire :
- Eau (plus polaire)
- Méthanol
- Acétonitrile
- Acide acétique
- Propanol
- Tétrahydrofurane
- Acétate d'éthyle
- Éther diéthylique
- Chloroforme
- Dichlorométhane
- Toluène
- Cyclohexane
- n-Hexane (moins polaire)
Mode opératoire
L'exemple ci-dessous montre les différentes étapes de la procédure pour la préparation, l'élution et la révélation de plaques de CCM pendant le suivi de l'avancement d'une réaction chimique. On considère que la phase stationnaire est un gel de silice standard comportant un indicateur fluorescent.
Chaque trait est à écrire au crayon à papier, car les encres des plumes ou des stylos sont solubles dans la plupart des éluants, donc fausseraient la chromatographie.
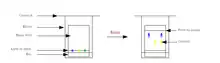
- On trace un trait horizontal (la ligne de base) à environ 1 cm du bas de la plaque de CCM. Les marques D, B et M représentent respectivement le produit de Départ, le brut réactionnel et le point Mixte (un mélange de D et B). Le point mixte permet de mieux visualiser les taches lorsqu'elles sont très proches ou lorsque l'étape d'élution est imparfaite.
- On dépose, à l'aide d'un capillaire ou d'une microseringue, une petite quantité d'une solution du produit de départ sur les marques D et M et une petite quantité du brut réactionnel sur les marques B et M. Dans cet exemple, le produit de départ est incolore (cercle en pointillé) alors que le brut réactionnel est légèrement coloré.
- On prépare à côté, un éluant qui recouvrira le fond de la cuve sur environ 5 mm de hauteur, et on laisse saturer la cuve. (C'est-à-dire : laisser la cuve fermée et laisser les vapeurs de l'éluant 'remplir' le volume de la cuve, environ 5-10 min).
- On place la plaque de CCM dans la cuve contenant l'éluant. Le solvant monte le long de la plaque par capillarité. Lorsqu'il arrive presque en haut de la plaque, on sort celle-ci de la cuve, on marque la ligne de front (là où l'éluant s'est arrêté de migrer) et on laisse l'éluant s'évaporer. Ici, on ne voit que les taches 3 et 5 puisque les autres sont incolores. On observe que la tache 5 n'a que très légèrement migré au-dessus de la ligne de base.
- Pour visualiser les différentes taches, on commence par placer la plaque sous une lampe UV à 254 nm. La plaque apparaît en vert fluorescent et les produits qui absorbent les UV apparaissent sous forme de taches sombres. On utilise cette méthode de détection en priorité car elle n'endommage pas la plaque. Dans cet exemple, on voit que le brut réactionnel contient encore du produit de départ (tache 4) mais la taille de la tache indique qu'il y en a moins qu'en début de réaction. On observe la formation d'au moins trois nouveaux produits (1, 2 et 5) : 1 et 2 sont moins polaires que le produit de départ, et 5 est plus polaire. Il semble que le produit 5 est majoritaire dans le brut réactionnel (le produit 2 est beaucoup moins visible) mais tous les produits ne révèlent pas avec la même intensité aux UV.
- On plonge la plaque dans une solution acide de vanilline (il existe de nombreux autres révélateurs) et l'on chauffe la plaque jusqu'à ce que des taches colorées apparaissent. Ici on observe un autre produit (3) qui n'était pas visible aux UV. La tache 1 est à peine visible ; elle l'était beaucoup plus sous lampe UV. La surprise vient de la tache 2 : elle n'était que faiblement visible en UV mais elle révèle très intensément avec la vanilline. Il est fort possible que ce soit le produit majoritaire de la réaction et non le produit 5 comme le laissait supposer la détection UV.
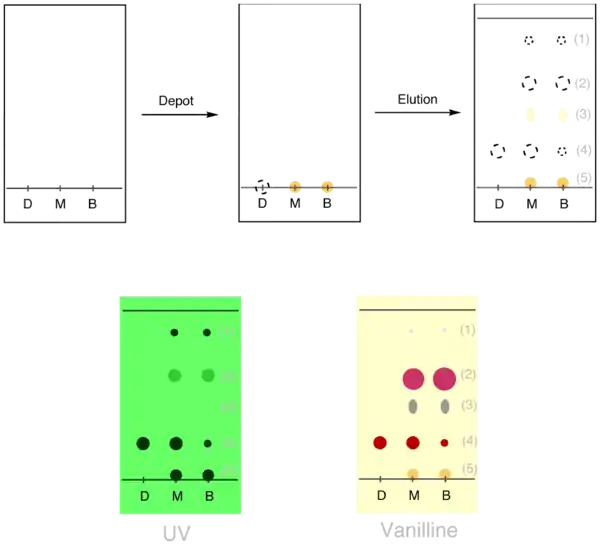
Conclusion : il se produit bien quelque chose lors de cette réaction chimique. Plusieurs produits sont formés mais l'un (no 2) semble nettement majoritaire. Il faudra refaire une CCM un peu plus tard pour suivre la disparition de la tache 4 (produit de départ) dans la colonne B (brut réactionnel) ce qui signifiera que la réaction est terminée. Ensuite, une chromatographie sur colonne permettra d'isoler les différents produits et d'effectuer des analyses plus poussées pour s'assurer que le produit 2 est bien le produit attendu.
Révélateurs
Lien vers le site du Club de Chromatographie sur Couche Mince : http://www.clubdeccm.com/PDF/Dyeing_Reagents_TLC.pdf ce document PDF très complet donne une description exhaustive (appuyée de références bibliographiques) de 335 révélateurs.
Révélation au permanganate de potassium
- 10 g de K2CO3
- 1,5 g de permanganate de potassium (KMnO4)
- 150 ml d'eau distillée
- 1,25 ml d'hydroxyde de sodium (NaOH) en solution à 10 %
On l'utilise en spray ou par trempage et cela produit une coloration jaune/marron des produits oxydables sur un fond violet/rose. Il est utilisable sur les plaques Alumine et Silice. L'avantage par rapport à d'autres produits de révélation est qu'il n'est pas nécessaire de chauffer (on peut donc révéler les plaques sur plastique).
La vanilline
Il est parfois considéré (à tort) que la vanilline comme révélateur est difficile à préparer. Il est vrai que dans certains cas, la solution va virer au violet en l'espace de quelques heures et devenir inutilisable. La raison est très simple : lorsque ce révélateur est apparu, on utilisait presque exclusivement de l'éthanol à 96 % qui est le solvant pour cette préparation. À l'heure actuelle, on utilise principalement l'éthanol absolu (<0,02 % d'eau) pour toute opération qui demande un solvant contenant peu d'impuretés, or la présence d'eau (5-10 %) est absolument nécessaire pour que le révélateur reste stable. La recette actualisée est donc :
- Ajouter 2 ml d'acide sulfurique (H2SO4) à 200 ml d'éthanol à 90-96 % (ou 190 ml d'éthanol absolu et 10 ml d'eau désionisée),
- Ajouter 800-1 000 mg de vanilline et agiter jusqu'à dissolution complète,
- Conserver à l'abri de la lumière.
Ce révélateur est utilisé en spray ou par trempage suivi d'un chauffage à environ 200 °C jusqu'à ce que les taches apparaissent.
On peut noter que ce type de révélation produit souvent des couleurs intenses dans tout le spectre visible et que la couleur d'une tache est caractéristique du composé présent. Il est ainsi possible de :
- Différencier deux composés ayant le même Rf juste par la couleur, bien que cela soit rare,
- Détecter la présence d'un groupe fonctionnel particulier pour des molécules simples ; par exemple, la présence d'un groupe O–THP est caractérisée par une tache d'un rouge intense.
Astuces
Éviter la marque au front de migration
Bien souvent, les plaques commerciales sont recouvertes d'un produit (gel de silice), qui vient perturber la révélation. En effet, on se retrouve bien souvent avec une ligne au niveau de ce front. Elle est souvent considérée (à tort) comme la marque des solvants utilisés. Mais une méthode simple pour éviter ce phénomène est de faire migrer intégralement la plaque dans le système de solvant que l'on va utiliser par la suite et de la laisser bien sécher avant utilisation. L'avantage principal de cette technique est de permettre de voir plus clairement si des produits ont migré sans être retenus par la phase solide.
Affiner les dépôts
Un dépôt idéal est une ligne fine faite en une seule fois. Cependant, en fonction de l'origine du produit déposé, cela n'est pas forcément facile. On peut utiliser un solvant fort (acétone/méthanol 90:10 sur de la silice par exemple) que l'on va utiliser pour faire migrer l'intégralité la fraction déposée et ce seulement sur quelques millimètres. Ainsi on se retrouve bien souvent avec une ligne bien nette ce qui permet de discriminer plus facilement des produits ayant des comportements relativement proches sur la plaque. Il faut par contre s'assurer du séchage complet de la plaque avant de poursuivre avec le développement.
Découpage d'une plaque souple
Les plaques sur support souple sont faites pour être découpées. Cependant, la phase solide se détache facilement de ce support, et au moment de la découpe s'émiette provoquant ainsi divers artefacts lors du développement de la plaque (effets de bord dans lesquels un côté de la plaque va migrer plus vite que l'autre). Pour éviter cela, lors de la découpe, on peut pencher les ciseaux à 45° dans le sens des aiguilles d'une montre (pour des ciseaux droitiers, l'inverse pour des gauchers) dans l'axe de la découpe.
Exemples
 CCM d'une encre noire (une encre noire est un mélange d'encres de plusieurs couleurs)
CCM d'une encre noire (une encre noire est un mélange d'encres de plusieurs couleurs)

Chromatographie bidimensionnelle sur couche mince
La chromatographie bidimensionnelle sur couche mince (ou CCM-2D) a deux applications principales :
- Aider à mieux identifier les constituants d'un mélange complexe,
- Détecter une dégradation d'un composé sur la phase stationnaire.
Séparation de mélanges complexes
Pour séparer des mélanges complexes de substances similaires, il peut être utile d'employer la chromatographie bidimensionnelle. La chromatographie bidimensionnelle sur couche mince s'effectue en deux étapes entre lesquelles on change de solvant et on tourne la plaque de 90°. Les interactions développées par le nouveau solvant seront différentes, ce qui modifiera la séparation dans cette deuxième dimension et permettra une meilleure séparation globale.
Détection d'une dégradation
Certains composés se dégradent au contact de la phase stationnaire et/ou du mélange de solvants utilisés. Une méthode simple pour détecter cette dégradation est d'utiliser la chromatographie bidimensionnelle sur couche mince.
Sur une plaque carrée, on dépose un peu de la solution à analyser dans un coin de la plaque à environ 1 cm de chaque bord. On procède à une première élution après laquelle on sèche rapidement la plaque. On procède alors à une seconde élution à 90° de la première avec le même éluant. Puisque la plaque est carrée et que le Rf d'un composé stable reste le même d'une élution à l'autre, les produits stables apparaissent sur la diagonale. En revanche, les composés qui se dégradent vont apparaitre en dehors de la diagonale car les produits de dégradation (qui sont formés pendant et entre les élutions) ont généralement des Rf différent du produit de départ.
Notes et références
- (en) « planar chromatography », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8)
Voir aussi
- Far-eastern blot (également appelé Thin Layer Chromatography Blot), une technique d'analyse des lipides.