Oxychalcogénure
Les oxychalcogénures sont une famille de matériaux composés d'anions oxydes et chalcogène (16e colonne du tableau périodique : S, Se, Te), et de cations métalliques. Par exemple La2O2S, BiOCuSe, Ce2O2S, Bi2O2Te, BiOCuTe, bien que les deux derniers exemples soient plus rares en raison du coût plus élevé du tellure. Leur première cristallisation date de 1900 avec l’oxyséléniure de manganèse[1], suivie en 1910 des oxyséléniures avec du phosphate[2]. De nos jours, les matériaux les plus étudiés sont ceux sous forme BiOCuSe en raison de leur performance thermoélectrique[3]. Cependant, il reste encore de nombreux matériaux non explorés et exploités qui pourraient avoir de meilleurs résultats en termes d’efficacité, de résistivité et de conductivité électrique.
Structure
Les oxychalcogénures adoptent une structure en couche dans laquelle on trouve une alternance de cations oxydes métalliques au caractère ionique et d'anions chalcogénures au caractère covalent[3]. Cette structure en couches est due au pouvoir polarisant des ions mis en jeu. Les gros cations faiblement chargés vont donc se trouver proches des anions oxydes (petits et fortement chargés), tandis que, inversement, les petits cations fortement chargés vont plutôt se trouver proches des anions chalcogénures (plus gros et moins chargés que les oxydes)[3]. On observe donc une séparation des anions oxydes et chalcogénures en fonction de leur pouvoir polarisant[3]. Il existe différents types de structures.
Structure (A2O2)Ch
C'est la structure la plus simple dans laquelle on trouve une alternance de cations (A2O2)2+ et d'anions Ch2−, où A est un élément de terre rare ou du bismuth et Ch est un élément chalcogène au degré d'oxydation -II. L'oxyde (A2O2)2+ a une coordinence tétraédrique type CaF2 tandis que les chalcogénures forment un plan. Des composés comme La2O2S, Ce2O2S ou Bi2O2Te par exemple présentent ce type de structure. Les composés contenant du tellure cristallisent dans le système quadratique, alors que ceux contenant du soufre ou du sélénium cristallisent dans un système rhomboédrique ou hexagonal (système trigonal)[3].
Structure (A2O2)Ch2
Cette structure reprend les mêmes principes que la structure (A2O2)Ch avec la cation (A2O2)2+ en coordinence tétraédrique type CaF2 et les anions chalcogénures, cette fois au degré d'oxydation -I forment un plan. Les composés qui adoptent cette structure cristallisent dans le système orthorhombique, La2O2S2 en est un exemple[3].
Structure (A4O4)Ch3
La structure (A4O4)Ch3 peut être décomposée comme une structure (A4O4)(Ch2)Ch dans laquelle on retrouve les chalcogénures des deux structures précédentes, deux au degré d'oxydation -I et un au degré d'oxydation -II, cependant le seul chalcogène connu dans cette structure est le sélénium. Les cations (A2O2)2+ quant à eux ont toujours une coordinence tétraédrique type CaF2[3].
Structure (AO)(MCh)
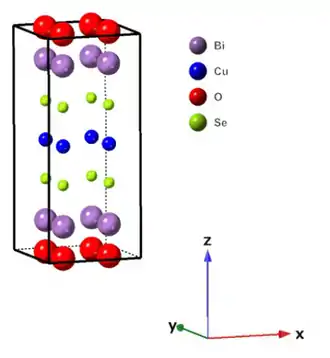
Comme pour les structures avec les couches Ch2− et (Ch2)2−, A est un élément de terre rare ou du bismuth pour former le cation (A2O2)2+. L'anion chalcogénure quant à lui est (M2Ch2)2− où M est un métal de transition monovalent (le plus souvent cuivre ou argent)[3]. La structure du cation (A2O2)2+ est de type PbO et celle de l'anion (M2Ch2)2− est de type anti-PbO. BiOCuSe et BiOCuTe sont des exemples de composés de structure (AO)(MCh). Ces composés cristallisent dans le système quadratique[4].
Structure (A2O2)(MCh2)
Dans cette structure, A peut être du lanthane ou cérium, M peut être du fer, zinc, manganèse ou cadmium et Ch du sélénium. Les deux couches (A2O2)2+ et (MCh2) adoptent une structure type CaF2. Pour la couche chalcogénure, le métal M occupe la moitié des sites tétraédriques de la structure. La2O2CdSe2 est un exemple de composé adoptant cette structure[3].
Structure (A2BO2)(M2Ch2)
Dans cette structure, A peut être du baryum ou du strontium, B peut être du manganèse, cobalt, nickel ou zinc, et Ch du soufre ou du sélénium. Les couches de cette structure sont une couche (M2Ch2)2− de type CaF2 et une couche (BO2)2+ qui forme un plan. Ces deux couches sont séparées par des rangées de cation A2+. Sr2ZnO2Cu2Se2 est un exemple de composé qui a cette structure[3].
Structure (A2B2O)(M2Ch2)
Cette structure est la même que la structure (A2BO2)(M2Ch2) avec une couche chalcogénure de type CaF2, une couche plane (B2O)2+, où ici le cation B est monovalent, ces deux couches étant séparées par des rangées de cation A+. Na2Cu4OSe2, qui peut être écrit (Na2Cu2O)(Cu2Se2) est un exemple de composé adoptant cette structure[3].
Synthèse
Les oxychalcogénures sont généralement synthétisés par des réactions à l'état solide dans des tubes en verre de silice évacués pour empêcher l'évaporation des éléments chalcogènes. Les oxychalcogénures La5Cu6O4S7 sont élaborés en chargeant du La2S3 du Cu et du KI dans un tube de silice fondue sous atmosphère d'argon dans une boîte à gants. Ce tube est scellé sous une atmosphère de 10−4 Torr puis placé dans un four contrôlé par ordinateur. L'échantillon est chauffé à 1 173 K à 1 K/min, maintenu à 1 173 K pendant 4 jours et refroidi à 0,05 K/min à 573 K ; puis le four est éteint. Le mélange réactionnel est lavé sans sels d'iodure avec de l'eau puis séché avec de l'acétone[5].
Pour le La2O3Mn2Se2 des poudres de La2O3 séchées et de Mn brillante et de Se sont soigneusement mélangées et pressées en pastilles à l'intérieur d'une boîte à gants remplie d'Ar. Les pastilles sont ensuite scellées dans un tube en quartz sous atmosphère d'argon. Ils sont lentement chauffés à 650 °C pendant 12 heures puis chauffés à 1 050 °C pendant 6 jours, avec deux rebroyages intermédiaires dans la boîte. Le tube de quartz est ensuite refroidi à l'air[6].
Les matériaux thermoélectriques à base de BiCuSeO peuvent être synthétisés par alliage mécanique, conduisant à des poudres nanocristallines monophasées. Cette nouvelle voie de synthèse permet la synthèse à la fois de matériaux non dopés, avec des concentrations en porteurs du même ordre de grandeur que celles observées pour des échantillons préparés selon une voie de synthèse classique, et des matériaux fortement dopés p. Il est à noter que les propriétés de transport électrique ne sont pas dégradées par rapport à la voie de synthèse conventionnelle. Les principales caractéristiques de cette nouvelle voie de synthèse sont que toutes les étapes peuvent être réalisées sous air à température ambiante, et qu'elle permet la synthèse de grandes quantités de poudre en quelques heures. Par rapport aux étapes de synthèse classiques, qui nécessitent de longs recuits à haute température sous argon dans des tubes de silice scellés, ces avantages ouvrent la voie aux applications industrielles des oxychalcogénures thermoélectriques[7].
Des découvertes récentes dans les oxyarséniures de fer et leur supraconductivité ont mis en évidence l'importance des systèmes d'anions mixtes. Les oxychalcogénures de cuivre mixtes sont apparus lorsque les propriétés électroniques des chalcogénures et des oxydes ont été prises en compte. Les chimistes ont commencé à poursuivre la synthèse d'un composé aux propriétés métalliques et à onde de densité de charge ainsi qu'à la supraconductivité à haute température. En synthétisant l'oxyséléniure de cuivre Na1.9Cu2Se2·Cu2O en faisant réagir Na2Se3.6 avec Cu2O, ils ont conclu qu'un nouveau type d'oxychalcogénures pouvait être synthétisé en faisant réagir des oxydes métalliques avec des flux de polychalcogénogénures.
Propriétés
Propriétés thermoélectriques
Les propriétés thermoélectriques de ces matériaux sont mis en avant de plus en plus car auparavant seuls les propriétés magnétiques étaient étudiés. La structure électronique des oxychalcogénures en couches (caractère bidimensionnel mis en avant) montre une superposition des structures électroniques qui sont stabilisées par des transferts de charge. Les matériaux de type p verront ainsi leur propriété de transport électrique caractérisé par la structure électronique de la couche (haut de la bande de valence). Quant aux matériaux de type n, la nature du bas de la bande de conduction détermine leur propriété de transport électrique[3].
La faible dimensionnalité des oxychalcogénures leur confère une certaine structure de bande anisotropique. En effet, une conduction électrique et thermique est observable selon certaines directions et plans. La propriété majeure des oxychalcogénures est la performance thermoélectrique. Cette dernière est ajustée par leur conductivité thermique qui est contrôlée par des changements de température. Ces matériaux ont une structure avec une alternance entre couche d’oxyde ionique et chalcogénure covalent. Cette dernière est la source d’une conduction électronique. De plus, le caractère covalent permet une semi conductivité de haute mobilité. Les interactions ioniques génèrent, quant à elles, une faible conductivité thermique[3].
La résistivité électrique est très élevée dans ces matériaux et présente une dépendance en température. Mais, ceci peut être un inconvénient car la résistivité peut limiter les performances thermoélectriques.
Propriétés électriques et magnétiques
BiOCuS, BiOCuSe et BiOCuTe sont des matériaux à bande interdite indirecte avec des valeurs de bande interdite de 0,66, 0,51 et 0,26 eV respectivement[8].
Les oxychalcogénures à cinq composants nouvellement synthétisés comme le Ca4Fe2Cu2Ch2O6 peuvent être caractérisés comme des semi-conducteurs ioniques antiferromagnétiques, où des blocs de chalcogénure non magnétique (Cu2Ch2) alternent avec des blocs d'oxyde antiferromagnétique (Ca4Fe2O6)[9].
Propriétés optiques
Pour l'etude des composés BiOCuS, BiOCuSe et BiOCuTe, les porteuses inter-bandes et libres dominent les constantes optiques avec un comportement semblable au métal pour les photons de haute énergie ce qui suggèrent que ces matériaux sont de bons candidats pour les dispositifs optoélectroniques, les matériaux de blindage et les détecteurs de rayonnement infrarouge[8].
Applications
De par leurs propriétés thermoélectriques, les oxychalcogénures sont utilisés en tant que semi-conducteurs (plus particulièrement ceux à base de BiCuSeO). En effet, ils ont une conductivité thermique et électronique intéressante[10].
Notes et références
- Fonzes-Diacon, H. (1990), A synthesized selenide and an oxyselenide of manganese, Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences, 130, 1025, 1025–6.
- Ephraim, F. et E. Majler (1910), Selenophosphates, Berichte der Deutschen Chemischen Gesellschaft, 43, 277–285.
- Son D. N. Luu et Paz Vaqueiro, Layered oxychalcogenides: Structural chemistry and thermoelectric properties, Journal of Materiomics, vol. 2, no 2, p. 131-140, .
- C. Barreteau, Matériaux céramiques thermoélectriques pour la production d’électricité propre, Other, université Paris-Sud, 2013.
- Fu Qiang Huang, Paul Brazis, Carl R. Kannewurf et James A. Ibers, Synthesis, Structure, Electrical Conductivity, and Band Structure of the Rare-Earth Copper Oxychalcogenide La5Cu6O4S7, Journal of Solid State Chemistry, 155, 366-371 (2000).
- L. Xie et H. G. Zhang, Magnetic properties and exchange bias effect of the layered manganese oxychalcogenides La2O3Mn2Se2, J. Appl. Phys., 113, 204506 (2013).
- V. Pele, C. Barreteau, D. Berardan et al., Direct synthesis of BiCuChO-type oxychalcogenides by mechanical alloying, Journal of Solid State Chemistry, 2013, vol. 203, p. 187-191.
- A K M F Ul Islam, M A Helal, M N H Liton, M Kamruzzaman et H M T Islam, First principles study of electronic structure dependent optical properties of oxychalcogenides BiOCuCh (Ch 5 S, Se, Te), J. Phys., 2016.
- D.V. Suetin et A.L. Ivanovskii, Electronic, magnetic properties and chemical bonding in layered oxychalcogenides Ca4Fe2Cu2S2O6 and Ca4Fe2Cu2Se2O6 from first principles calculations, Journal of Solid State Chemistry, 194100–105 (2012).
- W. Khan, S. Azam, M. Benali Kanoun et S. Goumri-Said, Optoelectronic structure and related transport properties of BiCuSeO-based oxychalcogenides: First principale calculations, vol. 58, août 2016, p. 86-93.