Membrane (biologie)
La membrane, en biologie cellulaire, est un assemblage de molécules en un double feuillet séparant la cellule de son environnement et délimitant le cytoplasme cellulaire, ainsi que les organites à l'intérieur de celui-ci[1]. La membrane est un ensemble complexe de lipides, de protéines et de sucres (ou oses) régulant les échanges de matière entre l'intérieur et l'extérieur de la cellule ou entre deux compartiments cellulaires par des transporteurs, bourgeonnement de vésicules, phagocytose, etc. Les composants-clé de la membrane biologique sont les phospholipides. Ils ont la capacité de s'auto-organiser en un double feuillet, leurs têtes hydrophiles pointant vers l'extérieur et leurs chaînes hydrophobes pointant vers l'intérieur de la membrane.
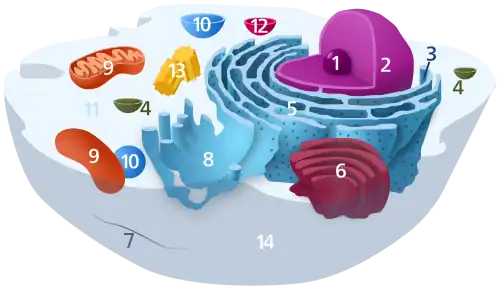
(1) Nucléole
(2) Noyau
(3) Ribosomes
(4) Vésicule
(5) Réticulum endoplasmique rugueux (ou granuleux) (REG)
(6) Appareil de Golgi
(7) Cytosquelette
(8) Réticulum endoplasmique lisse
(9) Mitochondries
(10) Vacuole
(11) Cytosol
(12) Lysosome
(13) Centrosome (constitué de deux centrioles)
(14) Membrane plasmique
On parle de membrane plasmique, ou plasmalemme, lorsque celle-ci délimite une cellule (le milieu intérieur est alors le cytoplasme). On parle de membrane intracellulaire, ou endomembrane, lorsqu'elle délimite un organite (p.ex. membrane mitochondriale, nucléaire, lysosomiale, etc.).
Histoire
- 1665 : Robert Hooke observe pour la première fois des cellules à l'aide d'un microscope à deux lentilles. Il utilise cette appellation dans son sens originel qui désigne une petite chambre.
- 1632–1723 : Antoni van Leeuwenhoek observe pour la première fois des protozoaires, des bactéries et des globules rouges grâce à son microscope.
- 1813 : Eugène Chevreul décrit le concept d'acide gras. Il publie en 1823 ses « Recherches chimiques sur les corps gras d'origine animale ».
- 1847 : Théodore Nicolas Gobley isole la lécithine du jaune d'œuf[2]. Il est de fait le découvreur des phospholipides.
- 1855 : Von Nägeli et Carl Eduard Cramer créent le concept de membrane en tant que barrière pour expliquer les phénomènes osmotiques.
- 1890 : Lord Raleigh réalise une série d'expériences sur l'interface eau-huile et calcule l'épaisseur d'un film d'huile à la surface d'une étendue d'eau.
- 1895-1899 : Charles Ernest Overton découvre que la capacité d'une substance à traverser la membrane dépend de son caractère hydrophobe. Il formule l'hypothèse d'une membrane composée de lipides.
- 1917 : Irving Langmuir étudie la structure des films d'huile à la surface de l'eau. Il formule l'hypothèse d'une monocouche d'acide gras s'orientant verticalement, le groupe carboxyl orienté vers l'eau et la chaîne alkyle orientée vers l'air[3].
- 1925 : Gorter et Grendel démontrent la capacité de certains lipides à former des simples et des doubles couches. Ils montrent également que la surface des lipides extraits des globules rouges est égale à deux fois la surface de ces cellules. Ils sont ainsi les premiers à formuler l'hypothèse d'une membrane cellulaire formée d'une double couche de lipides[4].
- 1935 : James Frederic Danielli et Hugh Davson formulent l'hypothèse d'une membrane cellulaire composée d'une bicouche de lipides en sandwich entre deux couches de protéines[5].
- 1965 : Bangham, Standish et Watkins synthétisent les premiers liposomes à partir de lécithine d'œuf déshydratée[6].
- 1972 : Jonathan S. Singer et Garth L. Nicholson repensent l'hypothèse de Danielli et Davson et décrivent le modèle de la mosaïque fluide. La membrane est toujours organisée en bicouche mais les têtes polaires des phospholipides sont directement en contact avec l'eau. Les protéines membranaires « flottent » dans ou en surface des lipides[7].
Bicouche lipidique

Une membrane est composée d'une bicouche de lipides amphipathiques ou amphiphiles, des phospholipides dans la plupart des cas. Chaque lipide membranaire est constitué d'une tête polaire hydrophile orientée vers l’extérieur de la membrane et d'une queue hydrophobe (chaîne d'acide gras saturée ou insaturée) orientée vers l'intérieur. L'épaisseur d'une membrane est d'environ 7,5 nm. La membrane cytoplasmique est qualifiée de « dynamique » de par son constant renouvellement.
Auto-organisation des lipides membranaires
En milieu aqueux, les lipides amphiphiles s'organisent spontanément sous forme de micelles ou de liposomes selon la taille de la partie hydrophobe. Les parties hydrophobes se rassemblent et les têtes hydrophiles sont exposés au milieu aqueux. Si la partie hydrophobe est peu encombrante, les lipides formeront des micelles, sinon ils formeront des liposomes (avec membrane en bicouche lipidique). Cette disposition se fait naturellement car elle permet au système d'avoir une entropie plus élevée[8].
Modèle de la mosaïque fluide
Le terme de mosaïque fluide, dû à Singer et Nicolson[7], est souvent employé pour décrire à la fois la composition et le comportement dynamique des membranes biologiques :
- mosaïque car la composition de la membrane est très hétérogène à la fois dans l'espace et le temps. Ainsi, l'existence de protéines intégrales (membranaires), de lipides différents (une différence de composition entre le feuillet interne et externe est aussi observée), de sucres complexes, existant 'presque' indépendamment les uns des autres, explique la dénomination de mosaïque.
- fluide car les phospholipides et les protéines membranaires peuvent se mouvoir dans le plan de la membrane. De plus, la membrane est un corps parfaitement déformable dans les 3 directions de l'espace. Par exemple, la membrane peut onduler : les phospholipides peuvent en effet exécuter trois mouvements: par diffusion latérale, par rotation, et par flip-flop (le flip-flop est cependant plus rare pour les phospholipides que pour les stérols intégrés dans la membrane plasmique). Ce dernier mouvement doit être catalysé par des enzymes, les flipases. De plus, les queues hydrophobes des phospholipides peuvent produire des mouvements de flexion (ou battement).
Les principaux composants influant sur la fluidité d'une membrane sont les phospholipides insaturés et le cholestérol :
- Les phospholipides avec une chaine d'acide gras insaturée fluidifient la membrane en diminuant les interactions de van der Waals ;
- En grande quantité, le cholestérol rigidifie la membrane en gênant la diffusion latérale des éléments mais, en quantité adaptée, il la fluidifie et diminue la température de gel de la membrane en gênant les interactions de van der Waals[9].
Membrane et tension de surface
Globalement, la tension superficielle d'une membrane biologique est nulle : ce n'est pas une bulle de savon qui éclate au moindre contact ! En revanche, cette tension peut être localement non nulle. D'une part, les têtes polaires des lipides, peu fluides, ont tendance à se compacter en créant localement un pic négatif de tension. D'autre part, les queues hydrophobes, très fluides, ont tendance à occuper beaucoup d'espace, créant localement un pic de tension positif. Les pics de tension positif et négatif s'équilibrant, la tension superficielle globale reste nulle.
Composition
Les parts des différents constituants (glucides, protéines et lipides) varient d'un type cellulaire à l'autre. On peut néanmoins donner en exemples les valeurs trouvées pour le globule rouge :
- Lipides : 40 % (55 % de phospholipides, 25 % de cholestérol et 20 % de glycolipides)
- Glucides : 8 % (glycocalyx)
- Protéines : 52 %
De plus, cette composition est généralement asymétrique. Autrement dit, chaque feuillet de la membrane a une composition particulière. Cette asymétrie de composition est bien entendu à mettre en relation avec une asymétrie de fonction. En termes de lipides membranaires, la couche externe est constituée majoritairement de glycolipides, de cholestérol, de sphingomyéline et de phosphatidylcholine, et la couche interne est constituée en majorité de cholestérol, de phosphatidylinositol, de phosphatidylsérine, et de phosphatidyléthanolamine. Attention toutefois, un lipide membranaire de la couche externe peut passer dans la couche interne et vice versa grâce notamment au phénomène dit de flip-flop, phénomène qui consiste en l'échange de position d'un lipide de la couche externe avec un lipide de la couche interne.
On trouve du reste sur la couche externe de toutes les membranes plasmiques des cellules des résidus sucrés formant un cell-coat, un « manteau » de protection pour la cellule. Ces oses se branchent de façon covalente sur les lipides et protéines de la membrane. Un lipide sur dix est glycosilé alors que la grande majorité des protéines (transmembranaires et périphériques externes) le sont.
Propriétés des membranes
Perméabilité sélective
En premier lieu, les membranes biologiques constituent une barrière sélective entre l'intérieur et l'extérieur d'une cellule ou d'un compartiment cellulaire (organite). Elles présentent donc la propriété de perméabilité sélective, qui permet de contrôler l'entrée et la sortie des différentes molécules et ions entre le milieu extérieur et celui intérieur. Cela permet à chaque organite cellulaire, mais également à la cellule tout entière d'avoir une composition propre différant de celle extérieure.
En elles-mêmes, les membranes ne sont perméables qu'aux petites molécules hydrophobes (O2, N2, glycérol, ...), par diffusion simple. Mais elles servent de support à de nombreuses protéines transmembranaires ayant pour rôle de réguler les échanges transmembranaires (ex : canaux ioniques pour les transferts d'ions, aquaporines pour le transfert d'eau par osmose, ...). Il est possible de distinguer différents types de transfert à travers la membrane :
- Le transport passif : transport de composés sans consommation d'énergie (le long du gradient électrochimique). Il existe deux sortes de transport passif :
- La diffusion simple : diffusion de composés directement à travers la bicouche lipidique ;
- La diffusion facilitée : transport de composés à travers la bicouche lipidique grâce à une protéine de transport. (petites molécules (de masses moléculaires inférieures à environ 500-700 u))
- Le transport actif : transport de composés à travers la bicouche lipidique grâce à une protéine de transport et une consommation d'énergie sous forme d'ATP (contre le gradient électrochimique).
Le transport à travers les membranes de molécules plus grosses se fait par endocytose (vers l'intérieur) et exocytose (vers l'extérieur).
Plus généralement, la membrane sert de barrière sélective à l'information biologique. Cette information prend la forme d'une hormone, d'un sucre, d'une protéine, etc. Elle est captée par des récepteurs membranaires, des protéines capables de reconnaître spécifiquement un composé. Cette reconnaissance enclenche un mécanisme de signalisation cellulaire aboutissant à une réaction de la cellule face au signal qu'elle a reçu.
Capacité à se sceller
Les membranes ont la capacité de fusionner et de se séparer. Ce mécanisme est prépondérant dans les phénomènes d'exocytose et d'endocytose.
Notes et références
- (en) « Structure and dynamics of Membranes », Handbook of Biological Physics Vol. 1A and 1B, ed. R. Lipowsky and E. Sackmann, Amsterdam: Elsevier, 1995.
- (fr) Gobley N.T., « Recherches chimiques sur le jaune d'œuf - Examen comparatif du jaune d'œuf et de la matière cérébrale », J Pharm Chim, vol. 11:409, 1847.
- (en) Langmuir I, « The constitution and fundamental properties of solids and liquids. II. Liquids », J Am Chem Soc, vol. 39:1848, 1917.
- (en) Gorter E. et Grendel F., « On bimolecular layers of lipoids on the chromocytes of the blood », J Exp Med, vol.41(4):439-443, 1925.
- (en) Danielli J.F. et Davson H., « A contribution to the theory of permeability of thin films », J Cell Comp Physiol, vol. 5:495-508, 1935.
- (en) Bangham A.D., Standish M.M. and Watkins J.C., « Diffusion of univalent ions across the lamellae of swollen phospholipids », J Mol Biol,vol. 13(1):238-252, 1965.
- (en) S. J. Singer et Garth L. Nicolson, « The Fluid Mosaic Model of the Structure of Cell Membranes », Science, vol. 175, , p. 720–731 (ISSN 0036-8075 et 1095-9203, PMID 4333397, DOI 10.1126/science.175.4023.720, lire en ligne, consulté le )
- (fr) Yann Brassaglia, Biologie Cellulaire 2e édition, collection "Sciences fondamentales", édition Maloine, 2004, p.7-8, (ISBN 2 224 02862 8)
- (fr) Yann Brassaglia, Biologie Cellulaire 2e édition, collection "Sciences fondamentales", édition Maloine, 2004, p.11, (ISBN 2 224 02862 8)
Voir aussi
Bibliographie
- Phillip Eichman, « From the lipid bilayer to the fluid mosaic: a brief history of membrane models », University of Minnesota: Sociology, History and Philosophy of Science: teachers' network news, vol.9(2), 1999.
Articles connexes
Lien externe
- Cyberlipid.org, « Chronological history of lipid science »