Dioxyde d'azote
Le dioxyde d'azote est un composé chimique de formule NO2. Concentré, il se présente comme un gaz brun-rouge toxique suffocant à l'odeur âcre et piquante caractéristique. C'est un précurseur de la production industrielle de l'acide nitrique HNO3 et un polluant majeur de l'atmosphère terrestre produit par les moteurs à combustion interne (à Diesel majoritairement) et les centrales thermiques ; il est responsable à ce titre du caractère eutrophisant et acidifiant des « pluies acides » non soufrées (le NO2 combiné à l'ozone troposphérique anthropique forme des nitrates très solubles dans l'eau). Il est aussi responsable de la présence d'acide nitrique (où ce dernier se forme par hydratation du NO2) :
| Dioxyde d'azote | |
  Structure du dioxyde d'azote. |
|
| Identification | |
|---|---|
| Nom UICPA | dioxyde d'azote |
| No CAS | |
| No ECHA | 100.030.234 |
| No CE | 233-272-6 |
| No RTECS | QW9800000 |
| PubChem | 3609161 |
| ChEBI | 33101 |
| SMILES | |
| InChI | |
| Apparence | gaz brun rougeatre ou liquide brun ou jaune, d'odeur âcre[1]. |
| Propriétés chimiques | |
| Formule | NO2 [Isomères] |
| Masse molaire[2] | 46,005 5 ± 0,000 8 g/mol N 30,45 %, O 69,55 %, |
| Moment dipolaire | 0,316 ± 0,010 D[3] |
| Propriétés physiques | |
| T° fusion | −11,2 °C[1] |
| T° ébullition | 21,2 °C[1] |
| Solubilité | dans l'eau : réaction[1] |
| Masse volumique | 1,45 g·cm-3 (liquide)[1] |
| Pression de vapeur saturante | à 20 °C : 96 kPa[1] |
| Point critique | 157,85 °C, 20,17 MPa[4] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 9,586 ± 0,002 eV (gaz)[5] |
| Précautions | |
| SGH[6] | |
   Danger |
|
| SIMDUT[7] | |
    A, C, D1A, D2B, E, |
|
| Transport | |
| Inhalation | Mortel, apparition d'acide nitrique dans les poumons par réaction avec l'eau |
| Écotoxicologie | |
| Seuil de l’odorat | bas : 0,05 ppm haut : 0,14 ppm[8] |
| Unités du SI et CNTP, sauf indication contraire. | |
Apparence
Pur, il présente une coloration brunâtre (vapeurs rutilantes) et une odeur douceâtre. C'est une des odeurs que l'on perçoit dans les rues polluées par la circulation automobile.

Structure
La structure plus stable de NO2 est O-N·-O avec un angle de 134 degrés et le point représentant cet électron célibataire sur l'atome d'azote, et des tirets entre les deux N-O en plus de l'existence de la liaison « normale » N-O. Les charges formelles seraient plus élevées que celles de la structure présentée ; sa présence sur l'atome d'azote est plus proche de la réalité, bien que tout ceci n'est qu'une question de densité de probabilité de présence de l'électron en cause. Il passe « plus de temps » sur l'azote que sur un des deux oxygènes[9].
Sa structure radicalaire le rend très réactif vis-à-vis des molécules organiques.
Équilibre monomère-dimère
Ce gaz a un équilibre permanent, mais dépendant des conditions de température et de pression, avec son dimère, le peroxyde d'azote N2O4 :
Cette dimérisation, exothermique, est favorisée à basses températures. Le peroxyde d'azote N2O4, corps diamagnétique incolore peut être obtenu en un solide fondant à −11,2 °C[10]. Et il se retransforme réversiblement en NO2, le monomère paramagnétique coloré, en une réaction endothermique à plus hautes températures.

Agent polluant
L'électron non-apparié du dioxyde d'azote en fait un oxydant et un poison violent : son inhalation donne une réaction instantanée avec l'eau de la muqueuse interne des poumons, conduisant à la production d'acide nitrique.
Constamment émis par la plupart des véhicules, des centrales électriques thermiques à combustible (charbon, principalement) et des activités industrielles, le dioxyde d'azote est aussi un précurseur d'autres polluants, notamment d'ozone troposphérique (polluant en hausse dans toute l'Europe, malgré les efforts entrepris)[11] et de nitrates, ces derniers étant à l'origine de pluies acides et, par suite, d'une acidification et d'une eutrophisation des eaux douces.
Évolutions locale et mondiale
Des années 1960 à 2002, les taux de NOx et d'ozone, mesurés dans les basses couches de la troposphère (là où nous respirons) ont suivi des courbes comparables, proches de la courbe d'augmentation du transport routier, traduisant l'inefficacité des pots catalytiques à froid, et une pollution par une grande partie des moteurs diesel, cachée par les fabricants, jusqu'au scandale de l'Affaire Volkswagen (Dieselgate), aggravée par l'augmentation constante du nombre de véhicules[12].
Notamment parce qu'il s'agit d'un précurseur de l'ozone troposphérique, il est apparu intéressant de le mesurer dans la colonne d'air plus en hauteur ce qui s'est avéré longtemps difficile et couteux (préleveurs aéroportés, ballons, etc.). Puis des satellites ont été dotés de capteurs permettant de le mesurer de plus en plus précisément.
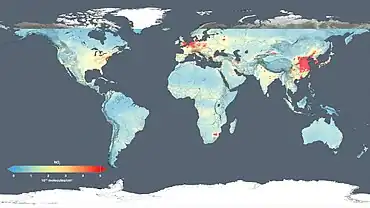
Les scientifiques de la NASA ont en 2017 produits de nouvelles cartes satellitaires mondiales haute résolution sur la qualité de l'air, permettant notamment un suivi plus précis de ce paramètre dans l'espace et dans le temps, dans diverses régions et 195 villes du monde. Ce travail a été présenté lors d’une réunion de l’Union américaine de géophysique à San Francisco et publiés dans le Journal of Geophysical Research. Il montre que les évolutions récentes de concentration de la plupart des polluants et en particulier du NO2 « ne sont pas aléatoires » (Bryan Duncan, scientifique de la NASA, en sciences de l'atmosphère au Goddard Space Flight Center à Greenbelt (Maryland), pilote de ce travail) et « quand les gouvernements décident de construire quelque part ou de règlementer un polluant », l'impact est visible par les satellites. Duncan et son équipe ont examiné les données collectées de 2005 à 2014 par l'instrument de surveillance de l'ozone néerlando-finlandais à bord du satellite Aura de la NASA. Cet instrument détecte aussi le dioxyde d'azote, qui contribue grandement aux smogs urbains. Les Hot-spots de pollution par le NO2 sont presque situés dans les régions industrielles et dans et autour des grandes villes de pays développés et en développement. La NASA étudie les tendances annuelles du NO2 dans le monde et cherche à les expliquer en comparant les enregistrements satellitaires aux informations sur les émissions des pays et les réglementations en matière de contrôle des émissions, de produit intérieur brut national et de croissance urbaine. Des études et cartes antérieures basées sur les données de satellites à faible résolution ne repéraient pas les variations sur de courtes distances. Cette nouvelle carte montre des informations plus cohérentes sur la localisation des problèmes et sources de pollution, et peuvent aider les pays émergents ou les régions ne disposant pas (ou peu) de stations de surveillance de l’air au sol. Les tendances varient beaucoup selon la région considérée.
- Les États-Unis et l'Europe sont encore parmi les plus gros émetteurs de NO2, mais ont aussi enregistré les réductions les plus spectaculaires de 2005 à 2014 (en partie en exportant leur industrie vers des pays émergents à main-d’œuvre moins chère) ; le NO2 a diminué de 20 à 50 % aux États-Unis et jusqu'à 50 % en Europe de l’Ouest, en grande partie grâce aux réglementations environnementales qui ont poussé certaines améliorations technologiques permettant de réduire les émissions polluantes des voitures et des centrales électriques.
- En Chine (l’« usine du monde », encore en pleine croissance), le pays a au contraire augmenté de 20 à 50 % ses émissions de dioxyde d'azote, principalement dans les plaines du nord. Mais trois conurbations — Beijing (Pékin), Shanghai et le delta de la rivière des Perles — ont vu leurs émissions diminuer jusqu'à 40 %.
- En Afrique, Johannesbourg et Pretoria émettent le plus de NO2 dans tout l'hémisphère sud, mais la carte des tendances à haute résolution montre une situation complexe avec des responsabilités partagées entre les villes et centrales électriques et les zones industrielles voisines, qui expliquent des études antérieures apparemment contradictoires dans cette région note Anne Thompson, co-auteur de l’étude.
- Au Moyen-Orient, l'augmentation des niveaux de dioxyde d'azote depuis 2005 en Irak, au Koweït et en Iran correspond probablement à la croissance économique de ces pays. Lors des guerres (en Syrie à partir de 2011) les images satellitales montrent une forte baisse des taux de dioxyde d'azote, probablement à la suite de la baisse de l'activité économique et aux déplacements de millions de personnes)[13].
Valeurs seuil
Dans ses lignes directrices relatives à la qualité de l'air[14], l'OMS propose les lignes directrices suivantes pour NO2 :
- 40 μg/m3 moyenne annuelle ;
- 200 μg/m3 moyenne horaire.
Ces valeurs sont analogues à celles fixées en France par le code de l’environnement[15] :
- 40 μg/m3 en moyenne annuelle civile (objectif de qualité) ;
- 200 μg/m3 en moyenne horaire (seuil d'information et de recommandation).
Mesures
Pour ces raisons, le NO2 est l'un des facteurs (« sous-indice ») généralement pris en compte dans le calcul des indices de qualité de l'air (Indice Atmo en France par exemple). Selon le Certu (2005), « vis-à-vis de la pollution chronique le polluant qui actuellement est le moins bien maîtrisé est le dioxyde d’azote » ; « De plus la baisse du NO2 n’est pas proportionnelle à la baisse des polluants primaires »[16]. Il s'ajoute à une production naturelle de NO2, lors des incendies de forêt et dans les nuages et la moyenne troposphère en cas d'activité orageuse[17].
En tant que « polluant toxique » et parce qu'il est de plus en plus présent dans l'air (il est notamment devenu l'un des polluants majeurs à Paris[18]), le dioxyde d'azote fait l'objet d'un suivi obligatoire par les observatoires de la pollution de l'air, par des capteurs actifs ou dans le cadre de réseaux de surveillance par des échantillonneurs passifs[19] et il est réglementé par la Directive européenne CEE no 85-203 et le décret du .
En France, sa valeur limite horaire est de 200 µg/m3, fréquemment dépassée dans les grandes villes et près des grands axes routiers ou aéroports en l'absence de vent ou de circulation de l'air.
Le Laboratoire central de la préfecture de police considère le monoxyde d'azote NO comme « un très bon indicateur de la pollution d'origine automobile, compte tenu de la part croissante des véhicules à moteur diesel dans le parc français » mais que « les mesures de restriction de circulation éventuelles auraient un effet plutôt réduit sur les teneurs en NO2 »[20]. Les moteurs Diesel comptent en effet parmi les premières sources d'émission de ce gaz. Les cartes satellitaires[21] de la pollution par NO2 montrent trois foyers principaux comme sources, mais aussi que les routes des navires de commerce et de guerre sont tracées par le NO2, notamment en mer Rouge et dans l'océan Indien entre la pointe sud de l’Inde et l’Indonésie. Au-dessus de la mer, le taux d'UV est augmenté et les moteurs marins n'ont pas bénéficié des progrès de l'automobile. De plus, leur fioul est souvent de mauvaise qualité (plus riche en soufre et plus lourd). Dans les grandes villes de France, selon le CERTU, toute l'année « les seuils de recommandation ne sont pratiquement jamais atteints pour le NO2 », alors que les autres polluants présentent souvent des pics saisonniers[16].
En Europe, ce polluant, très associé à la circulation automobile, a lentement diminué dans l'air des années 1980 à la fin des années 1990, puis cette amélioration a cessé ou est devenue très légère. Si la circulation devait augmenter en Europe, la pollution par le NO2 pourrait à nouveau augmenter[16]. Une jurisprudence européenne de 2014 (de la Cour de justice de l'Union européenne) confirme que le respect des valeurs limites de NO2 fixées par la directive européenne sur la qualité de l'air ambiant est une « obligation de résultat » pour les États membres[22].
Le charbon actif adsorbe très efficacement le dioxyde d'azote, tant qu'il n'est pas saturé, mais il est inenvisageable de l'utiliser pour épurer l'air des villes. Par contre toute limitation du nombre de voitures, de la circulation ou de la vitesse sur autoroute s'accompagne d'une diminution du NO2 (ainsi que des microparticules fines PM10[17]).
Évaluation des taux de NO2
Elle se fait grâce à des capteurs spécifiques que l'on cherche au moins depuis les années 2000 à améliorer, dont pour mieux mesurer ce gaz dans les moteurs thermiques, et/ou dans leur pot catalytique pour rétroactivement adapter le fonctionnement du moteur de manière à le rendre moins polluant, ce qui nécessite des capteurs en temps réel, plus performants, permettant une détection sélective et étant résistant aux hautes températures des gaz d'échappement[23] - [24], pour, in fine, mieux réduire (dans le moteur) ou détruire (dans une nouvelle génération de pots catalytiques).
Autre usage
Il a été utilisé au XIXe siècle pour la conservation de la viande.
Références
- DIOXYDE D'AZOTE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, Handbook of Chemistry and Physics, CRC, , 89e éd., 2736 p. (ISBN 142006679X et 978-1420066791), p. 9-50
- (en) Klotz, Irving M. et Rosenberg, Robert M., Chemical Thermodynamics, Basic Concepts and Methods, Wiley-VCH Verlag, , 564 p. (ISBN 978-0-471-78015-1 et 0-471-78015-4), p. 98
- (en) David R. Lide, Handbook of Chemistry and Physics, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008).
- « Dioxyde d'azote » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009.
- « Nitrogen dioxide », sur hazmap.nlm.nih.gov (consulté le )
- (en) Duward Felix Shriver, Peter William Atkins et Cooper Harold Langford, Inorganic chemistry, Oxford/Melbourne/Tokyo, Oxford University Press, , 706 p. (ISBN 0-19-855232-7, 9780198552321 et 0198552319)
- (en) A.F. Holleman et Egon Wiberg (trad. Mary Eagleson, William Brewer), Inorganic chemistry, San Diego, Berlin, New York, Academic Press De Gruyter, , 1884 p. (ISBN 978-0-12-352651-9, OCLC 301686300, lire en ligne).
- Ba M et Elichegaray C (2003), La pollution par l’ozone : des concentrations en hausse malgré des efforts à l’échelle européenne. Les données de l’Environnement (Ifen) n, 88.
- L'énergie de demain, Technique, environnement économie, sous la direction de J.L. Bobin, E Huffer et H Nifenecker (Groupe ÉNERGIE de la Société française de physique) Des combustibles fossiles 11. Les effets sanitaires. voir le graphique p. 271
- NASA et le NO2 dans l'air de 195 villes ; pour afficher et télécharger des cartes haute qualité de la qualité de l’air URL : http://svs.gsfc.nasa.gov/12094
- Organisation mondiale de la santé, Lignes directrices OMS relatives à la qualité de l’air : particules, ozone, dioxyde d’azote et dioxyde de soufre - Mise à jour mondiale 2005 : Synthèse de l'évaluation des risques, Genève, Organisation mondiale de la santé, 25 p. (lire en ligne), p. 17
- Code de l'Environnement (www.legifrance.gouv.fr), Article R221-1
- Sampic J. (2005), Rapport : « Évolution de la qualité de l'air en France » [PDF], CERTU (Centre d’études sur les réseaux, les transports, l'urbanisme et les constructions publiques), coll. « Pollution », 2005, voir notamment p. 23.
- Bertrand Bessagnet, Jean-Marc Brignon, Anne-Christine Le Gall, Frédérik Meleux, Simone Schucht et Laurence Rouïl, Politiques combinées de gestion de la qualité de l'air et du changement climatique [PDF], partie 1 : enjeux, synergies et antagonismes, 91 p., INERIS, Rapport d'étude 2009, N° DRC-09-103681-02123A, réalisé pour le MEEDDAT/DGEC, p. 18.
- René Alary, Jacques Donati et Henri Viellard, « La pollution automobile à Paris. Influence du trafic et des conditions météorologiques », Pollution atmosphérique, no 141, 8 avril 2014 (résumé).
- Papazian Meybeck, M. et Massa, D. (2014), Étude de la distribution du dioxyde d'azote sur l'agglomération toulousaine par la méthode des échantillonneurs passifs, été 1996-hiver 1996/1997-Évolution sur cinq ans : 1991/92-1996/97, 2268-3798.
- René Alary et Jacques Donati, « La pollution automobile à Paris. Influence du trafic et des conditions météorologiques », sur lodel.irevues.inist.fr, (consulté le ).
- ESA, « Une carte mondiale de la pollution de l’air a pu être établie grâce au capteur SCIAMACHY d’Envisat », European Space Agency, (lire en ligne, consulté le ).
- Radisson L., Le respect des valeurs limites de NO2 dans l'air ambiant, une obligation de résultat - Voilà les États membres prévenus, Actu-environnement, 19 novembre 2014.
- Pinter, Z. (2002). Caractérisation de couches épaisses de semi-conducteur WO3 et WO3/TiO2 pour la réalisation de capteurs à NO2 (Doctoral dissertation, Villeurbanne, INSA).
- Gao, J. (2011). Étude et mise au point d'un capteur de gaz pour la détection sélective de NOx en pot d'échappement automobile (Doctoral dissertation, École nationale supérieure des mines-Saint-Étienne).
Voir aussi
Bibliographie
- Diane Thomas, NO (oxydes d'azote), Techniques Ingénieur, juin 2009 (extraits avec Google Livres).
- (en) W. Cholz et P. Rabl, « Unexpectedly low decrease of NO2 air pollution–correlation with ozone concentration and altered exhaust emissions », dans Conference Proceedings of the 15th Transport and Air Pollution Conference, Reims, (lire en ligne [PDF]), p. 264-269.
Articles connexes
Liens externes
- Pollution de l'air par le dioxyde d'azote et santé, résumé de GreenFacts de rapports scientifiques de l'OMS.