Hexaméthylènediamine
L’hexaméthylènediamine (HMD) est un composé organique de formule semi-développée H2N(CH2)6NH2.
| Hexaméthylènediamine | ||
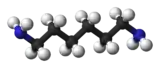 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | Hexane-1,6-diamine | |
| Synonymes |
1,6-diaminohexane, 1,6-hexanediamine |
|
| No CAS | ||
| No ECHA | 100.004.255 | |
| PubChem | 16402 | |
| SMILES | ||
| Apparence | solide blanc | |
| Propriétés chimiques | ||
| Formule | C6H16N2 [Isomères] |
|
| Masse molaire[1] | 116,204 6 ± 0,006 3 g/mol C 62,02 %, H 13,88 %, N 24,11 %, |
|
| Propriétés physiques | ||
| T° fusion | 42 à 45 °C[2] | |
| T° ébullition | 204 à 205 °C[2] | |
| Solubilité | 490 g l−1 à 20 °C (eau)[2] | |
| Masse volumique | 0,89 g cm−3 à 25 °C[2] | |
| T° d'auto-inflammation | 305 °C | |
| Point d’éclair | 94 °C[2] | |
| Limites d’explosivité dans l’air | 0,7 - 6,3 % | |
| Pression de vapeur saturante | 25 Pa à 20 °C[3] | |
| Thermochimie | ||
| ΔfH0solide | −205 kJ mol−1 | |
| Propriétés optiques | ||
| Indice de réfraction | 1,439[2] | |
| Précautions | ||
| SGH | ||
  |
||
| NFPA 704 | ||
| Directive 67/548/EEC | ||
| Écotoxicologie | ||
| DL50 | 750 mg kg−1 (rats, oral)[4] | |
| LogP | 0,386 | |
| Composés apparentés | ||
| Autres composés |
Cadavérine (pentyl-1,5-diamine) |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
Ce solide blanc hygroscopique a une forte odeur d’amine, semblable à celle de la pipéridine.
Synthèse
Cette diamine aliphatique est préparée par hydrogénation de l’adiponitrile de formule NC(CH2)4CN :
- NC(CH2)4CN + 4 H2 → H2N(CH2)6NH2
Les premières synthèses industrielles étaient réalisées en présence d'ammoniac et avec l'aide d'un catalyseur. On utilisait en général du cobalt, du fer ou du nickel de Raney. La formation de produits secondaires tels que le 1,2-diaminocyclohexane ou l'hexaméthylèneimine était observée.
Rhône-Poulenc a développé un procédé utilisant comme catalyseur du nickel en suspension dans de la soude. La réaction est réalisée à 75 °C et 20 bar et une sélectivité satisfaisante est observée[5].
Environ un million de tonnes sont produites annuellement.
Utilisations
Sa bifonctionnalité lui permet de servir de monomère pour la synthèse de polymères. Elle est surtout utilisée pour fabriquer plusieurs polyamides, en particulier le Nylon 6-6 via la polycondensation avec l’acide adipique[6].
Comme toutes les diamines primaires, elle est bivalente dans les polyamidifications et tétravalente quand elle intervient comme agent de réticulation avec les résines diépoxyde.
Toxicité
L’hexaméthylènediamine est modérément toxique.
Stabilité
Comme tous les composés organiques, elle est incompatible avec les oxydants forts.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Hexamethylenediamine » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- 1,6-hexanediamine, sur chemicalbook.com.
- Entrée du numéro CAS « 124-09-4 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais) (JavaScript nécessaire).
- Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- Gilles Lefebvre et Alain Chauvel, « Hexaméthylènediamine », Techniques de l'ingénieur, (lire en ligne).
- Georges Mollard, « Polyamide 6-6 », Techniques de l'ingénieur, (lire en ligne
 ).
).

