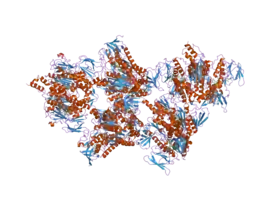Dihydrolipoyl déshydrogénase
La dihydrolipoyl déshydrogénase (DLD), également appelée dihydrolipoamide déshydrogénase, est la dernière des trois enzymes du complexe pyruvate déshydrogénase (PDC), du complexe alpha-cétoglutarate déshydrogénase et du complexe 3-méthyl-2-oxobutanoate déshydrogénase, constitués chacun d'une décarboxylase, d'une transacétylase et d'une réductase.
Le complexe pyruvate déshydrogénase
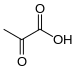
Le PDC catalyse la décarboxylation oxydative du pyruvate en acétyl-CoA, réaction qui réalise notamment la liaison entre la glycolyse et le cycle de Krebs ; les autres enzymes du complexe sont la pyruvate déshydrogénase (E1) et la dihydrolipoamide S-acétyltransférase (E2). Cette réaction s'écrit globalement :
Le mécanisme en est assez complexe, et peut être résumé par le schéma simplifié ci-dessous :
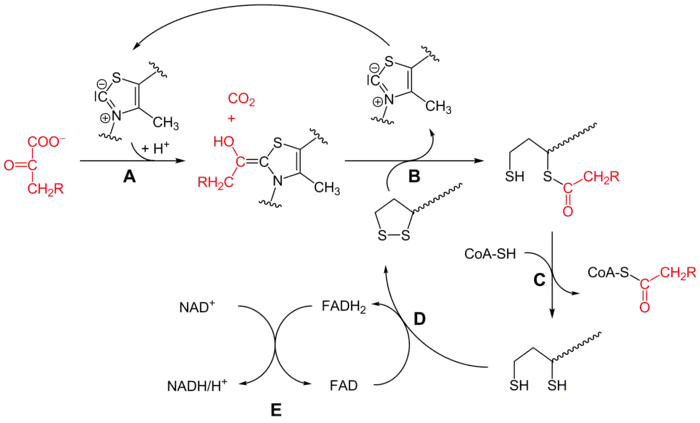
- la pyruvate déshydrogénase (E1) catalyse les étapes A et B avec la thiamine pyrophosphate (TPP),
- la dihydrolipoamide S-acétyltransférase (E2) catalyse l'étape C avec le lipoamide et la coenzyme A (CoA-SH),
- la dihydrolipoyl déshydrogénase (E3) catalyse les étapes D et E avec la FAD et la NAD+.
La dihydrolipoyl déshydrogénase
| N° EC | EC |
|---|---|
| N° CAS | |
| Cofacteur(s) | FAD |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
La DLD est une flavoprotéine qui, outre sa participation aux trois complexes enzymatiques que sont le complexe pyruvate déshydrogénase, le complexe alpha-cétoglutarate déshydrogénase et le complexe 3-méthyl-2-oxobutanoate déshydrogénase, catalyse plus simplement la réduction du lipoamide en dihydrolipoamide.
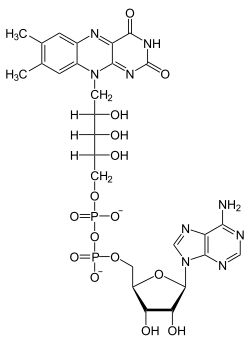
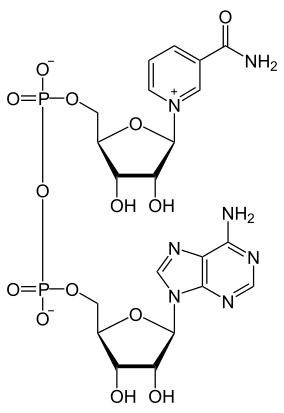
Son confacteur est la flavine adénine dinucléotide (FAD), qui transfère au nicotinamide adénine dinucléotide (NAD+) les deux atomes d'hydrogène libérés par le dihydrolipoamide lors de son oxydation en lipoamide.
Notes et références
- (en) Ewa M. Ciszak, Anna Makal, Young S. Hong, Ananthalakshmy K. Vettaikkorumakankauv¶ Lioubov G. Korotchkina et Mulchand S. Patel, « How Dihydrolipoamide Dehydrogenase-binding Protein Binds Dihydrolipoamide Dehydrogenase in the Human Pyruvate Dehydrogenase Complex », Journal of Biochemical Chemistry, vol. 281, no 1, , p. 648-655 (PMID 016263718, DOI 10.1074/jbc.M507850200, lire en ligne)
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.