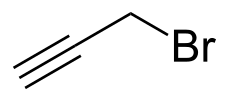
Bromure de propargyle
Le bromure de propargyle, également connu sous le nom de 3-bromo-1-propyne, est un composé organobromé de formule chimique HC≡CCH2Br. Il est constitué de propyne avec un substituant brome sur le groupe méthyle. Il a un effet lacrymogène, comme les composés apparentés. Le composé est un réactif utile en synthèse organique.
| Bromure de propargyle | |||
| |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 3-bromoprop-1-yne | ||
| Synonymes |
3-bromo-1-propyne, |
||
| No CAS | |||
| No ECHA | 100.003.135 | ||
| No CE | 203-447-1 | ||
| PubChem | 7842 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore à jaunâtre d'odeur âcre[1] | ||
| Propriétés chimiques | |||
| Formule | C3H3Br [Isomères] |
||
| Masse molaire[2] | 118,96 ± 0,004 g/mol C 30,29 %, H 2,54 %, Br 67,17 %, |
||
| Propriétés physiques | |||
| T° fusion | −61 °C[1] | ||
| T° ébullition | 89 °C[1] | ||
| Solubilité | eau : 14,9 g·l-1 à 25 °C[3] sol. in éthanol, éther diéthylique, benzène, tétrachlorure de carbone, chloroforme[3] |
||
| Masse volumique | 1,57 g·cm-3 à 20 °C[1] | ||
| T° d'auto-inflammation | 324 °C[1] | ||
| Point d’éclair | 18,0 °C (coupelle ouverte)[1] - [3] 10,0 °C (coupelle fermée)[3] |
||
| Limites d’explosivité dans l’air | min 3 vol.%[1] | ||
| Pression de vapeur saturante | 72 hPa à 20 °C[1] 310 hPa à 50 °C[1] 535 hPa à 65 °C[1] |
||
| Propriétés optiques | |||
| Indice de réfraction | 1,4922 à 20 °C[3] | ||
| Précautions | |||
| SGH[1] - [3] | |||
   |
|||
| NFPA 704[3] | |||
| Transport[1] | |||
|
|||
| Écotoxicologie | |||
| DL50 | 53 mg/kg (rat, oral)[1] - [3] 29 μg/kg (0,029 mg/kg) (cobaye, oral)[3] |
||
| Unités du SI et CNTP, sauf indication contraire. | |||
Applications
Dans les années 1960, le bromure de propargyle a été utilisé pour la première fois comme un pesticide gazeux du sol appelé « Trizone »[4].
Le bromure de propargyle peut également être utilisé comme intermédiaire pour la synthèse de composés organiques, y compris les produits agrochimiques et pharmaceutiques. Il forme par exemple un réactif de Grignard à basse température[5].
Production
Le bromure de propargyle peut être produit par le traitement de l'alcool propargylique avec du tribromure de phosphore[6].
Réactions
Le bromure de propargyle peut être utilisé dans la métathèse des énynes sur des amines propargyliques, la propargylation des spirocétones, la production d'alcools allyliques et les complexes d'énones[7]
Les aldéhydes peuvent réagir avec du bromure de propargyle dans une réaction de type Barbier pour donner également des alcools d'alcyne[8].
Sécurité
Le bromure de propargyle est un lacrymogène et un agent alkylant[9]. Quand le 3-bromopropyne est dilué dans du toluène dans des proportions de 20-30% en masse de toluène, ses propriétés explosives sont pratiquement éliminées[3].
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Propargyl alcohol » (voir la liste des auteurs).
- Entrée « 3-Bromo-1-propyne » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 5 mars 200 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- PubChem CID 7842.
- Franz Müller et Arnold P. Applebyki, Weed Control, 2. Individual Herbicides, dans Ullmann's Encyclopedia of Industrial Chemistry, 2010, DOI 10.1002/14356007.o28_o01
- Diels-Alder Reaction of 1,2,4,5-Hexatetraene: Tetramethyl[2.2]paracyclophane-4,5,12,13-tetracarboxylate, Org. Synth., coll. « vol. », 41 p.
- « Process for Producing Propargyl Bromide » (consulté le )
- « Propargyl Bromide » (consulté le )
- Artur Jõgi et Uno Mäeorg, « Zn Mediated Regioselective Barbier Reaction of Propargylic Bromides in THF/aq. NH4Cl Solution », Molecules, vol. 6, no 12, , p. 964–968 (ISSN 1420-3049, DOI 10.3390/61200964, lire en ligne)
- « 3-Bromo-1-Propyne » (consulté le )


