Triisobutylaluminium
Le triisobutylaluminium, ou TiBA, est un composé organoaluminique de formule chimique ((CH3)2CHCH2)3Al. Il s'agit d'un liquide incolore pyrophorique qui réagit violemment avec l'eau, les alcools, l'oxygène, les oxydants, les acides et les bases. Il réagit également avec les aldéhydes et les cétones[3]. Il est utilisé essentiellement pour produire des alcools primaires et des alcènes terminaux[4].
| Triisobutylaluminium | |||
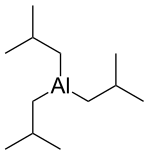
| |||
| Structure du triisobutylaluminium | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | tris(2-méthylpropyl)alumane | ||
| No CAS | |||
| No ECHA | 100.002.643 | ||
| No CE | 202-906-3 | ||
| PubChem | 16682931 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore[1] | ||
| Propriétés chimiques | |||
| Formule | ((CH3)2CHCH2)3Al | ||
| Masse molaire[2] | 198,324 3 ± 0,011 5 g/mol C 72,67 %, H 13,72 %, Al 13,6 %, |
||
| Propriétés physiques | |||
| Masse volumique | 0,782 g/cm3[1] à 20 °C | ||
| Précautions | |||
| SGH[1] | |||
    Danger |
|||
| NFPA 704[1] | |||
| Transport[1] | |||
|
|||
| Écotoxicologie | |||
| LogP | 4,11[1] (octanol/eau) pour le solvant hexane | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
Le triisobutylaluminium existe en équilibre avec son dimère, selon une constante de dissociation KD qui vaut 3,810 à 20 °C[5] :
- 2 ((CH3)2CHCH2)3Al [((CH3)2CHCH2)3Al]2.
Dans le dimère, la liaison carbone–aluminium est allongée et montre des indications d'une rotation restreinte. Par souci de simplification, on décrira le TiBA comme monomère dans cette page.
Production
Les composés trialkylaluminium sont produits industriellement en faisant réagir de la poudre d'aluminium, de l'hydrogène H2 et les alcènes souhaités. La synthèse du triisobutylaluminium se déroule en deux étapes. La première donne l'hydrure de diisobutylaluminium ((CH3)2CHCH2)2AlH à partir de l'isobutylène CH2=C(CH3)2 :
- 4 CH2=C(CH3)2 + 2 Al + 3 H2 ⟶ 2 ((CH3)2CHCH2)2AlH.
Une seconde étape consiste en l'addition supplémentaire d'isobutylène pour aboutir au triisobutylaluminium :
- CH2=C(CH3)2 + ((CH3)2CHCH2)2AlH ⟶ ((CH3)2CHCH2)3Al.
Réactions
Les alcènes terminaux sont rapidement éliminés des composés trialkylaluminium β-ramifiés. Les composés trialkylaluminium sont employés dans l'industrie pour la production de polymères. Le triisobutylaluminium est l'un de ces composés les plus courants et présente un taux de liaisons Al–H significatif à l'équilibre. La plus grande stabilité des composés trialkylaluminium linéaires par rapport aux ramifiés est à la base de l'obtention de composés trialkylaluminium linéaires à partir du triisobutylaluminium :
- ((CH3)2CHCH2)3Al + 3 RCH=CH2 ⟶ (RCH2CH2)3Al + 3 CH2=C(CH3)2.
Notes et références
- « Fiche du composé Triisobutylaluminum, 25% w/w in hexane », sur Alfa Aesar (consulté le ).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Pradyot Patnaik, A Comprehensive Guide to the Hazardous Properties of Chemical Substances, John Wiley & Sons, 2007, p. 607. (ISBN 0-470-13494-1)
- (en) Michael J. Krause, Frank Orlandi, Alfred T. Saurage et Joseph R. Zietz Jr., « Aluminum Compounds, Organic », Ullmann's Encyclopedia of Industrial Chemistry, (DOI 10.1002/14356007.a01_543, lire en ligne)
- (en) Martin B. Smith, « The monomer-dimer equilibria of liquid aluminum alkyls: II. Triisobutylaluminum », Journal of Organometallic Chemistry, vol. 22, no 2, , p. 273-281 (DOI 10.1016/S0022-328X(00)86043-X, lire en ligne)



