Nonan-5-one
La nonan-5-one ou dibutylcétone est un composé organique de la famille des cétones symétriques, de formule (CH3CH2CH2CH2)2CO.
| Nonan-5-one | |
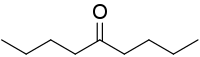
| |
| Identification | |
|---|---|
| Nom systématique | nonan-5-one |
| Synonymes |
dibutylcéone |
| No CAS | |
| No ECHA | 100.007.224 |
| No CE | 207-946-5 |
| No RTECS | RA8230000 |
| PubChem | 10405 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore à jaunâtre, inodore[1] |
| Propriétés chimiques | |
| Formule | C9H18O |
| Masse molaire[2] | 142,238 6 ± 0,008 8 g/mol C 76 %, H 12,76 %, O 11,25 %, |
| Propriétés physiques | |
| T° fusion | −5 °C[1] |
| T° ébullition | 188 °C[1] |
| Solubilité | 0,363 g·L-1 (eau, 25 °C))[1] |
| Masse volumique | 0,82 g·cm-3 (20 °C)[1] |
| T° d'auto-inflammation | 330 °C[1] |
| Point d’éclair | 65 °C[1] |
| Limites d’explosivité dans l’air | 0,8 vol.%, ~47 g/m3[1] |
| Pression de vapeur saturante | 0,4 hPa (20 °C) 0,74 hPa (25 °C) 0,9 hPa (30 °C) 3,5 hPa (50 °C) 55,2 hPa (100 °C)[1] |
| Propriétés optiques | |
| Indice de réfraction | =1,4195 (20 °C)[3] |
| Précautions | |
| SGH[4] | |
   Danger P405 et P501 |
|
| Écotoxicologie | |
| DL50 | 138 mg·kg-1 (souris, i.v.)[5] |
| LogP | 2,88[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés
La nonan-5-one se présente sous la forme d'un liquide incolore à jaunâtre, inodore[1]. Elle est combustible (point d'éclair de 63 °C[1]), mais faiblement inflammable (température d'auto-inflammation de 330 °C[1]). Au-dessus de son point d'éclair, ses vapeurs peuvent former un mélange explosif avec l'air. Plus légère que l'eau (densité de 0,82), elle y est très peu soluble, comme la plupart des alcanes supérieurs. Elle est peu voire très peu volatile.
Synthèse
La nonan-5-one peut être produite à partir de l'acide valérique (acide pentanoïque) par cétonisation[6]. Lui-même peut être obtenu à partir de l'acide lévulinique, qui peut à son tour être obtenu à partir du fructose.
Elle peut aussi être obtenue par réaction du tri-n-butylborane avec le cyanure de sodium, et réaction ultérieure avec l'anhydride trifluoroacétique et le peroxyde d'hydrogène[7]. Elle peut enfin aussi être obtenue à partir du but-1-ène[8].
Utilisation
La nonan-5-one sert dans la synthèse d'autre composés, par exemple la 5-nonancétoxime. Elle peut également servir de solvant[9].
La nonan-5-one a été étudiée comme potentiel carburant pour moteur Diesel.
Toxicologie
Voie métabolique
On s'attendait à ce que la nonan-5-one soit métabolisée en γ-dicétone. Des études métaboliques in vivo ont confirmé une ω-oxydation de la nonan-5-one en nonane-2,5-dione et en hexan-2-one. Des étapes ultérieures oxydatives et décarboxylatives produisent également l'hexane-2,5-dione. En dehors de ces métabolites, 38 % de la nonan-5-one est convertie en dioxyde de carbone. Aucune nonan-5-one non-altérée n'est détectée dans les urines après administration[10].
De ces métabolites, l'hexane 2,5-dione est sans doute le composé le plus neurotoxique. De tous les métabolites susmentionnés, on pense que la toxicité vient de la transformation métabolique en cette γ-dicétone[11].
Effets toxicologiques
Chez les rats, la neurotoxicité de la nonan-5-one est accrue par la butanone. Ceci suggère une induction des enzymes oxydantes microsomiales qui résulte en une plus grande production de métabolites toxiques. Il a été démontré que des expositions chroniques à ce composé produisent une neuropathie clinique, caractérisée par des gonflements axonaux géants remplis de neurofilaments. Elle a également entraîné une décoloration orange/brune des poils des rats[12].
Une autre étude a été réalisée sur des rats pour explorer l'augmentation de la toxicité de la nonan-5-one par la 5-méthyloctan-2-one. La combinaison de ces deux composés multiplie environ par six l'effet neurotoxique de la nonan-5-one. Un gonflement du foie a été observé lors de la seule exposition à la 5-méthyloctan-2-one, ce qui indique que l'activation métabolique des enzymes oxydatives hépatiques peut être la cause de l'augmentation de la toxicité en cas de co-administration[11].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « 5-Nonanone » (voir la liste des auteurs).
- Entrée « 5-Nonanone » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 4 avril 2020 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Lide, D.R., G.W.A. Milne (eds.). Handbook of Data on Organic Compounds. Volume I. 3rd ed. CRC Press, Inc. Boca Raton ,FL. 1994., p. V4: 3654
- Fiche Pubchem
- Jeppsson R., « Parabolic relationship between lipophilicity and biological activity of aliphatic hydrocarbons, ethers and ketones after intravenous injections of emulsion formulations into mice. », Acta Pharmacologica et Toxicologica, vol. 37(1), (PMID 1174281)
- Filoklis D. Pileidis et Maria-Magdalena Titirici, « Levulinic Acid Biorefineries: New Challenges for Efficient Utilization of Biomass », ChemSusChem, vol. 9, no 6, , p. 562–582 (PMID 26847212, DOI 10.1002/cssc.201501405, lire en ligne)
- Michael B. Smith, Organic Synthesis, Academic Press, , 1534 p. (ISBN 978-0-12-415884-9, lire en ligne), p. 529
- W. Carruthers, Some Modern Methods of Organic Synthesis, Cambridge University Press, , 526 p. (ISBN 978-0-521-31117-5, lire en ligne), p. 308
- « Numéro CAS 502-56-7 » dans la base de données Hazardous Substances Data Bank
- Bingham, E., Cohrssen, B. et Powell, C.H., Patty's Toxicology, John Wiley & Sons, (ISBN 978-0-470-41081-3), p. 6–316
- John L. O'Donoghue, Walter J. Krasavage, George D. DiVincenzo et Donald A. Ziegler, « Commercial-grade methyl heptyl ketone (5-methyl-2-octanone) neurotoxicity: Contribution of 5-nonanone. », Toxicology and Applied Pharmacology, vol. 62, no 2, , p. 307–316 (PMID 7058532, DOI 10.1016/0041-008X(82)90129-6)
- Mark A. Shifman, Doyle G. Graham, Jeff W. Priest et Thomas W. Bouldin, « The neurotoxicity of 5-nonanone: Preliminary report », Toxicology Letters, vol. 8, nos 4–5, , p. 283–288 (PMID 7268811, DOI 10.1016/0378-4274(81)90114-4)
