Chlorure de béryllium
Le chlorure de béryllium est un composé chimique de formule brute BeCl2. C'est un acide de Lewis utilisé comme catalyseur.
| Chlorure de Béryllium | |
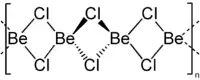
| |
| Identification | |
|---|---|
| Nom UICPA | chlorure de béryllium |
| No CAS | |
| No ECHA | 100.029.197 |
| No CE | 232-116-4 |
| PubChem | 24588 |
| SMILES | |
| InChI | |
| Apparence | Cristaux incolores à jaunes |
| Propriétés chimiques | |
| Formule | BeCl2 [Isomères] |
| Masse molaire[1] | 79,918 ± 0,004 g/mol Be 11,28 %, Cl 88,72 %, |
| Propriétés physiques | |
| T° fusion | 416 °C [2] |
| T° ébullition | 520 °C [2] |
| Solubilité | 151 g·l-1 |
| Masse volumique | 1,9 g·cm-3 à 20 °C [3] |
| Thermochimie | |
| S0gaz, 1 bar | 252,13 J·K-1·mol-1 [4] |
| S0liquide, 1 bar | 79,71 J·K-1·mol-1 [4] |
| ΔfH0gaz | −360,24 kJ·mol-1 [4] |
| ΔfH0liquide | −491,31 kJ·mol-1 [4] |
| ΔfH0solide | −496,22 kJ·mol-1 [4] |
| ΔvapH° | 105 kJ·mol-1 (1 atm, 482 °C)[5] |
| Précautions | |
| SGH[3] | |
   Danger |
|
| Transport[3] | |
| Inhalation | Toux. Mal de gorge. Essoufflement. Symptômes d'effets retardés. |
| Peau | Rougeur. Douleur. |
| Yeux | Rougeur. Douleur. Troubles de la vue. |
| Ingestion | Nausées. Vomissements. Douleurs abdominales. |
| Écotoxicologie | |
| DL50 | 92 mg·kg-1 (souris, oral) 11,987 mg·kg-1 (souris, i.p.) 86 mg·kg-1 (rat, oral) 5,32 mg·kg-1 (rat, i.p.) [6] |
| Unités du SI et CNTP, sauf indication contraire. | |
Utilisation
Le chlorure de béryllium est un précurseur dans la synthèse de composés organiques contenant du béryllium et une source pour la production de béryllium[2].
Propriétés physico-chimiques
Le chlorure de béryllium réagit de manière très exothermique avec l'eau en produisant du chlorure d'hydrogène[2]. C'est un produit très hygroscopique et il forme par contact avec de l'air humide un complexe tétravalent.
Production et synthèse
Le chlorure de béryllium peut être produit par chloration de l'oxyde de béryllium dans des conditions réductrices. La chloration du minerai est une étape de purification du métal[2].
Un mélange de béryl (un aluminosilicate naturel de béryllium) et de carbone sont chauffés à 800 °C en présence de dichlore ou alors fondus dans un four à arc électrique où ils forment du carbure de béryllium avant d'être chlorés. La réaction peut avoir lieu en présence de gaz chlorés tels le chlorure d'hydrogène, le tétrachlorure de carbone, le chlorure de soufre ou le phosgène. Les composés chlorés volatils sont ensuite séparés par condensation fractionnée ou par extraction liquide-liquide dans du chlorure de soufre, du trichlorure de phosphore, du chlorure de bore ou encore du phosgène[2].
La distillation dans un flux d'hydrogène permet de séparer facilement le chlorure de béryllium d'autres chlorures tels le chlorure de fer, le chlorure d'aluminium ou le chlorure de silicium[2]. Le chlorure de béryllium est ensuite utilisé pour obtenir le béryllium par réduction en présence de sodium en phase gazeuse à 250 °C. Ce procédé est toutefois mineur et le métal est produit de manière industrielle par électrolyse[2].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Günter Petzow, Fritz Aldinger, Sigurd Jönsson, Peter Welge, Vera van Kampen, Thomas Mensing, Thomas Brüning, Beryllium and Beryllium Compounds, Wiley-VCH Verlag GmbH & Co., coll. « Ullmann's Encyclopedia of Industrial Chemistry »,
- Entrée « Beryllium chloride » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 26 janvier 2010 (JavaScript nécessaire)
- (en) « Beryllium dichloride », sur NIST/WebBook, consulté le
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-4200-9084-0)
- (en) « Chlorure de béryllium », sur ChemIDplus, consulté le
