Caspase 3
La caspase 3 est une protéase à cystéine de la famille des caspases[3] (de l'anglais cysteine-dependent aspartate-directed proteases, qui interagit avec la caspase 8 et la caspase 9. Elle est codée chez l'homme par le gène CASP3, situé sur les chromosome 4. Des orthologues du gène CASP3 ont été identifiés chez un grand nombre de mammifères pour lesquels des données génomiques complètes sont disponibles. Des orthologues spécifiques ont également été relevés chez les oiseaux, les sauriens, les lissamphibiens et les téléostéens.
| Caspase 3 | ||
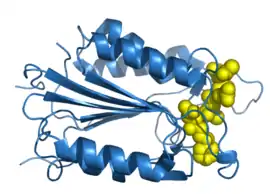 Caspase 3 humaine complexée avec un inhibiteur phénylpropylcétone (PDB 1RHK[1]) | ||
| Caractéristiques générales | ||
|---|---|---|
| Symbole | CASP3 | |
| N° EC | 3.4.22.56 | |
| Homo sapiens | ||
| Locus | 4q35.1 | |
| Masse moléculaire | 31 608 Da[2] | |
| Nombre de résidus | 277 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
La caspase 3 est semblable à la caspase 7 dans la mesure où elle clive les chaînes polypeptidiques au niveau des séquences Asp–Xaa–Xaa–Asp-|-[4] : ce dernier résidu d'aspartate est indispensable à l'enzyme, tandis que le premier résidu d'aspartate, côté N-terminal de la séquence, peut, dans certains cas, faire défaut ; le deuxième résidu est généralement hydrophile et le troisième est plutôt hydrophobe, bien que les séquences Asp–Ala–Xaa–Asp-|- et Asp–Val–Xaa–Asp-|- soient également clivées[5]. La spécificité des caspases pour leurs substrats a été largement mise à profit dans la conception d'inhibiteurs de caspases et de médicaments[6].
La caspase 3 possède de nombreux traits communs à toutes les caspases actuellement connues. Son site actif possède ainsi des résidus cystéine 163 et histidine 121 qui assurent la spécificité du clivage de la liaison peptidique du côté carboxyle du résidu d'aspartate du motif caractéristique à quatre acides aminés Asp–Xaa–Xaa–Asp-|-[7] - [8]. Cette spécificité permet aux caspases d'être particulièrement sélectives, étant 20 000 fois plus actives en présence d'aspartate qu'en présence de glutamate[9]. Les caspases sont présentes dans les cellules sous forme de proenzymes, appelées procaspases, qui contiennent une grande sous-unité N-terminale de 20 kDa suivie d'une petite sous-unité de 10 kDa[10].
L'activation séquentielle des caspases joue un rôle central dans le déclenchement de l'apoptose cellulaire. Les procaspases sont inactives jusqu'à ce qu'elles subissent un processus protéolytique au niveau de résidus d'aspartate conservés libérant les deux sous-unités, la grande et la petite, qui dimérisent en formant l'enzyme active. Cette protéine clive et active la caspase 6 et la caspase 7, tandis qu'elle-même est modifiée et activée par la caspase 8, la caspase 9 et la caspase 10.

Notes et références
- (en) Joseph W. Becker, Jennifer Rotonda, Stephen M. Soisson, Renee Aspiotis, Christopher Bayly, Sébastien Francoeur, Michel Gallant, Marga Garcia-Calvo, Andre Giroux, Erich Grimm, Yongxin Han, Dan McKay, Donald W. Nicholson, Erin Peterson, Johanne Renaud, Sophie Roy, Nancy Thornberry et Robert Zamboni, « Reducing the Peptidyl Features of Caspase-3 Inhibitors: A Structural Analysis », Journal of Medicinal Chemistry, vol. 47, no 10, , p. 2466-2674 (PMID 15115390, DOI 10.1021/jm0305523, lire en ligne)
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- (en) Emad S. Alnemri, David J. Livingston, Donald W. Nicholson, Guy Salvesen, Nancy A. Thornberry, Winnie W. Wong, Junying Yuan, « Human ICE/CED-3 protease nomenclature », Cell, vol. 87, no 2, , p. 171 (PMID 8861900, DOI 10.1016/S0092-8674(00)81334-3, lire en ligne)
- (en) Johnson Agniswamy, Bin Fang et Irene T. Weber, « Plasticity of S2–S4 specificity pockets of executioner caspase-7 revealed by structural and kinetic analysis », FEBS Journal, vol. 274, no 18, , p. 4752-4765 (PMID 17697120, DOI 10.1111/j.1742-4658.2007.05994.x, lire en ligne)
- (en) Bin Fang, Peter I. Boross, Jozsef Tozser et Irene T. Weber, « Structural and Kinetic Analysis of Caspase-3 Reveals Role for S5 Binding Site in Substrate Recognition », Journal of Molecular Biology, vol. 360, no 3, , p. 654-666 (PMID 16781734, DOI 10.1016/j.jmb.2006.05.041, lire en ligne)
- (en) Irene T. Weber, Bin Fang et Johnson Agniswamy, « Caspases: Structure-Guided Design of Drugs to Control Cell Death », Mini-Reviews in Medicinal Chemistry, vol. 8, no 11, , p. 1154-1162 (PMID 18855730, DOI 10.2174/138955708785909899, lire en ligne)
- (en) Andrew H. Wyllie, « Apoptosis: an overview », British Medical Bulletin, vol. 53, no 3, , p. 451-465 (PMID 9374030, lire en ligne)
- (en) David K. Perry, Miriam J. Smyth, Henning R. Stennicke, Guy S. Salvesen, Patrick Duriez, Guy G. Poirier et Yusuf A. Hannun, « Zinc is a potent inhibitor of the apoptotic protease, caspase-3. A novel target for zinc in the inhibition of apoptosis », Journal of Biological Chemistry, vol. 272, no 30, , p. 18530-18533 (PMID 9228015, DOI 10.1074/jbc.272.30.18530, lire en ligne)
- (en) Henning R. Stennicke, Martin Renatus, Morten Meldal et Guy S. Salvesen, « Internally quenched fluorescent peptide substrates disclose the subsite preferences of human caspases 1, 3, 6, 7 and 8 », Biochemical Journal, vol. 350, no Pt 2, , p. 563-568 (PMID 10947972, PMCID 1221285, DOI 10.1042/0264-6021:3500563, lire en ligne)
- (en) Guy S. Salvesen, « Caspases: opening the boxes and interpreting the arrows », Cell Death & Differentiation, vol. 9, no 1, , p. 3-5 (PMID 11803369, DOI 10.1038/sj/cdd/4400963, lire en ligne)
- (en) Heather A. Harrington, Kenneth L. Ho, Samik Ghosh et K. C. Tung, « Construction and analysis of a modular model of caspase activation in apoptosis », Theoretical Biology and Medical Modelling, vol. 5, , p. 26 (PMID 19077196, PMCID 2672941, DOI 10.1186/1742-4682-5-26, lire en ligne)