tert-Butyllithium
Le tert-butyllithium, abrégé tert-BuLi ou t-BuLi, est un composé chimique de formule LiC(CH3)3, isomère du n-butyllithium et du sec-butyllithium, qui sont moins basiques que lui. Cet organolithien est disponible dans le commerce en solution dans des hydrocarbures tels que le pentane et l'heptane ; on ne le prépare généralement pas au laboratoire. Il peut être obtenu en faisant réagir de la poudre de lithium métallique avec du bromure de tert-butyle BrC(CH3)3 :
| tert-Butyllithium | |
 Mésomérie du tert-butyllithium |
|
| Identification | |
|---|---|
| Synonymes |
1,1-Diméthyléthyllithium |
| No CAS | |
| No ECHA | 100.008.939 |
| No CE | 209-831-5 |
| PubChem | 638178 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C4H9Li [Isomères] |
| Masse molaire[1] | 64,055 ± 0,006 g/mol C 75 %, H 14,16 %, Li 10,84 %, |
| Précautions | |
| SGH[2] | |
     Danger |
|
| Transport[2] | |
| Unités du SI et CNTP, sauf indication contraire. | |
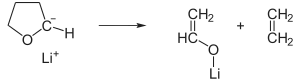
La molécule de tert-butyllithium est très polaire, étant ionisée à environ 40 %. Elle réagit comme un carbanion en vertu de l'une de ses formes de résonance. Elle est instable dans les éthers : sa demi-vie est de 60 minutes à 0 °C dans l'éther diéthylique, 40 minutes à −20 °C dans le tétrahydrofurane (THF), et environ 11 minutes à −70 °C dans le diméthoxyéthane ; avec le THF, il réagit de la façon suivante :

Le tertbutyllithium est une substance pyrophorique, c'est-à-dire qu'il peut facilement s'enflammer à l'air libre. Il est distribué commercialement dissous dans des solvants — des hydrocarbures — qui sont eux-mêmes combustibles. Des accidents mortels se sont produits en laboratoire lors de la manipulation de solutions de tert-BuLi[3], des traces de produit prenant feu sur les instruments après usage. De telles réactions, sur des quantités significatives de produit, sont susceptibles de s'emballer et de conduire à des incendies et des explosions lorsque le tert-BuLi est mis en présence d'éthers tels que l'éther diéthylique, le tétrahydrofurane (THF) et le diméthoxyéthane.
Les techniques de manipulation sous atmosphère inerte sont nécessaires afin de prévenir les accidents dus à la réaction du tert-butyllithium avec l'oxygène de l'air et avec l'humidité :
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Jyllian N. Kemsley, « Learning From UCLA », Chemical & Engineering News, vol. 87, no 31, , p. 29-31, 33-34 (lire en ligne)

