Tétrachlorure de germanium
Le tétrachlorure de germanium, ou chlorure de germanium(IV), est un composé chimique de formule GeCl4. Il s'agit d'un liquide incolore dégageant, au contact de l'humidité de l'air, des fumées à l'odeur acide due à l'acide chlorhydrique qu'elles contiennent. La réaction au contact de l'eau est violente, et conduit à l'hydrolyse du composé. L'ammoniac NH3 donne le diamine Ge(NH3)2, tandis que l'éthanolate de sodium NaOCH2CH3 donne l'ester orthoéthylique d'acide germanique Ge(OCH2CH3)4.
- GeCl4 + 2 H2O → GeO2 + 4 HCl ;
- GeCl4 + 6 NH3 → Ge(NH3)2 + 4 NH4Cl ;
- GeCl4 + 4 NaOCH2CH3 → Ge(OCH2CH3)4 + 4 NaCl.
| Tétrachlorure de germanium | |||
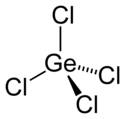
| |||
| Structure du tétrachlorure de germanium | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | tetrachlorogermane | ||
| Synonymes |
Chlorure de germanium(IV) |
||
| No CAS | |||
| No ECHA | 100.030.093 | ||
| No CE | 233-116-7 | ||
| No RTECS | LY5225000 | ||
| PubChem | 66226 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore à forte odeur acide | ||
| Propriétés chimiques | |||
| Formule | GeCl4 | ||
| Masse molaire[1] | 214,45 ± 0,02 g/mol Cl 66,13 %, Ge 33,86 %, |
||
| Propriétés physiques | |||
| T° fusion | −49,5 °C[2] | ||
| T° ébullition | 83 °C[2] | ||
| Solubilité | Réagit violemment au contact de l'eau[2] | ||
| Masse volumique | 1,88 g·cm-3[2] à 25 °C | ||
| Précautions | |||
| SGH[2] - [3] | |||
  Danger |
|||
| Transport[2] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
Il intervient comme intermédiaire dans la production du germanium métallique purifié. Son utilisation s'est sensiblement accrue depuis le début du siècle en raison de son utilisation comme réactif dans la fabrication des fibres optiques.
Production
La majeure partie de la production industrielle du germanium provient du traitement des poussières des fonderies de minerais de zinc et de cuivre, bien qu'une source importante se trouve également dans les cendres provenant de la combustion de certains types de charbon appelés vitrain (en). Le tétrachlorure de germanium est un intermédiaire de la purification du germanium métallique et de son oxyde, le dioxyde de germanium GeO2.
Le tétrachlorure de germanium peut être produit directement à partir du GeO2 par dissolution de l'oxyde dans l'acide chlorhydrique HCl concentré. Le mélange qui en résulte est traité par distillation fractionnée pour purifier et séparer le tétrachlorure de germanium GeCl4 des autres produits et impuretés. Le GeCl4 peut être hydrolysé à son tour avec de l'eau distillée et désionisée (ddH2O) pour produire du GeO2 pur, qui est ensuite réduit sous hydrogène H2 pour produire du germanium métallique.
La production de GeO2 dépend cependant de la forme oxydée du germanium extraite du minerai. Les minerais de sulfure de cuivre-plomb et de sulfure de zinc ZnS produisent du disulfure de germanium GeS2, qui est ensuite oxydé en GeO2 avec un oxydant tel que le chlorate de sodium NaClO3. Les minerais de zinc sont grillés et frittés et peuvent produire le GeO2 directement. L'oxyde est ensuite traité comme indiqué précédemment.
Au laboratoire, on prépare le tétrachlorure de germanium en faisant réagir du dioxyde de germanium pur avec de l'acide chlorhydrique concentré :
Applications
Le tétrachlorure de germanium est utilisé presque uniquement comme intermédiaire de plusieurs procédés produisant des matériaux optiques. Le GeCl4 peut être directement hydrolysé en dioxyde de germanium GeO2, un matériau qui présente plusieurs propriétés intéressantes.
Au cours de la fabrication de fibres optiques, le tétrachlorure de silicium SiCl4 et le tétrachlorure de germanium GeCl4 sont introduits avec de l'oxygène O2 dans une préforme en verre creux qui est soigneusement chauffée pour permettre l'oxydation des réactifs en leurs oxydes respectifs et la formation d'un mélange de verres. Le GeO2 présente un indice de réfraction élevé, ce qui permet de définir précisément l'indice de réfraction global de la fibre en modulant précisément le débit de GeCl4.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Germanium(IV) chloride 99.999% trace metals basis, consultée le 23 mars 2018.
- « Fiche du composé Germanium(IV) chloride, 99.9999% (metals basis) », sur Alfa Aesar (consulté le ).