Gaz à l'état de traces
Les gaz à l'état de traces, ou traces de gaz, parfois nommés gaz résiduels, sont des gaz présents en petites quantités dans un environnement tel que l'atmosphère d'une planète. Les traces de gaz dans l'atmosphère terrestre concernent des gaz autres que l'azote (78,1 %), l'oxygène (20,9 %) et l'argon (0,934 %) dont la combinaison y constitue 99,934 %, outre la vapeur d'eau.
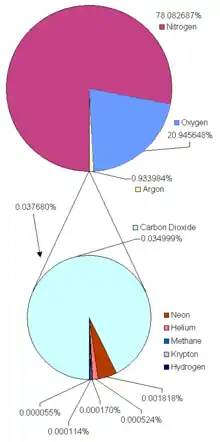
Abondance, sources et puits
L'abondance d'un gaz de ce type peut aller de quelques parties par billion (ppt) en volume à plusieurs centaines de parties par million en volume (ppm/v)[1]. Lorsqu'un gaz à l'état de trace est diffusé dans l'atmosphère, ce processus est appelé une source. Il existe deux types de sources possibles - naturelles ou anthropiques. Les sources anthropiques, au contraire des sources naturelles sont causées par l'activité humaine.
Certaines traces de gaz ont pour origine les processus biogéniques, le dégazage des terres émergées, les émissions océaniques, les émissions industrielles et la formation in situ[1]. Les sources biogéniques comprennent la photosynthèse, les excréments d'animaux, les termites, les rizières et les zones humides. Les volcans sont la principale source de gaz à l'état de traces provenant de la terre solide. L'océan mondial est également une source de plusieurs gaz traces, en particulier les sulfureux. La formation in situ de traces de gaz se produit par des réactions chimiques en phase gazeuse[1]. Les sources anthropiques sont causées par des activités humaines telles que la combustion de combustibles fossiles (dans les transports, notoirement), l'extraction de combustibles fossiles, la combustion de la biomasse et l'activité industrielle.
En revanche, un puits se produit lorsqu'un gaz à l'état de trace est retiré de l'atmosphère. Certains des puits de ce type se forment en raison de réactions chimiques dans l'atmosphère, principalement avec le radical OH, la conversion gaz-particules formant des aérosols, les dépôts humides et les dépôts secs[1]. L'activité microbiologique dans les sols crée d'autres puits.
Le tableau, ci-dessous, répertorie plusieurs gaz à l'état de traces, indiquant leur abondance, leur durée de vie atmosphérique, leurs sources et leurs puits.
Gaz à l'état de traces à la pression d'1 atm[1]
| Gaz | Formule chimique | Fraction de volume d'air par espèce | Temps de séjour ou durée de vie | Principales sources | Principaux puits |
|---|---|---|---|---|---|
| Gaz carbonique | CO2 | 419 ppm ≈ppmv (mai 2021)[2] |
En croissance, voir Remarque [A] |
Biologique, océanique, combustion, anthropique | photosynthèse |
| Néon | Ne | 18,18 ppmv | _________ | Volcanique | ________ |
| Hélium | He | 5,24 ppmv | _________ | Radiogène | ________ |
| Méthane | CH4 | 1,89 ppm (mai 2021)[3] |
9 années | Biologique, anthropique | OH |
| Hydrogène | H2 | 0,56 ppmv | ~ 2 ans | Biologique, photolyse HCHO | absorption du sol |
| Protoxyde d'azote | N2O | 0,33 ppmv | 150 ans | Biologique, anthropique | O(1D) dans la stratosphère |
| Monoxyde de carbone | CO | 40 – 200 ppbv | ~ 60 jours | Photochimique, combustion, anthropique | OH |
| Ozone | O3 | 10 – 200 ppbv (troposphère) | Jours – mois | Photochimique | photolyse |
| Formaldéhyde | HCHO | 0,1 – 10 ppbv | ~ 1,5 heures | Photochimique | OH, photolyse |
| Azote (diverses espèces) | NOx | 10 pptv – 1 ppmv | Variable | Sols, anthropiques, foudre | OH |
| Ammoniac | NH3 | 10 pptv – 1 ppbv | 2 – 10 jours | Biologique | conversion de gaz en particules |
| Dioxyde de soufre | SO2 | 10 pptv – 1 ppbv | Journées | Photochimique, volcanique, anthropique | OH, oxydation à base d'eau |
| Sulfure de diméthyle | (CH3)2S | plusieurs pptv – plusieurs ppbv | Journées | Biologique, océanique | OH |
A Le Groupe d'experts intergouvernemental sur l'évolution du climat (GIEC) déclare qu'« aucune durée de vie atmosphérique unique ne peut être donnée » pour le CO2[4]. Cela est principalement dû au taux de croissance élevé et à la grande ampleur cumulée des perturbations du cycle du carbone de la Terre par l'extraction géologique. et la combustion du carbone fossile[5]. En 2014, on s'attendait à ce que le CO2 fossile émis sous la forme d'une impulsion théorique de 10 à 100 Gigatonnes en plus de la concentration atmosphérique existante soit éliminé à 50 % par la végétation terrestre et les puits océaniques en moins d'un siècle environ. Une fraction substantielle (20-35 %) devrait également rester dans l'atmosphère pendant des siècles, voire des millénaires, où la persistance fractionnelle augmente avec la taille des impulsions[6] - [7]. Ainsi, la durée de vie du CO2 augmente à mesure que davantage de carbone fossile est extrait par l'homme.
Mélange et durée de vie
L'émission globale des gaz à l'état de traces d'origine humaine dans l'atmosphère terrestre est en augmentation. La plupart proviennent de l'activité industrielle de l'hémisphère nord plus peuplé. Les données de séries chronologiques provenant de stations de mesure du monde entier indiquent qu'il faut généralement 1 à 2 ans pour se fondre uniformément dans toute la troposphère[8] - [9].
Le temps de séjour d'un de ces gaz dépend de la quantité et du taux d'élimination. La relation (empirique) de Junge exprime le lien entre les fluctuations de concentration et le temps de séjour d'un gaz dans l'atmosphère. Il peut être exprimé sous la forme :
« fc = b /τr »
où fc est le coefficient de variation, τr est le temps de séjour en années et b est une constante empirique, que Junge avait initialement fixée à 0,14 ans[10]. À mesure que le temps de séjour augmente, la variabilité de la concentration diminue. Cela implique que les gaz les plus réactifs ont la plus grande variabilité de concentration en raison de leurs longévités plus courtes. À contrario, les gaz plus inertes sont non variables et se maintiennent plus longtemps. Lorsqu'elle est mesurée loin de leurs sources et de leurs puits, la formule peut être utilisée pour estimer les temps de séjour des gaz dans la troposphère[10].
Traces de gaz à effet de serre
L'eau (sous forme de vapeur), le dioxyde de carbone, le méthane, l'oxyde nitreux, l'ozone et les CFC font partie des principaux gaz à effet de serre. Ces gaz peuvent absorber le rayonnement infrarouge de la surface de la Terre lors de son passage dans l'atmosphère.
Le gaz à effet de serre le plus influent est la vapeur d'eau. Il se trouve fréquemment à des concentrations élevées, peut devenir un aérosol (nuages) ou en provenir. Il n'est donc généralement pas classé comme un gaz à l'état de traces. À l'échelle locale, la vapeur d'eau peut piéger jusqu'à 80 % du rayonnement IR sortant[11]. À l'échelle globale, elle est responsable d'environ la moitié de l'effet de serre total de la Terre[12].
Le dioxyde de carbone est le deuxième gaz à effet de serre le plus important et le gaz résiduel le plus abondant des sources artificielles[11]. Il contribue à environ 20 % de l'effet de serre total de la Terre[12]. Les gaz à effet de serre peuvent absorber le rayonnement infrarouge en raison de leur structure moléculaire. Le dioxyde de carbone, par exemple, a deux modes de vibration de base qui créent un fort moment dipolaire, provoquant sa forte absorption du rayonnement infrarouge[11].
En revanche, les gaz les plus abondants dans l'atmosphère (N2, O2 et Ar) ne sont pas des gaz à effet de serre. En effet, ils n'absorbent pas le rayonnement infrarouge car ils n'ont pas de vibrations avec un moment dipolaire[11]. Par exemple, les triples liaisons du diazote atmosphérique forment une molécule symétrique avec des états d'énergie vibrationnelle presque totalement inchangés aux fréquences infrarouges.
Le tableau suivant montre certains des principaux gaz à effet de serre à l'état de traces, leurs sources artificielles et une estimation de la contribution relative de ces sources à l'effet de serre accru qui influence le réchauffement climatique.
Principaux gaz à effet de serre et sources[11]
| Gaz | Formule chimique | Principales sources humaines | Contribution à l'augmentation (estimation de l'année 1995) |
|---|---|---|---|
| Gaz carbonique | CO2 | Combustion d'énergie fossile, déforestation | 55 % |
| Méthane | CH4 | Rizières, bovins et vaches laitières, décharges, production de pétrole et de gaz | 15 % |
| Protoxyde d'azote | N2O | Engrais, combustion du charbon, feux de biomasse | 6 % |
Références
- (en) John Wallace et Peter Hobbs, Atmospheric Science: An Introductory Survey, Amsterdam, Boston, Elsevier Academic Press, (ISBN 9780127329512)
- (en) « Trends in Atmospheric Carbon Dioxide », NOAA Earth System Research Laboratories (consulté le ).
- (en) « Trends in Atmospheric Methane », NOAA Earth System Research Laboratories (consulté le )
- (en) AR5 Climate Change 2013: The Physical Science Basis (lire en ligne), « Chapter 8 »
- (en) Pierre Friedlingstein, Matthew W. Jones, Michael O'Sullivan et Robbie M. Andrew, « Global Carbon Budget 2019 », Earth System Science Data, vol. 11, no 4, , p. 1783–1838 (ISSN 1866-3508, DOI 10.5194/essd-11-1783-2019, lire en ligne, consulté le )
- (en) Archer, « Atmospheric lifetime of fossil fuel carbon dioxide », Annual Review of Earth and Planetary Sciences, vol. 37, no 1, , p. 117–34 (DOI 10.1146/annurev.earth.031208.100206, Bibcode 2009AREPS..37..117A, lire en ligne)
- (en) Joos, F., Roth, R. et Fuglestvedt, J.D., « Carbon dioxide and climate impulse response functions for the computation of greenhouse gas metrics: A multi-model analysis », Atmospheric Chemistry and Physics, vol. 13, no 5, , p. 2793–2825 (DOI 10.5194/acpd-12-19799-2012, lire en ligne)
- (en) « AGAGE Data and Figures », Massachusettes Institute of Technology (consulté le )
- (en) « Long-term global trends of atmospheric trace gases », NOAA Earth System Research Laboratories (consulté le )
- (en) Slinn, « A Simple Model for Junge's Relationship between Concentration Fluctuations and Residence Times for Tropospheric Trace Gases », Tellus B: Chemical and Physical Meteorology, vol. 40, no 3, , p. 229–232 (DOI 10.3402/tellusb.v40i3.15909)
- (en) Trogler, « The Environmental Chemistry of Trace Atmospheric Gases », Journal of Chemical Education, vol. 72, no 11, , p. 973 (DOI 10.1021/ed072p973)
- (en) Gavin Schmidt, « Taking the Measure of the Greenhouse Effect », NASA Goddard Institute for Space Studies - Science Briefs,
Liens externes
- (en) « Trace Gases », sur web.archive.org, (consulté le ), description des gaz à l'état de traces atmosphériques
- Sur les gaz traces et leur rôle