Acide pénicillique
L'acide pénicillique est une mycotoxine polycétide produite par diverses espèces des genres Aspergillus (par exemple Aspergillus flavus) et Penicillium (Penicillium roqueforti). C'est aussi le principal produit de la dégradation de la pénicilline en milieu acide. Sa première synthèse pratique a été rapporté en 1947 par Ralph Raphael qui travaillait sur la pénicilline durant la Seconde Guerre mondiale[5].
| Acide pénicillique | |
| |
| Identification | |
|---|---|
| Nom systématique | 5-hydroxy-5-isopropényl-4-méthoxy-furan-2-one |
| No CAS | |
| No ECHA | 100.001.826 |
| No CE | 202-008-1 |
| PubChem | 1268111 |
| SMILES | |
| InChI | |
| Apparence | aiguilles[1] solide blanc[2] |
| Propriétés chimiques | |
| Formule | C8H10O4 |
| Masse molaire[3] | 170,162 6 ± 0,008 3 g/mol C 56,47 %, H 5,92 %, O 37,61 %, |
| Propriétés physiques | |
| T° fusion | 83 à 84 °C[1] |
| T° ébullition | 285,7 °C (760 mmHg)[2] |
| Solubilité | voir ci-dessous |
| Point d’éclair | 113,5 °C[2] |
| Précautions | |
| SGH[4] | |
 Attention |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés
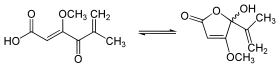
L'acide pénicillique se présente sous la forme d'aiguilles qui fondent vers 83 à 84 °C[1]. Il coexiste sous deux formes, une forme lactone et une forme cétone[6].
L'acide pénicillique est soluble dans l'acétone[7], modérément soluble dans l'eau froide (20 g·l-1) mais librement soluble dans l'eau chaude, l'alcool, l'éther, le benzène et le chloroforme. Il est légèrement soluble dans l'éther de pétrole chaud et pratiquement insoluble dans le pentane-hexane[1].
Son monohydrate se présente sous la forme de grands cristaux rhombiques monocliniques ou tricliniques transparents qui fondent vers 58 à 64 °C[1]
Activité biochimique
L'acide pénicillique induit des ruptures d'ADN simple et double brin. Il inhibe de manière irréversible la GDP-mannose déshydrogénase (DMG), une enzyme de synthèse des alginates. Il inhibe également l'aldose déshydrogénase musculaire, l'alcool déshydrogénase et la lactate déshydrogénase[4]. Il inhibe l'apoptose induite par ligand de Fas (FasL) en bloquant l'autotraitement de la caspase 8 dans le death-inducing signaling complex (en) (DISC)[8].
Utilisations
L'acide pénicillique a été utilisé pour étudier l'apoptose induite par ligand de Fas et la vabilité de cllules du lymphome de Burkitt chez les cellules de Raji[8]. Il a aussi été utilisé pour des essais biologiques de bioluminescence bactérienne [9] et étudier la génotoxicité des hépatocytes[10]
Notes et références
- (en) Budavari, S., The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals, Merck and Co, , p. 1218
- Fiche Alfa chemistry
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Penicillic acid, consultée le 25 septembre 2020.
- Ralph Raphael, « Synthesis of the Antibiotic, Penicillic Acid », Nature, vol. 160, , p. 261-262 (DOI 10.1038/160261c0)
- Cole, R. J. and R. H. Cox. Handbook of Toxic Fungal Metabolites. New York: Academic Press, Inc., 1981., p. 520
- Weast, R.C. (ed.). Handbook of Chemistry and Physics. 60th ed. Boca Raton, Florida: CRC Press Inc., 1979., p. C-412
- Masashige Bando, Makoto Hasegawa, Yasunori Tsuboi, Yasunobu Miyake, Masashi Shiina, Mika Ito, Hiroshi Handa, Kazuo Nagai, Takao Kataoka, « The mycotoxin penicillic acid inhibits Fas ligand-induced apoptosis by blocking self-processing of caspase-8 in death-inducing signaling complex », J Biol Chem., vol. 278, no 8, , p. 5786-93 (PMID 12482880, DOI 10.1074/jbc.M204178200)
- I E Yates, J K Porter, « Bacterial bioluminescence as a bioassay for mycotoxins », Applied and environmental microbiology, vol. 44, no 5, , p. 1072-5 (DOI 10.1128/AEM.44.5.1072-1075)
- H Mori, K Kawai, F Ohbayashi, T Kuniyasu, M Yamazaki, T Hamasaki, G M Williams, « Genotoxicity of a variety of mycotoxins in the hepatocyte primary culture/DNA repair test using rat and mouse hepatocytes », Cancer research, vol. 44, no 7, , p. 2918-23 (PMID 6722817)