Trifluorure de neptunium
Le trifluorure de neptunium est un composé chimique de formule NpF3. Il se présente sous la forme d'un solide violet cristallisé dans le système trigonal selon le groupe d'espace P3c1 (no 165)[4]. Il peut être obtenu en faisant réagir de l'oxyde de neptunium(IV) NpO2 avec du fluorure d'hydrogène dans un flux d'hydrogène H2 à 500 °C[4] :
| Trifluorure de neptunium | |
| |
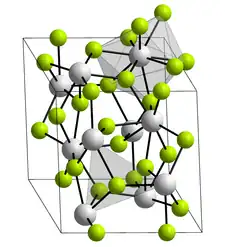
| __ Np3+ __ F− Structure cristalline du fluorure de neptunium(III) |
|
| Identification | |
|---|---|
| Synonymes |
fluorure de neptunium(III) |
| No CAS | |
| Apparence | solide violet[1] |
| Propriétés chimiques | |
| Formule | NpF3 |
| Masse molaire[2] | 294 g/mol F 19,39 %, Np 80,63 %, |
| Propriétés physiques | |
| T° fusion | 1 425 °C[3] |
| Cristallographie | |
| Système cristallin | trigonal[4] |
| Classe cristalline ou groupe d’espace | P3c1 (no 165) [4] |
| Paramètres de maille | a = 712,9 pm, c = 728,8 pm[4] |
| Précautions | |
 Composé radioactif |
|
| Unités du SI et CNTP, sauf indication contraire. | |
On peut également l'obtenir en faisant réagir une solution aqueuse de neptunium avec des sels de fluorure dans un milieu faiblement acide :
Le tétrafluorure de neptunium NpF4 est réduit en trifluorure de neptunium NpF3 par un flux d'hydrogène H2[4] :
Réactions
Le trifluorure de neptunium est fluoré en hexafluorure de neptunium dans un flux de fluor F2 gazeux à 500 °C[5] :
L'oxydation du trifluorure de neptunium avec un mélange d'oxygène et de fluorure d'hydrogène conduit au tétrafluorure de neptunium NpF4[6] :
Il peut également se former du NpF4 et du NpO2 à la suite d'une réaction inhabituelle avec l'oxygène[7] :
Le neptunium métallique peut être obtenu à partir de ses composés par réduction, par exemple en faisant réagir du trifluorure de neptunium avec du baryum ou du lithium élémentaires à 1 200 °C :
Notes et références
- (de) A. F. Holleman, E. Wiberg, N. Wiberg, Lehrbuch der Anorganischen Chemie, 102e éd., Walter de Gruyter, 2007, p. 1969. (ISBN 978-3-11-017770-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Neptunium trifluoride », sur https://www.webelements.com/ (consulté le ).
- (de) C. Keller, « Die Chemie des Neptuniums », Fortschritte der Chemischen Forschung, 1969/70, 13/1, p. 69, DOI 10.1007/BFb0051170.
- (en) John G. Malm, Bernard Weinstock et E. Eugene Weaver, « The Preparation and Properties of NpF5; a Comparison with PuF5 », The Journal of Physical Chemistry, vol. 62, no 12, , p. 1506-1508 (DOI 10.1021/j150570a009, lire en ligne)
- (de) « Neptuniumverbindungen », sur https://www.spektrum.de/, (consulté le ).
- Manuel Gmelin de chimie minérale, Système no 71, Transuraniens, partie C, p. 101–104.


