Rectocolite hémorragique
La rectocolite hémorragique (RCH) ou colite ulcéreuse est une maladie inflammatoire chronique intestinale (MICI) qui affecte l'extrémité distale du tube digestif, c’est-à-dire le côlon et le rectum qui est toujours touché[1]. Son étiologie est inconnue, bien qu'une composante génétique constitue une hypothèse. Elle est classée dans les maladies auto-immunes. C'est une maladie qui agit par poussée et qui ne se guérit pas, ce qui nécessite un traitement médicamenteux à vie. L'objectif des traitements est que les rémissions durent le plus longtemps possible.
| Médicament | Nicotine (d), olsalazine (en), cortisol, balsalazide (en), azathioprine, sulfasalazine, acide 5-aminosalicylique, prednisone, étanercept, certolizumab pegol, Symbicort, vedolizumab, budésonide, méthotrexate, golimumab, adalimumab, tofacitinib, ustekinumab, prednisolone, tacrolimus, mercaptopurine hydrate (d), infliximab, bétaméthasone, olsalazine (en), balsalazide (en), acide 5-aminosalicylique et budésonide |
|---|---|
| Spécialité | Gastro-entérologie |
| CISP-2 | D94 |
|---|---|
| CIM-10 | K51 |
| CIM-9 | 556 |
| OMIM | 191390 |
| DiseasesDB | 13495 |
| MedlinePlus | 000250 |
| eMedicine | 183084 |
| MeSH | D003093 |
| Patient UK | Ulcerative-colitis-pro |
![]() Mise en garde médicale
Mise en garde médicale
Son diagnostic repose essentiellement sur les examens cytologiques qui accompagnent les prélèvements lors d'une coloscopie.
Tout comme la maladie de Crohn, elle peut s'accompagner de manifestations extra-intestinales : articulaires, cutanées, oculaires, etc.
Les malades atteints de RCH ou de la maladie de Crohn sont parfois sujets à la laxophobie.
Symptômes

La maladie évolue par poussées inflammatoires de la muqueuse du côlon, qui peuvent durer des mois et se répéter plusieurs fois par an, entrecoupées de période d'accalmie.
Le diagnostic de la RCH est posé sur un ensemble d'éléments cliniques et paracliniques. Le tableau clinique regroupe des signes digestifs et des signes extradigestifs[2].
Les symptômes digestifs sont principalement constitués d'une diarrhée chronique et sanglante (plusieurs semaines à plusieurs mois), hémorragique dans les poussées graves, très douloureuse et accompagnée fréquemment de glaires mélangées ou non aux selles. Les patients souffrent de brulures rectales (ténesme), de coliques expulsives et d'épreintes (faux besoins).
Il peut exister des manifestations extra-intestinales, principalement ostéoarticulaires (rhumatisme axial et périphérique) mais aussi hépatobiliaires (cholangites sclérosantes primitives), oculaires (conjonctivites et uvéites) ou cutanées (aphtes buccaux, érythèmes noueux, pyoderma gangrenosum).
La fatigue est un symptôme classique, présent même en dehors des poussées. Les poussées sévères s'accompagnent fréquemment d'amaigrissement, d'anémie et/ou de fièvre.
Diagnostic
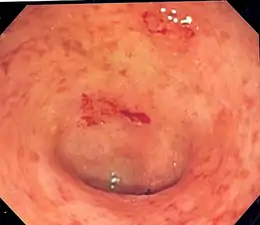
La coloscopie montre typiquement un aspect inflammatoire du côlon, naissant au niveau du rectum et remontant plus ou moins haut de manière continue. Cette continuité des lésions est parfois inconstante[3]. La sévérité de la maladie dépend en partie de son extension.
La calprotectine fécale peut être utilisé comme un marqueur non invasif de l'activité de la maladie et pour évaluer la réponse à la thérapie ou une rechute[4].
Diagnostic différentiel
Le diagnostic de la RCH peut être difficile à faire car la maladie peut avoir, à tort, été étiquetée comme un trouble fonctionnel digestif, intestinal (TFD, TFI ou colopathie fonctionnelle).
On peut facilement la confondre avec la maladie de Crohn (pouvant toucher tout le tube digestif), car la RCH est aussi une MICI (maladie inflammatoire chronique intestinale). Cependant, les ulcères causés par la maladie de Crohn tendent à être transmuraux (d'erroder toute l'épaisseur de l'intestin), alors que ceux associés à la RCH se limitent à la muqueuse et la sous-muqueuse [5]. Au contraire de la maladie de Crohn, la RCH ou colite ulcéreuse se limite au gros intestin et au rectum, et ne peut toucher d'autres parties du tube digestif.
Si le diagnostic peut ne pas être porté avec certitude entre ces deux entités lors des premières poussées, on parle alors de colite indéterminée. Dans la plupart des cas, l'évolution de la pathologie et de ses signes cliniques permet, après plusieurs mois ou années, de finir par déterminer avec précision la maladie concernée et donc d'adapter au mieux la stratégie thérapeutique. Il arrive cependant que la colite reste indéterminée, le débat actuel étant de savoir si ce n'est pas une troisième entité des MICI.
Certaines colites infectieuses peuvent aussi présenter un tableau trompeur.
Incidence - Prévalence
L'incidence est supérieure à celle de la maladie de Crohn et est estimée dans les pays occidentaux à entre 9 et 20 cas annuels sur 100 000 personnes[6]. Les occidentaux sont plus touchés que les autres populations, notamment les blancs (2 à 5 fois plus)[7]. Elle débute préférentiellement chez les jeunes adultes entre 20 et 40 ans. Il existe des prédispositions familiales qui peuvent faire évoquer un facteur génétique[8].
En France, de nombreux nouveaux cas sont diagnostiqués chaque année (probablement de l'ordre de 2 000 à 2 500 cas), avec un nombre total de cas d'environ 40 000. La RCH est ainsi une maladie peu fréquente mais ne fait plus partie des maladies rares.
Facteurs de risque et facteurs protecteurs
Les causes de cette maladie sont encore en grande partie inconnues. C'est une maladie auto-immune, ce qui signifie que le système immunitaire s'attaque à ses propres cellules.
Il existe une prédisposition génétique avec plusieurs gènes identifiés[9] (20 % des malades ont un proche souffrant d'une MICI). La part génétique semble cependant plus en rapport avec la sévérité de la maladie qu'avec le risque de déclencher cette dernière[10]. Plusieurs mutations favorisant la rectocolite hémorragique sont également associées avec la maladie de Crohn[11].
Un facteur déclenchant environnemental (infection bactérienne digestive[12]) joue un rôle dans la survenue d'une cascade inflammatoire non contrôlée.
Il s'agit donc d'une maladie multifactorielle au même titre que la maladie de Crohn ou la polyarthrite rhumatoïde, autres maladies proches.
Les infections durant l'enfance pourraient être protectrices, ce qui expliquerait en partie la plus grande prévalence de la maladie dans les pays riches et dans les milieux urbains[13]. Le tabagisme serait également protecteur[14] avec même une possible aggravation de la maladie en cas d'arrêt du tabagisme[15]. La survenue d'une appendicite durant l'enfance ou l'adolescence semble diminuer le risque ultérieur de survenue d'une rectocolite, une appendicectomie faite à titre systématique ne semblant, par contre, pas protectrice[16]. L'explication de cette corrélation est peu claire.
Le stress ne semble pas avoir de rôle favorisant[17].
La maladie peut s'exacerber pendant une grossesse[18] mais le fait d'allaiter serait protecteur[19].
Physiopathologie
La physiopathologie de la rectocolite hémorragique reste peu connue.
La lésion concerne les cellules de l'épithélium digestif séparant la lumière (contenant le bol alimentaire avec de nombreux germes), du reste de l'organisme. Il n'est toutefois pas clair si cette lésion est cause de la maladie ou conséquence. Il existe ainsi une diminution de sécrétion de mucus, une altération des jonctions inter-cellulaires, une augmentation de l'apoptose (mort programmée cellulaire), ces dernières étant probablement secondaires à la sécrétion de plusieurs cytokines dont l'interleukine 13[20].
Les germes du tube digestif (microbiote commensal) semblent jouer un rôle : la maladie ne se développe pas dans un modèle animal dont le tube digestif a été stérilisé[21]. Il existe des arguments pour que cela soit également le cas chez l'être humain[22].
Le facteur de nécrose tumorale-alpha (TNFα) est retrouvé en quantité élevée dans les selles[23] et le mucus intestinal, même dans les phases inactives de la maladie[24], ce qui peut expliquer l'efficacité des médicaments ciblant cette molécule dans le traitement de la rectocolite hémorragique. Il existe également une composante immunologique avec une activation de certains lymphocytes T[6].
Évolution
La maladie se caractérise par des phases de poussées entrecoupées de phases de rémissions. La sévérité des symptômes et le risque de récidive sont en rapport avec l'extension des lésions à la coloscopie[6].
Les complications sont, à court terme, la survenue d'une colectasie (dilatation toxique du côlon) ou une colite aigüe grave (poussée très sévère d'emblée).
Il existe, après 10 ans d'évolution, une majoration du risque de cancer colorectal[25]. Ce risque est surtout important en cas d'atteinte étendue[26] et nécessite une surveillance régulière par coloscopie. Le traitement médical au long cours par mesalazine[27] ou par azathioprine[28] pourrait diminuer le risque de cancérisation.
La mortalité ne semble pas être augmentée par rapport au reste de la population[29].
Personnalités atteintes de rectocolite hémorragique
- Le Premier ministre japonais Shinzo Abe était atteint de cette maladie depuis l'adolescence. L'aggravation de son état de santé l'avait contraint à annoncer sa démission le [30].
- Le chanteur Dan Reynolds du groupe Imagine Dragons, diagnostiqué à l'âge de 21 ans[31].
- Le militant de la la diffusion libre de la connaissance Aaron Swartz était atteint de cette maladie, lui causant maux de ventre et épisodes dépressifs chroniques[32].
Traitement
La prise en charge de la rectocolite hémorragique a fait l'objet de la publication de plusieurs recommandations. Les dernières européennes[33] datent de 2008, celles américaines de 2019[4].
Traitement d'attaque (aigu)
- Pour les poussées légères à modérées, on utilise des salicylés (5ASA/mesalazine) à forte dose. Dans les formes rectales, la voie d'administration locale (suppositoire) est préférable[34]. Dans les formes plus étendues, une double voie d'administration (orale et suppositoire) est choisie[35].
- Pour les poussées moyennes ne répondant pas aux salicylés, on peut utiliser des corticoïdes comme la béclométasone en comprimés gastro-résistants. La béclométasone est un corticoïde ayant l'avantage de n'agir que dans le côlon, il est donc quasiment dépourvu des effets secondaires classiques des corticoïdes. La réponse est bonne dans huit cas sur dix, avec cependant certaines formes exigeant la poursuite prolongée du traitement (cortico dépendance) dans un cas sur cinq[36].
- Pour les poussées moyennes et sévères, on prescrit plutôt des corticoïdes (comme la prednisolone) par voie générale (orale ou injectable).
Dans les formes corticodépendantes (si on diminue la dose de corticoïde les signes cliniques réapparaissent) ou corticorésistantes (même les corticoïdes ne permettent pas de faire disparaitre les signes cliniques), et aussi dans les formes sévères de la maladie on introduit de plus en plus un traitement par immunosuppresseur (azathioprine[37] ou méthotrexate). Le gain d'efficacité reste cependant faible[38].
- Pour les poussées graves ou en cas d'échec des précédents traitements, on peut utiliser la ciclosporine[39] (immunosuppresseur), l'infliximab[40] ou l'adalimumab[41] (Inhibiteurs du TNF ou anti-TNF alpha).
Le tofacitinib est aussi utilisé pour traiter la maladie. Il y a un intérêt pour ses propriétés inhibiteurs de la Janus kinase 1 et 3.
Le filgotinib a été efficace dans un essai contre placebo sur une cohorte de 1 348 malades à la dose de 200 mg[42].
Ose Immunotherapeutics étudie l'impact d'un traitement à base de OSE-127, un anticorps monoclonal qui cible le récepteur CD127[43].
Chirurgie
Utilisée en dernier recours, la chirurgie est le seul traitement permettant de « guérir » la maladie (si le rectum et le côlon sont enlevés). Un tiers des formes sévères aboutissent à ce traitement[44] (statistiques datant de la période d'avant l'utilisation des inhibiteurs du TNF).
Traitement d'entretien (préventif)
Le traitement d'entretien utilise les salicylés (5ASA ou mesalazine)[45] ou dans les formes plus sévères, l'azathioprine, la mercaptopurine[46] ou la méthotrexate (immunosuppresseurs). les patients ayant répondu à l'infliximab peuvent poursuivre ce traitement pour la prévention des récidives des rechutes[6].
Régime
Le régime est d'un intérêt discuté car aucun essai clinique sérieux n'a été mené à ce sujet. Cependant les malades connaissent souvent des difficultés de digestion et sont sujets aux ballonnements. Il est recommandé d'éviter les aliments ou boissons aggravant ces symptômes.
Les probiotiques semblent avoir une efficacité pour entretenir la rémission de la rectocolite hémorragique[47].
Régime pauvre en fibres
En cas de poussée, le régime pauvre en fibres est généralement conseillé car il améliore le confort en diminuant les diarrhées et les douleurs abdominales. Si ce régime pauvre en fibres est instauré, celui-ci doit être riche en protéines et il faut également compenser les pertes en eau et en sels minéraux (particulièrement fer et calcium).
La principale restriction pourrait aussi être la consommation de sel en cas de traitement par corticoïde (habituellement l'utilisation de ce dernier est limitée à la période de poussée de la maladie).
En dehors des poussées l'alimentation doit redevenir aussi normale et équilibrée que possible afin d'éviter une quelconque carence. Le patient doit néanmoins éviter les aliments non supportés selon sa tolérance personnelle.
Régime en glucides spécifiques
Le régime en glucides spécifiques exclut l'ingestion de certains glucides dits complexes. Cela affranchit le système digestif d'aliments qu'il ne peut pas digérer complètement. Ce régime semble procurer un mieux-aller pour certains patients[48].
Traitement traditionnel alternatif
L'encens de Boswellia elongata (en), arbre à encens endémique au Yémen, est préconisé par des tradipraticiens pour lutter contre les inflammations, notamment (dans les douleurs) dentaires, articulaires et intestinales. Chez l'animal de laboratoire a été montrée la capacité des acides boswelliques extraits de l'encens à inhiber la production des leucotriènes, des molécules impliquées dans les mécanismes inflammatoires responsables de la maladie de Crohn et de la rectocolite hémorragique[49] - [50].
La berbérine améliore un peu les symptômes[51]. D'après une méta-analyse, la combinaison de probiotiques et de formules de médecine traditionnelle chinoise est plus efficace que l'acide 5-aminosalicylique[52]. L'indigo naturel est hautement efficace contre la colite ulcéreuse pédiatrique mais peut causer des effets secondaires graves[53].
L'administration de Thymus kotschyanus a montré une amélioration des symptômes[54].
Restauration de la barrière intestinale
L’atteinte de l’intégralité de la barrière intestinale et particulièrement le mucus est un des facteurs qui semble à être impliqué dans la pathogénie de la rectocolite hémorragique. Les phospholipides jouent ont un rôle important dans l’intégrité de cette barrière. La phosphatidylcholine composant principal représente plus de 90 % des espèces phospholipidiques, est en concentration significativement moindre chez les patients atteints de RCH. La substitution orale en phosphatydilcholine au cours d'une étude prospective, randomisée et contrôlée contre placebo, en double aveugle chez des patients atteints de RCH légère à modérée semble sûre mais inefficace[55].
Bactériothérapie fécale
La bactériothérapie fécale est un traitement médical développé à la fin du XXe siècle par le Dr Thomas J. Borody (en) et son équipe à Sydney, en Australie, principalement comme un traitement alternatif pour la colite pseudomembraneuse, il est à ce jour destiné à des patients souffrant de quelques maladies intestinales résistant aux traitements antibiotiques classiques, dont la RCH[56].
Pour la RCH, aucun agent pathogène n'a été trouvé à ce jour. Mais l'efficacité de la bactériothérapie fécale dans ce cas suggère que la cause de la RCH pourrait être une infection antérieure par un agent pathogène encore inconnu.
Cette infection initiale peut parfois se résoudre naturellement. Mais dans certains cas, un déséquilibre du microbiote intestinal du côlon pourrait conduire à un cycle inflammatoire (ce qui expliquerait la nature cyclique et récurrente de cette maladie). Ce cycle semble, au moins dans de nombreux cas, pouvoir être rompu par la recolonisation du côlon du malade par un complexe bactérien prélevé dans un intestin sain[57] - [58]. Certains médecins estiment que le traitement, effectué dans de bonnes conditions, est sûr et que de nombreux malades pourraient bénéficier de cette thérapie[59].
Prise en charge en France
En France, la rectocolite hémorragique (RCH) fait partie de la liste des ALD (affections de longue durée) uniquement en cas d'invalidité avérée, prise en charge à 100 % du ticket modérateur (après la signature de l'accord par le patient et son médecin référent). D'autres droits sont ouverts, notamment pour les salariés, les jours de carence des arrêts de travail ne s'appliquent qu'au premier arrêt sur une période de trois années. Des indemnités journalières (IJ) sont donc versées à concurrence d'un maximum de 360 IJ pour une période de trois années consécutives[60]. Ceci permet au malade de conserver une activité salariée sans pénaliser sa prise en charge médicale.
Notes et références
- « Rectocolite hémorragique : définition et facteurs favorisants », sur www.ameli.fr (consulté le )
- Marc-André Bigard, Marc-André Bigard, Laurence Choné, Guide pratique des maladies du tube digestif, Elsevier Masson, 2001. (ISBN 2901227627), 9782901227625. 331 pages. Chapitre RCH page 152
- (en) D'Haens G, Geboes K, Peeters M, Baert F, Ectors N, Rutgeerts P. « Patchy cecal inflammation associated with distal ulcerative colitis: a prospective endoscopic study » Am J Gastroenterol. 1997;92:1275-9.
- David T. Rubin, Ashwin N. Ananthakrishnan, Corey A. Siegel et Bryan G. Sauer, « ACG Clinical Guideline: Ulcerative Colitis in Adults », The American Journal of Gastroenterology, vol. 114, no 3, , p. 384–413 (ISSN 1572-0241, PMID 30840605, DOI 10.14309/ajg.0000000000000152, lire en ligne, consulté le )
- (en) Osmosis, « Ulcerative Colitis »
 , sur Osmosis.org
, sur Osmosis.org - (en) Ordás I, Eckmann L, Talamini M, Baumgart DC, Sandborn WJ. « Ulcerative colitis » Lancet 2012
- colite ulcéreuse, personnes à risque
- (en) Orholm M, Munkholm P, Langholz E, Nielsen OH, Sørensen TI, Binder V. « Familial occurrence of inflammatory bowel disease » N Engl J Med. 1991;324:84-8.
- (en) Silverberg MS, Cho JH, Rioux JD et al. « Ulcerative colitis-risk loci on chromosomes 1p36 and 12q15 found by genome-wide association study » Nat Genet. 2009;41:216-220
- (en) Bouma G, Crusius JB, García-González MA et al. « Genetic markers in clinically well defined patients with ulcerative colitis (UC) » Clin Exp Immunol. 1999;115:294-300
- (en) Anderson CA, Boucher G, Lees CW et al. « Meta-analysis identifies 29 additional ulcerative colitis risk loci, increasing the number of confirmed associations to 47 » Nat Genet. 2011;43:246-252
- (en) García Rodríguez LA, Ruigómez A, Panés J, « Acute gastroenteritis is followed by an increased risk of inflammatory bowel disease » Gastroenterology 2006;130:1588-1594
- (en) López-Serrano P, Pérez-Calle JL, Pérez-Fernández MT, Fernández-Font JM, Boixeda de Miguel D, Fernández-Rodríguez CM. « Environmental risk factors in inflammatory bowel diseases. Investigating the hygiene hypothesis: a Spanish case-control study » Scand J Gastroenterol. 2010;45:1464-1471
- (en) Mahid SS, Minor KS, Soto RE, Hornung CA, Galandiuk S. « Smoking and inflammatory bowel disease: a meta-analysis » Mayo Clin Proc. 2006;81:1462-1471
- (en) Beaugerie L, Massot N, Carbonnel F, Cattan S, Gendre JP, Cosnes J. « Impact of cessation of smoking on the course of ulcerative colitis » Am J Gastroenterol. 2001;96:2113-2116
- (en) Frisch M, Pedersen BV, Andersson RE, « Appendicitis, mesenteric lymphadenitis, and subsequent risk of ulcerative colitis: cohort studies in Sweden and Denmark » BMJ 2009;338:b716
- (en) Vidal A, Gómez-Gil E, Sans M et al. « Life events and inflammatory bowel disease relapse: a prospective study of patients enrolled in remission » Am J Gastroenterol. 2006;101:775-781
- (en) Diav-Citrin O., Park YH., Veerasuntharam G. et al. « The Safety of mesalamine in human pregnancy : a prospective controlled cohort study » Gastroenterology 1998; 114 : 23-8.
- (en) Klement E, Cohen RV, Boxman J, Joseph A, Reif S. « Breastfeeding and risk of inflammatory bowel disease: a systematic review with meta-analysis » Am J Clin Nutr. 2004;80:1342-1352
- (en) Heller F, Florian P, Bojarski C et al. « Interleukin-13 is the key effector Th2 cytokine in ulcerative colitis that affects epithelial tight junctions, apoptosis, and cell restitution » Gastroenterology 2005;129:550-564
- (en) Taurog JD, Richardson JA, Croft JT et al. « The germfree state prevents development of gut and joint inflammatory disease in HLA-B27 transgenic rats » J Exp Med. 1994;180:2359-2364
- (en) Frank DN, Robertson CE, Hamm CM et al. « Disease phenotype and genotype are associated with shifts in intestinal-associated microbiota in inflammatory bowel diseases » Inflamm Bowel Dis. 2011;17:179-184
- (en) Braegger CP, Nicholls S, Murch SH, Stephens S, MacDonald TT, « Tumour necrosis factor alpha in stool as a marker of intestinal inflammation » Lancet 1992;339:89-91
- (en) Masuda H, Iwai S, Tanaka T, Hayakawa S. « Expression of IL-8, TNF-alpha and IFN-gamma m-RNA in ulcerative colitis, particularly in patients with inactive phase » J Clin Lab Immunol. 1995;46:111-123
- (en) Eaden JA, Abrams KR, Mayberry JF. « The risk of colorectal cancer in ulcerative colitis: a meta-analysis » Gut 2001;48:526-535
- (en) Ekbom A, Helmick C, Zack M, Adami HO. « Ulcerative colitis and colorectal cancer. A population-based study » N Engl J Med. 1990;323:1228-33.
- (en) Velayos FS, Terdiman JP, Walsh JM. « Effect of 5-aminosalicylate use on colorectal cancer and dysplasia risk: a systematic review and metaanalysis of observational studies » Am J Gastroenterol. 2005;100:1345-53.
- (en) Beaugerie L, Seksik P, Bouvier AM et al. « Thiopurine therapy is associated with a three-fold decrease in the incidence of advanced colorectal neoplasia in IBD patients with longstanding extensive colitis: results from the CESAME Cohort » Gastroenterology 2009;136(5 suppl 1):A-54. Abstr 281
- (en) Jess T, Gamborg M, Munkholm P, Sørensen TI, « Overall and cause-specific mortality in ulcerative colitis: meta-analysis of population-based inception cohort studies » Am J Gastroenterol. 2007;102:609-17.
- Philippe Mesmer et Philippe Pons, « Le premier ministre japonais, Shinzo Abe, démissionne pour raisons de santé », Le Monde, (lire en ligne
 , consulté le ).
, consulté le ). - (it) Vera Martinella, « Il cantante degli Imagine Dragons: «Ho mal di schiena atroci, soffro di spondilite» », sur Corriere della Sera, (consulté le )
- « Aaron Swartz : sur les traces d’une étoile filante du Net », sur http://www.telerama.fr/, (consulté le ).
- (en) Travis SP, Stange EF, Lémann M et al. for the European Crohn's and Colitis Organisation (ECCO) « European evidence-based Consensus on the management of ulcerative colitis: Current management » J Crohn's Colitis 2008;2:24-62.
- (en) Marshall JK, Irvine EJ, « Rectal corticosteroids versus alternative treatments in ulcerative colitis: a meta-analysis » Gut 1997;40:775-81.
- (en) Marteau P, Probert CS, Lindgren S et al. « Combined oral and enema treatment with Pentasa (mesalazine) is superior to oral therapy alone in patients with extensive mild/moderate active ulcerative colitis: a randomised, double blind, placebo controlled study » Gut 2005;54:960-5.
- (en) Faubion WA, Loftus EV, Harmsen WS, Zinsmeister AR, Sandborn WJ, « The natural history of corticosteroid therapy for inflammatory bowel disease: a population-based study » Gastroenterology 2001;121:255-60.
- (en) Ardizzone S, Maconi G, Russo A, Imbesi V, Colombo E, Bianchi Porro G. « Randomised controlled trial of azathioprine and 5-aminosalicylic acid for treatment of steroid dependent ulcerative colitis » Gut 2006;55:47-53
- (en) Leung Y, Panaccione R, Hemmelgarn B, Jones J. « Exposing the weaknesses: a systematic review of azathioprine efficacy in ulcerative colitis » Dig Dis Sci. 2008;53:1455-61.
- (en) Lichtiger S, Present DH, Kornbluth A. et al. « Cyclosporine in severe ulcerative colitis refractory to steroid therapy » N Engl J Med. 1994;330:1841-1845
- (en) Rutgeerts P, Sandborn WJ, Feagan BG et al. « Infliximab for induction and maintenance therapy for ulcerative colitis » N Engl J Med. 2005;353:2462-76.
- (en) Reinisch W, Sandborn WJ, Hommes DW. et al. « Adalimumab for induction of clinical remission in moderately to severely active ulcerative colitis: results of a randomised controlled trial » Gut 2011;60:780-7.
- (en) « Gilead and Galapagos Announce Positive Topline Results of Phase 2b/3 Trial of Filgotinib in Moderately to Severely Active Ulcerative Colitis » http://investors.gilead.com/news-releases/news-release-details/gilead-and-galapagos-announce-positive-topline-results-phase-2b3
- (en) « OSE Immunotherapeutics and Servier Amend the Global Licensing Option Agreement for IL-7R Antagonist OSE-127 in Autoimmune Diseases », GlobeNewswire, (lire en ligne, consulté le ).
- (en) Turner D, Walsh CM, Steinhart AH, Griffiths AM. « Response to corticosteroids in severe ulcerative colitis: a systematic review of the literature and a meta-regression » Clin Gastroenterol Hepatol. 2007;5:103-10.
- (en) Kruis W, Jonaitis L, Pokrotnieks J et al. the International Salofalk OD Study Group. « Randomised clinical trial: a comparative dose-finding study of three arms of dual release mesalazine for maintaining remission in ulcerative colitis » Aliment Pharmacol Ther. 2011;33:313-22.
- (en) Gisbert JP, Linares PM, McNicholl AG, Maté J, Gomollón F. « Meta-analysis: the efficacy of azathioprine and mercaptopurine in ulcerative colitis » Aliment Pharmacol Ther. 2009;30:126-37.
- (en) Sang LX, Chang B, Zhang WL, Wu XM, Li XH, Jiang M. « Remission induction and maintenance effect of probiotics on ulcerative colitis: a meta-analysis » World J Gastroenterol. 2010;16:1908-15.
- (en) Obih C, Wahbeh G, Lee D, Braly K, Giefer M, Shaffer ML, Nielson H, Suskind DL. « Specific carbohydrate diet for pediatric inflammatory bowel disease in clinical practice within an academic IBD center. » Nutrition 2016;32(4):418-25. DOI 10.1016/j.nut.2015.08.025.
- (en) Mothana RA, « Anti-inflammatory, antinociceptive and antioxidant activities of the endemic Soqotraen Boswellia elongata Balf. f. and Jatropha unicostata Balf. f. in different experimental models », Food Chem Toxicol, vol. 49, no 10, , p. 2594-9. (PMID 21777643, DOI 10.1016/j.fct.2011.06.079)
- I. Gupta, A. Parihar, P. Malhotra et G. B. Singh, « Effects of Boswellia serrata gum resin in patients with ulcerative colitis », European Journal of Medical Research, vol. 2, no 1, , p. 37–43 (ISSN 0949-2321, PMID 9049593, lire en ligne, consulté le )
- Shuangyuan Hu, Pengfei Wei, Wei Li et Qingsong Liu, « Pharmacological effects of berberine on models of ulcerative colitis: A meta-analysis and systematic review of animal studies », Frontiers in Pharmacology, vol. 13, , p. 937029 (ISSN 1663-9812, PMID 36147325, PMCID 9486070, DOI 10.3389/fphar.2022.937029, lire en ligne, consulté le )
- Yu Hu, Zhen Ye, Yingqi She et Linzhen Li, « Efficacy and Safety of Probiotics Combined With Traditional Chinese Medicine for Ulcerative Colitis: A Systematic Review and Meta-Analysis », Frontiers in Pharmacology, vol. 13, , p. 844961 (ISSN 1663-9812, PMID 35321324, PMCID 8936956, DOI 10.3389/fphar.2022.844961, lire en ligne, consulté le )
- Takahiro Kudo, Keisuke Jimbo, Hirotaka Shimizu et Itaru Iwama, « Qing-Dai for pediatric ulcerative colitis multicenter survey and systematic review », Pediatrics International: Official Journal of the Japan Pediatric Society, vol. 64, no 1, , e15113 (ISSN 1442-200X, PMID 35831249, DOI 10.1111/ped.15113, lire en ligne, consulté le )
- Fatemeh Vazirian, Sara Samadi, Mohammadreza Abbaspour et Amirmahdi Taleb, « Evaluation of the efficacy of Thymus kotschyanus extract as an additive treatment in patients with ulcerative colitis: a randomized double-blind placebo-controlled trial », Inflammopharmacology, vol. 30, no 6, , p. 2145–2152 (ISSN 1568-5608, PMID 35723850, DOI 10.1007/s10787-022-00991-3, lire en ligne, consulté le )
- Marcel Vetter et Markus F. Neurath, « Emerging oral targeted therapies in inflammatory bowel diseases: opportunities and challenges », Therapeutic Advances in Gastroenterology, vol. 10, no 10, , p. 773–790 (ISSN 1756-283X, PMID 29051788, PMCID 5638182, DOI 10.1177/1756283X17727388, lire en ligne, consulté le )
- (en) Borody T, Warren E, Leis S, Surace R, Ashman O, « Treatment of ulcerative colitis using fecal bacteriotherapy », J Clin Gastroenterol, vol. 37, no 1, , p. 42–7 (PMID 12811208, DOI 10.1097/00004836-200307000-00012) PDF
- (en) Borody T, Warren E, Leis S, Surace R, Ashman O, Siarakas S, « Bacteriotherapy using fecal flora: toying with human motions », J Clin Gastroenterol, vol. 38, no 6, , p. 475–83. (PMID 15220681, DOI 10.1097/01.mcg.0000128988.13808.dc, lire en ligne [PDF])
- Taobi Huang, Jinlan Xu, Maoying Wang et Ke Pu, « An updated systematic review and meta-analysis of fecal microbiota transplantation for the treatment of ulcerative colitis », Medicine, vol. 101, no 30, , e29790 (ISSN 0025-7974, PMID 35905229, PMCID 9333500, DOI 10.1097/MD.0000000000029790, lire en ligne, consulté le )
- (en) Michael S. Silverman, Ian Davis, Dylan R. Pillai « Success of Self-Administered Home Fecal Transplantation for Chronic Clostridium difficile Infection » Clin Gastroenterol Hepatol. 2010;8(5):471-3. DOI 10.1016/j.cgh.2010.01.007
- « Arrêt de travail supérieur à 6 mois », sur www.ameli.fr (consulté le )
Voir aussi
Articles connexes
Liens externes
- Ressources relatives à la santé :
- Orphanet
- (en) Classification internationale des soins primaires
- (en) Diseases Ontology
- (en) DiseasesDB
- (en) Héritage mendélien chez l'humain
- (en) Héritage mendélien chez l'humain
- (en) Medical Subject Headings
- (en + es) MedlinePlus
- (en) NCI Thesaurus
- (en) PatientLikeMe
- (no + nn + nb) Store medisinske leksikon
- (cs + sk) WikiSkripta
- http://afa.asso.fr Association François-Aupetit (AFA) - Association nationale de malades pour vaincre la maladie de Crohn et la RCH, reconnue d’utilité publique depuis 1996
- Association CROHN-RCUH en Belgique
- Crohn et Colite Canada
- Association Suisse de la Maladie de Crohn et Colite ulcéreuse (ASMCC)
- (en) « National Association for Colitis and Crohn's disease (UK) »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?)
- (en) Crohn's and Colitis Foundation of America