Hydroperoxyde de tert-butyle
L'hydroperoxyde de tert-butyle est un hydroperoxyde de formule semi-développée (CH3)3C-OOH. Il est surtout utilisé comme source de radicaux pour des polymérisations et pour des réactions d'époxydation, en particulier pour l'époxydation de Sharpless.
| Hydroperoxyde de tert-butyle | |
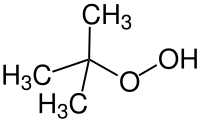
| |
| Identification | |
|---|---|
| Nom UICPA | peroxyde de 1,1-diméthyléthyle |
| Synonymes |
tert-butylhydroperoxyde |
| No CAS | |
| No ECHA | 100.000.833 |
| PubChem | 6410 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore avec une odeur âcre |
| Propriétés chimiques | |
| Formule | C4H10O2 [Isomères] |
| Masse molaire[1] | 90,121 ± 0,004 5 g/mol C 53,31 %, H 11,18 %, O 35,51 %, |
| pKa | 12,8 à 20 °C[2] |
| Propriétés physiques | |
| T° fusion | −8 °C[3] |
| T° ébullition | 75 °C (décomposition)[3] |
| Solubilité | 130-150 g·l-1 (eau, 20 °C)[3] |
| Masse volumique | 0,896 g·cm-3 à 20 °C[3] |
| Point d’éclair | 26 °C[3] |
| Thermochimie | |
| ΔfH0gaz | −234,9 kJ·mol-1[4] |
| ΔfH0liquide | −294 kJ·mol-1[4] |
| ΔvapH° | 46,568 kJ·mol-1 à −120,15 °C[4] |
| PCI | −2 710 kJ·mol-1[4] |
| Précautions | |
| NFPA 704[5] | |
| Directive 67/548/EEC[3] | |
 C  O  N |
|
| Transport[3] | |
| Écotoxicologie | |
| DL50 | 320 mg·kg-1 (souris, oral) 246 mg·kg-1 (souris, i.p.) 370 mg·kg-1 (rat, oral) 87 mg·kg-1 (rat, i.p.) 790 mg·kg-1 (rat, peau)[2] |
| CL50 | 500 ppm (rat, 4 heures) 350 ppm (souris, 4 heures)[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Synthèse
Plusieurs voies de synthèse sont possibles[6] :
- réaction du peroxyde d'hydrogène et de l'isobutylène ou du tert-butanol en présence d'acide sulfurique ;
- réaction entre le tert-butanol et l'acide peroxysulfurique. Cette dernière réaction est toutefois dangereuse car un intermédiaire explosif est produit ;
- auto-oxydation de l'isobutylène par l'oxygène.
Références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Hydroperoxyde de tert-butyle », sur ChemIDplus, consulté le 13 janvier 2010
- Entrée « tert-Butyl hydroperoxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 13 janvier 2010 (JavaScript nécessaire)
- (en) « tert-Butyl hydroperoxide », sur NIST/WebBook, consulté le 13 janvier 2010
- , CAMEO Chemicals
- (en) Jose Sanchez, Terry N. Myers, Peroxides and Peroxide Compounds, Organic Peroxides, Wiley-VCH Verlag GmbH & Co, coll. « Kirk‑Othmer Encyclopedia of Chemical Technology »,
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.

