Chlorure de (cyclooctadiène)rhodium dimérique
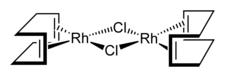
Le chlorure de (cyclooctadiène)rhodium dimérique, ou dimère de chlorure de (cyclooctadiène)rhodium, est un composé organométallique de formule chimique [(η4-C8H12)Rh(µ-Cl)]2, couramment abrégée [RhCl(COD)]2 ou Rh2Cl2(COD)2, où « COD » représente le ligand 1,5-cyclooctadiène C8H12. Il s'agit d'un solide jaune orangé stable à l'air et couramment employé comme précurseur de catalyseurs homogènes[4]. La molécule est un dimère dont les atomes de rhodium ont une géométrie plane carrée, typique pour un complexe de métal de transition ayant une configuration électronique en d8, tandis que le cœur Rh2Cl2 est quasiment plan[5], par opposition à la structure fortement déformée du chlorure de (cyclooctadiène)iridium dimérique [(η4-C8H12)Ir(µ-Cl)]2, dans lequel l'angle dièdre vaut 86°.
| Chlorure de (cyclooctadiène)rhodium dimérique | |
| |
| Structure du chlorure de (cyclooctadiène)rhodium dimérique | |
| Identification | |
|---|---|
| Synonymes |
dimère de chloro(1,5-cyclooctadiène)rhodium(I) |
| No CAS | |
| No ECHA | 100.031.949 |
| No CE | 235-157-6 |
| PubChem | 6436379 |
| SMILES | |
| InChI | |
| Apparence | solide de couleur ambrée[1] |
| Propriétés chimiques | |
| Formule | C16H24Cl2Rh2 |
| Masse molaire[2] | 493,079 ± 0,019 g/mol C 38,97 %, H 4,91 %, Cl 14,38 %, Rh 41,74 %, |
| Propriétés physiques | |
| T° fusion | 256 °C[1] |
| Solubilité | insoluble dans l'eau[1] |
| Précautions | |
| SGH[3] | |
  Attention |
|
| NFPA 704[1] | |
| Unités du SI et CNTP, sauf indication contraire. | |
Il peut être obtenu en chauffant une solution de chlorure de rhodium(III) trihydraté RhCl3·3H2O avec le 1,5-cyclooctadiène dans l'éthanol aqueux en présence de carbonate de sodium Na2CO3[4] - [6] :
- 2 RhCl3·3H2O + 2 C8H12 + 2 CH3CH2OH + 2 Na2CO3 ⟶ [(η4-C8H12)Rh(µ-Cl)]2 + 2 CH3CHO + 8 H2O + 2 CO2 + 4 NaCl.
Il est utilisé principalement comme source d'unités cationiques électrophiles « [Rh(COD)]+ » :
- [RhCl(COD)]2 + n L ⟶ [LnRh(COD)]+Cl− (où L = PR3, un alcène, etc. et n = 2 ou 3).
Il est ainsi possible de lier des phosphines chirales à l'atome de rhodium. Les complexes chiraux qui en résultent peuvent catalyser des hydrogénations asymétriques (en)[7]. Le chlorobis(cyclooctène)rhodium dimérique [(η2-C8H14)2Rh(µ-Cl)]2 est un complexe apparenté et encore plus réactif.
Le dimère réagit avec diverses bases de Lewis (L) pour former des adduits RhCl(L)(COD).
Notes et références
- « Fiche du composé Chloro(1,5-cyclooctadiene)rhodium(I) dimer », sur Alfa Aesar (consulté le ).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Chloro(1,5-cyclooctadiene)rhodium(I) dimer », sur https://pubchem.ncbi.nlm.nih.gov/, PubChem, (consulté le ).
- (en) G. Giordano, R. H. Crabtree, R. M. Heintz, D. Forster et D. E. Morris, « Di-μ-Chloro-Bis(η4-1,5-Cyclooctadiene)-Dirhodium(I) », Inorganic Syntheses: Reagents for Transition Metal Complex and Organometallic Syntheses, vol. 28, (DOI 10.1002/9780470132593.ch22, lire en ligne)
- (en) D. J. A. De Ridder et P. Imhoff, « Di-µ-chloro-bis[(cis,cis-η4-1,5-cyclooctadiene)rhodium(I)]: a redetermination », Acta Crystallographica Section C, vol. C50, , p. 1569-1572 (DOI 10.1107/S0108270194001459, lire en ligne)
- (en) J. Chatt & L. M. Venanzi, « Olefin Complexes of Rhodium », Nature, vol. 177, no 4514, , p. 852-853 (DOI 10.1038/177852b0, Bibcode 1956Natur.177..852C, S2CID 4296682, lire en ligne)
- (en) William S. Knowles, « Asymmetric Hydrogenations (Nobel Lecture 2001) », Advanced Synthesis & Catalysis, vol. 345, nos 1-2, , p. 3-13 (DOI 10.1002/adsc.200390028, lire en ligne)
