Allocation à la reproduction
En biologie, l’allocation à la reproduction, ou effort reproducteur, est une mesure de la proportion d’énergie allouée à la reproduction pour une période fixée.

Bien que la mesure précise de l'allocation à la reproduction soit difficile, chez les végétaux, la mesure directe de l’allocation la plus commune est la mesure de biomasse pour un organe spécifique, ou la masse dédiée à une fonction précise. Cela nécessite de poser les hypothèses que la répartition de la biomasse reflète l’allocation des ressources limitantes, et que les différentes fonctions utilisent les mêmes ressources limitantes[1].
D’un point de vue évolutif, une composante fondamentale de la vie d’un organisme ou d’un génotype est sa reproduction ou sa réplication, dans le but de contribuer aux générations futures par la transmission de ses gènes.
L'énergie totale que possède un organisme est distribuée en différentes catégories de dépenses d'énergie : les fonctions de survie, de croissance, de maintenance, de défense et la fonction de reproduction. Un individu dans son environnement est limité par la disponibilité des ressources, et donc par l’énergie allouable à ces différentes fonctions, d'où sa stratégie de reproduction afin de maximiser la fitness (ou valeur sélective).
Il existe donc un compromis évolutif (trade-off dans la littérature scientifique) d’allocation des ressources entre les différents traits d'histoire de vie. L’expression d’un trait étant coûteuse, toute énergie allouée à un trait n’est plus disponible pour l’expression d’un autre.
Dans la théorie des histoires de vie, les investissements reproducteurs peuvent être compris en termes de compromis pour l'allocation de ressources entre la reproduction et l'investissement parental.
Généralités
Stratégie d’histoire de vie
C'est une réponse adaptative à la sélection par l’environnement.
Il existe une très grande variété de stratégies reproductives observées dans la nature. Celles-ci reposent sur une diversité de stratégies d’allocation à la reproduction. Or, la diversité des stratégies observées reflètent la diversité des pressions de sélection.
La théorie des stratégies reproductive, qui tente d’expliquer cette diversité, a été mise en forme à partir des années 1960 par une série de travaux, comme ceux de R. H. MacArthur et E. O. Wilson, G. C. Williams[2], ou encore Eric Pianka[3] (et beaucoup d’autres).
Cette théorie repose sur le postulat suivant :
En jouant sur les différentes possibilités de succès reproducteurs, la sélection naturelle aurait « façonné » les stratégies reproductives (et donc d’allocation à la reproduction), de telle façon à ce que chacune correspondent à un optimum local maximisant la valeur sélective d’un individu (ou d’un génotype) dans un environnement particulier.
Cette théorie suit le modèle historique d’optimisation qui consiste à maximiser les bénéfices apportés en matière de valeur sélective par un trait d’histoire de vie donné, par rapport aux coûts que celui-ci engendre. Il s’agit donc d’analyser l’optimisation des stratégies d’allocation qui maximisent la valeur reproductive d’un individu, et donc l’espérance du nombre de descendants à la naissance.
La théorie stipule que l’habitat (i.e. l’environnement biotique et abiotique) dans lequel évoluent les organismes sélectionne, le long de la gamme des combinaisons physiologiquement possibles, la stratégie reproductive optimale.
On peut alors se demander quel facteur environnemental détermine :
- la quantité à investir dans un acte de reproduction donné (1)
- la quantité à allouer à un chaque descendant (2)
- quand (à quel âge) se reproduire (3)
L’interaction entre les réponses adaptatives (1) et (2) va déterminer la taille de portée ou de ponte, ou plus généralement le nombre de descendants produits par épisode de reproduction.
Ronald Fisher[4] fut le premier à poser le problème :
« Il serait intéressant de savoir, non pas seulement par quels mécanismes physiologiques est déterminée la répartition entre les nutriments à allouer aux gonades et ceux à allouer à l’organisme parental, mais également quelles circonstances dans l’histoire de vie et l’environnement rendrait profitable la tendance à allouer une part plus ou moins importante de ressources disponibles à la reproduction. (R. Fisher, 1930). »
Valeur reproductive
La valeur reproductive (en) (VR)[2] est l’espérance à chaque âge, de production actuelle et future de descendants. Elle prend en compte la contribution d’un individu à la génération suivante, relativement à la contribution des autres individus. C’est la somme de la reproduction courante (= accomplie) et de la valeur reproductive résiduelle (=future) VRR.
- VR = reproduction actuelle + Valeur Reproductive Résiduelle (VRR) = ce qui a déjà été accompli + ce qu’il reste à accomplir (en matière de reproduction)
Williams[5]décrit la Valeur Reproductive Résiduelle (VRR) comme l’espérance de reproduction future, c’est-à-dire la somme des reproductions (fécondités) à chaque âge futur, conditionnellement à la survie jusqu’à cet âge, et relativement à l’accroissement de la population.
L'histoire de vie favorisée par la sélection naturelle sera celle pour laquelle la VR est la plus élevée. Un individu jeune a une VRR très grande, car la majeure partie de sa fitness reste à accomplir. Sa contribution future pour l’accroissement de la population reste donc à faire. Plus l’individu vieillit, plus sa VRR diminue, et sa reproduction accomplie augmente. Cela signifie qu’il a déjà accompli une grande partie de sa fitness, et qu’il lui en reste peu à accomplir. Ainsi, au cours de la vie de l’individu, la reproduction actuelle augmente et la VRR diminue. Il existe donc un trade-off entre l’allocation à la reproduction courante et l’allocation à la reproduction future.
La VR va donc changer en fonction de l’âge des individus, avec la reproduction accomplie et la VRR. Les VR aux différents âges sont intimement liées. En effet, maximiser sa VR à un âge contraint les valeurs aux âges futurs. Elle est faible pour les jeunes individus qui ont une faible probabilité de survivre jusqu’à l’âge de la maturité sexuelle. Pour ceux qui survivent, elle augmente de façon constante à mesure que l’âge de la première reproduction approche, et qu’il est de plus en plus certain que les individus vont atteindre l’âge de se reproduire. La VR diminue chez les individus sénescents, et leur survie devient plus faible.
Effort reproducteur
L'investissement reproducteur, s’il est trop important dans une saison de reproduction donnée, augmente la proportion de gènes transmit à la descendance à cet âge, mais réduit les probabilités de reproduction future, par exemple en entraînant un affaiblissement prononcé de l’animal pouvant aller jusqu’à la mort[6].
Les conditions qui conduisent vers un fort effort reproducteur :
- Forte mortalité extrinsèques des adultes
- Survie constante des descendants
- Environnement variable mais prédictible, avec hausse de l’effort reproducteur dans les années favorables à la survie des jeunes.
Les conditions qui conduisent vers un faible effort reproducteur :
- Environnement imprédictible pour la survie des jeunes
- Environnement variable mais prédictible, avec baisse de l’effort reproducteur dans les années défavorables à la survie des jeunes.
Les espèces sémelpares devraient avoir un effort reproducteur plus fort que les espèces itéropares.
Optimisation de l'effort reproducteur
Modèle d'optimisation
Considérant F, la fécondité, comme fonction de l'effort reproducteur, on s'attend à voir F augmenter si l'effort reproducteur, θ, augmente. La fonction F(θ), est de forme convexe si la survie de jeunes (sJ) décroit avec le nombre de jeunes produits (favorise les soins aux jeunes). Elle est de forme concave si cette survie augmente avec la fécondité (favorise la thermorégulation, la sursaturation pour les prédateurs…)[7].
La survie des adultes (sA) est aussi fonction de l'effort reproducteur, sA(θ). Cette fonction est décroissante, la survie des adultes décroit quand l'effort reproducteur augmente.
Ces deux fonctions peuvent être superposées (schéma). On voit donc clairement que :
- soit la survie est favorisé, l'effort reproducteur θ est alors petit
- soit la fécondité est favorisé, l'effort reproducteur θ est grand.
Quelle est donc la valeur optimale de θ ? Quel est le meilleur compromis entre survie et reproduction ?
L'optimum de θ est le génotype qui maximise la fitness λ. Dans ce cas simple on additionne simplement F(θ) et sA(θ), on obtient ainsi la courbe λ(θ).
En sachant déterminer l'effort reproducteur optimum, on peut déterminer l'effet de changement sur les taux de survie aux différents stades de vie. Les changements de taux de survie adultes et jeunes changent les optimums mais dans des sens différents. Si sJ est faible et sA fort, alors il n'y aura pas beaucoup de jeunes, car ils ont une forte probabilité de mourir, mais de l’énergie pourra être gardée pour les futures reproduction, car le taux de survie de l'adulte est fort ; au contraire, si sJ est fort et sA faible, alors il est préférable pour l'adulte de faire beaucoup de jeunes, car il a peu de chance de pouvoir en refaire et ces jeunes ont une forte chance de survivre. C'est alors le ratio sJ/sA qui est important et qui prédit l'effort reproducteur optimum, le maximum de ce ratio étant le θ optimum.
Un rapport sJ/sA élevé correspond à de l'itéroparité (plusieurs reproductions par individu) alors qu'un sJ/sA faible suggère de la sémelparité (une seule reproduction).
Malgré tout, le nombre de jeunes observés est en général plus faible que celui attendu par le calcul de l'optimum. Cela peut être dû au fait que tous les génotypes possibles ne sont pas présents dans la nature : il peut donc être impossible pour une espèce d'atteindre l'optimum prédit.
La variabilité temporelle peut aussi expliquer le fait que le nombre de descendants soit inférieur à celui attendu. Introduire un paramètre de variabilité temporelle, e, dans la survie juvénile conduit à un optimum de l'effort reproducteur plus faible.
Considérons 2 types d'années :
- Bonne année : sJg = sJ + e
- Mauvaise année : sJb = sJ – e
Si les deux types d'années ont la même fréquence, après deux années l'accroissement de la population sera :
λg λb = [B (sJ + e) sA] [B (sJ – e) sA] = sJ²B² + 2sABsJ + sA² -B²e²
Le résultat obtenu abaisse l'optimum au cause d'un paramètre négatif supplémentaire (dans l'exemple:-B²e²), paramètre présent alors que la variabilité moyenne (e-e)/2 = 0 est nulle.
Optimisation des Stratégies d'acquisition des ressources
En 1976, Eric Pianka[3] met en relation la théorie de stratégies reproductives avec la théorie des stratégies d’acquisition optimale des ressources. Cette dernière stipule que la sélection naturelle optimise l’énergie assimilée par unité de temps.
L’analyse du budget en temps et en énergie d’un individu permet d’évaluer l’influence de l’acquisition des ressources sur l’allocation à la reproduction et vice-versa.
Les organismes sont limités en matière de temps disponible pour les activités d’approvisionnement et de reproduction. Le budget total de temps va être déterminé en fonction du rythme d’activité et de la capacité à « économiser » du temps en réalisant plusieurs activités simultanées. Par exemple, les lézards mâles, en s’élevant sur un perchoir, surveillent la venue de prédateurs et de proies potentiels, tout en surveillant leurs partenaires femelles, empêchant ainsi la venue de mâles compétiteurs.
Le temps passé à acquérir des ressources apporte un gain de matière et d’énergie, mais peut également avoir un coût énergétique. Ce coût dépend de la disponibilité et de l’accessibilité des ressources. Une période de temps allouée est donc profitable en matière d’approvisionnement si les gains en matière et en énergie excèdent les pertes inévitables dues aux coûts énergétiques de l’approvisionnement. Une augmentation du temps voué à l’approvisionnement augmente l’assimilation de matière et d’énergie de l’individu, et donc entraine un gain de fitness en termes de matière et d’énergie que l’organisme va pouvoir allouer à ses différentes fonctions. La sélection naturelle devrait donc agir dans le sens d’une maximisation des quantités de matière et d’énergie par unité de temps, et donc du temps consacré à l’approvisionnement.
Cependant, cela implique une réduction du temps « disponible » pour toutes les activités de reproduction. Ces gains d’énergie correspondent donc à une perte de temps disponible pour la reproduction. Si on considère les critères de reproduction, les mécanismes évolutifs devraient favoriser une plus grande allocation de temps et d’énergie à la reproduction.
Il y a donc un trade-off entre l’acquisition des ressources par unité de temps et l’effort reproducteur. La budgétisation optimale de temps et d’énergie entre les activités d’approvisionnement et de reproduction dépend donc de la façon dont va varier le bénéfice énergétique apporté par l’approvisionnement, par rapport au coût énergétique résultant de la reproduction.
Ceci dépend des conditions de l’environnement. Ainsi, pour des conditions favorables à l’approvisionnement (grande disponibilité des ressources, faible abondance de prédateurs…), l'optimum devrait tendre vers un approvisionnement accru au détriment des autres activités. Inversement, des conditions défavorables, dues à une forte abondance de prédateurs ou à des conditions physico-chimiques défavorables, devraient sélectionner un temps d’approvisionnement plus faible, et donc une allocation plus importante à la reproduction. Les mécanismes évolutifs vont donc sélectionner une interaction optimale entre des stratégies d’allocation à la reproduction et des stratégies d’acquisition des ressources de façon à maximiser la valeur sélective de l'individu.
Variation de l'Effort reproducteur optimal en fonction de l'habitat
La théorie démographique des stratégies reproductives, postulée pour la première fois par Williams[2] en 1966 stipule que l’allocation en temps et en énergie à la reproduction se fait aux dépens de la survie et la croissance, et donc de l’espérance d’une reproduction future, en raison d’un investissement somatique réduit. La théorie est donc basée sur l’idée qu’il existe un trade-off entre l’effort reproducteur actuel et l'espérance de reproduction future. Cette hypothèse se résume en trois postulats :
- Une augmentation de l’effort reproducteur induit inévitablement une augmentation de la reproduction courante (donc du succès reproducteur à un âge donné) et une réduction de l’investissement somatique.
- Si la reproduction se fait aux dépens de l’investissement somatique, le coût « somatique » réduit la probabilité de survie jusqu’à la période de reproduction suivante et /ou réduit l’énergie disponible pour une reproduction future (coûts sur la fécondité).
- Si la reproduction entraine un coût sur la survie et la fécondité, l’effort reproducteur varie inversement avec la valeur reproductive résiduelle.
De ce fait, la sélection naturelle optimiserait les stratégies reproductives à chaque âge, pour maximiser la valeur reproductive des individus, en jouant sur l’effort reproducteur courant au regard de l’espérance de reproduction future. L’optimisation se fait en maximisant le bénéfice accordé par l’allocation à un acte reproducteur présent et réussi, et en minimisant le coût engendré sur la reproduction future. Ceci dépend de la probabilité de survivre et de se reproduire à chaque âge dans un environnement donné. Cette probabilité repose notamment sur la disponibilité des ressources dans le milieu, de la variabilité et prévisibilité de l’environnement, ainsi que de la présence potentielle de prédateurs ou de parasites.
Il existe une corrélation positive entre l’âge d’un individu et sa taille corporelle : il est toujours payant de continuer à allouer de l’énergie dans sa croissance plutôt qu’à sa reproduction, si la fertilité potentielle augmente avec la taille. Une taille corporelle importante apporte une meilleure compétitivité, une plus faible vulnérabilité, et une quantité plus importante de réserves énergétiques allouables à la reproduction et donc un succès reproducteur plus important.
La classification de Levins[8] (1968) classe les habitats selon deux types :
Habitat à fort Coût de Reproduction
- Habitat plutôt stable
- Habitat dans lequel la fitness est très sensible à la taille des individus. C’est donc un habitat où il y a une forte compétition entre les individus. Dans ce cas seuls les meilleurs compétiteurs survivent et se reproduisent.
- une augmentation de la reproduction actuelle induirait une croissance réduite, donc une aptitude compétitive future réduite, une survie réduite et donc une Valeur Reproductive Résiduelle réduite.
- Inversement, une reproduction réduite permet une croissance accrue et donc un évitement des causes de mortalité (ex : prédation…). En effet les individus de petites tailles ont une faible compétitivité, et sont sujets à une plus forte mortalité due à la prédation.
Habitat à faible Coût de Reproduction
- Habitat plutôt instable
- Habitat dans lequel la fitness est insensible à la taille des individus, la mortalité étant inévitable et indiscriminée. Toute diminution de la reproduction induisant un accroissement de la taille est susceptible d'être inutile à l'avenir.
- Absence de concurrence
- Mortalité préférentielle des plus grands individus (prédation sélective). Donc diminuer la reproduction en faveur de la croissance, peut accroitre le risque de prédation et donc diminuer la survie future (en effet une plus grosse proie peut être plus attrayante pour un prédateur car elle apporte plus d’énergie).
Dans les habitats à fort coût de reproduction, les pressions de sélection constituées par les conditions du milieu vont faire tendre l’optimum vers un investissement reproducteur plus faible que l’investissement somatique, et vont donc maximiser la valeur reproductive au détriment de l’effort reproducteur. Tandis que dans les habitats à faible coût de reproduction, l’optimum tend vers un investissement reproducteur plus important que l’investissement somatique. Il y aura alors maximisation de l’effort reproducteur par rapport à la valeur reproductive résiduelle.
Bien sur, il existe tout un continuum d'habitats allant de faible à fort coût de reproduction, le long duquel l'effort reproducteur sera plus ou moins important en fonction des conditions présentes dans l'habitat.
Sémelparité et Itéroparité
L’interaction des histoires de vie avec l’environnement dans lequel évoluent les individus, ainsi que l’existence d’un trade-off entre l’effort reproducteur courant et l’allocation à la reproduction future, sont à l’origine de l’existence des stratégies de reproduction itéropare et sémelpare.
.
En matière d’allocation d’énergie à la reproduction, la sémelparité est associée à un investissement reproducteur maximal pour un seul et unique acte de reproduction. Ceci se fait au détriment de l’investissement somatique, et donc de la survie. C’est une stratégie d’allocation de « tout-ou-rien ». La stratégie sémelpare maximise la fécondité courante. Il en résulte une espérance de reproduction future de zéro.
L’itéroparité est associé quant à elle à une allocation répétée au cours de la vie d’un individu, et donc à plusieurs efforts reproducteurs âge-spécifiques. Ne pas se reproduire à un âge donné maximise la valeur reproductive résiduelle, et donc le succès reproducteur futur. Cela mène à une fécondité courante de zéro.
L’itéroparité et la sémelparité sont donc étroitement liées à des stratégies d’allocation différentes. Ces deux stratégies vont être sélectionnées individuellement en réponses aux conditions de l’habitat dans lequel vivent les organismes tout en cherchant à maximiser les bénéfices en matière de valeur reproductive par rapport aux coûts.
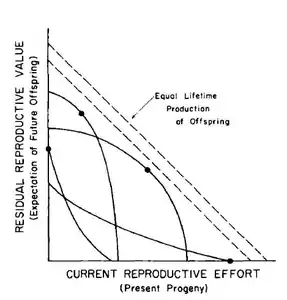
Le trade-off entre la reproduction courante et l’espérance d’une reproduction future à un âge donné, peut être représenté graphiquement en représentant la valeur reproductive résiduelle en fonction de l’effort reproducteur courant à un instant (ou un âge) donné[3]. Les formes hypothétiques du trade-off représentent les différentes possibilités avec lesquelles varient les bénéfices en matière de reproduction future par rapport aux coûts sur la reproduction courante (et vice versa). En tout point de cette relation, la seule façon d’augmenter la valeur reproductive résiduelle est de diminuer l’effort reproducteur courant, et vice versa.
Les points sur les courbes représentent les optimums pour un âge donné, c’est-à-dire les stratégies reproductives sélectionnées par l’environnement pour lesquelles la valeur reproductive est maximale. Les courbes concaves correspondent à une évolution vers une stratégie d’allocation « tout-ou-rien » sémelpare : l’effort reproducteur sélectionné est soit nul, soit maximal. Les courbes convexes correspondent à l’évolution vers une stratégie itéropare : l’effort reproducteur sélectionné est à un niveau intermédiaire à l’âge considéré.
On peut alors réitérer l’optimisation de la valeur reproductive à chaque âge au cours de la vie d’un individu et modéliser la stratégie d’allocation sélectionnée dans un environnement donné. La courbe noire reliant tous les points d’optimums représente la stratégie optimale qui maximise l’espérance de reproduction totale durant la vie d’un individu.
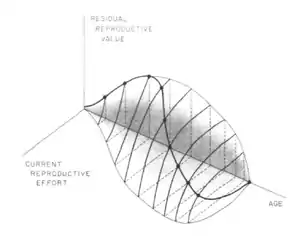
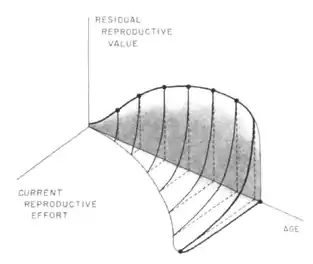
La forme de la surface à trois dimensions reflète les conditions environnementales immédiates et la stratégie courante de l’organisme. En effet, les contraintes physiologiques et environnementales influencent la forme du trade-off. Ainsi, divers facteurs comme la disponibilité des ressources, l’abondance des prédateurs, ainsi que les conditions abiotiques, interagissent à chaque instant avec les contraintes physiologiques de l’individu pour déterminer la forme de la surface.
Des conditions favorables pour une reproduction immédiate augmentent le coût sur l’investissement somatique, et donc augmente l’effort reproducteur. Il en est de même pour des conditions défavorables pour la survie. Inversement, les mauvaises conditions pour une reproduction immédiate ou/et des conditions favorable à la survie vont engendrer un effort reproducteur plus faible.
Exemple : Dans un habitat de faible densité, la fitness des végétaux coloniaux dépendrait de la fécondité, alors que dans un habitat de forte densité, une forte fécondité peut compromettre la capacité compétitive du végétal à survivre. Pour des raisons similaires, les végétaux qui se reproduisent une fois par an (annuelle ou monocarpique pérenne) devraient avoir une allocation à la reproduction plus élevée que les végétaux qui se reproduisent plusieurs fois (itéropare pérenne) car ils maximisent leur reproduction actuelle en sacrifiant la reproduction future (à l'exception de certaines espèces)[1].
Plasticité
L’histoire de vie n’est pas une propriété fixe qu’un organisme présente quelles que soient les conditions environnementales. Elle est le résultat de forces évolutives à long terme, mais aussi une réponse plus immédiate de l’organisme à son environnement. La possibilité d’un génotype à s’exprimer différemment selon l’environnement est appelée plasticité phénotypique[5]. Un organisme, grâce à la plasticité, peut allouer différemment son énergie (dans la gamme des possibles de l'espèce) selon son environnement afin de maximiser sa fitness.

Prenons pour exemple les faucons crécerelles. Il a été montré que les faucons étaient capables de moduler leur taille et date de ponte en fonction de la qualité de leur territoire[5]. Les différences observées pour différents niveaux de qualité d'un territoire ne sont pas génétiques, mais sont dues à de la plasticité phénotypique.
La combinaison optimale est celle qui maximise la VR totale (valeur de la ponte actuelle + VRR des parents). La valeur de la ponte actuelle augmente avec la taille de la ponte, et la valeur de chaque œuf varie avec la date de ponte. La VRR diminue donc avec l’effort parental (nombre d’heures par jour à chasser pour augmenter la ponte), et l’effort parental diminue avec l’augmentation de la qualité du territoire (nombre de proies attrapées par heure de chasse).
La VRR est donc plus faible avec :
- une plus grande ponte ;
- à des moments particuliers, les moins productifs de l'année ;
- dans les territoires de faibles qualités.
Chaque individu s’approche donc de son optimum en matière de taille et date de ponte selon l’environnement, le territoire, dans lequel il se trouve. On parle de plasticité car il n’y a pas une date de ponte unique, mais une gamme de possibilité selon l’habitat. La plasticité permet donc de répondre différemment à la variabilité de l’habitat.
Stratégies r et K
La variabilité environnementale joue beaucoup sur les taux de survie :
- Un environnement instable (grande variabilité) entraîne un taux de survie faible, les pressions de sélection vont alors favoriser les individus qui se reproduisent tôt et donc une reproduction précoce, et ainsi les cycles de vie courts : ces organismes sont sélectionnés par Sélection r.
- Un environnement stable (faible variabilité) va avoir comme conséquence des taux de survie plutôt élevé et stables. la compétition dans cet environnement étant très forte, les organismes les plus compétitifs seront sélectionnés. Il y aura donc une pression sur l'allocation à la survie (croissance et maintien des structures de l'organisme) et donc une reproduction plus tardive. Les organismes à cycle de vie long seront ainsi sélectionnés par Sélection K.
De telles évolutions sont visibles lorsqu'il y a une forte pression de sélection. C'est notamment le cas avec les pressions anthropiques, comme les pêcheries : sous la forte pression de sélection dû à la pêche, les poissons tendent à avoir un taux de croissance réduit, mais aussi à se reproduire de plus en plus tôt (étant donné que les taux de survie diminuent)[9].
Évolution du soin parental

L’investissement parental comprend la préparation des nids et terriers, l’approvisionnement en nourriture et la protection des œufs ainsi que des jeunes après leur naissance[10].
Les modèles de soin parentaux sont très variables dans la nature. Le soin parental aurait évolué plusieurs fois de façon répétitive ; par exemple chez les poissons à nageoires rayonnées, les analyses phylogéniques suggèrent que l’émergence indépendante du soin parental s’est produit 33 fois[11].
La diversité des stratégies de soins parentaux chez différentes espèces est surprenante, allant d’un soin minimal (exemple de la garde accidentelle d’œufs ayant éclos dans leur territoire[12]) au cas extrême qui résulte en la mort du parent (exemple chez les araignées[13]). Encore plus frappante, cependant, est la diversité dans le fait que le soin au jeune est dispensé ou non. En effet, il y a une variation remarquable dans la présence ou l’absence du soin parental au sein et entre les hauts groupes taxonomique.
De façon générale, le soin parental serait un trait dérivé acquis lorsque le bénéfice du soin dépasse son coût pour une meilleure fitness. Ainsi, le soin est certainement favorisé et donc sélectionné, lorsque :
- Le bénéfice relatif du soin est grand. Wilson[14] a suggéré que cela se produit dans des environnements avec une ressource en énergie limitée (et/ou une forte prédation).
- Le coût du soin est relativement bas (exemple : le soin constitue un critère de sélection sexuelle[15] - [16]).
Plusieurs études et observations sur les soins parentaux ont été menées, mais il n’y a cependant aucun modèle général expliquant l’évolution de ce comportement.
Taille et nombre de descendants
Chez les animaux avec un soin parental, on s’attend à un trade-off entre le nombre de jeunes et la survie des jeunes pris en charge. Ainsi, lorsque la survie des juvéniles baisse, l’optimum de taille de ponte baisse également. Basé sur ce trade-off, une taille de ponte intermédiaire est souvent la plus productive en termes de succès reproducteur. Aussi, plus le trade-off est important, plus l’optimum de taille de ponte est grand[7].
Price[17] résume 53 expériences d’additions d'œufs. Il a trouvé que dans 28 des 53, la survie de nidation était plus faible dans une couvée expérimentalement agrandie et dans aucun cas n'était meilleure.
Sélection naturelle (composante génétique)
Selon David Lack[18], la sélection naturelle devrait favoriser les génotypes ayant le plus grand succès reproductif. Pour émettre cet argument sur l'évolution, il est supposé que l'expression phénotypique des différentes tailles de ponte au sein d'une espèce a une composante génétique telle que les différences de tailles de ponte sont héritables. Deuxièmement, le trade-off entre la taille de ponte et la survie des juvéniles est le reflet des différences entre les génotypes et non simplement dû à une variabilité phénotypique ou environnementale. Généralement, les oiseaux qui pondent plus d'œufs que la moyenne une année, tendent également à pondre plus les années suivantes[19]. De plus, une sélection artificielle chez les poulets a conduit à une augmentation significative dans le taux de pontes[20]. Ainsi il semblerait y avoir un composant héritable pour la taille de ponte chez beaucoup d'oiseaux.
Environnement, pression des prédateurs
- Climat
Plusieurs familles d'oiseaux montrent une énorme variation dans la taille de ponte. Au sein d'espèces très apparentées, les espèces de plus basse latitude ont généralement une ponte plus petite[21]. Dans certaines espèces avec une large couverture géographique, comme le Rouge-gorge familier, cette tendance est visible intraspécifiquement. Si les conditions de milieu varient, il se produit une réduction de la nichée (en) par l'élimination du poussin en moins bonne santé (généralement le plus jeune).
Dans les communautés tropicales, qui ont une grande variété de nids et de prédateurs mangeant les œufs, des études démographique montrent généralement un plus grand taux de prédation des nids[22]. Ceci va favoriser l'évolution vers de plus petites pontes.

- Habitat, forme du nid
Les oiseaux faisant leurs nids dans des trous (comme le Pic vert, le Merlebleu, les passereaux et certains perroquets) ont une plus grande ponte que les oiseaux au nid ouvert. Encore une fois, cette observation est cohérente puisque les jeunes de ces nids à trou souffrent généralement moins de la prédation que les oiseaux avec des nids plus exposés. Cela va donc favoriser une taille de ponte plus grande. Aussi, avec cet ajout de protection, les oiseaux à nid de trou prolongent la durée de la nidation[7].
- Île vs continent
Les espèces vivant dans une île ont souvent une ponte inférieure aux espèces apparentées (ou à la même espèce) se trouvant sur le continent. Cette observation est valable principalement pour les comparaisons îles-continent en zone tempérée[21]. Les îles manquent généralement de nombreux prédateurs - en conséquence, vu le modèle de succès reproductif durant une année, on aurait attendu le contraire, c'est-à-dire plus de ponte associée à une faible mortalité des juvéniles attendue sur les îles.
Différences d’investissement entre mâles et femelles
Dans certaines espèces seules les femelles fournissent un soin parental (surtout chez les mammifères), tandis que dans d’autres ce sont surtout les mâles (chez beaucoup de poissons), et parfois les deux sexes investissent équitablement (la plupart des oiseaux)[23]. Répartition du soin parental chez différents groupes :
- Invertébrés : Rare, mais lorsque cela se produit ce sont souvent les femelles seules[24] - [25].
- Poissons : Le ratio mâle seulement/Biparental/Femelle seulement est de 9/3/1[26].
- Amphibiens : Femelles seules et Mâles seuls tout aussi communs. Faible fréquence d’un soin biparental[27] - [28].
- Reptiles : Soit les femelles seules soit les deux parents[26].
- Oiseaux : Dans 90 % des espèces, il y a un soin biparental (dont 9 % avec une aide au soin d’apparentés), mais les femelles investissent souvent plus dans le soin. Dans les espèces restantes il y a un soin de la part des femelles seules, les mâles prodiguant seuls les soins étant plus rare[29] - [30].
- Mammifères : Soin des femelles dans toutes les espèces. Dans 95 % des espèces, les femelles fournissent seules le soin. Dans 5 % des cas les mâles aident aux soins. Dans aucun cas les mâles sont seuls à investir dans le soin[10].
Pourquoi les femelles investissent généralement plus que les mâles ? Ceci peut être retracé au dimorphisme gamétique où les petits gamètes (spermatozoïdes) sont en compétition pour les ressources de la femelle (ovocyte). David Queller[31] a montré qu’il y a deux raisons principales pour lesquels les femelles investissent plus.
- La première est qu’il y a une chance non négligeable que la femelle ait été fécondée par un autre mâle. Le mâle n’a donc pas intérêt à perdre du temps et de l’énergie, et donc réduire sa fitness, dans une portée qui pourrait contenir la progéniture d’autres mâles.
- La deuxième raison est que, même dans une espèce où un seul mâle peut féconder la femelle pour chaque portée, étant donné qu’il y a compétition entre les mâles, ceci va entrainer une certaine variance dans le succès reproducteur des mâles (les plus compétiteurs se reproduiront plusieurs fois alors que certains échoueront) ; les mâles ayant réussi à se reproduire plusieurs fois ne vont donc pas apporter de soin parental. Cette situation crée un feedback positif où les mâles seront de moins en moins enclins à fournir un soin parental[32].
Anisogamie
Il semble probable que la reproduction sexuée soit apparue sous la forme d’une reproduction isogame (fécondation impliquant des gamètes possédant la même morphologie). Aujourd’hui, l’isogamie est un phénomène rare, même chez les organismes unicellulaires[33]. L'évolution vers l'anisogamie semble avoir été le fait d'une sélection disruptive (en)[34]. Ce type de sélection favorise les extrêmes d'un trait et élimine peu à peu la valeur moyenne. Par définition, les individus femelle sont ceux qui produisent les gros gamètes et donc les mâles produisent des petits gamètes.
Les gros gamètes ont donc pu être sélectionnés car leur taille augmente leur chance de survie, alors qu'un parent produisant beaucoup de petits gamètes augmente ses chances de voir au moins l'un d'eux rencontrer l'autre type de gamète et le féconder.
Une autre explication serait que les petits gamètes ne transmettent pas de contenu cytoplasmique. Cela évite ainsi tout conflits entre les organites des 2 types de gamètes pouvant produire une descendance non viable.
Dans la majorité des cas, la femelle, en produisant un plus gros gamète riche en réserve, a un investissement par descendant plus important que le mâle ; elle est le sexe limitant. Chez les espèces apportant des soins importants aux jeunes, le sexe limitant sera cependant celui qui s'occupe le plus de sa descendance, cette action très coûteuse en énergie demandant un investissement plus important.
Cette différence d'investissement permet au sexe limitant un choix de son partenaire, et conduit, chez le sexe non limitant, à l'évolution de caractères sexuels secondaires[35].
Stratégies de reproduction
Robert Trivers[36] fut le premier à mettre en évidence les liens entre les différences d’investissement dans la production des gamètes chez mâles et femelles et autres formes d’investissement parental, et la compétition sexuelle. Le sexe avec le moins d’investissement parental a un plus gros potentiel de taux de reproduction[37]. Ainsi, en général, un mâle peut potentiellement fertiliser les ovocytes à un taux beaucoup plus rapide que la femelle peut les produire[38]. Ce qui veut dire que lorsque la femelle peut augmenter son succès reproductif en augmentant la quantité de ressources qu’elle investit dans ses œufs et sa progéniture, le mâle, lui, peut augmenter son succès en allant s’accoupler avec de nombreux autres femelles[39].
Là où les femelles investissent plus dans leur descendance que les mâles, les comportements de parade et d’accouplement sont de loin une stratégie de compétition pour la reproduction puisque les femelles choisiront les mâles offrant les meilleurs ressources et gènes pour leur progéniture. Ces comportements et la compétition entre mâles ont un coût. Il va donc encore y avoir une différence d’allocation à la reproduction entre mâle et femelle, cette fois-ci dans l’acquisition d’armes et d’ornements destinés à plaire à l’autre sexe.

Le coût des ornements sexuels a été démontré dans l’expérience de manipulation chez l’hirondelle rustique (Hirundo rustica), où les mâles avec des filets expérimentalement allongés ont plus de succès reproducteur[40]. Cependant, ces mâles sont handicapés par ce trait lors de la recherche de nourriture ; ils attrapent des proies plus petites et ont un plus petit filet et des plumes de moins bonne qualité lors de la mue suivante. Cela entraîne une diminution de leur succès reproducteur l’année suivante[41].
Notes et références
- (en) Fakhri A. Bazzaz, Nona R. Chiariello, Phyllis D. Coley et Louis F. Pitelka, « Allocating Resources to Reproduction and Defense », BioScience, vol. 37, no 1, , p. 58-67
- (en) George C. Williams, « Natural Selection, the costs of reproduction, and a refinement of Lack's principle », American Naturalist, vol. 100, , p. 687-690
- (en) Eric R. Pianka, « Natural selection of Optimal Reproductive tactics », American Zoologist, vol. 16, , p. 775-784
- (en) Ronald A. Fisher, The Genetical Theory of Natural Selection, Nabu Press, , 304 p. (ISBN 978-1-178-75727-9 et 1178757277, lire en ligne)
- Modèle:Ouvrag
- (en) Michael F. Hirshfield et Donald W. Tinkle, « Natural Selection and the Evolution of reproductive Effort », Proceedings of the National Academy of Sciences, vol. 72, no 6, , p. 2227-2231
- (en) J.R. Ted J. Case, An illustrated guide to theoretical ecology, Oxford University Press, (réimpr. 1999), 449 p. (ISBN 978-0-19-508512-9 et 0195085124), « Chapter 7 : Life History Trade-Offs »
- Micheal Begon, Colin R. Townsend, John L. Harper, Ecology: From Individuals to Ecosystems, John Wiley & Sons, 2006 (réimpr. 1986), 752 p. (ISBN 1405111178) et (ISBN 978-1405111171)), « Chapter 4 : Life, Death and Life Histories »
- (en) Stephen R. Palumbi, « Humans as the World’s Greatest Evolutionary Force », Science, vol. 293, no 5536, , p. 1786-1790 (DOI 10.1126/science.293.5536.1786)
- (en) T. H. Clutton-Brock, « The Evolution of Parental Care », Journal of Evolutionary Biology, vol. 5, no 4, , p. 719–721 (DOI 10.1046/j.1420-9101.1992.5040719.x)
- (en) Judith E. Mank, Daniel E. L. Promislow et John C. Avise, « Phylogenetic Perspectives in the Evolution of Parental Care in Ray-Finned Fishes », Evolution, vol. 59, no 7, , p. 1570-1578 (JSTOR 3449179)
- (en) Anthony A. Echelle, « Behavior of the pupfish, Cyprinodon rubrofluviatilis », Copeia, vol. 1973, no 1, , p. 68–76 (JSTOR 1442359)
- (en) Theodore A. Evans, « Offspring Recognition by Mother Crab Spiders with Extreme Maternal Care », Proceedings: Biological Sciences, vol. 265, no 1391, , p. 129-134 (JSTOR 50991)
- (en) Edward Wilson, Sociobiology : The New Synthesis, Harvard University Press, , 720 p. (ISBN 978-0-674-00235-7 et 0674002350, lire en ligne)
- (en) Jeffrey R. Baylis, « The evolution of parental care in fishes, with reference to Darwin's rule of male sexual selection », Environmental Biology of Fishes , vol. 6, no 2, , p. 223-251 (DOI 10.1007/BF00002788)
- (en) Douglas W. Tallamy, « Insect Parental Care », BioScience, vol. 34, no 1, , p. 20-24 (JSTOR 1309421)
- (en) Trevor Price, « Maternal and paternal effects in birds: effects on offspring fitness. Maternal effects as adaptations », Oxford University Press, vol. 202, , p. 226
- (en) David Lack, « The Significance of Clutch-size », Ibis, vol. 89, , p. 302-352 (DOI 10.1111/j.1474-919X.1947.tb04155.x)
- (en) Mark S. Boyce et C. M. Perrins, « Optimizing Great Tit Clutch Size in a Fluctuating Environment », Ecological Society of America, vol. 68, no 1, , p. 142-153 (DOI 10.2307/1938814, JSTOR 1938814)
- (en) Alexis L. Romanoff et A.J. Romanoff, Avian Egg, Oxford University Press, , 918 p. (ISBN 978-0-471-73227-3 et 0471732273), « Chapter 7 : Life History Trade-Offs »
- (en) Martin L. Cody, « A General Theory of Clutch Size », Evolution, vol. 20, no 2, , p. 174-184 (DOI 10.2307/2406571, JSTOR 2406571)
- (en) Robert E. Ricklefs, « The Temporal Component of Diversity Among Species of Birds », Evolution, vol. 20, no 2, , p. 235-242 (DOI 10.2307/2406576, JSTOR 2406576)
- (en) Nicholas B. Davies, John R. Krebs et Stuart A. West, Introduction to Behavioral Ecology, Blackwell Science Ltd, (réimpr. 1981), 520 p. (ISBN 978-1-4051-1416-5 et 1405114169, lire en ligne), chap. 8 (« Parental Care and Family Conflicts »)
- (en) David W. Zeh et Robert L. Smith, « Paternal Investment by Terrestrial Arthropods », American Society of Zoologists, vol. 25, no 3, , p. 785–805 (DOI 10.1093/icb/25.3.785)
- (en) Douglas W. Tallamy, « Sexual selection and the evolution of exclusive paternal care in arthropods », Journal of Evolutionary Biology, vol. 60, no 5, , p. 559–567 (DOI 10.1006/anbe.2000.1507)
- (en) J.D. Reynolds, N.B. Goodwin et R.P. Freckleton, « Evolutionary transitions in parental care and live bearing in vertebrates », Philosophical Transactions of the Royal Society of London, vol. 357, , p. 269-281 (DOI 10.1098/rstb.2001.0930)
- (en) C.W. Beck, « Mode of fertilization and parental care in anurans », Animal Behavior, vol. 55, , p. 439–449 (DOI 10.1006/anbe.1997.0619)
- (en) K. Summers, C.S. McKeon et H. Heying, « The evolution of parental care and egg size: a comparative analysis in frogs », Proceedings of the Royal Society of London, vol. 273, , p. 687–692 (DOI 10.1098/rspb.2005.3368)
- (en) D. Lack, « Ecological Adaptations for Breeding in Birds », Science, vol. 163, no 3872, , p. 1185-1187 (DOI 10.1126/science.163.3872.1185)
- A. Cockburn, « Prevalence of different modes of parental care in birds », Proceedings of the Royal Society of London, Series B, vol. 273, , p. 1375-1383 (DOI 10.1126/science.163.3872.1185)
- (en) D.C. Queller, « Why do females care more than males? », Proceedings of the Royal Society of London, Series B, vol. 264, , p. 1555-1557 (DOI 10.1098/rspb.1997.0216)
- (en) H. Kokko et M.D. Jennions, « Parental investment, sexual selection and sex ratios », Journal of Evolutionary Biology, vol. 21, , p. 919-948 (DOI 10.1111/j.1420-9101.2008.01540.x)
- Étienne Danchin, Luc-Alain Giraldeau, Frank Cézilly, Écologie comportementale, Éditions Dunod, (lire en ligne), p. 240.
- (en) M. G. Bulmer et G. A. Parker, « The evolution of anisogamy: a game-theoretic approach », Proceedings of the Royal Society of London, vol. 269, no 1507, , p. 2381-2388 (DOI 10.1098/rspb.2002.2161)
- (en) T. H. Clutton-Brock et A. C. J. VINCENT, « Sexual selection and the potential reproductive rates of males and females », Nature, vol. 351, , p. 58-60 (DOI 10.1038/351058a0)
- (en) R.I. Trivers, « Parental investment and sexual selection », dans Bernard Grant Campbell, Sexual selection and the descent of man, 1871-1971, Chicago, Aldine, , 139-179 p.
- (en) T. H. Clutton-Brock et G. A. Parker, « Potential Reproductive Rates and the Operation of Sexual Selection », The Quarterly Review of Biology, vol. 67, no 4, , p. 437-456 (JSTOR 2832015)
- (en) K. Nakatsuru et D.L. Kramer, « Is sperm cheap? Limited male fertility and female choice in the lemon tetra (pisces, characidae) », Science, vol. 216, no 4547, , p. 753-755 (DOI 10.1126/science.216.4547.753)
- (en) A.J. Bateman, « Intra-sexual selection in Drosophila », Heredity, vol. 2, , p. 349-368
- (en) A.P. Møller, « Female choice selects for male sexual tail ornaments in the monogamous swallow », Nature, vol. 332, , p. 640-642 (DOI 10.1038/332640a0)
- (en) A.P. Møller, « Viability costs of male tail ornaments in a swallow », Nature, vol. 339, , p. 132-135 (DOI 10.1038/332640a0)
Annexes
articles connexes
Bibliographie
- (en) J.R. Ted J. Case, An illustrated guide to theoretical ecology, Oxford University Press, (réimpr. 1999), 449 p. (ISBN 978-0-19-508512-9 et 0195085124), « Chapter 7 : Life History Trade-Offs »
- (en) Micheal Begon, Colin R. Townsend et John L. Harper, Ecology : From Individuals to Ecosystems, John Wiley & Sons, (réimpr. 1986), 752 p. (ISBN 978-1-4051-1117-1 et 1405111178), chap. 4 (« Life, Death and Life Histories »)
- (en) Nicholas B. Davies, John R. Krebs et Stuart A. West, Introduction to Behavioral Ecology, Blackwell Science Ltd, (réimpr. 1981), 520 p. (ISBN 978-1-4051-1416-5 et 1405114169, lire en ligne), chap. 8 (« Parental Care and Family Conflicts »)