n-Hexane
Le n-hexane, ou parfois simplement hexane, est un hydrocarbure saturé de la famille des alcanes de formule brute C6H14.
| Hexane | ||
| ||
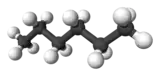 | ||
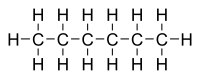
| Formule développée et représentation 3D de l'hexane | ||
| Identification | ||
|---|---|---|
| Nom UICPA | hexane | |
| Synonymes |
n-hexane |
|
| No CAS | ||
| No ECHA | 100.003.435 | |
| No CE | 203-777-6 | |
| PubChem | 8058 | |
| SMILES | ||
| InChI | ||
| Apparence | liquide incolore, volatil, d'odeur caractéristique[1] | |
| Propriétés chimiques | ||
| Formule | C6H14 [Isomères] |
|
| Masse molaire[2] | 86,175 4 ± 0,005 8 g/mol C 83,63 %, H 16,37 %, |
|
| Moment dipolaire | 0,09 D[3] | |
| Diamètre moléculaire | 0,587 nm[3] | |
| Propriétés physiques | ||
| T° fusion | −95,3 °C[4] | |
| T° ébullition | 68,73 °C[5] | |
| Solubilité | 9,5 mg·l-1 (eau, 25 °C)[4] | |
| Paramètre de solubilité δ | 14,9 MPa1/2 (25 °C)[6] | |
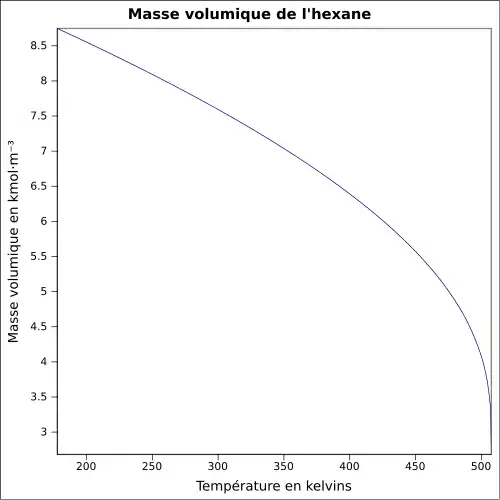
| Masse volumique | 0,659 4 g·cm-3[7]
|
|
| T° d'auto-inflammation | 225 °C[1] | |
| Point d’éclair | −22 °C (coupelle fermée)[1] | |
| Limites d’explosivité dans l’air | 1,1–7,5 %vol[1] | |
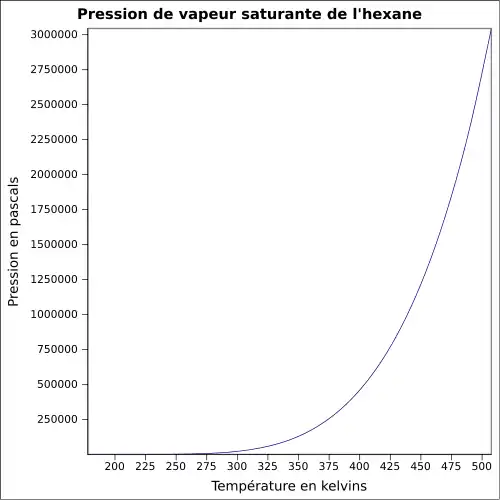
| Pression de vapeur saturante | 151 mmHg (25 °C)[4]
|
|
| Viscosité dynamique | 0,309 mPa·s à 24,95 °C[9] | |
| Point critique | 2 990 kPa[5], 234,45 °C[10] | |
| Vitesse du son | 1 083 m·s-1 à 20 °C[11] | |
| Thermochimie | ||
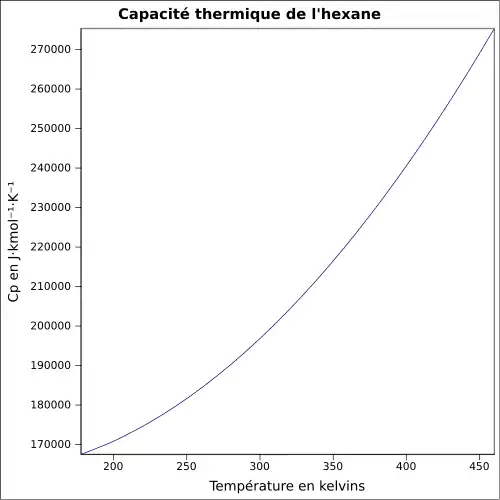
| Cp | ||
| PCS | 4 163,2 kJ·mol-1 (25 °C, liquide)[13] | |
| Propriétés optiques | ||
| Indice de réfraction | 1,3723[3] | |
| Précautions | ||
| SGH[14] | ||
    Danger |
||
| SIMDUT[15] | ||
  B2, D2A, |
||
| Transport | ||
| Écotoxicologie | ||
| DL50 | 25 000 mg·kg-1 (rat, oral)[4] 5 000 mg·kg-1 (souris, oral)[16] 45 ml·kg-1 (rat, oral)[16] 3 000 mg·kg-1 (lapin, cutané)[16] 28 710 mg·kg-1 (rat, oral)[16] |
|
| CL50 | 48 000 ppm pendant 4 heures (rat, inhalation)[4] 48 000 ppm pendant 4 heures (souris, inhalation)[16] |
|
| LogP | 3,9[1] | |
| Seuil de l’odorat | bas : 65 ppm haut : 248 ppm[17] |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
Usage et mise en garde
L'hexane est un solvant utilisé en chimie organique (notamment pour les réactions et les extractions). Il est important de respecter les règles de sécurité concernant ce composé en raison de sa toxicité.
Celle-ci se manifeste par la formation d'un métabolite, l'hexan-2,5-dione, un composé di-carbonylé, qui s'accumule dans le système nerveux central et qui est très toxique. Ce dernier peut être dosé dans les urines pour déceler une éventuelle intoxication.
L'hexane est en conséquence couramment remplacé par le cyclohexane, notamment pour la chromatographie préparative. Si l'usage de l'hexane est préféré, il convient de se protéger efficacement, en particulier grâce à des hottes aspirantes.
137 ouvriers travaillant pour le sous-traitant d'Apple Wintek ont été intoxiqués au n-hexane en 2009[18]. Quatre en seraient morts[19].
Notes et références
- n - HEXANE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1)
- (en) « N-Hexane », sur ChemIDplus, consulté le 12 février 2009
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Pressures. Part I. Aliphatic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 35, no 4, , p. 1461 (DOI 10.1063/1.2201061)
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.289
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) Makio Iwahashi, Yoshimi Yamaguchi, Yoshio Ogura et Masao Suzuki, « Dynamical Structures of Normal Alkanes, Alcohols, and Fatty Acids in the Liquid State as Determined by Viscosity, Self-Diffusion Coefficient, Infrared Spectra, and 13CNMR Spin-Lattice Relaxation Time Measurements », Bulletin of the Chemical Society of Japan, vol. 8, , p. 2154-2158 (DOI 10.1246/bcsj.63.2154)
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Temperatures. Part I. Aliphatic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 32, no 4, , p. 1411 (DOI 10.1063/1.1556431)
- (en) William M. Haynes, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 91e éd., 2610 p. (ISBN 9781439820773, présentation en ligne), p. 14-40
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-858-6)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Hexane normal » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- (en) « Hexane » (consulté le )
- « n-Hexane », sur hazmap.nlm.nih.gov (consulté le )
- « Un nouveau scandale frappe Apple en Chine », Le Parisien, (lire en ligne).
- « Workers protest over pay, toxic chemicals », sur China Daily (consulté le ).
Liens externes
- hexane sur NIST Chemistry WebBook
- Fiche toxicologique de l'INRS
- Fiche internationale de sécurité