N,N-Diméthylaniline
La N,N-diméthylaniline, ou plus simplement diméthylaniline (DMA) est un composé aromatique de formule C6H5N(CH3)2. C'est l'isomère de la diméthylaniline, dérivé diméthylé de l'aniline, où les deux groupes méthyle sont portés par l'azote du groupe amine, d'où le nom N, N-diméthylaniline dans la nomenclature UICPA. Il s'agit donc d'une amine aromatique tertiaire, qui se présente normalement sous forme d'un liquide huileux incolore lorsqu'il est pur, mais dont les échantillons commerciaux sont généralement jaunâtres.
| Diméthylaniline | |
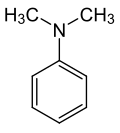  Structure de la diméthylaniline |
|
| Identification | |
|---|---|
| Nom UICPA | N,N-diméthylaniline |
| Synonymes |
DMA |
| No CAS | |
| No ECHA | 100.004.085 |
| No CE | 204-493-5 |
| SMILES | |
| Apparence | Liquide incolore à jaunâtre |
| Propriétés chimiques | |
| Formule | C8H11N [Isomères] |
| Masse molaire[1] | 121,179 6 ± 0,007 4 g/mol C 79,29 %, H 9,15 %, N 11,56 %, |
| Diamètre moléculaire | 0,622 nm [2] |
| Propriétés physiques | |
| T° fusion | 2 °C |
| T° ébullition | 194 °C |
| Paramètre de solubilité δ | 19,3 J1/2·cm-3/2 (25 °C)[2] |
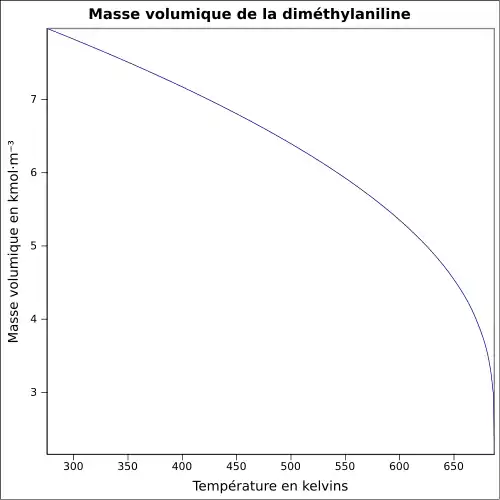
| Masse volumique | 956 kg·m-3
|
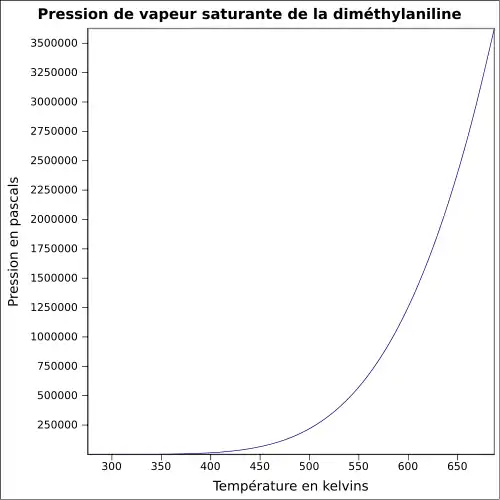
| Pression de vapeur saturante | |
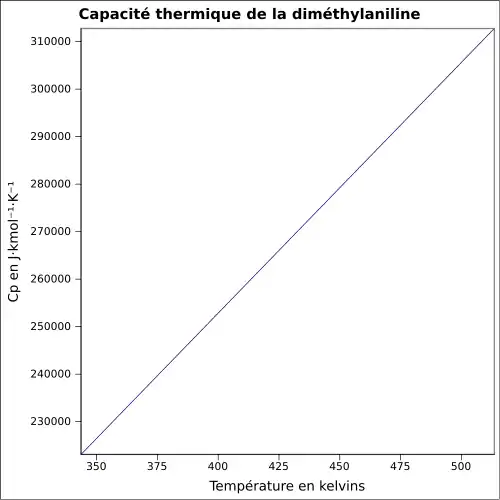
| Thermochimie | |
| Cp | |
| Propriétés optiques | |
| Indice de réfraction | 1,558 2 [4] |
| Précautions | |
| Directive 67/548/EEC | |
 T  N |
|
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[5] | |
| Écotoxicologie | |
| Seuil de l’odorat | bas : 0,001 ppm haut : 0,2 ppm[6] |
| Unités du SI et CNTP, sauf indication contraire. | |
Préparation et réactions
La diméthylaniline est produite industriellement par alkylation de l'aniline en présence d'un catalyseur acide[7] :
La DMA donne la plupart des réactions de l'aniline. Elle est faiblement basique, et réagit avec les électrophiles. Sa nitration donne du tétryl (ou tétralyte), un dérivé à quatre groupes nitro utilisé autrefois comme explosif. Elle peut être lithiée avec le butyllithium. Sa méthylation donne un sel d'ammonium quaternaire[8] :
- C6H5N(CH3)2 + (CH3O)2SO2 → [C6H5N+(CH3)3][CH3OSO3]−
Applications
La diméthylaniline est utilisée dans la réticulation de résines polyester et vinyl ester. Elle intervient également comme précurseur dans d'autres synthèses organiques.
Il s'agit d'un précurseur important de la chimie des colorants, on le retrouve dans les synthèses du vert malachite, du violet de gentiane ou encore de l'hélianthine.
Références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1).
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50.
- (en) J. G. Speight et Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.289.
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme », sur monographs.iarc.fr, CIRC, (consulté le ).
- « Dimethylaniline », sur hazmap.nlm.nih.gov (consulté le ).
- Thomas Kahl, Kai-Wilfrid Schröder, « Aniline » dans Ullmann's Encyclopedia of Industrial Chemistry 2007, John Wiley & Sons, New York.
- (en) J. Jacques et A. Marquet, « Selective α-Bromination of an Aralkyl Ketone with Phenyltrimethylammonium Tribromide: 2-Bromoacetyl-6-methoxynaphthalene and 2,2-Dibromoacetyl-6-Methoxynaphthalene », Organic Syntheses, vol. 53, , p. 111 (DOI 10.15227/orgsyn.053.0111).