Formiate d'éthyle
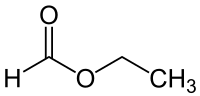
Le formiate d'éthyle est l'ester éthylique de l'acide formique et a pour formule semi-développée HCOOCH2CH3. Dans l’industrie il est utilisé comme solvant, voire comme arôme dans l’industrie alimentaire.
| Formiate d'éthyle | |
| |
| Identification | |
|---|---|
| Nom UICPA | formiate d'éthyle |
| Synonymes |
méthanoate d'éthyle |
| No CAS | |
| No ECHA | 100.003.384 |
| No CE | 203-721-0 |
| PubChem | 8025 |
| ChEBI | 52342 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C3H6O2 [Isomères] |
| Masse molaire[1] | 74,078 5 ± 0,003 4 g/mol C 48,64 %, H 8,16 %, O 43,2 %, |
| Propriétés physiques | |
| T° fusion | −80 °C[2] |
| T° ébullition | 54 °C[2] |
| Solubilité | 105 g·l-1 (eau,20 °C) [2] |
| Paramètre de solubilité δ | 20,9 J1/2·cm-3/2 (25 °C)[3] |
| Masse volumique | 0,917 82 g·cm-3 à 20 °C [4]
|
| T° d'auto-inflammation | 445 °C [2] |
| Point d’éclair | −20 °C [2] |
| Limites d’explosivité dans l’air | 2,7–16,5 %vol [2] |
| Viscosité dynamique | 0,402 mPa·s à 20 °C [4]
|
| Thermochimie | |
| Cp | 144,3 J·K-1·mol-1 (liquide,25 °C) [5] |
| Précautions | |
| SGH[2] | |
  |
|
| SIMDUT[6] | |
  B2, D2B, |
|
| NFPA 704[7] | |
| Transport[2] | |
| Écotoxicologie | |
| DL50 | 1,85 g·kg-1 (rat, oral) [8] |
| LogP | 0,27 [2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Exposition
Le formiate d'éthyle est classé dans la catégorie generally recognized as safe (considéré comme sans danger) par la Food and Drug Administration[9].
Selon l'Occupational Safety and Health Administration (OSHA), le formiate d'éthyle peut irriter les yeux, la peau, les muqueuses et le système respiratoire de l'homme et des autres. C'est aussi un dépresseur du système nerveux central[10].
L'OSHA considère la limite d'exposition admissible à une période de 8 heures exposé à un environnement contenant 100 parties par million (300 milligrammes par mètre cube).
Utilisation
Dans l’industrie, le formiate d’éthyle est utilisé comme solvant pour dissoudre le nitrate de cellulose, l'acétate de cellulose et différentes résines[11].
Il peut être utilisé comme substitut à l'acétone. Les travailleurs peuvent être aussi exposé au formiate d'éthyle [10] :
- pendant l'application par pulvérisation, au pinceau ou par trempage de vernis :
- pendant la fabrication de verre de sécurité;
- pendant la fumigation du tabac, de céréales et de fruits séchés (comme alternative au bromure de méthyle dans le système de quarantaine du Département de l'Agriculture des États-Unis[9]).
Il est également utilisé comme arôme alimentaire pour des saveurs fruitées[4] - [12] et aussi pour son odeur caractéristique du rhum[13] (et partiellement celle des framboises[14]).
Dans l'espace
Des astronomes ont détecté du formiate d'éthyle dans des nuages de poussière dans une zone de la Voie lactée appelée Sagittarius B2. Les astronomes de l'Institut Max-Planck de radioastronomie à Bonn, en Allemagne, ont utilisé le radiotélescope de Pico Veleta de l'IRAM en Espagne pour analyser le spectre de radiation émis par les régions chaudes près d'une étoile nouvelle. Le formiate d'éthyle fait partie des 50 molécules identifiées par les astronomes[15]. Pour s'amuser, il est donc possible de dire que la galaxie a une odeur de rhum ou de framboise.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Ethyl formate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 27 juillet 2010 (JavaScript nécessaire)
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- (en) Hiannie Djojoputro et Suryadi Ismadji, « Density and Viscosity Correlation for Several Common Fragrance and Flavor Esters », Journal of Chemical & Engineering Data, vol. 50, no 2, , p. 727-731 (DOI 10.1021/je050001c)
- (en) R Fuchs, « Heat capacities of some liquid aliphatic, alicyclic, and aromatic esters at 298.15 K », J. Chem. Thermodyn., vol. 11, no 10, , p. 959-961 (DOI 10.1016/0021-9614(79)90044-2)
- « Formate d'éthyle » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 27 juillet 2010
- UCB Université du Colorado
- (en) « Formiate d'éthyle », sur ChemIDplus, consulté le 27 juillet 2010
- (en) « Alternative fumigants: Ethyl Formate »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), University of California (consulté le )
- (en) « Occupational Safety and Health Guideline for Ethyl Formate », OSHA (consulté le )
- (en) Dieter Stoye, Solvents, Wiley-VCH Verlag GmbH & Co, coll. « Ullmann's Encyclopedia of Industrial Chemistry », (DOI 10.1002/14356007.a24_437, présentation en ligne)
- (en) Karl-Georg Fahlbusch, Franz-Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe, Horst Surburg, Flavors and Flagrances, Wiley-VCH Verlag GmbH & Co, coll. « Ullmann's Encyclopedia of Industrial Chemistry », (DOI 10.1002/14356007.a11_141, présentation en ligne)
- formiate d’éthyle futura-sciences, consulté le 12 août 2020
- (en) Ian Sample, « « Galaxy's centre tastes of raspberries and smells of rum, say astronomers » », The Guardian, (lire en ligne, consulté le )
- (en) Ian Sample, « Galaxy's centre tastes of raspberries and smells of rum, say astronomers », The Guardian, (lire en ligne, consulté le )
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Ethyl formate » (voir la liste des auteurs).




